摘要
吸入皮质类固醇(IC)的长期治疗可能会衰减肺功能下降,减少慢性阻塞性肺病(COPD)患者的患者中的气道炎症,并且停止IC治疗可能导致进一步的肺功能下降。我们假设在COPD中的长期ICS治疗后ICS退出后,气道炎症增加。
在GL1研究(GL1)中,114例中重度COPD患者被随机分为丙酸氟替卡松(500µg,每日2次)、氟替卡松/沙美特罗(500/50µg,每日2次)或安慰剂治疗6个月或30个月。在5年随访研究(GL2)中,患者在接受医生治疗期间进行前瞻性随访。在基线、30个月(GL1结束)和7.5年(GL2结束)采集支气管活检和诱导痰,以评估炎症细胞计数。使用线性混合效应模型对数据进行分析。
在GL1期间使用IC的患者,使用GL2期间的0-50%(n = 61/85),GL2支气管CD3显着增加+(每年的fold change按GL2 - GL1计算为2.68,95% CI 1.87-3.84), CD4+(1.91, 95% CI 1.33-2.75)和CD8+细胞(1.71,95% CI 1.15-2.53)和肥大细胞(1.91,95% CI 1.36-2.68)。GL2、巨噬细胞(2.10,95% CI 1.55-2.86)、中性粒细胞(1.92,95% CI 1.39-2.65)和淋巴细胞(2.01,95% CI 1.46-2.78)的痰总细胞数均显著增加。
ICS停药增加了中-重度COPD患者的气道炎症,提示ICS在COPD中的抗炎作用在ICS停药后没有得到维持。
摘要
长期停用ICS会增加COPD患者的气道炎症,因此无法实现持续的疾病改善http://ow.ly/h5vp305cmot.
介绍
慢性阻塞性肺疾病(COPD)的特征是气道慢性炎症,伴有中性粒细胞、巨噬细胞和CD8+t细胞是主要的炎症细胞类型[1].随着病情发展到更严重的气流限制,气道炎症随时间增加[2-4.].除了戒烟外,目前还没有一种治疗方法可以阻止呼吸道的炎症过程。
根据目前的准则,建议用吸入的皮质类固醇(ICS)治疗严重和非常严重的COPD患者频繁加剧。迄今为止,很少有试验使用支气管活组织检查和支气管肺泡灌洗(BAL)来评估IC在COPD中的抗炎作用。最近的荟萃分析表明,COPD中12-26周的ICS治疗减少了CD4+和CD8.+支气管活检的细胞计数[5.-10].此外,ICS降低了BAL患者的中性粒细胞和淋巴细胞计数,但增加了巨噬细胞计数[9.那11-13].我们的研究组之前已经表明,吸入氟替卡松30个月的治疗可以减少支气管CD3的数量+,CD4+, CD8+和肥大细胞,并减少痰中性粒细胞,巨噬细胞和淋巴细胞计数[8.].
IC的中断可能会增加加剧的数量[14-16],加速COPD患者肺功能下降[17-22].然而,关于停用ICS对气道炎症的影响知之甚少。与ICS持续6周的COPD患者相比,随机组ICS停药的COPD患者中痰中性粒细胞百分比增加[23].我们之前的研究表明,ICS治疗6个月后停药增加了支气管CD3+对痰炎细胞无显著影响[8.].长期治疗后停用ICS对气道炎症的影响尚未研究,但它们与评估支气管炎症的持续减少和可能的疾病改善作用高度相关。
我们假设,在先前被随机分为30个月ICS治疗的COPD患者停用ICS后,在随后的5年前瞻性随访中,支气管活检和痰中炎症细胞计数将增加。此外,我们还研究了ICS停药后炎症变化是否与肺功能下降的变化相关。
材料和方法
研究设计和参与者
糖果患者(Groningen和Leiden大学皮质类固醇在阻塞性肺病中)研究(GL1)被纳入观察到的后续研究(GL2)。总随访时间为5年。研究设计的细节先前描述了[8.那20.].在GL1中,114例中度至严重COPD患者的患者被随机化为四个治疗臂中的四个治疗臂中的一种(Glaxosmithkline,荷兰),每次每天30个月(FP)两次,每次两次:1)丙酮酮500μg(F30);2)FP配萨尔梅尔,500/50μg,单吸入器(FS30);3)6个月FP随后24个月安慰剂(F6);4)安慰剂。在GL2期间,患者根据目前的指导方针由自己的医生治疗[24,提示大多数患者间歇性使用或不使用ICS。GL2结束时,由患者药房提供送药清单。莱顿大学医学中心和格罗宁根大学医学中心伦理委员会批准了GL1和GL2。所有患者均单独提供GL2的书面知情同意书。
结果和测量
本研究的主要结果是停用ICS对支气管活检固有层炎症细胞计数的影响。因此,随访5年(GL2)后,按照标准化方案进行纤维支气管镜检查,与GL1的支气管镜检查一致[25].根据目前的建议进行支气管活组织检查[26[基于通过评价用苏木精 - 曙红染色的部分测定的最大薄层丙蛋白,选择每位患者的两个活组织检查。用针对T淋巴细胞(CD3,CD4和CD8),巨噬细胞(CD68),中性粒细胞弹性蛋白酶(NE),肥大细胞胰蛋白酶(AA1)和嗜酸性粒细胞(eg2),根据之前的协议[25].由于在GL1中缺乏明显的ics诱导的浆细胞变化,我们在当前的分析中没有包括这些细胞。使用图像分析软件(ImageJ, version 1.48i, National Institutes of Public Health, Bethesda, MD, USA)计数支气管细胞。亚上皮细胞以加权平均数计算,以每0.1 mm的细胞数表示2.每种活组织检查分析的Lamina Propria的最小选定区域为20000μm2.基线和30个月后的支气管细胞计数数据(GL1)以前曾有报道[8.].
二次结果是ICS中断对诱导痰中炎症细胞计数的影响。在GL2的第二和第五年中进行痰液诱导。出于安全原因,痰仅在1秒内(FEV)患者患有后支气管扩张剂强制呼气量诱导的患者1)≥1.2L。根据完整的样品方法处理诱导的痰[27].每个样本用May-Grünwald-Giemsa染色以获得不同的细胞计数。如果≤80%的细胞包括鳞状细胞,则认为痰标本足够。差异细胞计数表示为每10个细胞计数4.mL非鳞状有核细胞。基线和30个月后的痰细胞计数(GL1)以前有报道[8.].
统计分析
所有患者的数据用于分析,并使用SPSS 22.0软件(SPSS Inc.,Chicago,IL,USA)进行统计分析。因为在F6和安慰剂组之间治疗30个月后,炎性细胞计数在FS30和F30组之间没有差异,因此FS30和F308.[我们将这些组合成两组增加功率:F6 /安慰剂和FS30 / F30。在GL2期间使用的ICS使用被回顾性分为两组:使用IC的患者0-50%的时间,以及使用IC的时间50-100%的时间。对于GL2的分析,我们专注于在GL2期间使用IC 0-50%的患者,因为它们形成了最大的亚组(85名患者中的61名)。基于患者药房的信息,在5年内的每日IC(μg,μg)的日剂量(μg,eysode over)作为每日分类(μg/天)除以使用IC的总时间(天)。
对每个受试者采用随机截距的线性混合效应模型,使用来自GL1和GL2的所有自然对数转化的炎症测量作为结果变量和恒等协方差矩阵。对原始联合治疗组和GL2期间ICS的使用进行分层分析。与GL1 (GL2 - GL1)相比,GL2中的炎症细胞计数的变化通过模型中的两个时间变量进行评估:时间1 (GL1开始发生的时间:0-7.5年)和时间2 (GL2开始发生的时间:0-5年;在GL1期间,此值为零)。为了评估原始FS30/F30组与原始F6/安慰剂组之间的细胞计数变化,使用了一个具有相同时间变量的线性混合效应模型,其中包括这些时间变量与原始联合治疗组之间的交互项。由于完成5年前瞻性随访的患者样本量有限,可能的混杂因素(年龄、性别和医疗中心)未纳入模型。吸烟不太可能是一个主要的混杂因素,如前所述后HOC分析(8.].我们使用Spearmans相关系数评估GL2炎症是否发生变化与GL1与同期肺功能变化有关。
由于GL1期间细胞数量减少,GL2结束时细胞数量增加,因此斜率不同,我们计算了变化率。因此,数据以GL2 - GL1之间每年的折数变化(95%置信区间)表示,这是通过取线性混合效应模型估计值的反对数计算的。推断p≤0.05有统计学意义。
结果
114名患者的数据用于GL1的分析;92名患者完成GL1,85名患者开始,61名完成GL2 [8.那20.].除了后支气管扩张剂FEV之外,原始组合治疗组的患者特征在基线和GL2的开始情况下都相似1,在原始组合F6 /安慰剂组中GL2开始时显着降低,而不是原始的FS30 / F30组(表1).大多数患者(85例中61例)在GL2期间0-50%的时间内使用ICS, GL2期间BDP当量的平均每日ICS剂量为1019±554µg (表2),在原联合治疗组间差异无统计学意义。29例患者在GL2结束时进行了支气管活检(表3),这29例患者中有21例在GL2期间0-50%的时间使用ICS。随访2年和5年,分别有47例和33例患者的痰标本可供分析(表3).图1显示每组患者的数量和可用的样本数量。
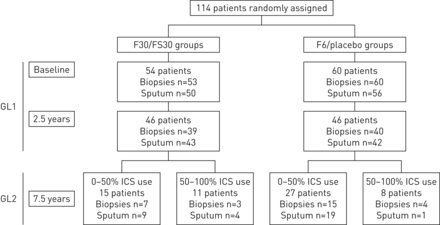
原始联合治疗组GL1、GL2患者人数及可用支气管活检、痰标本。GL1: glold -1研究,研究的第一部分;GL2: glold -2研究,随访研究;F6:氟替卡松治疗6个月,随后安慰剂治疗24个月;F30:氟替卡松治疗30个月;FS30:氟替卡松和沙美特罗治疗30个月;ICS:吸入型皮质类固醇激素。
支气管活检
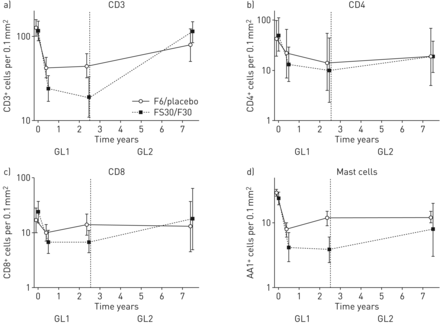
原始FS30/F30联合组患者GL2期间使用ICS的0-50%的时间显示支气管CD3增加+细胞(使用GL2减去GL1(GL2-GL1)2.68,95%CI 1.87-3.84,P <0.001),CD4+细胞(1.91,95%CI 1.33-2.75,P = 0.001),CD8+与GL1相比,GL2末端的肥大细胞(1.71,95% CI 1.15-2.53, p=0.008)和肥大细胞(1.91,95% CI 1.36-2.68, p<0.001)图2,补充图S1,补充表S1)。在GL2期间停止IC或使用IC 0-50%的时间增加了CD3的数量+细胞(GL2-GL1每年fold change 1.78, 95% CI 1.21-2.64, p=0.04), CD8+与原始联合F6 /安慰剂组相比,在原始联合FS30 / F30组中,细胞(1.73,95%CI 1.05-2.85,P = 0.033)和肥大细胞(1.52,95%CI 1.06-2.17,P = 0.023)。
支气管活检的几何平均细胞计数(每0.1 mm2Lamina Propria)对于那些在原始组合治疗组FS30 / F30和F6 /安慰剂中使用吸入皮质类固醇(ICS)0-50%的患者。误差栏代表95%CI。虚线表示GL1和GL2之间的分离。支气管A)CD3+细胞,b)CD4+CD8细胞,c)+细胞和D)肥大细胞(AA1+提出了)。数据采用自然对数转化细胞数平均值的反对数进行计算。GL2期间50% - 100%使用ICS的患者人数太少,因此没有显示在图中。GL1: glold -1研究,研究的第一部分;GL2: glold -2研究,随访研究;F6:氟替卡松治疗6个月,随后安慰剂治疗24个月;F30:氟替卡松治疗30个月;FS30:氟替卡松和沙美特罗治疗30个月。
痰
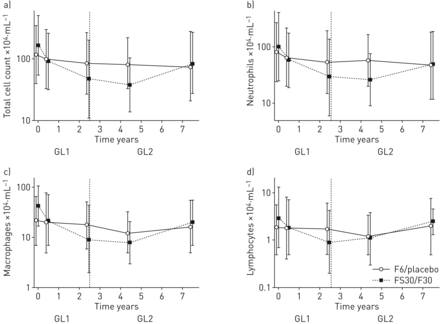
患者在最初FS30 / + 30组使用ICS 0 - 50%的时间在GL2痰细胞总数较高(褶皱变化每年GL2-GL1 1.90, 95%可信区间1.42 - -2.54,p < 0.001)以及更高的痰巨噬细胞计数(2.10,95%可信区间1.55 - -2.86,p < 0.001),中性粒细胞(1.92,95%可信区间1.39 - -2.65,p < 0.001)和淋巴细胞(2.01,95% CI 1.46-2.78, p<0.001)图3,补充图S2,补充表S2)。ICS的中止或使用ICS 0 - 50%的时间在GL2增加痰细胞的总数(表示为褶皱变化每年GL2-GL1 1.66, 95%可信区间1.12 - -2.46,p = 0.012),痰中性粒细胞(1.68,95%可信区间1.09 - -2.58,p = 0.018),巨噬细胞(1.90,95%可信区间1.26 - -2.85,p = 0.002)和淋巴细胞(1.73,95%可信区间1.09 - -2.74,p=0.020),原始FS30/F30联合组与原始F6/安慰剂联合组比较。
几何平均痰细胞计数(×104.每毫升)用于原始组合治疗组FS30 / F30和F6 /安慰剂。误差栏代表95%CI。使用吸入皮质类固醇(IC)的患者的数据(ICS)0-50%的GL2期间的时间为A)总痰细胞,B)中性粒细胞,C)巨噬细胞和D)淋巴细胞。数据采用自然对数转化细胞数平均值的反对数进行计算。GL2期间50% - 100%使用ICS的患者人数太少,因此没有显示在图中。GL1: glold -1研究,研究的第一部分;GL2: glold -2研究,随访研究;F6:氟替卡松治疗6个月,随后安慰剂治疗24个月;F30:氟替卡松治疗30个月;FS30:氟替卡松和沙美特罗治疗30个月。
肺功能下降与炎症细胞的关系
后支气管扩张剂FEV的加速率1与原始FS30/F30组患者的痰中巨噬细胞增加相关(Rs=−0.63,p=0.04),支气管中性粒细胞计数有增加趋势(Rs=−0.60,p=0.07) (图4A和B.分别)。
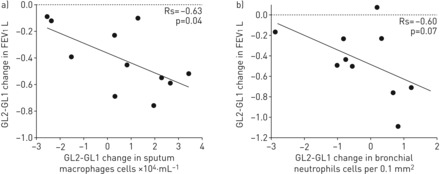
后支气管扩张器FEV的变化(终止GL2减去GL1(GL2-GL1)之间的相关性1A)改变自然对数转化的痰巨噬细胞(GL2-GL1,表示为细胞数×10的表示4.每mL)和b)天然对数转化的支气管中性粒细胞的变化。每个点代表一个患者。FEV.1: 1秒内用力呼气量;GL1: glold -1研究,研究的第一部分;GL2: glold -2研究,随访研究。
讨论
本研究表明,中重度COPD患者既往长期ICS治疗后停用ICS,支气管t淋巴细胞、肥大细胞及多种痰细胞增多。此外,我们发现GL2期间肺功能下降的加速与痰中巨噬细胞的增加有显著相关性,并与支气管中性粒细胞呈趋势。这些结果表明,ICS积极治疗期间气道炎症得到抑制,长期停用ICS治疗后可能复发。
我们观察到,在之前随机接受30个月ICS治疗后,未使用或仅间歇使用ICS的中重度COPD患者的支气管活检和痰中几种炎症细胞计数在5年随访期间显著增加。这些独特的数据证实并扩展了我们研究组之前的研究结果,即ICS治疗6个月后停用ICS增加了支气管CD3的数量+在30个月的随访中,与继续ICS治疗的患者相比,对痰炎症细胞无显著影响[8.].另一项开放标签的试点研究显示,仅ICS停用6周与ICS继续使用相比,痰中性粒细胞百分比增加[23].综上所述,本研究提供了关于COPD患者既往长期使用ICS后长期停用ICS后气道炎症复发的新数据。
在这项纵向研究中,我们发现在中-重度COPD患者中,肺功能下降与痰中巨噬细胞计数增加相关,其中大多数患者未接受ICS治疗。此外,还发现与较高的支气管中性粒细胞相关的趋势。先前的一项研究表明,较高的痰中性粒细胞计数与更快的FEV下降有关1在使用ICS的严重COPD患者中[3.].此外,痰中性粒细胞百分比与FEV之间的相关性较弱1预测的百分比是在横断面研究中发现的[4.].痰中性粒细胞中的这些发现可能不仅通过研究设计的差异,而且在研究中的研究中的差异,COPD的严重程度或表型以及治疗的持续时间和IC的持续时间差异。最近的研究阿恩等.发现基线血嗜酸性粒细胞百分比高的COPD患者接受氟替卡松治疗时FEV速度较慢1与安慰剂治疗患者相比下降[28].然而,在GL2期间停止或继续使用ICS的患者中,我们没有检测到基线血嗜酸性粒细胞增多与GL2期间肺功能下降之间的关系。迄今为止,这是唯一一项表明长期停用ICS后肺功能下降和炎症变化之间存在关联的长期研究。
我们研究的一个优势是在5年的随访中,肺功能监测和痰液和支气管活检的有效性的长期随访。这是独一无二的,因为之前的研究没有如此长时间的治疗和长期的后续治疗,根据目前的指导方针,在现实环境中。需要注意的是,在本研究中,ICS停药的效果在支气管活检中比在痰中更明显,强调了在调查COPD时不仅要研究痰细胞计数的重要性。
尽管如此,我们的研究有一些局限性。首先,预期的是,完成完整研究的患者的数量是有限的,特别是在分别考虑原始治疗组时。因此,为了增加功率,我们组合原始的FS30和F30组,以及F6和安慰剂组,因为F6和安慰剂组在GL2开始时没有差异,但仅在GL1期间的前6个月治疗之后。从支气管活组织检查和痰样品的患者群体的小尺寸可用,使得与肺功能的相关性下降不太强烈。尽管数量相对较低,但我们仍然检测到临床和组织学结果之间的关联。其次,GL2是一种预期(非随机化)观察研究,大多数患者(85分中为85分)停止了他们的IC或使用了GL2期间的时间0-50%的时间(表2).对药物的坚持没有检查,反映了日常实践。这可能导致GL2期间ICS使用的错误分类,这可能会影响我们的结果。然而,当目前的分析只纳入GL1期间依从性的患者时,也发现了类似的结果(数据未显示)。由于进行支气管镜检查的病人数目有限(图1),持续使用ICS的患者的比较与在GL2期间不能停用ICS。第三,用不同批次的抗体对炎症细胞进行免疫组化染色,并使用与GL1不同的相机和图像分析软件计数[29].我们不能排除这些差异影响了我们的数据。然而,GL1和GL2中发现的支气管炎症细胞计数在可比范围内,并不能解释组间和组内观察到的差异。最后,支气管炎症在气道上的分布是不均匀的[30.].由于我们只能从中央气道采集样本,因此本研究无法调查小气道ICS撤药的效果。考虑到这些因素,我们仍然有信心,我们的数据提供了长期停用ICS长期治疗后气道炎症相关变化的新观点。
我们如何解释我们的结果?在研究的第一部分(GL1)中,我们发现在中度严重的COPD患者30个月ICS治疗期间,在30个月的ICS治疗期间发现支气管炎炎症和肺功能下降的减少[8.].在目前的研究(GL2)中,我们观察到先前长期治疗后ICS停药导致CD3增加的预期相反效果+,CD4+和CD8.+这进一步扩展了我们之前的观察,即停用ICS会导致肺功能下降复发[20.].与ICS戒断相比,ICS治疗的相反结果与ICS取出对我们研究的第二个观察阶段的气道炎症相比,可以被视为验证,并强烈支持我们的研究结果的合理性。我们的数据表明,IC对肺功能和炎症的影响是短暂的,没有持续疾病修饰。
在过去的25年里,发表了许多关于ICS是否对COPD患者有益的研究[31].在我们的研究中,中重度COPD患者在ICS治疗期间对肺功能和气道炎症有短暂的积极影响,但在ICS停药后没有维持[20.].目前COPD患者的选择可能代表了一种对类固醇治疗有反应的特殊表型[32,在这些患者中,长期ICS治疗可能需要继续维持所观察到的随时间推移对肺功能和气道炎症进程的有益作用。
总之,目前的数据表明,ICS中止在5年之后的30个月的ICS使用一组moderate-severe COPD患者诱发复发生产支气管和痰炎症细胞,部分伴有更快速的肺功能下降。这些数据表明,该组COPD患者停用ICS后,ICS没有持续的疾病改善活性,这与哮喘患者的观察结果一致。
补充材料
披露
补充材料
注:Hiemstraerj - 00839 - 2016 - _hiemstra
H.A.M Kerstjens.erj - 00839 - 2016 - _kerstjens
L.I.Z.昆兹erj - 00839 - 2016 - _kunz
科学博士PostmaERJ-00839-2016_POSTMA
J.K.是ERJ-00839-2016_SONT.
P.J.斯德克已ERJ-00839-2016_Sterk.
确认
作者感谢所有患者对我们研究的充分配合。
闪胎研究组包括以下参与者。H.F.Kauffman和D. de Reus(ververogology);H..Boezen,D.F.Jansen和J.M.Vonk(流行病学部);M.D.W.Barentenen,W. Timens和M. Zeinstra-Smit(病理学部);A.J.Lutejn,T.Van der Molen和G. Ter Veen(一般练习部);M.M.E. Gosman, N.H.T. ten Hacken, H.A.M. Kerstjens, M.S. van Maaren, D.S. Postma, C.A. Veltman, A. Verbokkem, I. Verhage and K. Klooster (Dept of Pulmonology; all University of Groningen and University Medical Center Groningen, Groningen, the Netherlands). H.A. Thiadens (Dept of General Practice); J.B. Snoeck-Stroband and J.K. Sont (Dept of Medical Decision Making); J. Gast-Strookman, P.S. Hiemstra, K. Janssen, K.F. Rabe, A. van Schadewijk, J.A. Schrumpf, J. Smit-Bakker, J. Stolk, A.C.J.A. Tiré, H. van der Veen, M.M.E. Wijffels and L.N.A. Willems (Dept of Pulmonology; all Leiden University Medical Center, Leiden, the Netherlands). P.J. Sterk (Dept of Respiratory Medicine, Academic Medical Centre, University of Amsterdam, Amsterdam, the Netherlands). T.S. Lapperre (Dept of Respiratory and Critical Care Medicine, Singapore General Hospital, Singapore, Singapore). T. Mauad (University of São Paulo, São Paulo, Brazil).
脚注
本文提供了补充材料www.qdcxjkg.com.
支持声明:该研究由荷兰科学研究组织(批准号940-35-033)、荷兰肺基金会(前荷兰哮喘基金会;批准号93.96.3),葛兰素史克(荷兰;批准号SCO107656)、格罗宁根大学医学中心和莱顿大学医学中心。资金来源在数据的设计、收集和分析、手稿的写作或提交手稿发表的决定中没有作用。本文的资金信息已存入资助者打开注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com.
- 已收到2016年4月28日。
- 公认2016年10月18日。
- 版权©2017人队