摘要
特发性肺纤维化(IPF)是一种预后不良的进行性肺疾病。IPF在病理上似乎是异质性的,发现约40%的IPF患者循环抗体水平升高,针对自身抗原V型胶原蛋白(col(V))。
根据一种有针对性的精准医学方法,我们进行了一期研究,以测试IW001的安全性和探索IW001的潜在疗效。IW001是一种col(V)口服免疫疗法,用于治疗抗体阳性IPF患者。我们将30例抗体阳性IPF患者分成3组,在24周的时间内每日给药。
所有患者完成治疗,无严重不良事件、急性加重或ipf相关住院。在已发表的IPF试验中,最低剂量组的肺功能下降与安慰剂组的报告相当。相比之下,最高剂量队列显示出强迫容和基质金属蛋白酶7稳定的趋势,以及C1q与抗col(V)抗体结合的减少。
IW001可能调节对col(V)的免疫应答,可能是col(V)反应性IPF患者的一种新的治疗方法。
摘要
IW001是安全的,并改善具有V型胶原蛋白抗体的IPF患者的生物标志物和肺功能http://ow.ly/LirbO
简介
特发性肺纤维化(IPF)是一种病因不明的慢性间质性肺疾病。肺泡上皮的重复性、广泛性损伤和异常伤口修复过程似乎是IPF发病背后的驱动因素[1],其特征是肺内细胞外基质不受控制的沉积,导致肺功能丧失。预后极差,诊断后中位生存期约为3年[1,2].
IPF的病理生理学尚不清楚。IPF的发病或延续涉及多种失调过程,包括凝血、炎症、适应性免疫和成纤维细胞活性[3.- - - - - -5].研究尚未确定IPF患者个体通路的相对重要性如何或是否存在差异[6].对患者子集进行分类的能力将允许实施精准医疗方法来治疗受影响的患者[7].
体液自身免疫在IPF中的作用是一个新兴的研究课题。80% IPF患者>血浆中存在自身抗体,包括热休克蛋白70和K-α1微管蛋白特异性自身抗体[8,9].在同样的研究中也检测到抗肺抗原的自反应性t细胞,这支持了一种观点,即对自身抗原的持续适应性免疫反应可能在一些IPF患者的疾病进展中发挥重要作用。先前的研究表明,40-60%的IPF患者可能出现针对V型胶原蛋白(col(V))的自身免疫反应[10,11].
Col(V)是一种次要的胶原蛋白,主要存在于主要的肺胶原蛋白i型的原纤维中。Col(V)有许多功能,包括在肺结构内提供弹性[10],组织和维持胶原纤维的空间结构[12],控制纤维网的形成和其他胶原纤维的直径,并将基质胶原连接到基底膜。肺损伤可导致暴露这种通常隔离的抗原,使其可用于激活自身免疫反应[13].持续的自身免疫反应可能导致异常的肺重构,IPF患者的肺活检显示col(V)水平升高与纤维化和疾病进展相关,并且是生存的预测因素[12].Vittalet al。[10]报道col(V)在IPF肺中高度过表达。此外,临床前研究已证实抗col(V)自身免疫可导致肺纤维化改变[11,14].
口服免疫疗法(OIT)可诱导食物过敏和自身免疫性疾病的临床脱敏。临床前动物研究表明,口服或鼻腔给药纯化col(V)可抑制针对它的体液和细胞介导免疫反应,导致与肺移植排斥反应相关的纤维化肺组织保存[15,16和博莱霉素诱导的肺纤维化[10].
在这项一期临床试验中,我们假设抗col(V)抗体(Ab)的IPF患者中存在OIT伴col(V) (IW001)+这将是一种诱导抗原特异性免疫反应改变和稳定肺功能的安全有效的方法。这项开放标签、多中心的研究旨在评估三种不同剂量的IW001在抗col(V) Ab IPF患者中的安全性、耐受性、生物学和临床效果+.
材料与方法
研究设计
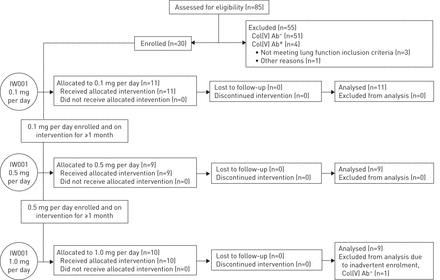
临床试验设计描述在图1.共有85例IPF患者(根据美国胸科学会(ATS)/欧洲呼吸学会(ERS)/日本呼吸学会(JRS)/Asociación拉丁美洲(Latinoamericana de 188bet官网地址Tórax) (ALAT)标准诊断[17)从11个临床地点筛选抗col(V)抗体。34例为抗col(V) Ab+在这些患者中,有30名患者符合所有进入标准并被纳入研究。患者接受了三个剂量组的治疗:每天0.1、0.5和1.0 mg的IW001(牛col(V)口服溶液),持续24周。患者按顺序进入研究(剂量从低到高)。队列1的患者每天接受0.1 mg的IW001治疗。当这个低剂量队列的登记完成,并且所有队列1的患者都接受了≥30天的治疗时,队列2被登记。队列2的患者每天给予0.5 mg。当这个中剂量队列的登记完成并且所有队列2的患者治疗≥30天时,队列3被登记。队列3的患者每天给予1.0 mg。在研究报名时,第3和第6个月,患者接受了体格检查和肺功能研究。每个月采集血液进行生物标记。
试验设计。队列1的患者接受IW001治疗,每天口服0.1 mg,持续24周。当该队列登记完成且所有第1队列患者治疗≥30天时,第2队列被登记。第2队列患者口服IW001 0.5 mg /天,持续24周。当该队列登记完成且所有第2队列患者治疗≥30天时,第3队列被登记。第3队列患者口服IW001,每日1.0 mg,持续24周。Col(V): V型胶原;阿瑟:抗体。
本临床试验的主要纳入标准包括:年龄35-75岁(含);IPF (ATS/ERS/JRS/ALAT标准)诊断[17])在过去48个月内;用力肺活量(FVC)≥预测值的50%;肺对一氧化碳的扩散能力>为预测值的35%;抗col(V) IgG抗体阳性(Ab+).主要排除标准包括:使用全身皮质类固醇和/或免疫抑制剂;对牛类产品过敏;近期吸烟;任何活动性感染;不稳定心血管疾病;或任何可能干扰IW001吸收的情况。
抗col(V) Ab检测
使用专利流式细胞仪珠法在患者血浆中检测col(V)抗体(ImmuneWorks, Indianapolis, in, USA) [18].使用66名成年、不吸烟的正常志愿者的血清,根据免疫原性白皮书[19].
外周血生物标志物分析
C1q
ELISA法测定血清中C1q与抗col(V)抗体结合的数量。在96孔板中,将患者源性热灭活血清添加到4孔,涂有IW001 (col(V))。孵育和洗涤后,在两口井中加入一定量的C1q (Sigma-Aldrich, St Louis, MO, USA),其余井用缓冲液处理。在用辣根过氧化物酶共轭抗C1q检测Ab (MyBiosource, San Diego, CA, USA)检测后,用C1q处理过的孔的OD值减去未处理过C1q的孔的光密度(ODs),以确定C1q结合的变化。
基质金属蛋白酶7
使用Quantikine MMP7 ELISA试剂盒(R&D Systems, Minneapolis, MN, USA),根据制造商协议检测血浆基质金属蛋白酶(MMP)7水平。
血清白蛋白
血清白蛋白检测由Covance中心实验室(Indianapolis, IN, USA)使用模块化分析仪(Roche Diagnostics, Indianapolis, IN, USA)进行。在反应pH值下,溴甲酚紫选择性地与白蛋白结合。颜色的强度是用光度法测定的,它与白蛋白的总含量成正比。
统计分析
数据以平均值±表示扫描电镜除非另有说明。使用Prism软件(GraphPad software, Inc., La Jolla, CA, USA)进行统计分析。
在回归分析中使用了非参数检验,并且在比较0.1 mg / d组和1.0 mg / d组的结果时也使用了非参数检验。在所有情况下,p值<0.05被认为有统计学意义。1例患者被纳入高剂量组(每天1mg),其抗col(V) Ab结果后来被发现为阴性(实验室处理错误)。因此,该患者的数据被纳入安全性分析,但被排除在疗效分析之外。所有的患者都完成了研究,因此没有对丢失的数据进行处理。
结果
1期临床试验患者的人口统计及其与col(V) Ab状态的关系
85例筛查患者中34例(40%)为col(V) Ab+.在这些患者中,有30名患者入选表1显示基线患者人口统计数据。1例患者被纳入高剂量组(每天1mg),其抗col(V) Ab结果后来被发现为阴性(实验室操作错误)。因此,该患者的数据被包括在安全性分析中,但被排除在疗效分析之外。
IW001安全配置文件
试验的主要终点是安全性/耐受性。在11例患者中,共报告了26个被认为可能与IW001相关的不良事件。所有人都被评为轻度或中度。这些总结在表2.大多数不良事件是胃肠道紊乱,包括腹泻和软便。未观察到IPF的急性加重或住院。100%入选的患者完成了试验;没有患者因任何原因过早停用。
IW001对肺功能的影响
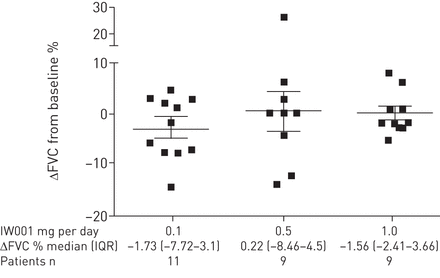
本一期临床试验的次要目标是确定肺功能的变化。结果显示,在IW001 (图2),计算为(24周时的植被覆盖度(升)-基线时的植被覆盖度(升)/基线时的植被覆盖度(升)。0.1 mg / d队列的患者表现为平均±扫描电镜24周治疗期间与基线相比的变化为- 2.75±1.87%。相比之下,每日剂量为0.5 mg组患者的平均变化为0.57±3.90%,最高药物剂量组(每日剂量为1.0 mg)患者的平均变化为0.33±1.44%。
IW001治疗24周后,与基线相比(Δ)用力肺活量(FVC)的变化表明肺功能下降的潜在缓解。采用IW001治疗24周后测量患者的fvc。与基线相比的百分比变化计算为ΔFVC=(24周时的植被覆盖率(升)-基线时的植被覆盖率(升))/基线时的植被覆盖率(升)。图中数据以均数±表示扫描电镜对于每个队列。IQR:四分位范围。
由于个别IPF患者可能经历肺功能的显著降低(通过肺活量测量),这可能会扭曲该组患者的平均变化,我们还对本试验中预测的个体肺活量%的变化进行了分类分析。在一项为期6个月的研究中,使用FVC %的绝对下降预测为5%作为中位生存时间减少的预测因子appalaet al。[20.],表3显示在最低药物剂量队列的11名患者中,有4名患者的FVC在24周内下降≥5%。相比之下,在中等剂量队列(每天0.5 mg)的9名患者中,只有2名患者出现了类似的FVC下降。在最高药物剂量队列(每日1.0 mg)中,没有患者的FVC下降≥5%。
IW001对生物标志物的影响
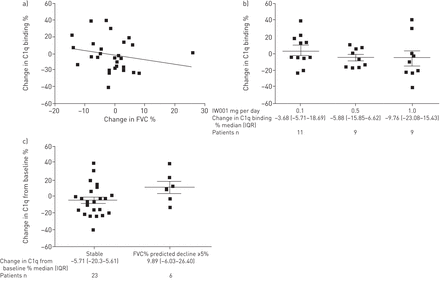
C1q被选为IW001免疫效果的生物标志物,因为C1q与抗col(V)抗体结合的减少表明IW001对潜在的抗col(V) Ab结合和活性的影响。评估C1q与抗col(V)抗体的结合,并与IW001治疗的反应相关。图3a表示C1q结合百分比变化与FVC结合百分比变化之间的相关性;图3b显示,每天接受0.1 mg IW001的患者,C1q与抗col(V)抗体的结合略有增加,而每天接受0.5 mg和1.0 mg IW001的患者,C1q结合呈剂量依赖性下降。
a)强迫肺活量(FVC)与基线相比百分比变化与C1q结合的相关性。在试验开始和IW001治疗24周后收集患者血液样本。治疗24周后,C1q结合到抗V型胶原蛋白(col(V))抗体的基线变化百分比与FVC基线变化百分比进行对比。与基线相比的百分比变化计算为(24周时的植被覆盖度(升)-基线时的植被覆盖度(升))/基线时的植被覆盖度(升),以及(24周时C1q OS -基线时C1q OD)/基线时C1q OD。n = 29个病人。斯皮尔曼非参数相关:r=−0.2729,p=0.1520。b) C1q与抗col(V)抗体结合。治疗24周后,患者热灭活血清中C1q结合抗col(V)抗体的基线变化百分比计算为(24周时的C1q OD -基线时的C1q OD)/基线时的C1q OD,并在每个队列中报告。图中数据以均数±表示扫描电镜对于每个队列。低剂量与高剂量的比较:曼-惠特尼非参数检验p=0.4033。c) FVC与C1q结合的相关性。在24周的治疗过程中,预测FVC %下降≥5%的患者(n=6)与治疗24周后C1q与抗col(V)抗体结合变化更稳定的FVC患者(n=23)进行比较。报告每组治疗24周后C1q结合到抗col(V)抗体的基线变化百分比,计算为24周时预测的FVC % -基线时预测的FVC %。图中数据以平均值±表示扫描电镜每一组。稳定患者与FVC %预测≥5%下降患者的比较:Mann-Whitney非参数检验p=0.071。OD:光密度;IQR:四分位范围。
我们分析了C1q结合对抗col(V)抗体的影响,这些患者来自所有三个队列,在IW001治疗过程中预测FVC %下降≥5%(绝对)(n=6),并将这些结果与显示稳定肺功能的患者(n=23)进行比较。24周后,与肺功能稳定且C1q结合活性在治疗过程中下降的患者相比,FVC明显降低的患者抗col(V)抗体的C1q结合水平更高(图3c)。
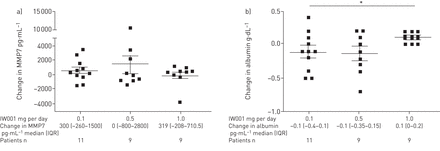
MMP7已被证明是一种可预测IPF进展的生物标志物[21- - - - - -23].在基线和第24周测定血浆MMP7水平。与基线相比,MMP7增加585.5±463.3 pg·mL−1在24周内每天摄入0.1毫克的队列中(图4a).相比之下,MMP7增加了1416±1252 pg·mL−1在每天0.5毫克的队列中在接受每日1.0 mg剂量的队列中,在相同的治疗期间,血清MMP7水平平均下降(−65.33±492.2 pg·mL)−1).
a)血浆基质金属蛋白酶(MMP)7水平。在试验开始和IW001治疗24周后采集血液样本。每个队列在治疗24周后报告血浆MMP7水平的绝对变化。图中数据以均数±表示扫描电镜对于每个队列。低剂量与高剂量的比较:Mann-Whitney非参数检验,p=0.8197。b)血清白蛋白水平。在试验开始和IW001治疗24周后采集血液样本。报告每个队列在治疗24周后血清白蛋白水平的绝对变化,并以24周时的白蛋白g·dL计算−1−基线白蛋白(g·dL)−1.图中数据以均数±表示扫描电镜对于每个队列。低剂量与高剂量的比较:Mann-Whitney非参数检验,p=0.0413。IQR:四分位范围。*: p < 0.05。
为了检验IW001对治疗患者整体健康状况的影响,测量了血清白蛋白水平,因为最近的研究表明IPF患者的死亡率与之呈负相关[22,24].在24周的治疗期间,接受IW001最低剂量(0.1 mg / d)的患者血清白蛋白水平下降,而在0.5 mg / d剂量时,血清白蛋白水平略有升高。相比之下,每日剂量为1.0 mg的患者血清白蛋白水平与队列1 (图4b)。
讨论
IW001 OIT在col(V) Ab中的6个月开放临床试验+IPF患者表现出一些有趣的观察结果。IPF患者中抗col(V)抗体的发生率约为40%。col(V) OIT在所有患者中都是安全且耐受性良好的,并且似乎导致了肺功能和循环MMP7水平稳定的剂量依赖性趋势,以及C1q与抗col(V)抗体结合的降低。最后,IW001诱导血清白蛋白的剂量依赖性增加,血清白蛋白水平的降低与IPF患者的生存率降低有关。
指规数影响美国和欧洲约50万人[25],其发病率似乎正在增加,正如多个国家通过登记处和其他流行病学工具报告的那样[6,26].这强调了需要有效的治疗,对老年患者的慢性使用是安全的;然而,这一目标仍然难以实现。肺移植虽然有时有效,但只适用于某些IPF患者[1].在IPF中改变凝血、炎症、氧化应激和成纤维细胞过度沉积细胞外基质的作用已在众多临床试验中得到验证。考虑到构成IPF的多种病理生理学,高靶向治疗可能不足以在疾病进展中产生可检测的差异[6].
Col(V)是一种小型胶原蛋白,通常隔离在肺间质内,因此对免疫系统隐藏。肺重塑是IPF的一个特征,导致col(V)暴露和过表达,这反过来又与抗col(V)免疫的发展有关,表明IPF的发病机制与自身免疫有关。具体来说,高达60%的IPF患者具有抗col(V)反应性t细胞[27正如目前的研究和Vittalet al。[10155例IPF患者中40%的>表现出特异性全身Ab反应。
到目前为止,在临床试验活动中缺乏的一种方法是测试改变的适应性免疫反应在调节这些患者的纤维化反应中可能很重要的可能性。因为我们的数据表明,≥40%的IPF患者对col(V)有持续的自身免疫反应,这种自身抗原可能不仅在这部分患者的疾病进展中起作用,而且表明通过治疗改变自身免疫反应可能会减少纤维化反应并稳定肺功能。其他自身抗体,包括热休克蛋白70抗体和抗肺抗原的自反应t细胞存在于80% IPF患者的血浆中[8,9].总的来说,这支持了对自身抗原的持续适应性免疫反应可能在抗col(V)抗体检测阳性的IPF患者的疾病进展中发挥重要作用的观点。
因为IgG同型结合C1q和激活补体级联的能力各不相同,在使用最高剂量IW001治疗的患者中看到的C1q结合减少表明这些患者的抗col(V)抗体池发生了变化。C1q的结合亲和力取决于抗体重链中的一个氨基酸序列[28].在目前的研究中观察到的C1q结合减少可能表明Ab的氨基酸序列发生了变化,导致一种对结合补体亲和力较低的Ab以及先前存在的抗col(V) Ab增加。C1q结合发生这种变化的其他可能性可能包括从补体结合抗体的选择性丢失到b细胞中发生的同型转换改变,这是一个值得进一步研究的话题。然而,治疗后抗col(V) Ab的降低并不能解释C1q结合降低的原因,因为在试验期间抗col(V) Ab水平基本保持不变,那些抗col(V) Ab升高的患者C1q结合下降最大(数据未显示)。此外,所有治疗组中均存在这四种IgG亚型。这种改变的结合机制是正在进行的研究的主题。
OIT通过给肠道注射自体抗原已被证明可抑制体液和细胞介导的免疫反应[29,30.].这可能是由于调节性t细胞(treg)的激活,treg通过阻断针对相同自身抗原激活的效应t细胞的反应来维持免疫自我耐受。在这项临床试验中,我们没有观察到treg (CD4+CD25+FoxP3+t细胞)(数据未显示)。然而,我们确实观察到在肺功能稳定、MMP7下降、血清白蛋白升高和C1q结合下降的最高剂量队列中抗col(V) Ab总体上升。有趣的是,推测在目前的研究中报道的IW001的有益作用可能与抑制抗体的诱导有关,抑制抗体可以阻止抗col(V) Ab免疫复合物介导的col(V)反应性t细胞的激活,这一机制已在花生OIT的成功试验中在ige抗原复合物中被调用[31].未来的试验将研究iw001诱导的OIT机制。
伤口愈合和组织重建也涉及到MMP7的产生,在IPF患者中,MMP7水平的升高与疾病严重程度的增加有关[23].因此,我们的数据显示,在接受最高测试剂量IW001的患者中,MMP7水平趋于稳定,以及较低的MMP7水平与24周治疗后稳定的FVC之间的相关性,支持IW001可能改变疾病病理和该疾病持续的纤维化反应的观点。值得注意的是,在0.5 mg队列中MMP7的增加主要是由一名患者驱动的,MMP7稳定的直接证据是队列3的第75百分位为710 pg·mL−1与1500 pg·毫升−1第一组。
血清白蛋白最近被报道与IPF患者的死亡率有关。具体来说,血清白蛋白的下降与这些患者死亡率的增加有关[22,24].虽然血清白蛋白可能不被认为是一种生物标志物,但这些最近的研究表明,与白蛋白增加或维持相关的治疗方法可能反映出IPF患者的有益效果。事实上,目前研究中的数据显示IW001诱导血清白蛋白的剂量依赖性效应,在试验结束时,最高队列显示白蛋白水平增加。同一队列显示了植被覆盖度和生物标志物的良好趋势。
当前研究的一个潜在局限性是缺乏指定的安慰剂组。然而,肺功能测试显示,服用最低剂量(每天0.1毫克)的患者显示出与两个主要IPF临床试验的安慰剂组相似的肺功能平均下降。事实上,在这些约165名患者的研究中,安慰剂组在第24周观察到的FVC分别下降了- 80.7 mL和- 92.1 mL [32,33],而我们的低剂量下降了- 85.4 mL。由于本试验为一期试验,因此纳入的患者总数可能较低,当单独检查时,每个终点可能具有有限的解释价值。然而,对数据的集体检查显示,所有终点都指向高剂量组(每天1毫克)患者的受益方向,包括所有生物标志物、血清白蛋白和肺功能的阳性趋势。
虽然这项研究的目的不是评估疾病进展或死亡率,但我们这些临床结果的一系列替代标记的集体变化表明,IW001治疗可以改变这些患者的疾病的基础生物学。未来的概念验证临床试验将在更多IPF患者中对IW001进行更长时间的测试,与安慰剂组相比,可能验证这种方法对IPF患者的一个重要子集是有效的治疗。更多的研究阐明了C1q结合和MMP7水平在IW001 IPF患者治疗过程中的作用,这可能会提高我们对如何保护这些患者肺功能的认识。
总之,这是第一个治疗IPF患者的前瞻性定义子集的临床试验,特别是那些抗col(V) Ab+,使用col(V)的OIT方法。IW001似乎是安全且耐受性良好的,显示出基于C1q与抗col(V) Ab结合减少的生物活性,并可能对基于FVC趋势的疾病进展产生有益影响。iw001对IPF患者的治疗效果有待进一步的col(V) OIT研究。
确认
感谢CreateWrite公司(印第安纳波利斯,IN, USA)的Lana Christian提供的专业写作和编辑帮助,以及B2S咨询公司(印第安纳波利斯,IN, USA)的Rocco Brunelle提供的统计方面的专业帮助。这项研究是由其他临床试验研究人员的努力促成的:Michael Busk, Mark Farber(印第安纳大学医学院,印第安纳波利斯,美国),Mary Strek(芝加哥大学医学院,芝加哥,伊利诺斯州,美国),James Allen(俄亥俄州立大学医学院,哥伦布,OH,美国),Jesse Roman(路易斯维尔大学医学院,路易斯维尔,肯塔基州,美国),Steven Sahn(南卡罗莱纳医科大学,查尔斯顿,南卡罗来纳州,美国),Joao de Andrade(阿拉巴马大学伯明翰医学院,伯明翰,美国),Yolanda Mageto(佛蒙特大学,伯林顿,佛蒙特,美国),Marilyn Glassberg(迈阿密大学医学院,迈阿密,佛罗里达州,美国),Lisa Lancaster(范德比尔特大学医学院,纳什维尔,田纳西州,美国)和Sean Studer(纽瓦克贝斯以色列医学中心,纽瓦克,美国新泽西州)。
脚注
编辑评论见欧元呼吸2015;45: 1218-1220 [10.1183/09031936.00237114].
支持声明:本研究由ImmuneWorks, Inc. (Indianapolis, IN, USA)资助。
临床试验:本研究注册于www.clinicaltrials.gov带有标识符号NCT00873860.
利益冲突:可以在本文的在线版本中找到相关信息www.qdcxjkg.com
- 收到了2014年6月10日。
- 接受2014年10月31日。
- 版权所有©ERS 2015