文摘
特发性肺纤维化(IPF)是一种肺衰老相关疾病的特点是myofibroblast人口的扩张和异常肺改造。脱氢表雄酮(DHEA)、类固醇pro-hormone随年龄而夸张的下降与慢性退行性疾病有关。
我们量化脱氢表雄酮的血浆水平及其硫酸盐形式(硫酸脱氢表雄酮(DHEA - s)在137年IPF患者和58控制和检查脱氢表雄酮对人体肺成纤维细胞的影响。
等离子体脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s显著降低男性IPF患者(中位数(范围)脱氢表雄酮:4.4 (0.2 - -29.2)与6.7 (2.1 - -15.2)ng·毫升−1(p < 0.01);硫酸脱氢表雄酮(dhea - s: 47 (15.0 -211)与85.2(37.6 - -247.0)μg·dL−1,p < 0.001),而女性只有硫酸脱氢表雄酮(dhea - s显著下降(32.6 (15.0 - -303.0)与68.3(16.4 -171)μg·dL−1,p < 0.001)。脱氢表雄酮引起的纤维母细胞增殖减少和增加大约1/2成纤维细胞凋亡,可能通过激活caspase-9内在途径。这种效果是伴随着upregulation几个pro-apoptotic蛋白质(伯灵顿和细胞周期蛋白依赖性激酶抑制剂CDNK1A)的差别,对这些基因的抗凋亡蛋白,如细胞凋亡的细胞抑制剂(c-IAP) 1和c-IAP2。脱氢表雄酮也明显降低转换引起的增长factor-β1-induced胶原蛋白生产和纤维母细胞myofibroblast分化,以及抑制血小板源生长因素成纤维细胞迁移。
这些发现表明脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s的不成比例的减少IPF患者和表明这个分子有多个antifibrotic属性。
文摘
脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s是IPF患者异常下降,这肾上腺类固醇有很强的antifibrotic效果在体外http://ow.ly/nD9sz
介绍
特发性肺纤维化(IPF)是一种原因不明的慢性肺病导致进步的和不可逆转的破坏肺架构(1,2]。这种疾病令人沮丧的预测,平均生存∼诊断(2 - 3年之后3]。IPF患者通常是50 - 70岁和疾病的频率随着年龄的增加显著(4]。一些研究表明,至少在某种程度上,相关的老化协会可以加速缩短的端粒5]。然而,连接老化和IPF的机制在很大程度上是未知的(1,6]。
脱氢表雄酮(DHEA)及其硫酸酯(硫酸脱氢表雄酮(DHEA - s)是人类最丰富的肾上腺类固醇(7]。血液脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s水平达到一个高峰年龄在25和30年,此后逐渐下降,因此,60岁,只有10 - 20%浓度的相应值在年轻的成年人7]。
异常减少脱氢表雄酮与免疫衰老有关,与衰老发生的免疫系统下降(8),以及一些慢性疾病也与老年人有关,如。胰岛素抵抗、动脉粥样硬化、系统性动脉高血压和干燥综合征(9- - - - - -11]。因此,脱氢表雄酮已被建议作为一个ageing-protective分子。
在这项研究中,我们分析了等离子体和支气管肺泡灌洗(BAL)的脱氢表雄酮水平和硫酸脱氢表雄酮(DHEA - s IPF患者和年龄组。我们进一步研究了脱氢表雄酮能否影响扩散,迁移和人类肺成纤维细胞的细胞凋亡,以及成纤维细胞的分化myofibroblasts和胶原蛋白合成。我们的结果表明,脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s是IPF患者异常下降,这个肾上腺类固醇antifibrotic带来很大的影响在体外。
材料和方法
研究人群
血浆样本从137年连续获得IPF患者,87男性和女性(64.1±9.9岁)诊断呼吸疾病研究所(内心),墨西哥城,墨西哥,和从58岁,sex-matched控制。男性和28女性健康的捐赠者,30(56.5±4.6岁)参加人员的内心的和从我们的戒烟计划,根据他们愿意参与这项研究。内心的生物伦理委员会批准了这项协议,并签署同意了从病人和控制。
拜尔港进行了如前所述[12)在三个控制捐助者(58±7.7岁)和12 IPF患者(62.8±4.6岁),所有男性。
对照组进行了简要病史排除其他疾病,如糖尿病、心血管疾病、内分泌疾病或癌症。也证实了IPF的诊断根据美国胸科学会/欧洲呼吸学会指南(188bet官网地址2]。
脱氢表雄酮/硫酸脱氢表雄酮(DHEA - s分析
等离子体和落下帷幕的脱氢表雄酮水平是衡量使用固相125年我未及(脱氢表雄酮RIA DSL 9000;西门子医疗解决方案诊断,洛杉矶,美国CA)和由化学发光测定硫酸脱氢表雄酮(DHEA - s(脱氢表雄酮SC化学发光LKDS-1;西门子医疗诊断解决方案)。
细胞培养
人类正常的肺成纤维细胞,CCD25-Lu从美国获得的文化集合类型。肺成纤维细胞原代细胞从正常和IPF行了描述(13]。CCD25-Lu细胞系在DMEM培养,而主要是在火腿F-12培养基培养他们补充10%胎牛血清,100 U mL−1青霉素和100μg·毫升−1链霉素。细胞培养是维持在37°C调湿大气中5%的二氧化碳。通过台盼蓝排斥细胞生存能力评估。
生长速率测定
手机号进行四唑比色WST1化验(罗氏,曼海姆,德国),所述[13]。成纤维细胞被镀成96孔酶标(10 000个细胞·厘米−2)和培养有或没有脱氢表雄酮的浓度50,100年和200年μM 24、48和72 h。在实验结束时,介质被新的取代介质包含WST1解决方案和吸光度分析ELISA板读者(Sinergy HT、BioTek Winooski, VT,美国)。脱氢表雄酮对增长率的影响被表示为一个百分比的控制。之前使用这些脱氢表雄酮浓度(14- - - - - -16]。
溴脱氧尿苷掺入
细胞被播种密度的000厘米−2在96 -微型板块,可以附加在一夜之间和治疗有或没有脱氢表雄酮(50,100年和200年μM) 24和48 h。纤维母细胞增殖是评估通过分析5′-bromo-2′脱氧尿苷(BrdU)并入新合成DNA使用细胞增殖ELISA(罗氏)[17]。光密度测量使用ELISA板读者(Sinergy HT BioTek)在450/595 nm。扩散被表示为一个百分比的控制。
细胞凋亡检测
凋亡的检查是通过流式细胞术使用双重染色法和异硫氰酸荧光素(FITC)共轭膜联蛋白V和propidium碘(膜联蛋白染色设备;美国BD生物科学,圣何塞,CA)根据制造商的指示,如前所述[18]。简单地说,1×106膜联蛋白的细胞在100年μL缓冲区是沾propidium碘染色解决方案和膜联蛋白V-FITC染色方案。细胞培养在黑暗中在室温下15分钟和数据获得使用FACSAria流式细胞分析仪(美国正欲,圣何塞,CA)。数据分析使用FlowJo 8.7软件(树明星,Inc .)、亚什兰,美国)。
半胱天冬酶的活动
成纤维细胞细胞溶解在半胱天冬酶缓冲(10毫米Tris-HCl, 10毫米不2阿宝4,130毫米氯化钠,1% (v / v)特里同x - 100)。蛋白质浓度由布拉德福德评估方法和半胱天冬酶活动化验使用荧光方法如前所报道(19),在一个发光光谱仪(Sinergy HT BioTek) 380/430 - 460 nm。乙酰基四肽耦合4-methycoumaryl-7-amide被用作基质:Ac-DEVD-AMC (caspase-3/7/8)和Ac-LEHD-AMC (caspase-9) (PeptaNova GmdH, Sandhausen,德国)。结果表示为单位的荧光的变化(UF)·分钟−1·毫克−1蛋白底物后解理。
人类细胞凋亡抗体阵列
35 apoptosis-related蛋白质表达谱的测量使用一系列人类细胞凋亡工具包(蛋白质组分析器数组ARY009;研发系统,明尼阿波利斯,美国制造商的指示所述后(20.]。说点像素被测密度术量化。数据被表示为叠化和武断地认为是生物重要变化> 30%。
迁移分析
纤维母细胞迁移是化验使用24-well collagen-coated Boyden钱伯斯(Chemicon,微孔,贝德福德,妈,美国)与一个8-μm孔隙大小描述(21]。细胞(2×105)被播种在参议院和脱氢表雄酮(100μM),血小板源生长因子(PDGF) ng·25毫升−1(研发系统)或者两者都添加了含0.5毫升的众议院中有5%牛血清白蛋白(BSA)。孵化后8 h迁移细胞被量化根据制造商的指示。
西方墨点法
成纤维细胞是细胞溶解里帕缓冲区(西格玛奥德里奇,圣路易斯,密苏里州,美国)包含多个蛋白酶抑制剂(Calbiochem,默克公司,达姆施塔特,德国)。样品的蛋白质(40μg)分离10% sds - page电泳,转移到硝化纤维素膜(生物Rad,赫拉克勒斯、钙、美国)和标准协议后阻塞。一夜之间,膜被孵化在4°C主要抗体:α-smooth肌肉肌动蛋白(SMA) (1:50 0;西格玛奥德里奇),caspase-9 (1:50 0;Abcam、剑桥、马、美国)和β-tubulin (1:50 0;圣克鲁斯生物技术有限公司、达拉斯、TX,美国)。孵化与二次抗体结合辣根过氧化物酶(anti-mouse和anti-rabbit免疫球蛋白;英杰公司生活技术,大岛屿,美国纽约)进行1 h在室温和信号呈现与西方超级信号Pico增强化学发光检测系统(美国热科学,罗克福德,IL)。信号是对β-tubulin正常化。
免疫荧光
成纤维细胞是镀在盖玻片和无血清培养基培养48 h单独或包含100μM脱氢表雄酮,ng·5毫升−1转化生长因子(TGF) -β1或两者兼而有之。细胞被固定丙酮/甲醇在4°C, permeabilised Triton x - 100和0.5%孵化与人类单克隆抗体(西格玛奥德里奇)α-SMA一夜之间在4°C调湿室。细胞治疗一个affinity-purified山羊anti-mouse免疫球蛋白DyLight 549 (Biocare医疗、和谐、钙、美国)1 h在湿润在室温下室。幻灯片与4,复染色6-diamidino-2-phenylindole (DAPI)安装介质(圣克鲁斯生物技术有限公司)。
胶原蛋白测定
成纤维细胞被播种到25厘米2培养瓶和无血清培养系统,直到70%融合和刺激与脱氢表雄酮(100μM), TGF-β1 ng(5毫升−1)或两个48 h。上层清液渗出,lyophilised resuspended 100μL的体积。胶原蛋白浓度是由比色Sircol可溶性胶原蛋白测定(英国Carrickfergus Biocolor有限公司)根据制造商的指示22]。光密度测量在555 nm使用ELISA板读者(Sinergy HT BioTek)。胶原蛋白浓度表示为相对于控制。
统计分析
等离子体水平结果不是正态分布和对数转换的统计分析。自学习小组没有遵循正态分布,我们使用非参数方法的描述性统计(中值和范围)和统计分析(Mann-Whitney紫外线测试)。在体外数据给出均值±sd。差异是由单向方差分析或Wilcoxon测试评估。p < 0.05被认为是显著的。数据分析使用统计软件SPSS对Windows, 14.0版本(美国SPSS Inc .,芝加哥,IL)。
结果
脱氢表雄酮、硫酸脱氢表雄酮(DHEA - s IPF患者减少
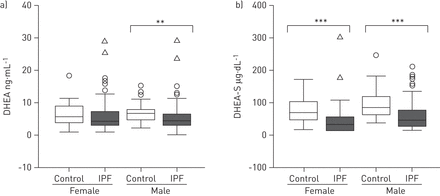
等离子体脱氢表雄酮和硫酸脱氢表雄酮(DHEA - s水平测量通过放射免疫检定法和化学发光分析,分别在137年IPF患者和58控制。见图1分子都显著降低男性IPF患者(中位数(范围)脱氢表雄酮:4.4 (0.2 - -29.2)与6.7 (2.1 - -15.2)ng·毫升−1(p < 0.01);硫酸脱氢表雄酮(dhea - s: 47 (15.0 -211)与85.2(37.6 - -247.0)μg·dL−1,p < 0.001),而女性只有硫酸脱氢表雄酮(dhea - s显著下降(32.6 (15.0 - -303.0)与68.3(16.4 -171)μg·dL−1,p < 0.001)。脱氢表雄酮女性显示无意义的倾向于减少(4.3 (0.9 - -28.9)与5.7 (0.98 - -18.3)ng·毫升−1,p = 0.2)。
硫酸脱氢表雄酮(硫酸脱氢表雄酮(dhea - s)是减少患者的特发性肺纤维化(IPF)。等离子体的水平)脱氢表雄酮(DHEA)和b)考察了硫酸脱氢表雄酮(DHEA - s放射免疫检定法和化学发光分析在男性和女性健康的捐赠者和IPF患者。在每个箱子代表值和框第25和第75百分位数。胡须代表5和95百分位数。开放的三角形和圆形代表异常值。* *:p < 0.01;* * *:p < 0.001。
硫酸脱氢表雄酮(dhea - s浓度也显著减少BAL样本IPF患者(2.31±0.61与1.37±0.14μg·dL−1;p < 0.01)。没有观察脱氢表雄酮水平差异。
没有临床和功能参数之间的相关性被发现(如。用力肺活量)和脱氢表雄酮、硫酸脱氢表雄酮(DHEA - s等离子体浓度(数据没有显示)。
脱氢表雄酮减少肺成纤维细胞增殖
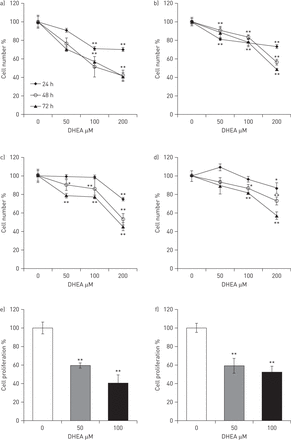
细胞生长是量化的WST1扩散试验CCD25-Lu正常细胞系以及在三个主要的细胞系,一个来自正常的肺和两个从IPF肺。基底条件下没有观察到的增长率的差异之间的IPF和控制成纤维细胞(152±10%与157±7%,48小时和214.0±2.99%与200.4±10.1%在72 h)所示图2脱氢表雄酮治疗造成的剂量和时间降低细胞生长。一般来说,这种影响是显著和脱氢表雄酮浓度≥50μM后48 h。脱氢表雄酮对人体肺成纤维细胞增殖的抑制作用是证实了通过测量BrdU并入DNA (图2 e和f)。在正常和IPF成纤维细胞,脱氢表雄酮导致细胞增殖明显降低浓度从50μM。
脱氢表雄酮(DHEA)降低增长速度和扩散在正常和特发性肺纤维化(IPF)的人类肺成纤维细胞。增长率是衡量WST1试验在两个正常(a和b)和两个IPF (c和d)人类肺纤维母细胞细胞系在24日,48和72 h脱氢表雄酮浓度增加的缺失或存在(50,100年和200年μM)。细胞增殖以5′-bromo-2′脱氧尿苷(BrdU)并入DNA在e) 24小时正常和f)没有IPF成纤维细胞系或存在浓度增加脱氢表雄酮(50和100μM)。数据表示为±sd从三个独立的实验。*:p < 0.05;* *:p < 0.01。
脱氢表雄酮肺成纤维细胞发生凋亡
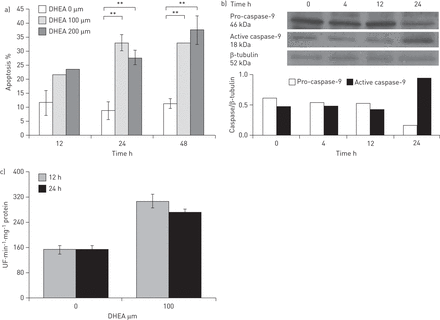
脱氢表雄酮对细胞死亡的影响被研究了100年和200年的使用浓度μM。检测细胞凋亡早期,DHEA-treated和控制成纤维细胞化验易位的磷脂酰丝氨酸从内到外质膜的传单使用膜联蛋白V绑定化验。所示图3一,文化在24和48 h脱氢表雄酮浓度引起成纤维细胞凋亡显著增加。检查是否脱氢表雄酮诱导细胞凋亡的外在或内在途径我们评估caspase-8 caspase-9免疫印迹。与100年刺激μM脱氢表雄酮诱导增加活性caspase-9肺成纤维细胞在24小时(图3 b)。激活pro-caspase-9证实了氟量计(图3 c)。没有观察到变化与pro-caspase-8(数据没有显示)。我们检查是否脱氢表雄酮诱导细胞凋亡在IPF成纤维细胞和如果是caspase-9抑制的影响。我们发现基底细胞凋亡(2.8±1.3%)增加到6.1±0.6%当细胞受到100μM脱氢表雄酮(p < 0.05)。Caspase-9抑制剂减毒DHEA-induced纤维母细胞凋亡(3.6±0.3%;p < 0.05)。
脱氢表雄酮(DHEA)人类肺成纤维细胞的凋亡。CCD25-Lu)正常成纤维细胞系孵化12、24和48 h在没有或存在浓度增加脱氢表雄酮(100年和200年μM)胎牛血清中补充。细胞凋亡和坏死被fluorescence-activated量化细胞分选仪使用荧光素isothiocyanate-conjugated膜联蛋白V和propidium碘,分别。细胞凋亡水平表示为收购事件的总数的百分比在至少三个独立的实验。数据表示为±sd。* *:p < 0.01。b)代表pro-caspase-9免疫印迹分析和主动caspase-9表达总溶解产物从正常的人类获得CCD25-Lu肺成纤维细胞系。成纤维细胞暴露在100年μM脱氢表雄酮为0,4、12和24小时,β-tubulin作为加载控制正常化光密度分析。c) Caspase-9活动也由荧光化验方法使用Ac-LEHD-AMC作为底物在正常细胞溶解产物暴露12和24小时中有或没有100μM脱氢表雄酮。数据表示为±sd从三个独立的实验。超滤:单位的荧光。
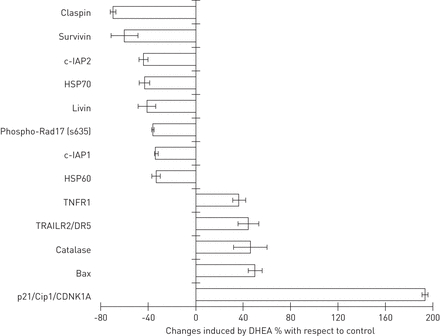
进一步探讨凋亡/ anti-apototic蛋白可能参与DHEA-induced细胞死亡,我们用人类细胞凋亡抗体阵列(图4)。我们的结果表明,脱氢表雄酮增加一些凋亡受体,如肿瘤坏死因子受体1 (TNFR1)(36.5±5.2%)和TRAILR2 (43.9±8.7%)。增加的水平pro-apoptotic标记伯灵顿(49.7±6%)和细胞周期蛋白依赖性激酶抑制剂的CDNK1A (p21 / Cip1 / CDNK1A),抑制细胞周期进展(23),也被检测到。此外,脱氢表雄酮诱导的水平减少几个抗凋亡蛋白,如细胞凋亡的细胞抑制剂c-IAP1 (34±1.5%), c-IAP2(44.4±3.7%),生存素(60.5±11%),claspin(70±2.2%)和推荐(41.6±7%)。
影响脱氢表雄酮(DHEA)蛋白参与细胞凋亡。35 apoptosis-related蛋白质表达谱的测量使用一系列人类细胞凋亡工具包中描述的方法。正常成纤维细胞CCD25-Lu治疗有或没有100μM脱氢表雄酮24 h抗体和细胞溶解产物被用于数组。数据表示为百分数变化±sd对未经处理的控制。数据显示这些蛋白质变化> 30%是观察到的地方。c-IAP:细胞凋亡抑制剂;HSP:热休克蛋白;TNFR1:肿瘤坏死因子(TNF)受体1;TRAILR2: TNF-related凋亡诱导配体受体2;CDNK:细胞周期蛋白依赖性激酶抑制剂。
脱氢表雄酮抑制PDGF-induced肺成纤维细胞的迁移
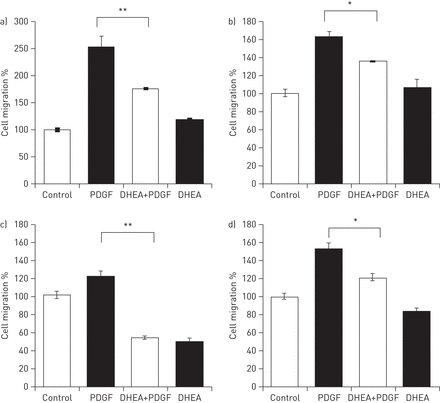
脱氢表雄酮对细胞迁移的影响被研究了在两个正常使用collagen-coated Boyden钱伯斯(图5 a和b)和两个IPF (图5 c和d)纤维母细胞细胞系。细胞迁移的数量仅在介质的存在加上5% BSA作为控制,而PDGF的纤维母细胞化学引诱物,用作积极控制。所示图5,PDGF-induced纤维母细胞迁移被脱氢表雄酮显著降低正常的人类肺和IPF的成纤维细胞。约30 - 70%的PDGF-BB-induced纤维母细胞迁移是被100年μM脱氢表雄酮。
脱氢表雄酮(DHEA)抑制血小板源生长因子(PDGF)全身的肺成纤维细胞的迁移。细胞迁移试验在正常执行(a和b)和特发性肺纤维化(c和d)肺成纤维细胞孵化8 h 100年缺席(控制)或存在μM脱氢表雄酮和/或ng·25毫升−1PDGF-BB collagen-covered Boyden室中描述的方法。数据表示为±sd从三个独立的实验。*:p < 0.05;* *:p < 0.01。
脱氢表雄酮抑制TGF-β1-induced myofibroblast分化成纤维细胞
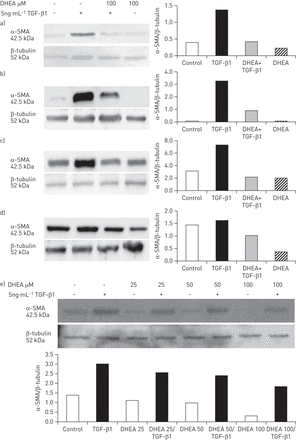
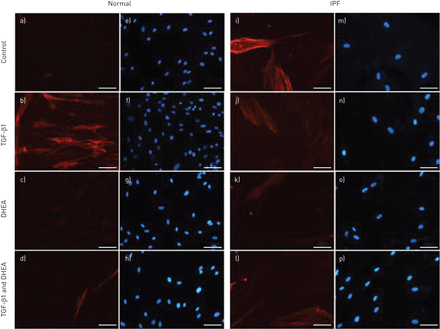
脱氢表雄酮在α-SMA的表达的影响,myofibroblasts的标志,使用两种不同的方法被免疫印迹检测。同时在第一种方法中,成纤维细胞培养48 h TGF-β1和脱氢表雄酮。作为例证图6100μM脱氢表雄酮浓度诱导强烈减少TGF-β1-inducedα-SMA正常(图6 a和b)和IPF (图6 c和d成纤维细胞。在第二个方法中,第一次刺激成纤维细胞TGF-β1 48 h,然后用脱氢表雄酮治疗额外48 h,而不删除生长因子。所示图6 e观察,一个抑制作用与100年μM脱氢表雄酮在正常的人类肺成纤维细胞。纤维母细胞的衰减myofibroblast分化脱氢表雄酮是证实了免疫荧光,在正常的肺成纤维细胞(图7 a -)和IPF成纤维细胞(图7 i p)。
脱氢表雄酮(DHEA) myofibroblast分化诱导的抑制纤维母细胞转化生长因子(TGF) -β1。代表西方滴α-smooth肌肉肌动蛋白(α-SMA)总溶解产物的成纤维细胞暴露于ng·5毫升−1TGF-β1和/或在胎牛血清脱氢表雄酮补充中48 h。正常(a和b)和特发性肺纤维化成纤维细胞(c和d)与TGF-β1同时刺激和100年μM脱氢表雄酮。光密度分析,每个实验都是包含在右边的面板。脱氢表雄酮引起的2到4倍减少TGF-β1诱导α-SMA表达(p < 0.05)。e)正常成纤维细胞被刺激TGF-β1 48 h脱氢表雄酮浓度增加和随后(25、50和100μM)额外的段没有删除TGF-β1 48 h。β-tubulin内容被用作加载控制正常化。
脱氢表雄酮(DHEA)抑制α-smooth肌肉引起的肌动蛋白(α-SMA)表达式转化生长因子(TGF) -β1在正常(a)和特发性肺纤维化(IPF) (i p)肺成纤维细胞。代表免疫荧光染色α-SMA从人类正常(模拟)和IPF(我)成纤维细胞刺激有或没有ng·5毫升−1TGF-β1和/或100μM脱氢表雄酮48 h。同时染色用4核,6-diamidino-2-phenylindole (DAPI)也是蓝色(超高频、mp)所示。酒吧= 40μm规模。
脱氢表雄酮减少TGF-β1-induced胶原蛋白的生产
调查是否脱氢表雄酮对胶原合成的影响,人类的肺成纤维细胞与TGF-β1刺激和胶原蛋白在细胞培养上清液测定。所示图8胶原蛋白生产增加2 -和3倍刺激与TGF-β1 Sircol试验评估。这种效应被脱氢表雄酮显著降低100μM在正常的人类肺成纤维细胞(图8 a和b;p < 0.01)和IPF-derived成纤维细胞(图8 c和d;p≤0.05)。
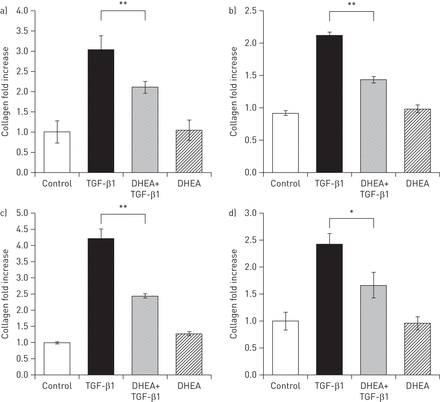
脱氢表雄酮(DHEA)降低转化生长因子(TGF) -β1-induced胶原蛋白的生产。正常(a和b)和特发性肺纤维化(c和d)肺成纤维细胞治疗有或没有ng·5毫升−1TGF-β1和/或100μM脱氢表雄酮48 h。胶原蛋白浓度条件媒体被Sircol胶原蛋白可溶性分析量化。数据表示为±sd从三个独立的实验。*:p≤0.05;* *:p < 0.01。
讨论
IPF累进,通常是致命的肺部疾病主要发生在老年人中的原因不明的1,4,6]。然而,链接与IPF老化的机制,仍然难以捉摸,虽然加速缩短端粒可能影响肺泡上皮细胞再生,似乎和表观遗传过程,提出了妥协的上皮细胞和成纤维细胞(1,5,6,24]。
脱氢表雄酮、硫酸脱氢表雄酮(DHEA - s合成pro-hormones人体肾上腺皮质分泌的。硫酸脱氢表雄酮(DHEA - s是亲水的存储形式,循环血液中,证据表明,亲脂性的脱氢表雄酮的形式转化细胞雄激素和雌激素。循环脱氢表雄酮的浓度和硫酸脱氢表雄酮(DHEA - s在成年后逐渐下降,这在60 - 70岁的水平只有10 - 20%的年轻人中发现。
降低循环水平已经与炎症的发病率和恶性过程(25,26]。因此,血液硫酸脱氢表雄酮(dhea - s水平独立发现和反向与免疫衰老有关,自身免疫性疾病,非酒精性脂肪肝,胰岛素抵抗、动脉粥样硬化和系统性动脉高血压(8- - - - - -11,27]。证据表明,低水平的硫酸脱氢表雄酮(dhea - s预测因各种原因死亡,心血管疾病和缺血性心脏病在年长的男性28]。此外,它最近表明,长期脱氢表雄酮替换可能会降低胰岛素抵抗和改善葡萄糖耐量老年人,超重或肥胖的女性和男性与糖耐量异常(29日]。
在我们的研究中我们发现,据我们所知,第一次IPF患者有一个不成比例的减少硫酸脱氢表雄酮(dhea - s相比同年龄组的循环水平。研究其他纤维化疾病很少,虽然更高级的非酒精脂肪肝,显示的存在严重纤维化,也与低水平的循环硫酸脱氢表雄酮(dhea - s[密切相关26,30.]。然而,与公认的保护相关的潜在机制,antifibrotic脱氢表雄酮的作用是未知的。
在这种情况下,重要的是要强调,研究处理脱氢表雄酮对其影响机制,主要是在成纤维细胞、稀缺和展示了矛盾的结果。例如,关于胶原蛋白的合成,据报道,脱氢表雄酮诱导适度增加在皮肤成纤维细胞胶原基因表达,但没有对胶原蛋白合成的影响31日]。相比之下,类似于我们的结果,脱氢表雄酮治疗导致明显降低的胶原I型信使rna和蛋白质合成的胶原I型心脏成纤维细胞(32]。
关于细胞凋亡,在文献中也相互矛盾的结果。因此,尽管据报道,脱氢表雄酮对细胞凋亡有保护作用在人类角质细胞和神经元中被永久地传颂33,34),在其他细胞类型,如人类肝癌细胞和肺动脉平滑肌细胞,脱氢表雄酮诱导细胞凋亡(15,35]。因此,很可能脱氢表雄酮的细胞反应是相关的细胞类型和/或细胞组织起源。
在目前的研究中,我们评估了脱氢表雄酮对一些重要的影响肺纤维发生的过程,包括迁移、增殖、凋亡和由人类肺成纤维细胞胶原合成,以及纤维母细胞myofibroblast分化。脱氢表雄酮使用因为硫酸脱氢表雄酮(DHEA - s是亲水的循环血液中的存储形式,而脱氢表雄酮是函数形式和类固醇激素合成中使用的主要形式。由于这个原因,尽管硫酸脱氢表雄酮(DHEA - s形式通常发现减少血液不同的慢性疾病相关的老化的研究,这是用于脱氢表雄酮在体外或在活的有机体内实验(36]。
成纤维细胞迁移到受伤的地区应对化学引诱物的信号分子,及其随后的扩张病变,是两个重要的profibrotic机制。在这种背景下,我们的结果表明,脱氢表雄酮是一种有效的抑制剂的PDGF-induced通过1型胶原基质成纤维细胞迁移以及成纤维细胞增殖,尽管具体途径,促进这些活动仍有待确定。
IPF的肺成纤维细胞的疫源地,成纤维细胞进行表型变化与后续myofibroblasts upregulation细胞外基质的大分子(1]。这个过程中起着关键的纤维发生的角色在这个疾病myofibroblasts持续和导致病理性瘢痕的形成。在这方面,我们发现TGF-β1-induced myofibroblast分化成纤维细胞,通过α-SMA表达的评估,由脱氢表雄酮显著降低剂量依赖性的方式。衰减的myofibroblast分化也在IPF-derived成纤维细胞免疫荧光观察到。
纤维化疾病(IPF的特点是纤维胶原沉积增加,我们认为脱氢表雄酮会抑制肺成纤维细胞胶原合成。并联myofibroblast分化的抑制作用,我们发现脱氢表雄酮压抑TGF-β1-induced胶原蛋白合成。
成纤维细胞的原因和myofibroblasts坚持IPF成纤维细胞的焦点和抗细胞凋亡尚不清楚。TGF-β1起着重要的作用,促进两个myofibroblast prosurvival信号通路,粘着斑激酶和蛋白激酶B (37,38]。因此,我们下一个检查脱氢表雄酮的影响成纤维细胞细胞死亡。使用fluorescence-activated细胞分选仪分析量化细胞凋亡的程度,我们发现脱氢表雄酮促进纤维母细胞的细胞死亡,时间的方式。重要的是,我们的研究结果还表明,脱氢表雄酮治疗导致激活caspase-9,表明脱氢表雄酮激活细胞凋亡的内在途径。进展的内在途径导致线粒体细胞色素C的释放到胞质,诱导apoptosome procaspase-9激活的形成,进而劈开,从而激活,下游效应还存在39- - - - - -41]。确定其他分子可能参与DHEA-induced pro-apoptotic精细平衡和抗凋亡的变化因素,我们采用人类细胞凋亡抗体阵列。这个数组允许半定量分析的变化发生在关键的细胞凋亡和检查点通路蛋白。相当重要的抗凋亡蛋白(c-IAP1 c-IAP2,生存素,claspin)表达下调,进一步支持证据表明内在凋亡通路被激活,而增加的死亡受体(TNFR1和TRAILR2)表明内在和外在凋亡通路之间的串扰。
所有这些发现正常和IPF成纤维细胞提供了强有力的证据表明脱氢表雄酮对fibroproliferative疾病可以作为一种antifibrotic化合物,包括,但不限于,肺纤维化,尽管这些不同的细胞内机制参与生物效应需要探索。
在这种情况下,重要的是要强调的细胞受体和胞内信号通路脱氢表雄酮对其影响目前不清楚。此外,由于脱氢表雄酮是一种多功能类固醇广泛的生物效应,分子机制可能不同。虽然脱氢表雄酮结合膜相关蛋白已经证明,明确证据DHEA-specific膜受体包括隔离和测序的基因缺乏所谓的受体(42]。有人提出脱氢表雄酮可能通过雌激素/雄激素受体发挥其影响。然而,其他研究已经表明,脱氢表雄酮在增殖和凋亡的影响是独立的两种受体(43,44),而一些研究涉及一个受体可能与g蛋白(42,43]。在过去的十年,一系列的孤儿受体,即过氧物酶体扩散激活受体,孕烷X受体和本构androstanol受体,已报告,有证据表明脱氢表雄酮(或其代谢物)绑定到或激活这些新特征受体(36]。
相关信号通路,表明脱氢表雄酮影响细胞周期阻断磷脂酰肌醇3-kinase通路(15]。也有证据表明,脱氢表雄酮负调节增殖作用的蛋白激酶(MAPK)通路在人类,通过小说MAPK磷酸酶,抑制p38-MAPK级联(45]。此外,在肺动脉高压的实验模型,脱氢表雄酮预防激活RhoA-ROCK(ρ激酶)信号通路,尽管细胞目标不确定46]。
总之,我们的研究结果表明,循环的脱氢表雄酮水平/硫酸脱氢表雄酮(DHEA - s是IPF下降,表明脱氢表雄酮对成纤维细胞表现出强烈的antifibrotic影响,影响迁移,增殖,分化myofibroblasts,胶原蛋白合成和生存。这些发现可能开辟新的治疗选择这种破坏性的肺部疾病。
脚注
支持声明:这部分支持的工作Conacyt格兰特干杯- 2009 - 01 - 113590。
利益冲突:没有宣布。
- 收到了2012年2月14日。
- 接受2012年10月11日。
- ©2013人队