抽象的
肺动脉高压(PAH)患者在低肺容量时可能表现出呼气流量减少,这可能会促进运动诱导的动态高充气(DH)。本研究旨在研究潜在的运动相关DH对进行症状限制增量心肺循环运动试验(CPET)的PAH患者呼吸困难强度的影响。
25名年轻(年龄均值±SD.38±12岁)无肺功能障碍的非吸烟PAH患者和10名年龄匹配的非吸烟健康受试者在耐受限度内进行CPET。通过CPET评估呼吸模式、操作肺容积(来自吸气容量(IC)测量)和呼吸困难强度(Borg量表)。
IC减少(IE。DH)在PAH患者(平均0.15L)中逐渐整个CPET,而它在所有健康受试者中增加(0.45L)。在PAH患者中,15名(60%)在整个运动中表现出IC的降低(平均0.50升),而在剩余的10(40%)患者中,IC增加(平均为0.36L)。PAH患者的呼吸困难强度和通风更大,而不是CPET任何阶段的对照,而吸气储备体积较低。
我们得出结论,这些年轻的非莫斯莫治疗患者没有肺活量阻塞的患者,诱导的机械约束和过度的透气性需求发生,并且与嗜血症无关。
劳力性呼吸困难是肺动脉高压(PAH)患者寻求医疗注意的最常见的主诉。随着疾病的发展,它会无情地发展,导致生活质量的显著降低[1].以前关于PAAH中脱腹肿瘤的机制的研究主要并主要集中在呼吸道不适的心血管决定因素[2- - - - - -4].然而,呼吸力学异常可导致并加重这些患者的劳力性呼吸困难。例如,肺动脉高压患者在肺活量测量时,在低肺容量时呼气流量可能减少(即在50%和75%的用力肺活量(FVC)被呼出后测量瞬时用力呼气流量(FEF)50%和FEF.75%(分别)低于预期),尽管保留了1秒的用力呼气量(FEV1/ / fvc比率[5- - - - - -7].几项研究表明,这种发现可能在某些PAH队列中很常见[5- - - - - -7],已将其与PAH中伴随淋巴细胞浸润的气道壁增厚的偶发描述联系起来[5并提出了其他一些推测性的解释机制,可能是生物的,也可能是机械的[6,7].无论他们的原因是什么,低肺体积的呼气流量减少意味着操作潮气量(VT)范围比通常通过RV的增加(RV /总肺容量(TLC)比率的增加而变得更接近残余体积(RV)。强制和潮汐呼气流量之间的差异降低促进动态肺过货膨胀(DH,在逆向的通气需求增加的条件下,呼气肺体积(EELV)的逐步增加。DH增加呼吸肌肉必须克服的机械吸气载荷以产生微小通风(V”E),将隔膜放置在机械缺点,并降低了能力VT在锻炼过程中适当扩展,从而施加“限制性”机制[8,9].呼吸困难随之而来,如在运动期间慢性阻塞性肺病(COPD)和慢性心力衰竭(CHF)的流动限制患者清楚地显示[8- - - - - -11.].
我们假设,在肺测量显示肺容量低时呼气流量减少的肺动脉高压患者中,这种事件序列会发生。为了验证这一假设,我们检测了运动诱导的通气增加对年轻非吸烟、非阻塞性PAH患者手术肺容量的影响。我们还研究了DH的假定贡献和相应的力学约束VT在此设置中扩展到举行的呼吸困难。
材料与方法
患者和控制
我们研究了25例不吸烟的连续临床稳定的特发性或遗传性PAH患者[12.,根据现行循证临床实践指南诊断[13.,14.],具有正常的体重指数(BMI),没有趋势透气缺陷的肺活动力证据[15.].该样本大小提供了80%的功率,以检测在增量循环心肺运动测试(CPET)的标准化工作速率下以标准化的工作速率测量的呼吸困难强度(Borg Scale)中的显着差异(双面α= 0.05),基于相关差异Borg评分~1.5,Borg评级的标准偏差是我们的实验室发现的变化。如果在前面的三个月中临床上稳定,则患者纳入研究中,如果他们在前几个月的三个月内临床稳定,以及他们在参考中心临床随访框架内的CPET计划。一个10岁的健康受试者的对照组,所有这些受试者,所有终身的非乐者和患者肺炎15.],从两项研究中取出[16.,17.].该研究是根据赫尔辛基宣言中概述的原则进行的。主题提出了知情同意,并研究了法国呼吸医学协会机构审查委员会的批准(Comitéd'Quepationsde Recherche Dealonationnelle,SociétédePneumologiede langueFrançaise,Cepro 2010-020)。有关详细信息,请参阅在线补充材料。
程序
根据推荐标准进行肺功能测试[18.- - - - - -20.].测量结果表示为预测正常值的百分比[21.];预测吸气容量(IC)按预测TLC减去预测功能剩余容量计算。进行有症状限制的渐进CPET的程序以前已作过描述[8,9].使用修改的10点Borg规模评估呼吸困难和腿部不适的强度[22.,在运动期间和运动高峰期的每分钟。吸气流量储备是吸气肌限制/疲劳的间接指标,采用Johnson.et al。[23.].有关详细信息,请参阅在线补充材料。
通风限制指数
基于TLC在运动过程中没有显著变化的假设,在静止、运动过程中每一秒测量一次IC操作后的肺容积。为了确保这是实际情况,在CPET完成之前和之后立即测量了TLC。DH定义为IC的任何下降(以绝对值或TLC的百分比表示,IE。从静止到峰锻炼的IC / TLC(%))如前所述[8,24.].吸气储备体积(IRV)至TLC的比例(IRV / TLC(%))和VT集成电路(VT/ IC(%))均被视为机械约束的指标VT扩张 [23.].
统计分析
除非另有说明,否则变量总结为平均值±SD..使用Statview 5.0(Abacus Concepts,San Francisco,CA,USA)或Prism 4.0(GraphPad Software,Inc.,San Diego,CA,USA)进行统计程序。单向ANOVA用于评估对照组之间静态肺功能参数的差异,PAH患者,开发DH(PAH-H)和没有(PAH-NH)的人。在常见的标准化运动工作速率(WR)(20 w:iso-)(20 w:iso-)(20 w:iso-)(20 w:iso-WR 1和60 W; ISO-WR 2),以及使用未配对的T检验的峰值练习,具有适当的Bonferroni调整进行多种比较。Pearson相关性用于在标准化运动WR(依赖变量)和并发相关的独立变量之间Borg Dyspnoea评分之间的关联(IE。运动测量V”E,呼吸模式,肺容积,心血管和代谢参数,基线肺功能测量)。当I型误差的p值<0.05时,差异被认为是显著的。
结果
总结了参与者及其休息肺功能测量的特征表格1.20例患者被诊断出具有特发性PAH和5名遗传性PAH。根据纽约心脏协会(NYHA)分类,七名患者七名患者在II级分类,13级和III级。值得注意的是,所有患者根据指导方针接受了PAH特异性药物治疗[13.,14.],且在前三个月的临床表现稳定。多环芳烃特异性药物治疗概述见表S1。
生理组对CPET的反应
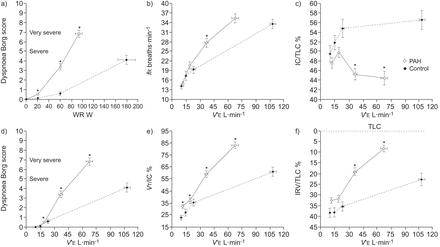
总结了对CPET的生理和感知响应表2..与对照组相比,V”E在所有PAH患者中,在任何次最大WR均显著升高,而在峰值运动时显著降低(图S1)。与对照组相比,肺动脉高压组的呼吸困难强度在任何给定的WR和V”E(图1)。呼吸困难/耗氧量(V”O2)和呼吸困难/V”EPAH患者的斜坡也比对照对象更大(6.9±2.8和0.12±0.04与2.0±1.0和0.04±0.02;p < 0.05)。PAH患者呈现出相对较快和浅的呼吸模式(图1)。在前20 W运动期间,患者和对照组的IC均增加;此后,IC仅在PAH患者中持续下降,而在健康对照组中持续上升(表2.和图1)。平均而言,PAH患者的静止峰值IC变化为-0.15±0.46升,对照组0.45±0.16L。IRV / TLC(%)和VT/ IC(%)在PAH患者中显着差异,而不是给定WR的对照受试者V”E(表2.和图1)。
运动性呼吸困难强度(Borg评分)是随着a)工作速率(WR)和d)分钟通气(V”E)在有限的肺动脉高血压患者(PAH)作为整个组(n = 25)和健康对照组(n = 10;固体符号和虚线)的患者中的限制性循环循环术。b)呼吸频率(fR)及e)潮气量(VT)表示为吸入能力(IC)的百分比(VT/ IC(%))被显示为响应增加V”E在症状限制性的循环循环术中,PAH作为整个组和健康对照受试者的患者。c)IC和F)吸气储备体积(IRV),两者都表达为总肺容量(TLC)的百分比,响应于增加而显示V”E在症状限制性的循环循环术中,PAH作为整个组和健康对照受试者的患者。限制约束VT与健康受试者相比,肺动脉高压组在运动期间的扩张明显更大,从以下(IC降低)和以上(IRV降低)。数据以平均值±表示SE.在静止、20 W (iso-WR 1)、60 W (iso-WR 2)和高峰运动时的值。*: p < 0.05,多环芳烃与健康在休息,以常见的标准化运动工作 - 率(20 w和60 w)或峰值运动。
鉴定PAH患者的两个亚组
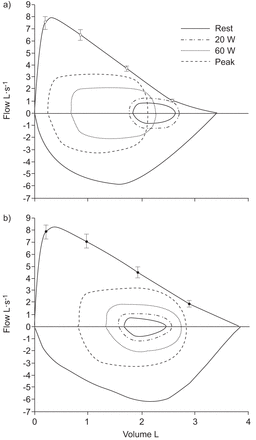
基于IC的休息时间变化,15(60%)PAH患者在运动期间表现为DH(PAH-H组,IC -0.50±0.15升),而剩下的10名患者没有(PAH-NH集团,IC+ 0.36±0.18 L)(图2)。PAH-H和PAH-NH患者的治疗均稳定,具有令人满意的血液动力学和临床反应,如休息,右心房压力,NYHA功能等级和6分钟步行距离所示表3)。比较两组其余患者的特征和肺功能表3.PAH-H患者表现为FEF降低75%与PAH-NH相比,休息血管测定仪(ERV)呼气储备体积(ERV)(表3)。值得注意的是,TLC在CPET中没有在PAH-H组中改变(5.2±1.1与5.3±1.1L分别;p = 0.4)或在PAH-NH组中(5.6±1.1与分别为5.6±1.0 L;p = 0.9)。多环芳烃- h和多环芳烃- nh组对CPET的生理和知觉反应总结在表4..在休息时获得的所有代谢和心脏通风测量在这两个群体中都相似,如图所示V”O2和V”E运动反应(包括iso-WR 1, iso-WR 2和peak)相对于WR表达,V”O2以及产生二氧化碳(V”有限公司2)(表4.和图3)。当绘制呼吸模式的测量时,响应模式也相似V”E(图3)。尽管有这些相似之处,但呼吸困难/V”O2和呼吸困难/V”E斜坡较陡峭的PAH-H-在PAH-NH(8.1±2.2和0.14±0.04与分别为5.1±2.7和0.09±0.03;p < 0.05)。在整个运动过程中,两组的手术肺容积也不同。值得注意的是,在前20 W运动期间,PAH-H和PAH-NH患者的IC均增加;此后,IC只在PAH-H患者中持续下降,而在PAH-NH患者中持续上升(表4.和图2)。休息至60瓦IC / TLC的变化在PAH-H和PAH-NH之间具有显着差异(7.2±2与-5±3%;p < 0.05)。此外,休息至60W的IRV / TLC(%)的变化在PAH-H(18±5%)显着不同(18±5%),而不是PAH-NH(7±5%; P <0.05)(图3)。尽管在操作肺容量行为上存在这些差异,pah和pah之间在运动高峰时的吸气储备流量没有统计学差异(1.7±0.3)与2.0±0.3 l·s−1;p = 0.6)(图2)。最后,PAH-H中的呼吸困难评级显着大于给定WR的PAH-NH患者V”E(表4.和图3)。
最大和潮汐流量环(平均数据)静止和肺动脉高血压(PAH)a)患者的休息和增量循环运动,用过度结雾(PAH-H; n = 15,年龄40±11 YRS)和B.)没有过度下的(Pah-NH; n = 10,年龄35±13 YRS)。潮流体积环休息,早期运动(在20次为20次),运动晚期(60 W)和峰值运动。注意PAH-H运动期间动态吸气能力的显着降低。与PAH-NH相比。
a)吸氧(V”O2b)分钟通风(V”E肺动脉高压伴高膨胀(PAH-H)患者(n = 15)和非高膨胀(PAH-NH)患者(n = 10)在症状受限的增量周期运动中,)对工作速率(WR)的响应。V”E响应于c)增加了V”O2和d)二氧化碳生产(V”有限公司2)在pah和pah患者的症状限制的增量周期运动。运动性呼吸困难强度(Borg评分)是对e)增加的WR和h的反应)V”E在pah患者和PAH-NH患者的症状限制的增量周期运动中。F)呼吸频率(fRi)潮气量(VT)表达为吸气能力(IC)的百分比显示响应增加V”E在PAH-H和PAH-NH的症状限制的增量周期运动中。g)IC和J)吸气储备体积(IRV)表示为响应增加的总肺容量(TLC)的百分比显示V”E在PAH-H和PAH-NH的症状限制的增量周期运动中。数据以平均值±表示SE.在静止、20 W (iso-WR 1)、60 W (iso-WR 2)和高峰运动时的值。PAH-H *: p < 0.05与PAH-NH在休息时,在普通的标准化运动WRs(20和60 W)或在高峰运动时。
与运动性呼吸困难相关
在整个组的PAH患者中(n = 25),其余到60w的呼吸困难Borg评分差异与IC/TLC评分差异(Δ)(%)密切相关(R = -0.70, 95% CI -0.857 - -0.422;p < 0.05)和ΔIRV / TLC (%) (R = -0.78, 95%可信区间-0.897 - -0.555;p < 0.05)。因此,Borg对呼吸困难评分的差异中约有50-60%的差异是由动态呼吸力学的变化引起的。值得注意的是,正如在COPD文献中预测的那样,ΔIRV/TLC(%)被ΔIC/TLC(%)强烈预测(R = 0.73, 95% CI 0.466-0.871;p < 0.05)。Borg对呼吸困难评分的差异也与Δ相关V”E/最大通气能力(MVC)(%)(r = 0.59,95%CI 0.257-0.799; P <0.05)。运动过程中呼吸困难的变化与任何其他基线肺功能变量或与在靠在右心导管或奈赫官能类别中获得的任何心血管变量相关的任何其他基线肺功能变量无关。
讨论
本研究的主要发现如下:1)在任何给定的WR中,运动性呼吸困难评分较高,V”O2和V”E在PAH患者中与对照科目相比;2)PAH患者运动期间的透气异常包括更高的通气需求,显着的DH和相对较快和浅的呼吸模式;3)休息肺功能试验证实,大多数PAH患者(60%)在低肺体积下表现出降低的呼气流量;4)操作肺量的DH相关变化(如。IC/TLC和IRV/TLC的降低)解释了肺动脉高压患者周期运动过程中呼吸困难的Borg评分差异的50-60%。
我们研究的患者是年轻的非吸烟者,他们患有特发性和遗传性PAH。他们的bmi正常,没有肺功能障碍的证据,并且在治疗中保持稳定,血流动力学和临床反应令人满意,这从静息时心输出量、右心房压力、NYHA功能等级和6分钟步行距离(表3)。这些患者的运动不耐受性轻度至中等,症状有限V”O2预计正常值平均减少23% (表2.),尽管多环芳烃的药物治疗。我们感到满意的是,PAH患者运动能力的降低并非动机努力减少的结果:患者在运动高峰时报告了难以忍受的运动症状,呼吸交换率在峰值>1.15。
在运动过程中,在给定功率输出时,呼吸困难强度等级较高,而呼吸困难/V”O2和呼吸困难/V”E在PAH患者中陡峭的斜坡比对照受试者较陡峭。在PAH患者中报道了类似或略低较低的呼吸困难强度,患有比我们更糟糕的纽约州官能的级别,但低得多V”E和wr [25.].潜在的“呼吸道”(而不是“心血管”)在我们的PAH患者中携带的呼吸呼吸困难的贡献者:1)动态通风机械和肌肉功能的更大异常会导致呼吸困难因其给出的任何V”E与健康相比;2)由于肺气燃气交换,解剖或心脏代谢异常的较高通气驱动/需求;或3)两者的组合。
异常动态通风力学
呼吸困难/V”E在我们的PAH患者的运动过程中,坡度持续升高,提示内在机械负荷增加和/或通气肌功能无力。25例肺动脉高压患者的静息肺功能检查显示15例明显的机械异常(IE。Pah-h)。这些患者在最大流量曲线的努力独立部分上表现出一致和均匀的呼气流量率,而FEV1/VC比值、TLC、VC、IC均得到保留。这些肺活量异常是否真正反映了周围气道阻塞仍有争议[5- - - - - -7].然而,在PAH中已经描述了小型气道功能障碍[5,6];它的机制理解得很差。他们可以包括间隙内空间内的肥大血管和远端气道之间的空间竞争[26.]小气道墙增厚,气道粘液塞,气道高光,老化或烟草吸烟的伴随效果,或这些因素的各种组合[5].在我们的研究中,我们排除了老年患者,以及有吸烟史、哮喘和其他心肺系统疾病的患者。此外,PAH-H和PAH-NH患者的疾病持续时间没有差异。需要进行病理研究,以了解表现出小气道功能障碍的PAH患者与没有小气道功能障碍的PAH患者之间气道形态的差异。
无论PAH相关的小气道功能障碍的机制如何,减少静息ERV和潮汐流量曲线中的最大流量曲线的形状和限制(显示FEF的还原75%)意味着,在我们的PAH-H患者中,操作VT比正常情况下更靠近RV。结果,我们的PAH-H患者的呼气流量限制倾向增加。事实上,尽管PAH-H患者在休息呼吸时没有表现出呼气流量限制,但他们在运动的相对早期(20w时,图2)。事实上,我们的PAH-H患者展示了IC的初步增加(从休息到20 W),他们能够适应他们的VT在ERV中,由于可用的呼气流量(储备)在该肺容量(图2)。在这种情况下,呼吸困难强度的上升减弱(表4.和图3)。相比之下,从20w到峰值运动,PAH-H患者的扩张能力不再增强VT由于在该肺部量不再可用的呼气流(储备),通过侵入ERV。作为结果,VT仅通过侵入IRV侵蚀IRV继续增加,并且在透气性需求增加的条件下,PAH-H的IC在PAH-H中减少了大致(DH)。在加速通风响应期间,运动IC在PAH-H中平均降低0.50升至峰锻炼。在40至80年的健康受试者中报告了类似的DH水平[27.,轻至重慢性阻塞性肺病患者[9- - - - - -11.),瑞士法郎(8,28.],最近也被R克明et al。[29.]在毛细血管前肺动脉高压患者的异质组中,但低得多V”E和WR比在我们更加均质的PAH患者中。另外,r克明et al。[29.并没有描述我们在患者中观察到的与运动相关的肺体积变化的双重模式。这种二元性,如果在大量人群中得到证实,对于选择治疗性干预以减少运动诱发的DH是很重要的。此外,他们既没有测量呼吸困难的强度,也没有将他们在运动中观察到的呼吸力学变化与呼吸困难联系起来[29.].
在肺动脉高压患者中,IC的动态下降反映了什么?由于TLC在整个运动过程中保持稳定,我们可以假设动态IC的下降反映了EELV变化率的增加,IE。DH。另一种解释是吸气肌肉性能下降[30.,31.].我们不能排除吸气肌无力或疲劳在我们的患者中导致IC降低,以及伴随的呼吸模式的改变。事实上,多环芳烃患者的呼吸肌肉功能障碍已被怀疑[30.,31.],主要是受到严重影响的pah [32.].然而,多环芳烃- h和多环芳烃- nh患者的吸气潮流量接近最大可用吸气流量的相似百分比(IE。类似的吸气流量储备,表明峰锻炼的吸气肌的吸气流动储备相似(但在不同的操作肺量上发生),因此不太可能存在吸气肌约/疲劳。如果这确实如此,IC会在PAH患者中减少,在运动期间没有在运动期间实际上没有发展DH的患者那么多于那些在努力开发DH的人中。因此,PAH-H患者不太可能遭受吸气肌肉力量的损害,这足以防止他们在自愿操纵期间达到TLC。PAH-H患者与PAH-NH患者类似于其一般特征,严重程度,持续时间和疾病的医学管理。
无论其原因如何,在我们的PAH-H患者中观察到的运动期间DH的快速发展可能具有感觉的后果,如各种心肺疾病的患者清楚报道[8- - - - - -11.].DH导致吸气肌肉的弹性负荷和功能弱点,从而对抗严重的机械限制VT在逐步增加中央神经驱动的背景下展开展开[8,9,33.]:VT从下面的eELV被截断,并由TLC封套和IRV相对减少约束。因此,与可比较WR的年龄匹配的PAH-NH,PAH-H患者相比V”E在动态EELV中显示出大幅度的增加,更大的比率VT到IC,并标明IRV减少。虽然PAH患者(全部包括在一起或PAH-H或PAH-NH),但在运动期间没有表现出通气限制,传统上由比例决定V”E到MVC超过至少85%[23.,34.在大多数Pah患者中,显着的通气限制和随函附上的呼吸困难显而易见。在运动期间,这在COPD和CHF患者中已经充分了解[8,11.,35.].普遍认为,在这种环境中,呼吸困难产生了有意识地意识到在增加呼吸努力(或神经驱动到呼吸)和同时钝化的胸体积位移之间的越来越多的差异。我们认为这是我们的PAH-H患者的情况,因此,他们报告的呼吸困难至少是由于呼吸力学改变的部分[33.].实际上,在标准化的WRS上,呼吸困难强度显着较高,动态IRV在PAH-H组中比在PAH-NH组和对照对象中比例地下降。DH和随后的约束的概念VT通过呼吸困难强度与减少的动态IC / TLC(%)(R = -0.70; P <0.05)和IRV / TLC(%)(r = -0.78;P <0.05)以标准化的运动刺激。但是,我们意识到相关性并不一定意味着因果关系和其他机制(如。心理方面可能在呼吸困难感知中发挥作用。需要进一步研究来确定这一点。
增加通气需求
我们在PAH患者循环运动期间的透气性需求增加的结果证实了先前发表的研究[2,36.].简而言之,峰值V”E减少,反映了降低的峰值症状限制V”O2.与对照科目相比,V”E在任何给定的次最大WR和V”O2.对运动的过度通气反应的机制超出了本研究的目的,因此并非完全阐明。然而,可以想到,减少氧输送/利用,解剖和通风/灌注异常的组合刺激V”E在运动过程中,在PAH患者的程度上比对照科目更大,如下所示:1)更大V”E/V”有限公司2(斜率和比率)和V”E/V”O2;2)更大的死亡空间滴流量比(在存在低动脉二氧化碳张力(P,有限公司2),在肺动脉高压患者的运动中没有进一步显著下降);3)较早出现无氧通气阈值(数据未显示);4)心动频率越大/V”O2斜坡(数据未显示);5)较低的V”O2/心脏频率(IE。与健康受试者相比,肺动脉高压患者在整个运动过程中观察到的氧脉冲。此外,肺动脉高压的过度通气可能是由于肺泡过度通气所致P,有限公司2设置点(2].该设定点已被证明受以下影响:1)代谢酸中毒由于行程的卒中体积响应受损[37.,38.];2)运动诱导的低氧血症;3)同情刺激[39.];4)肺血管中血压响应受体的刺激增加。我们的数据没有提供这些不同因素在肺动脉高压过度运动通气中的相对贡献。
不管机制如何,都增加了V”E在肺血管术处的低肺体积下的降低的呼气流情况下,可能有贡献,以加速降低IC和更大的呼吸困难强度。相关性分析证实了呼吸困难强度等级之间的关联和V”E/ MVC(%)(r = 0.59; p <0.05)。越高V”E在PAH中最终反映了透气肌肉的相对增加的中央神经驱动和收缩肌肉努力(相对于最大可能的值)。
限制
没有食管压力测量在这项研究中,选择合理的探索性研究的性质和我们的担忧使它尽可能接近观测,我们必须承认,减少动态集成电路可能是由于要么DH,吸气肌肉无力或疲劳,或两者的组合。不管其机制如何,PAH-H中动态IC的持续下降可能具有生理和临床意义。鉴于样本量较小,我们必须小心避免将我们的研究结果推广到更大的PAH人群。进一步的研究需要更大的样本量,并在运动过程中进行食道压力测量,以明确阐明肺动脉高压患者呼吸力学改变的生理机制。
结论
本研究首次探讨了潜在的dh诱发的关键机械约束对接受症状受限递增CPET的非吸烟特发性和遗传性PAH年轻患者呼吸困难强度的影响。该研究证实,在一定比例的特发性和遗传性PAH患者(60%)中,尽管FEV保存,但肺活量测量显示,低肺容量时呼气流量减少1/ VC比率。它表明,这些异常促进了DH,响应于可以通过通风/灌注不匹配和其他因素而放大的运动相关的通风增加。虽然PAH中的运动相关的呼吸困难具有重要的心血管决定簇[2- - - - - -4,我们的研究结果表明,异常的动态呼吸力学可能有助于在运动过程中形成这种症状。值得注意的是,我们观察到的手术肺容积的变化(如。IC / TLC和IRV / TLC的减少)解释了与呼吸困难相关的运动相关差异的50-60%。鉴于这些变化的大小,这可能被认为是令人惊讶的,但可能反映了在心血管局部的顶部添加机械负担的事实对呼吸困难产生指数影响。这是必要的是,旨在减少或延迟与DH相关的机械约束的治疗干预可能是血管扩张剂的血管扩张剂,该血管扩张剂在低肺体积下表现出降低的呼气流量。然而,目前的数据不足以达到此结论。将来需要进行未来的研究,以确定PAH的环境中此类干预措施(包括支气管扩张剂)的确切指示和风险效益余额。
致谢
作者感谢C. Straus(巴黎大学06,Equipe de Recherche ER 10 UPMC, Laboratoire de Physio-Pathologie Respiratoire, Faculté de Médecine皮埃尔和玛丽居里(网站Pitié-Salpêtrière),巴黎,法国)帮助建立研究和输入手稿;致A. Féré、C. Thomas、N. Mecreant和T. Rouyer(法国探索职能呼吸器服务,Hôpital Antoine Béclère,法国Clamart),感谢他们为开展肺功能和心肺运动测试提供技术援助;X. Jaïs, l . Savale和D. Montani (Service de Pneumologie et Réanimation respiratory, Centre National de Référence de l'Hypertension Pulmonaire Sévère, Hôpital Antoine Béclère, Clamart, France)招募患者。
脚注
本文提供了补充材料www.www.qdcxjkg.com.
支持声明
1)欧盟第七框架计划,研究人员培训和职业发展支持项目(Marie Curie),国际再整合基金(IRG), fp7 -人-2010- rg,批准号:PIRG07-GA-2010-268396-EDPAH;2)辉瑞研究员发起的研究(IIR),批准号WS 942458。
兴趣表
P. Laveneziana,O. Sitbon,G. Simonneau,M. Humbert和T. Similowski的申报陈述可以找到www.www.qdcxjkg.com/site/misc/statements.xhtml.
- 收到了2011年12月20日。
- 接受2012年6月9日。
- ©2013人队