文摘
背景我们评估是否toll样受体(TLR) 2激活增强先天免疫反应鼻病毒感染,病毒诱导呼吸系统疾病的治疗策略。
方法我们使用小说TLR2受体激动剂治疗(INNA-X)前鼻病毒感染小鼠,在分化和INNA-X治疗人类支气管上皮细胞来自asthmatic-donors。我们评估病毒载量,招募免疫细胞,细胞因子,我和III型干扰素(IFN)生产,以及肺组织上皮细胞免疫转录组。
结果我们表明,在活的有机体内,单个INNA-X治疗先天免疫诱导启动的特点是低级IFN-λFas配体,趋化因子表达和气道淋巴细胞招聘。治疗7天前感染显著降低肺病毒载量增加IFN-β/λ表达式和抑制中性粒细胞炎症。皮质类固醇治疗增强INNA-X的抗炎作用。治疗前1天感染增加190个肺组织免疫基因的表达。这个组织基因表达的签名没有INNA-X治疗感染前7天,建议另一种机制,可能通过建立免疫细胞粘膜先天免疫。在体外INNA-X治疗诱导启动响应由调节IFN-λ,趋化因子和抗微生物基因表达之前加速响应感染浓缩核因子(NF) -κB-regulated基因和病毒载量下降,即使在上皮细胞来源于哮喘捐助者与内在延迟抗病毒免疫反应。
结论气道上皮细胞TLR2激活引发长时间的先天免疫启动,由早期NF-κB激活,IFN-λ表达式和淋巴细胞招聘。这种反应增强抗病毒先天免疫和减少病毒诱导气道炎症。
文摘
TLR2-agonist治疗呼吸道刺激气道上皮细胞'先天免疫系统迅速应对感染和减少病毒诱导炎症,包括皮质类固醇治疗的上下文和哮喘https://bit.ly/3g02Q4M
介绍
鼻病毒(RV)负责60%的年度全球呼吸道疾病(1,2]。下呼吸道感染可引起咳嗽、气短、胸闷、气喘、细支气管炎和肺炎3]。房车也加重的慢性呼吸系统疾病的主要原因,包括哮喘(4),慢性阻塞性肺疾病(COPD) (5,6),囊性纤维化(CF) [7,8和non-CF支气管扩张9]。目前,RV感染的治疗方法支持,减少症状但不限制病毒感染。
中性粒细胞炎症构成的主要应对病毒感染。然而,过度/长期中性粒细胞炎症会导致组织损伤和增加气道嗜中性粒细胞数量与恶化严重哮喘和慢性阻塞性肺病(10,11]。吸入激素(ICS)减少急性加重的风险,主要治疗方法为哮喘和慢性阻塞性肺病。然而,ICS治疗恶化病理疗效有限,特别是在减少中性粒细胞炎症在哮喘的上下文12]。此外,ICS治疗抑制抗菌免疫和增加容易继发感染和肺炎,慢性阻塞性肺病(中13]。
气道上皮细胞的主站点鼻病毒感染。通常toll样受体表达的上皮细胞等细胞内TLR3/7/8/9启动宿主抗病毒先天免疫,通过识别产生的病毒核酸复制病毒(14]。这种观察导致toll样受体激动剂的评价抗病毒疗法。然而,研究评估病毒核酸酸感性toll样受体激动剂治疗治疗窗窄,i型干扰素(IFN)的活化反应,炎症,流感样症状和细胞因子风暴15,16]。相比之下,TLR2表达在细胞表面和持续暴露共生的微生物群和潜在的病原体。因此,TLR2激活必须严格监管维护免疫内稳态(17),这可能会限制toll样受体激动剂治疗后意想不到的副作用。我们以前报道,TLR2受体激动剂治疗降低病毒载量和有限的传播流感在老鼠18),但TLR2受体激动剂的使用限制其他病毒感染仍然是未知的。
在目前的研究中,我们评估了TLR2受体激动剂治疗RV感染的效果,使用新颖的分子,INNA-X。INNA-X的聚乙二醇模拟合成diacylated lipopeptide年代-(2,3 -二(十六烷酰氧)丙基)半胱氨酸Pam2Cys [18),四个赖氨酸残基传统上用于提高溶解度被聚乙二醇取代。赖氨酸根被作为战略否定脱靶效应,作为紧密TLR2受体激动剂,观察Pam3Cys [19]。
鼻内交付INNA-X诱发小鼠的肺部先天免疫启动的特点是早期,低级IFN-λ和淋巴细胞招聘的表情。治疗前1天感染了抗病毒先天免疫签名在肺组织和抑制病毒载量。TLR2受体激动剂治疗7天前RV-A1感染抑制病毒载量和肺部炎症。治疗疗效持续每周连续当了疫苗接种。组合与吸入激素治疗同样有效地减少肺病毒载量和进一步降低病毒诱导炎症。在分化的主支气管上皮细胞(bec)在体外INNA-X治疗也推动了先天免疫,导致增加的早期表达IFN-λ和核因子(NF) -κB-regulated抗菌基因。之前进一步IFN-λ感应加速宿主抗病毒反应分化主要bec隔绝捐助者与哮喘。这是一个关键的发现,多个证据报道不足抗病毒反应在哮喘患者20.- - - - - -22]。我们的研究表明,airway-delivered TLR2受体激动剂治疗呼吸道上皮细胞提供持续气道先天免疫启动,是一种有效的策略来限制呼吸道病毒感染和侵染诱导气道炎症。
材料和方法
伦理语句
主支气管上皮细胞是由P.A.B.华克(澳大利亚纽卡斯尔大学,纽卡斯尔),获得健康的捐赠者或捐赠者与哮喘在支气管镜检查,以书面知情同意。所有实验与纽卡斯尔大学的安全委员会的批准(安全REF # 25/2016和R5/2017)。进行了动物实验,依照澳大利亚新南威尔士动物研究立法。实验协议- 2016 - 605进行审核和批准的纽卡斯尔大学动物保健和伦理委员会。
鼻病毒传播、净化和量化
鼻病毒菌株A1 (RV-A1)最初从临床分离纯化(由P.A.B.华克提供)。鼻病毒株A16 (RV-A16)最初购买的写明ATCC 757(应变11)。这两个菌株生长在RD-ICAM细胞和纯化如前所述23,24]。
TLR2兴奋剂RV-A1感染和管理在活的有机体内小鼠模型
从澳大利亚生物6-8-week-old雌性BALB / c小鼠(上;苔藓淡水河谷、澳大利亚)是用于所有实验。老鼠被安置在单独的通风笼HEPA过滤空气和食物/水随意。所有实验在生物安全柜在干净的条件下进行。INNA-X得到lyophilised Ena呼吸(澳大利亚墨尔本)的形式和resuspended无菌生理盐水。老鼠INNA-X鼻内处理的时间和剂量表示文本。老鼠感染鼻RV-A1 (2.5×106半数组织培养感染量(TCID50),如前所述23,24]。支气管肺泡灌洗(BAL)和肺部感染后的样本收获2天。
BAL细胞分析
小鼠气管插管,降低航空公司与哈佛商学院刷新(Hyclone;通用电气生命科学、北方莱德(悉尼)、澳大利亚)。上层清液储存在−80°C。细胞被RBC-lysed和白细胞浓度由血球计数决定。Cytospins进行和May-Grunwald +染色染色用于列举中性粒细胞、淋巴细胞和巨噬细胞的显微镜。
RNA分离和定量逆转录pcr (qRT)
顶肺叶收获在RNA-Later (Invotrogen品牌,通过Ambion许可,由热费希尔科学、北方莱德(悉尼)、澳大利亚),看在RNeasy裂解缓冲(RLT)(试剂盒,Chadstone(墨尔本),澳大利亚)含1%β-mercaptoethanol(2),细胞碎片颗粒状和上层清液储存在−80°C。气液界面(ALI)膜在RLT涡/ 2我,细胞膜被溶解产物是储存在−80°C。小鼠肺RNA是手动提取RLT溶解产物使用miRNeasy工具包(试剂盒)后,供应商的协议。阿里RNA提取的QiaCube(试剂盒)使用miRNeasy工具包(试剂盒)。RNA浓度测定Nanodrop和200 ng (ALI样本)或1000 ng(鼠肺)反向转录。qPCR进行一个使用TaqMan ABI7500或定量Studio 6 FAM-TAMRA试剂(生命技术/热费希尔科学、北方莱德(悉尼)、澳大利亚),包含火箭(试剂盒)mastermix, primer-probe组合中概述表S3。感兴趣的基因的绝对量化测定使用已知浓度的标准。感兴趣的基因是正常参考基因18岁。
气液界面的气道上皮细胞培养
获得初级bec moderate-severe持续哮喘捐助者在气液界面生长直到支流和分化(ALI),如前所述[25,26]。
bec获得从一个健康的捐赠者通过2淹没单层培养中被扩展使用Rho-associated蛋白激酶(岩石)抑制剂(最终浓度10µM)结合辐照纤维母细胞馈线细胞。维护媒体组成的33%扩大bec DMEM(高葡萄糖+谷酰胺)/ 67%火腿F12含有5% FCS,氢化可的松(最终浓度400 ng·毫升−1)、胰岛素(最终浓度µg·5毫升−1),rhEGF(最终浓度10 ng·毫升−1),霍乱毒素(最终浓度8.4 ng·毫升−1),腺嘌呤(最终浓度23.9µg·毫升−1青霉素链霉素)和0.2% (27三个段落)和他们的亚文化。一旦汇合的,这些bec被播种到聚酯transwell膜和分化如前所述25,26]。
TLR2受体激动剂剂量和房车接种人阿里bec
感染前24小时,分化上皮细胞是治疗水20 nM INNA-X BEBM最小饥饿媒体(Lonza;BEBM + 1%和0.5 lipoteichoic酸)。健康的捐赠者文化注射RV-A1或RV-A16(感染复数(MOI) 0.1) 2 h顶端文化表面上35°C。对哮喘捐赠文化,我是0.001。感染后,顶舱与PBS洗两次。饥饿媒体包含TLR2兴奋剂被放置在顶端舱(控制仅接受媒体)35°C。
样本收集来自阿里文化
阿里文化样本采集时间点显示的文本。顶端媒体被储存在−80°C的下游蛋白质分析。一半的transwell收集RLT缓冲区(试剂盒)含1% 2我分子分析半保留蛋白质分析里帕缓冲区包含蛋白酶抑制剂鸡尾酒(罗氏公司、北方莱德(悉尼)、澳大利亚)。
蛋白质定量的ELISA
蛋白质水平的气道细胞因子量化了Duoset ELISA(研发系统,明尼阿波利斯,美国)按照制造商的说明KC /白介素(IL) 8(处于)和TNF-α鼠标BAL样本。人类IL-29 / IL-28B Duoset ELISA (IFN-λ1/3)(研发系统)是用于BEC样本。
免疫转录组表达分析
纯化总RNA是杂交鼠标免疫学GX代码集(美国西雅图Nanostring / Bio-Strategy,布里斯班,澳大利亚)或人工免疫学面板版本2 (Nanostring),按照制造商的说明。原始数据是基于积极的控制质量控制检查和正常化,消极的控制和管家基因表达出口到Monash-DEGust轰/ Limma基因表达分析的平台。另外,原始数量导入到Nanostring高级分析平台自动使用标准的正常化,内置软件GENorm最佳管家检测,其次是识别度和路径分析,概述了在文本。
统计分析
数据从在活的有机体内老鼠实验(不包括转录组数据)被单向方差分析分析,与Holm-Sidak修正多重比较。所有数据从老鼠实验评估使用Anderson-Darling、正态分布和皮尔森,达和Shapiro-Wilk测试。任何组织,显著偏离正态分布使用非参数Mann-Whitney随后被分析,或克鲁斯卡尔-沃利斯(邓恩的修正多个比较)测试,显示在图传说。所有数据从健康控制阿里细胞培养与双向方差分析或单向方差分析进行分析,与Holm-Sidak校正或Mann-Whitney测试。时间进程进行评估的数据双向方差分析与Bonferroni调整为多个比较。弗里德曼测试邓恩的多个校正分析,或魏克森讯号等级测试的数据进行哮喘捐助者的假设非参数数据从不同的人类捐助者的性质。统计分析使用图垫棱镜8.3.0软件(La Jolla、钙、美国),α值为0.05。免疫转录组数据分析如图传说描述使用单变量t(鼠肺数据;美国西雅图nSolver软件,Nanostring), Benjamini Yekutieli纠正p值(BEC数据;nSolver软件),错误发现率(罗斯福)—假定值(轰/ Limma,纳什品尝平台、莫纳什大学、澳大利亚)或z分数的组合(nSolver提前分析平台)与后续单向方差分析和Holm-Sidak校正(图垫棱镜)。
结果
独自INNA-X治疗抑制鼻病毒感染,结合皮质类固醇
INNA-X是一种稳定的TLR2-specific受体激动剂与合适的特征在活的有机体内据说交付,否定了脱靶效应引起的阳离子赖氨酸的半个现有TLR2受体激动剂(28]。INNA-X激活两个老鼠和人类TLR2诱导下游NF-κB信号途径,发现在一个在体外记者系统(图S1)。我们比较INNA-X商业化TLR2-agonist Pam2CysSK4建立鼠标RV-A1感染模型中(23]。单剂量的小鼠治疗鼻INNA-X或Pam2CysSK4(浓度在2和10 pmol) 7天前RV-A1感染。这两种药物(在10 pmol /鼠标)显著降低肺病毒RNA,而只有2 pmol INNA-X剂量显著降低肺病毒载量(图S2)。
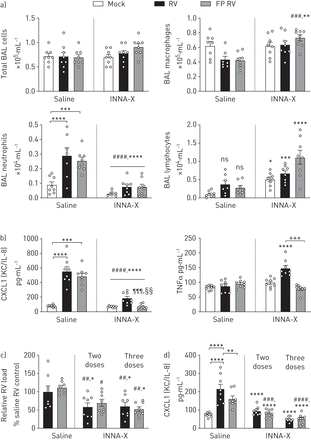
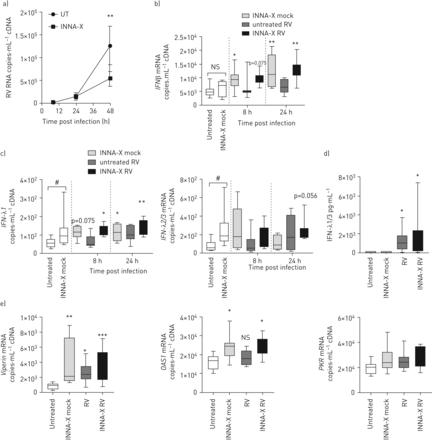
我们下一个评估INNA-X如何调节宿主抵抗RV-A1感染治疗。老鼠与低剂量治疗鼻内INNA-X (2 pmol),或结合吸入激素(ICS)丙酸(FP)(管理前1 h RV-A1感染;实验时间图1一个,正如前面发表)13]。感染后的端点测量2天(9天post-INNA-X治疗)。INNA-X治疗肺病毒载量显著降低了大约50%,不管皮质类固醇治疗(图1 b,图S3)。相比之下,丙酸治疗(没有INNA-X)显著增加病毒载量与生理盐水治疗相比,RV-A1感染小鼠(图1 b)。在缺乏INNA-X治疗,抗病毒的表达无显著增加IFN-β或观察-λ相比mock-infected老鼠(图1 c和d)。IFN-β(图1 c)和IFN-λ(图1 d)明显升高后INNA-X预处理,不遵循co-treatment卡松丙酸。因此,INNA-X RV-A1感染后治疗调节干扰素反应。
INNA-X治疗在活的有机体内降低肺病毒载量与皮质类固醇治疗相结合。实验时间。老鼠RV-A1感染和治疗7天前样品收集在感染后2天。为模拟感染小鼠,样本收集INNA-X治疗后9天。有些团体治疗卡松丙酸(FP)之前感染。b) RV-A1 RNA水平的肺部组织。c)干扰素(IFN) -β和(d) IFN-λ2/3 BAL样品中蛋白质含量。数据代表的意思是±扫描电镜老鼠,n = 8每组的代表至少两个独立的实验。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;* * * *:p < 0.0001,单向方差分析与Holm-Sidak修正为多个比较,相比之下,盐水房车控制(除非另有说明)。# # # #:p < 0.0001单向方差分析与Holm-Sidak修正为多个比较,而盐水FP房车。
ICS治疗或每周重复剂量并不影响INNA-X-mediated淋巴细胞招聘或抑制病毒诱导炎症
我们下一个量化的炎性细胞和细胞因子在BAL样本子集。无显著差异在观察白细胞总数INNA-X治疗(图2一个)。然而,淋巴细胞数量增加后INNA-X治疗组(包括mock-infected老鼠),相比saline-treated控件(图2一个)。增加巨噬细胞数量只在RV-A1-infected观察小鼠接受INNA-X和丙酸(图2一个)。气道嗜中性粒细胞数量是特殊的意义,中性气道炎症通常是与人类[RV-induced疾病的严重程度有关23,29日]。RV感染独自在saline-treated老鼠BAL中性粒细胞增加,由丙酸的治疗(图2一个)。相比之下,INNA-X治疗显著降低中性粒细胞数量到基线水平,无论丙酸co-treatment (图2一个)。识别潜在的机制这一观察,我们量化有关趋化因子和细胞因子。中性粒细胞趋化因子处于受控(鼠标引发/ KC)减少INNA-X治疗后,观察治疗后的最低水平INNA-X和丙酸(图2 b)。INNA-X治疗RV-A1-infected TNF-α生产老鼠增加了大约30%,由丙酸抑制co-treatment (图2 b)。总之,INNA-X治疗促进淋巴细胞招聘、抑制RV-induced中性粒细胞炎症,通过ICS co-treatment进一步支持。
INNA-X治疗在活的有机体内抑制rhinovirus-induced中性粒细胞炎症,促进淋巴细胞的招募。老鼠RV-A1感染和治疗7天前样品收集在感染后2天。模拟被感染的老鼠,样品收集INNA-X治疗后9天。有些团体治疗卡松丙酸(FP)之前感染。总细胞数和微分,巨噬细胞、中性粒细胞和淋巴细胞计数支气管肺泡灌洗(BAL)。b)蛋白水平的平衡细胞因子处于受控和TNF-α。在不同的实验中,小鼠治疗21天,和/或-14年和7 INNA-X紧随其后FP /车辆治疗和RV /模拟感染前和样本收获在感染后2天确定水平的c) RV-A1 RNA的顶端肺叶和d) BAL处于蛋白质。数据代表的意思是±扫描电镜老鼠,n = 8每组的代表至少两个独立的实验。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;* * * *:p < 0.0001,单向方差分析与Holm-Sidak修正为多个比较,相比之下,盐水房车控制(除非另有说明)。#:p < 0.05;# #:p < 0.01;# # #:p < 0.001;# # # #:p < 0.0001单向方差分析与Holm-Sidak修正为多个比较,而盐水FP房车。+ + +由Mann-Whitney: p < 0.001。¶¶¶:p < 0.001与盐水房车控制;§§:与生理盐水相比p < 0.01 FP房车克鲁斯卡尔-沃利斯和邓恩的修正多重比较。“ns”表示不显著(p > 0.05)。
我们也评估RV-A1感染后病毒载量和气道处于水平与多个剂量的预防性治疗小鼠INNA-X每周管理,2或3周(模型一个潜在的预防性治疗策略)。每周重复INNA-X治疗减少肺病毒载量,无论是单独或与丙酸co-treatment (图2 c;图S3)。INNA-X-mediated抑制RV-A1-induced处于表达式也是重复INNA-X后观察治疗(图2 d)。
TLR2受体激动剂的时机改变先天免疫启动特定的基因表达模式
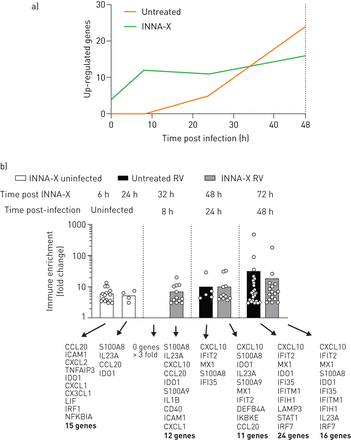
理解的机制调解INNA-X-induced保护,我们使用Nanostring技术特征肺组织免疫转录组。两个治疗方案进行了比较,结果评估INNA-X治疗后9天或3天。小鼠感染后7天或1天INNA-X治疗(图3一)。两种治疗方案显著降低肺RV-A1水平评估感染后的2天,证明INNA-X治疗前1天感染也有效(图3 b)。澄清机制,(度)在肺组织的差异表达基因的视觉使用轰/ Limma软件(30.]。集群的呈现度也使用欧几里德层次聚类热图软件(31日)(图3 c)。在未受感染的老鼠,多个CC和科学家趋化因子基因上调9和3天post-INNA-X治疗。在RV-A1-infected老鼠,我们注意到两个不同的基因表达模式以应对病毒感染,这取决于不同的时机INNA-X治疗。治疗INNA-X 1天前感染增强宿主肺组织免疫反应,以两个基因的上调集群(指定集群1和2)。上调集群丰富了抗病毒/干扰素刺激基因(IFI204 IRF7, mx₁, IFIT2)和多个CC和科学家趋化因子(图3 c)。这种反应与淋巴细胞数量增加,处于水平升高BAL样本(图S4)。这加剧了肺组织免疫反应没有明显感染后治疗前7天。相反,有一般治疗后肺组织免疫基因表达减少感染前7天,比未经处理的(生理盐水)RV-A1-infected组。基因簇1和2强调减少免疫签名在肺组织9天后处理RV-A1-infected集团(图3 c)。
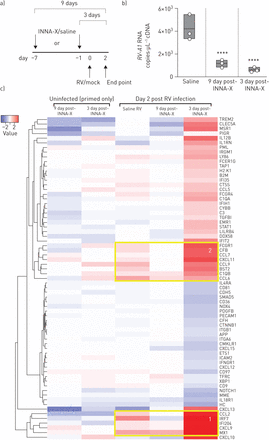
INNA-X治疗在活的有机体内相关基因表达模式显示增强抗病毒反应和先天免疫系统激活。实验时间。小鼠治疗7天或1天前RV-A1感染和样品收集在感染后2天。模拟被感染的老鼠,样本收集3天或INNA-X治疗后9天。b) RV-A1 RNA在顶端肺叶。c)的热图表示和欧几里得集群被轰的差异表达基因/ Limma分析(罗斯福Nanostring RNA表达的p值< 0.01)。n = 3老鼠每组。d)上调基因分数使用nSolver生成软件(p值< 0.05)进行过滤。n = 3老鼠每组。
更好地理解不同、治疗timing-related资料观察,我们使用Nanostring nSolver软件询问所有上调基因(图3 d;十大最高度上调基因为每个组)上市。在未受感染的老鼠在9和3天post-INNA-X治疗,我们观察到的低级IFN-λ先天免疫启动定义的表达式和pro-apoptotic Fas配体(Fasl)基因。趋化因子CCL7和CCL9轰中标识/ Limma分析也发现nSolver软件,显著上调INNA-X-treated老鼠。我们发现两倍上调基因在肺收获9天post-agonist治疗相比,3天后处理未受感染的老鼠。在RV-A1-infected老鼠,INNA-X治疗前1天感染190个基因表达明显上调。最高度诱导干扰素刺激基因识别,抗病毒分子Ifi204 IRF7, CXCL10, mx₁, STAT2和趋化因子CCL2, CXCL13。观察不同的基因表达谱与INNA-X治疗7天前感染。我们观察到低级(少于1/2)32基因的上调(相比之下,saline-treated 12基因小鼠),这与淋巴细胞反应有关(如。国际安全和发展理事会配体、BTLA)趋化因子(CCL6)和适应性免疫(图3 d)。完整的列表中包括基因表达的上调辅助数据文件S1。因此,趋化因子的存在3天后处理和调节淋巴细胞调节的证据9天后处理与观察淋巴细胞招聘模式一致。
INNA-X影射反应对RV-A1感染人类主要bec分化
定义哪些方面INNA-X治疗效果是由上皮细胞介导的,我们评估TLR2受体激动剂预处理RV-A1感染分化人类bec初级在体外。区分健康的捐赠者bec [27)与INNA-X预处理前24小时RV-A1感染。这些实验的主要目的是识别的作用机制(农业部)INNA-X分化主要人类BEC-RV感染模型(13,32]。使用从健康捐献者bec我们评估免疫基因的病毒载量和表达的时间进程使用Nanostring人类免疫学面板与n = 1 /计算/治疗。INNA-X抑制从24小时至48 h感染后病毒载量(图S5)。Nanostring-based免疫转录组分析显示先天免疫的证据启动IDO-1大于3倍上调表达,β-defensin (DEFβ-2)和csf,比未经处理的细胞在24 h后INNA-X治疗。这之前加速响应RV感染定义为26日上调基因在INNA-X 8 h感染后治疗样本,而未经处理的RV-A1-infected细胞基因之一。增强INNA-X-induced响应明显在24小时后感染。然而,48 h后感染,更多的基因(丰富干扰素(干扰素刺激基因(isg))在未经处理的细胞调节。这些数据表明,INNA-X治疗改善早期病毒感染的控制,减少以后IFN-driven响应的大小(图S5)。确认这个结果在BEC孤立的从不同的健康的捐赠者更多的实验复制/治疗/计算,我们使用条件改变(CR)扩大BEC数字重复研究n = 5次。再次反应进行分析之前和之后感染和病毒载量(治疗时间表所示图4一)。INNA-X治疗没有影响上皮屏障功能,由trans-epithelial电阻(TER) (图S6a)。

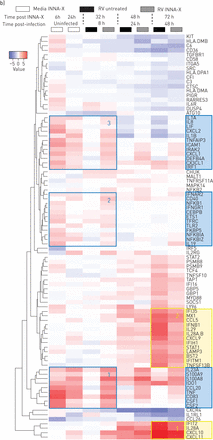
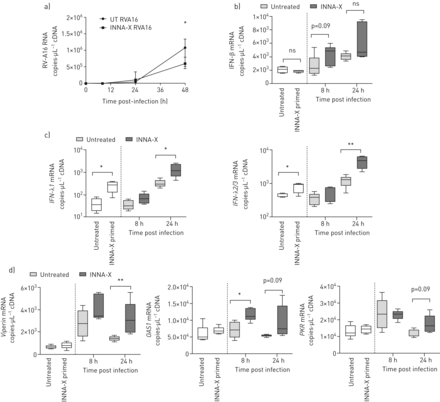
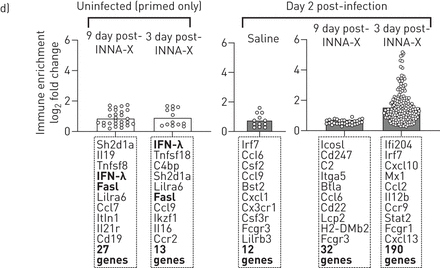
INNA-X治疗在体外降低病毒载量和增强快速先天免疫反应在人类支气管上皮细胞分化的文化。)时间线显示所有时间点后的收获INNA-X治疗和减少RV-A1 RNA表达在8日24和48 h后感染,从健康捐献者分化bec,药物治疗感染前1天。n = 5个重复,意味着±sd。* *:p < 0.01;* * * *:p < 0.0001双向方差分析与Sidak修正多重比较。b)欧几里得集群的热图的差异表达基因被轰/ Limma分析(过滤后通过罗斯福p值< 0.001)NF-κB先天免疫启动集群都用蓝色表示(DEG1 2 3)和干扰素(干扰素刺激基因(研究小组)纯度的浓缩铀的集群都用黄色表示。n = 5个重复。
INNA-X治疗显著抑制病毒载量,明显24 h感染后48 h后更明显(图4一)。免疫转录组分析使用人类免疫学Nanostring面板(总数594个基因)确定了三个不同的集群度编码分子浓缩NF-κB-regulated细胞因子/趋化因子,TNF超科/凋亡和抗微生物肽(图4 b;用蓝色框1 - 3)。调节度在这些集群定义INNA-X治疗后6 h和24小时快速响应RV-A1感染观察到8 h后感染(图4 b)。在感染后48 h两个不同的集群度明显,代表抗病毒基因(包括I / III型干扰素;图4 b;用黄色框1和2)。我们注意到我(IFN-β)型和III型IFN-λs (IL29 IL28A / B)在INNA-X-treated细胞少上调后计算,符合一个更有效的早期先天反应和随后的病毒清除。
想象RV-A1-infected bec动力学INNA-X-induced基因上调,我们绘制基因表达显著上调的总数(统计学意义;大于3倍)随着时间的推移,以及相对于未经处理的表达水平和细胞无毒性(图5一个)。这些结果表现为免疫富集,定义为调节基因的数量(点分)和基因表达的大小为每个基因(每个数据点)的高度。响应独自INNA-X(感染)之前是丰富NF-κB-regulated抗菌基因和趋化因子;其中许多后来上调8 h后感染。在这个计算,INNA-X-primed bec 12基因表达明显上调(大于3倍),以应对RV-A1感染,而未经处理的RV-A1-infected bec没有改变基因表达(即。0基因差异大于3倍;图5 b)。这种反应持续到24小时后感染(INNA-X治疗后11个基因上调与五个基因在未经处理的RV-A1-infected细胞;图5 b)。由48 h后感染老年病众多干扰素刺激基因很明显,表现出相似的基因表达谱与未经处理的RV-A1-infected bec INNA-X-treated细胞。然而,大小和数量在未经治疗的抗病毒基因表达的上调高,RV-A1-infected细胞相比INNA-X处理样品(图5 b)。调节基因的完整列表中辅助数据文件S2。
INNA-X治疗在体外增加抗病毒基因表达通路在人类支气管上皮细胞分化的文化。)动力学上调基因(由Nanostring >三倍)后从健康捐献者分化bec RV-A1 INNA-X之前感染治疗。b)免疫浓缩(差异基因的数量和大小)治疗后INNA-X和/或感染RV-A1,由Nanostring与列出的十大高表达基因在轴。数据被过滤Benjamini Yekutieli纠正p值< 0.05。n = 5个重复。
IFN-λ与加速应对INNA-X治疗后鼻病毒
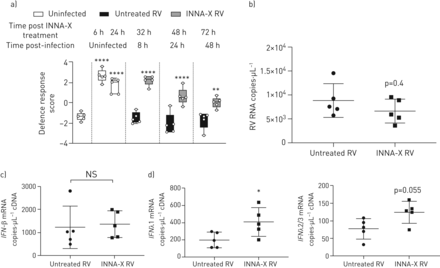
Nanostring-based通路分析确定“防御反应”分数增加(24基因;表S2在INNA-X-treated bec)。增加防御反应分数影射的细胞无毒性6 h和24小时post-INNA-X治疗,翻译在RV-A1感染增强防御反应。相比之下,没有净增加国防在未经处理的分数明显RV-A1-infected细胞突出治疗的潜力增加bec的先天免疫反应(图6)。这翻译对感染更有效的应对;8 h后感染仍有加强防御反应分数INNA-X细胞治疗是降低病毒载量(这个时候图6 b)。
INNA-X治疗在体外增强防御反应途径得分和早期上皮IFN-λRV-A1感染的反应。)时间表显示丰富防御反应分数(定义为Nanostring先进的基因表达分析平台)INNA-X治疗后6 - 24小时后在INNA-X INNA-X治疗和细胞治疗,8、24和48 h后感染,分化bec从健康的捐赠者。RNA表达在b) RV-A1 8 h后感染,c) IFN-β,d) IFN-λ1 IFNλ2/3。n = 5,意味着±sd(罪犯)。数据分析通过单向方差分析Holm-Sidak多个分析(a)或校正的曼惠特尼测试(罪犯)。*:p < 0.05;* *:p < 0.01;* * * *:p < 0.0001相比,相关的治疗控制。
类型I / III干扰素并不包括在“防御反应”通路基因集,我们也使用qPCR量化这些独立相关基因。IFN-β信使rna不是INNA-X治疗后持续上调的RV-A1感染(图6 c)。相比之下,IFN-λ1表达显著增加了INNA-X治疗和附近显著增加(p = 0.055)IFN-λ2/3表达式(图6 d)。
我们也评估INNA-X治疗感染的疗效的主要组鼻病毒株RV-A16 ALI-differentiated主要从健康捐献者人类bec, CR-expanded为n = 5重复提供足够的细胞。INNA-X治疗显著抑制RV-A16 48 h后病毒载量(图7)。再一次,没有upregulationIFN-β观察mRNA在24 h post-INNA-X治疗以及感染后(图7 b),而IFN-λ1和IFN-λ2/3表达显著增加了INNA-X治疗(INNA-X影射)以及24小时后感染(图7 c)。INNA-X治疗也显著增加isg的表达式viperin在24小时后感染OAS18 h后感染,有增加的趋势PKR指出在24小时后感染(图7 d)。
INNA-X治疗在体外降低病毒载量和增强早期上皮IFN-λRV-A16感染的反应。RV-A16 RNA的表达),b) IFN-β,c) IFN-λ基因表达在8 - 24小时后感染分化bec从健康捐献者(箱线图显示值和百分位数5% - -95%)。d) RNA的表达isg (Viperin、OAS1 PKR) 8 - 24小时后感染。数据分析通过双向方差分析Holm-Sidak多个分析(a)或校正的曼惠特尼测试(罪犯)。*:p < 0.05;* *:相比p < 0.01相关未经处理的控制。n = 5个重复。
INNA-X提高抗病毒反应RV-infected bec的哮喘患者
我们之前开发的低MOI RV-A1-infection模型使用bec隔绝捐助者与哮喘,这确定延迟RV-induced抗病毒免疫反应超出24小时后感染,与文化从健康对照组相比32]。我们应用该模型来确定INNA-X治疗也有效地抑制RV-A1感染,在固有的先天免疫缺陷的背景下(即。哮喘)。INNA-X治疗分化BEC文化来源于八个捐助者与哮喘并不影响障碍函数(图S6b)。预处理与INNA-X显著降低病毒载量在48小时后感染,而未经处理的控制(图8)。增加IFN-β表达的不是一个特性INNA-X反应在24小时处理后的细胞无毒性(图8 b)。然而,INNA-X预处理增加IFN-β水平8 h后RV感染/模拟感染,这进一步增加了24小时后感染/模拟感染(图8 b)。正如之前报道的(32),未经治疗的哮喘捐助者RV-infected bec未能诱导IFN-β24 h感染后(图8 b)。INNA-X预处理显著增加类型III IFN-λ1和IFN-λ2/3基因表达,促进了RV-A1 IFN-λ响应。INNA-X也增加了在感染后24 h IFN-λ1表达的细胞无毒性。单独感染没有诱导IFN-λ基因表达在未经处理的细胞(图8 c)。增强IFN-λ表达式8 h INNA-X治疗后没有对应显著增加IFN-λ蛋白质生产96 h后感染(图8 d),这表明低级,早期的表达式(而不是长期IFN-λ生产)与INNA-X治疗的保护作用有关。INNA-X治疗导致isg的重要表达viperin和OAS1,增加的趋势PKR、8 h后感染RV-A1-infected文化,而未经处理的,RV-A1-infected细胞没有显著的响应(山图8 e)。
INNA-X治疗在体外启动阻力RV-A1感染哮喘捐助者在人类支气管上皮细胞分化。IFN-βRV-A1 RNA的表达),b),和c)基因表达IFN-λ0 8和24小时后感染,和d)在顶端上层清液蛋白质含量在96 h后感染。e) isg (Viperin OAS1 PKR) RNA表达8 h后感染。n = 8捐助者与持久的中度至重度哮喘,中位数(四分位范围)(a)或箱线图显示值和5% - -95%百分位数(中)。数据分析通过双向方差分析Bonferroni调整(a),弗里德曼测试邓恩的修正((罪犯)用星号)或魏克森讯号等级测试(#,未受感染的比较)。* *:*:p < 0.05, p < 0.01, * * *: p < 0.001弗里德曼(通过测试)相比,未经处理的控制。#:p < 0.05相比,未经处理的控制通过魏克森讯号等级测试。
讨论
细胞表面通常,比如TLR2,识别各种各样的微生物分子和有越来越多的证据表明,细胞表面通常由病毒被激活。这使我们调查TLR2刺激能否促进呼吸道上皮RV感染的免疫反应。
目前的研究提供了三个重要的发展。首先,我们表明,单一剂量的INNA-X治疗能促进抵抗病毒感染至少7天。我们提供的证据表明,这种影响是通过促进快速和持续的先天免疫激活。其次,我们提供证据表明INNA-X-induced保护RV-A1感染时维护管理结合ICS(特别是丙酸)。最大风险的患者团体RV-induced呼吸道疾病(如。患有哮喘和慢性阻塞性肺病)通常是处理日常维护ICS (33),和ICS治疗(包括卡松丙酸)抑制抗病毒和抗菌免疫(13,34,35]。事实上,我们观察到ICS治疗TNF-αINNA-X-enhanced水平降低,IFN-βIFN-λ,在不改变保护RV感染。这是证据,INNA-X ICS治疗可能是一种有效的附加疗法通过支持抗病毒免疫,而无需增加干扰素生产。第三,INNA-X-mediated保护是实现哮喘donor-derived上皮细胞培养。内在缺陷上皮先天免疫在哮喘与易受病毒感染(20.- - - - - -22),我们已经表明在一定程度上是由于上皮细胞内在延迟先天免疫反应(32]。我们从哮喘捐助者未能确认bec干扰素的诱导表达感染后的24小时(32]。然而,预处理INNA-X影射上皮细胞应对RV-A1和显著增加表达IFN-β和IFN-λ。这是与RV-A1病毒载量下降有关。
INNA-X治疗的持续时间影响我们观察到的结果是一致的,T一个et al。(18),观察到增强小鼠流感间隙TLR2受体激动剂治疗7天前第一次感染和我们(我们的知识)表明,这是由于持续的低级先天免疫激活,导致一个增强/加速应对病毒感染和病毒载量下降(即。“先天免疫启动”)。为了更好地理解时间的影响,我们比较预处理感染之前天感染前7天。这个确定了两种机制的行动取决于时机INNA-X管理相对于病毒感染。治疗7天前RV-A1感染免疫基因表达降低肺组织的大小,而独自RV-A1感染。相比之下,治疗之前天感染导致了anti-RV健壮的浓缩的基因参与反应。尽管不同的对基因表达的影响,治疗时间明显抑制病毒载量。我们得出这样的结论:当RV感染不发生后立即受体激动剂治疗(约天)内,呼吸道粘膜是影射通过chemokine-mediated招聘的淋巴细胞,调节对房车的保护性反应。支持,免疫基因表达的上调大9天后处理为期3天的治疗后相比,符合所需的时间建立的粘膜淋巴细胞网络支持持久保护(36]。此外,与淋巴细胞调控相关的基因增加INNA-X早些时候治疗后如。BTLA [37]和ICOSL [38])。符合这一点,升高后,淋巴细胞的数量都观察到INNA-X治疗气道灌洗。此外,TLR2受体激动剂治疗为期3天前感染PR8(高度致命的流感病毒在小鼠)增加单核细胞、巨噬细胞、中性粒细胞和树突细胞数(39),强调长期先天免疫细胞介导的重要性启动保护自己不受病毒感染。
与分化的作用机制实验BEC文化来源于健康的捐赠者,INNA-X治疗引发的低级先天免疫激活RV感染之前,NF-κB-regulated基因的上调和RV感染的快速反应。这个反应是由两个截然不同的先天免疫激活的聚类分析。INNA-X单独治疗NF-κB-regulated基因的表达增加编码细胞因子(如。IL-1β)趋化因子(如。处于CXCL2) (40]和抗菌分子(如。IDO1 [41),calprotectin / S100A8-S100A9 [42随后])和这些基因调节前8 h后RV-infection INNA-X治疗。在未经处理的早期反应是完全没有,RV-infected细胞。第二波发生24 - 48 h后INNA-X治疗感染细胞和丰富了干扰素刺激基因的表达(isg)。很明显,48 h后感染,治疗细胞上调基因(由isg)比INNA-X-treated细胞,这些基因上调到更高的程度。基因表达的下降级INNA-X治疗细胞也在伊拉克研究小组观察到集群的热图的数据。我们认为这可能观察结果从降低病毒载量INNA-X后24 h后感染开始治疗,导致IFN-mediated末的活化反应下降。总的来说,数据是一致的一个INNA-X-induced早期启动免疫反应,导致对RV-A1加速反应,一个小群,低密度脂蛋白受体(LDLR)绑定亚型。INNA-X治疗bec是暂时性的增加ICAM-1基因表达促使调查主要集团RV-A16 (ICAM-1绑定)。RV-A16感染后,我们也观察到抑制病毒载量与增强III型干扰素和研究小组反应(Viperin和美洲国家组织),确认INNA-X功效对一个主要组(ICAM-1绑定)RV亚型。
Myristoylated(最高产量研究)房车衣壳VP4与TLR2和诱发炎性细胞因子基因表达(43]。我们没有看到rhinovirus-induced TLR2在未经处理的细胞激活8 h后感染,建议低感染复数在我们的研究可能限制早期暴露于病毒MyrVP4这样是不足以激活TLR2。INNA-X-mediated TLR2 TLR2激活启动可能降低了阈值,这样低级MyrVP4暴露在感染早期现在能够刺激先天免疫。我们也观察到调节表达TLR2本身基因表达评估(NF-κB蓝色集群2;图4),这可能会影响激活的门槛。支持,由INNA-X NF-κB基因签名上调也增强应对RV感染表明INNA-X和房车是激活一个常见的先天免疫网络。
其他呼吸道病毒有可能服从上皮细胞表面,TLR-primed先天免疫抵抗。例如,阻塞的TLR2受体集群分化14 (CD14)抑制流感免疫介质生产由单核细胞和巨噬细胞(44),我们已经报告了抵御流感病毒感染小鼠接受TLR2受体激动剂(18,39]。呼吸道合胞病毒(RSV)结合TLR4诱导早期NF-κB-mediated肺部先天免疫(45)和LPS激活TLR4-TRIF途径预防H5N1流感病毒感染(46]。冠状病毒的数据不太清楚,不过老鼠缺乏TLR4更容易引起老鼠的鼠科动物冠状病毒肝炎(47]。因此,现在有大量的证据支持的调查INNA-X的能力'气道上皮先天免疫对多个临床重要呼吸道病毒。
我们一直观察到早期的、低层次的老年病III型干扰素基因编码IFN-λ1 IFN-λ2/3,而不是I型(IFN-β)bec的健康的捐赠者和哮喘患者。虽然我型和III型干扰素抗病毒免疫作用是众所周知的通过endosomal TLR激活,现在越来越清楚的是,III型干扰素也可以诱导细胞表面,bacteria-sensing通常有一个重要的功能在上皮屏障和先天免疫内稳态48]。从临床/ host-fitness角度来看,早期的低级IFN-λs表达式与旷日持久,高级表达式类型的I / III干扰素是可取的和象征的更有效率,早期感染的控制。这个概念是优雅由G阿兰尼人et al。(49),使用流感感染研究表明IFN-λs第一干扰素生产和支撑气道上皮前线保护。
总之,我们表明,预防肺上皮细胞激活TLR2质数先天免疫,增强应对RV感染(主要和minor-group病毒)。这一改进的上皮细胞的能力迅速应对和控制病毒感染,和时间允许招聘相关的淋巴细胞感染和气道炎症的长期保护。
补充材料
可共享的PDF
确认
我们要感谢简读和克里斯蒂Nichol优先研究中心的健康的肺,纽卡斯尔大学和猎人医学研究所,与细胞培养协助维护。我们感谢马蒂鲍曼和米歇尔McGloin优先研究中心的健康的肺,纽卡斯尔大学和猎人医学研究所,对样品处理和分子技术的贡献参与生成qPCR和ELISA数据。我们感谢的管理人员重点研究中心(中国)健康的肺和生物猎人医学研究所的工作人员和纽卡斯尔大学提供实验室空间,基础设施和工作环境。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:j . Girkin所有鼠标和nanostring实验进行数据分析和解释执行,画数据,起草和编辑手稿和概念设计的手稿。的。厕所进行细胞培养实验,协助分析,解释和细胞培养实验和制图协助起草手稿。c . Esneau进行细胞培养实验和分子辅助分析。协助数据解释和起草/ s Maltby编辑稿件。f·麦克利参与实验设计,项目管理,数据解释和编辑稿件。b . Chua导致实验设计,解读nanostring分析和编辑了手稿。C.L. Grainge A.T.里德、pc Veerati和贡献资源和专长为实验平台使用有条件地“重编程”的细胞。P.A.B.华克贡献ALI-differentiation平台和支气管上皮细胞和概念提供输入。d .骑士和d·杰克逊提供概念性的输入和设计和回顾了手稿。 C. Demaison, F. Mercuri, D. Jackson and N.W. Bartlett designed the study, performed data interpretation, edited and finalised the manuscript and secured the funding and resources that made this study possible. N.W. Bartlett also supported figure development and had significant input into data interpretation.
利益冲突:j . Girkin报告拨款,个人费用咨询和非金融支持旅游会议从Ena疗法企业有限公司,在进行研究;,PCT专利/ AU2018/050295发布。
利益冲突:的。厕所报告赠款Ena疗法,在进行这项研究的。
利益冲突:c . Esneau没有披露。
利益冲突:美国Maltby没有披露。
利益冲突:f·麦克利Ena疗法的员工,和有PCT专利/ AU2018/050295待定,PCT专利/ AU2011/001225发布。
利益冲突:b .蔡是Ena疗法的创始人之一和股东企业有限公司
利益冲突:A.T.里德没有披露。
利益冲突:pc Veerati没有披露。
利益冲突:中一段Grainge没有披露。
利益冲突:P.A.B.华克没有披露。
利益冲突:d骑士报告从勃林格殷格翰集团资助,在提交工作。
利益冲突:d·杰克逊是Ena疗法企业的创始人和股东。有限公司,PCT专利/ AU2018/050295待定,PCT专利/ AU2011/001225发布。
利益冲突:c . Demaison Ena疗法的员工,和有PCT专利/ AU2018/050295待定,PCT专利/ AU2011/001225发布。
利益冲突:西北Bartlett报告拨款,个人费用咨询公司和其他从Ena疗法(股票期权),在进行研究;PCT专利/ AU2018/050295发行。
支持声明:这项工作是资助在纽卡斯尔大学的伙伴关系和Ena疗法企业有限公司结合创新连接澳大利亚政府的拨款,工业部门,创新和科学。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2020年5月5日。
- 接受2020年11月27日。
- 版权©2021人队。生殖权利和权限接触权限在}{ersnet.org