文摘
背景快速测试来评估严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)您迫切需要破译t细胞反应诱发的免疫保护性免疫和援助监控。
方法使用快速全血化验需要少量的血,我们测量定性、定量SARS-CoV-2-specific CD4 t细胞反应在31个医务工作者使用流式细胞仪。
结果100%的COVID-19恢复期的参与者显示检测SARS-CoV-2-specific CD4 t细胞反应。SARS-CoV-2-responding细胞也发现40.9%的参与者没有COVID-19-associated PCR-negative症状或测试。表型的评估表明,在COVID-19恢复期的参与者,SARS-CoV-2 CD4反应能力有限的内存显示早期分化表型产生干扰素(IFN) -γ。相反,在参与者没有症状,报道SARS-CoV-2 CD4反应在后期分化细胞丰富,coexpressing IFN-γ和肿瘤坏死factor-αGranzyme B。
结论这个概念验证研究提供了一个可伸缩的替代外周血单核细胞化验枚举和表型SARS-CoV-2-responding t细胞,因此代表了一个实用工具,适应性免疫监视由于自然感染或疫苗试验。
文摘
这个概念验证研究表明SARS-CoV-2 t细胞反应很容易使用快速检测全血测定要求最小的血容量。这样的试验中代表一个合适的工具来监控适应性免疫疫苗试验。https://bit.ly/3yZHtcL
介绍
爆发的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)感染(导致疾病称为COVID-19),第一次出现在武汉,中国,2019年12月,2020年3月12日被宣布为全球大流行,影响世界上的所有国家,包括非洲的1]。有迫切需要更好地理解临床表现和发病机制SARS-CoV-2为了开发相关工具,包括诊断、治疗和疫苗,停止疾病的传播,以及战略管理得最好这种疾病在所有人群。
COVID-19的临床范围很广,从无症状到轻微的流感样症状严重肺炎和死亡。理解什么是免疫保护SARS-CoV-2是预测长期的免疫力和告知疫苗的关键设计。虽然大部分重点一直放在b细胞和抗体反应,目前尚不清楚什么类型的免疫反应所带来的保护SARS-CoV-2 [2]。一些研究显示,t细胞反应SARS-CoV-2发病机制中可能发挥重要作用和报告表明病人缺乏b细胞可以恢复从SARS-CoV-2感染进一步突出t细胞免疫的可能的重要性(3,4]。此外,越来越多的证据表明,预先存在的存在,可交叉反应的记忆t细胞特有的感冒冠状病毒可能影响易感性SARS-CoV-2感染和部分解释COVID-19[的明显不同的临床表现5- - - - - -8]。
高效、灵敏、简单的评估人类t细胞免疫仍然是一个挑战。最常用的t细胞化验需要隔离的外周血单核细胞(PBMCs),需要大量的血。因此,全血化验可能比PBMC-based更有利的方法大大减少血容量(∼1毫升),使其更适用于儿科人群。等化验迅速,此外,它们不需要细胞分离,并保持生理细胞和可溶性环境,更好地模仿人类血液的条件。在这里,我们报告一个快速(∼7 h)整个blood-based SARS-CoV-2-specific t细胞反应的检测方法与简单的步骤,可以适应资源有限的情况下。这个快速适用的测定可以代表一个容易standardisable工具来评估SARS-CoV-2-specific适应性免疫监视t细胞反应的疫苗试验,了解什么是保护性反应或定义的患病率SARS-CoV-2 t细胞反应全民。
方法
研究人群
人口研究由医务工作者(卫生工作者)(n = 31日29%男性)招募了2020年7月和9月之间Groote Schuur医院在开普敦,受灾最严重地区的初始COVID-19流行在南非(9]。参与者根据1)机密报告COVID-19-associated症状,2)是否SARS-CoV-2 RNA PCR从鼻和咽拭子进行3)SARS-CoV-2 PCR的结果。根据这些标准,参与者被分为三组:1)人没有COVID-19-associated症状(n = 15), 2)测试人员报告症状但SARS-CoV-2 PCR-negative (n = 7),和3)人COVID-19-associated症状和测试SARS-CoV-2 pcr阳性(n = 9) (表1)。在所有组中,暴露于COVID-19病人相当(86.8 -100%)。所有的参与者与PCR-confirmed COVID-19有轻微的症状,不需要住院。血液样本得到的平均7.3周post-SARS-CoV-2测试人员与负面测试结果和4.7周那些确认阳性结果(p = 0.09)。所有与会者都无症状时取样。在四个SARS-CoV-2 pcr阳性的参与者,第二个样本1月后获得的。开普敦大学健康科学学院人类研究伦理委员会批准了这项研究(HREC 207/2020)和书面知情同意是获得所有的参与者。
在等离子体测量SARS-CoV-2 nucleocapsid-specific免疫球蛋白
测量SARS-CoV-2-specific抗体进行使用Elecsys Anti-SARS-CoV-2免疫测定(罗氏诊断、巴塞尔、瑞士)。这种半定量的电化学发光免疫测定措施SARS-CoV-2 nucleocapsid-specific免疫球蛋白。试验是由南非国家卫生实验室服务系统和解释根据制造商的指示(罗氏:版本1.0 2020 - 05)。结果报告为数值的形式截止指数(COI)(信号样本/截止),一个COI < 1.0对应不反应的等离子体和COI⩾1.0对应活性等离子体。在14天post-SARS-CoV-2 PCR证实,敏感性和特异性的Elecsys Anti-SARS-CoV-2免疫测定已被报道为99.5% (95% CI 97.0 - -100.0%)和99.80% (95% CI 99.69 - -99.88%),分别为(10- - - - - -12]。
SARS-CoV-2 pseudovirus中和试验
患者血浆评估SARS-CoV-2中和活动使用SARS-CoV-2 pseudovirus感染试验。根据艾滋病案例- - -用单循环传染性SARS-CoV-2假病毒颗粒的骨干SARS-CoV-2峰值蛋白质表达和萤火虫荧光素酶记者被生产hek - 293 tt细胞(13,14)质粒的cotransfection pnl4 - 3. -卢克。re / (arp - 3418;美国国立卫生研究院艾滋病试剂项目,日耳曼敦,医学博士)和pcDNA3.3-SARS-CoV-2-spikeΔ18 [15]。hek - 293 tt细胞培养上清液含有病毒粒子是收获3天post-transfection和孵化heat-inactivated病人血浆在5倍连续稀释60分钟37°C。等离子体/ pseudovirus混合物被用于转染hek - 293 t细胞稳定表达血管紧张素转换酶2受体(16]。细胞被感染后细胞溶解3天使用Promega细胞培养细胞溶解试剂(美国Promega生物科学,圣路易斯奥比斯波,CA)和荧光素酶活动的评估使用GloMax Explorer多模标(Promega生物科学)与荧光素酶检测系统(Promega生物科学)。
整个blood-based t细胞检测试验
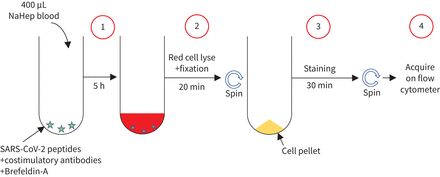
血液收集肝素钠管在3 h的收集和处理。整个blood-based SARS-CoV-2-specific t细胞检测化验是改编自先前报道的全血胞内细胞因子检测旨在量化分析结核分枝杆菌特殊t细胞在血液的小卷17]。然而,重大的修改,包括降低孵化时间和固定缓冲区的使用允许同时裂解红细胞简化处理时间,导致更快的收购的结果(18]。这里,我们适应这个化验检测SARS-CoV-2-specific t细胞使用合成SARS-CoV-2 PepTivator肽(Miltenyi研究,沃金,英国),包括15 mer序列11-amino-acid重叠覆盖的immunodominant部分蛋白质,和完整的核衣壳和膜蛋白的序列。肽都是结合在一个池,用于最终µg·1毫升的浓度−1。的工作流分析提出了图1。简单地说,400年µL全血与SARS-CoV-2上涨刺激,核衣壳和膜蛋白肽池在37°C 5 h的costimulatory CD28抗体和CD49d(1µg·毫升−1每一个;美国BD生物科学,圣何塞,CA)和Brefeldin-A(µg·10毫升−1;Sigma-Aldrich,圣路易斯,密苏里州,美国)。如果血液孵化与costimulatory抗体,Brefeldin-A和二甲基亚砜(DMSO)的克分子数相等的金额。红细胞裂解和白色细胞固定就表现为一个单一的步骤使用转录因子固定缓冲区(美国eBioscience,圣地亚哥,CA) 20分钟。在这个阶段细胞冻存冻结媒体(RPMI 50%胎牛血清,40%和10% DMSO)并存储在液态氮到批处理分析。
示意图显示方法和工作流的全血化验检测严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)特殊的适应性免疫反应。步骤1:400年µL heparinised (NaHep)全血培养5 h在存在SARS-CoV-2-specific肽池costimulatory抗体的存在(即。CD28和CD49d)和Brefeldin-A。步骤2:细胞培养20分钟在存在转录因子固定缓冲区,导致红细胞的同时溶解和细胞固定。步骤3:细胞染色为30分钟的优化面板fluorophore-labelled抗体。步骤4:样品获得流式细胞分析仪。控制样品处理类似的工作流没有SARS-CoV-2-specific肽池。
细胞染色进行冻存细胞解冻,洗和permeabilised转录因子烫/洗缓冲区(eBioscience)。细胞被染色在室温下30分钟对CD3抗体BV650, CD4 BV785, CD8 BV510, CD45RA Alexa 488年CD27 PE-Cy5, CD38 APC, HLA-DR BV605, ki - 67 PerCP-Cy5.5 PD-1 PE、Granzyme B (GrB) BV421干扰素(IFN) -γBV711,肿瘤坏死因子(TNF) -αPE-Cy7和白介素(IL) 2 PE /炫594,详细补充表S1。样本获得的BD LSR II流式细胞分析仪,分析使用FlowJo版本9.9.6(美国FlowJo、亚什兰或)。积极的回应被定义为任何细胞因子反应至少两次,如果细胞的背景。定义SARS-CoV-2-specific CD4 t细胞的表型,截止30事件使用。提供的控制策略补充图S1。
统计分析
进行图形化表达在棱镜版本8.4.3(美国GraphPad,圣地亚哥,CA)和JMP版本14.0.0 (SAS研究所卡里、数控、美国)。在棱镜进行了统计检验。非参数测试是用于所有的比较。克鲁斯卡尔-沃利斯检验邓恩的多重比较检验被用于多个比较,和Mann-Whitney Wilcoxon配对测试是用于无与伦比的和配对样本,分别。
结果
血清学评估SARS-CoV-2敏化作用
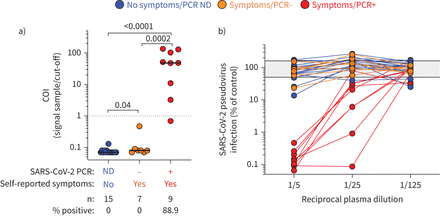
即使实时一最具体的技术检测急性SARS-CoV-2感染,积极率迅速下降只要10天post-symptom发病,尤其是患有轻度COVID-19 [19,20.]。因此,血清学检测提供了重要补充RNA测试来识别个人被SARS-CoV-2敏感。因此,评估潜在SARS-CoV-2敏化作用的参与者没有SARS-CoV-2 PCR测试执行或测试PCR-negative, SARS-CoV-2-specific抗体的存在(如。SARS-CoV-2 nucleocapsid-specific免疫球蛋白)测量和SARS-CoV-2 pseudovirus中和试验也在所有参与者中执行。在所有参与者积极SARS-CoV-2 PCR测试展出在体外anti-SARS-CoV-2中和活动和8的9(88.8%)检测到SARS-CoV-2 nucleocapsid-specific免疫球蛋白,没有一个参与者测试呈阴性反应的或没有进行PCR检测阳性SARS-CoV-2 nucleocapsid-specific免疫球蛋白(图2一个)或显示强劲的在体外anti-SARS-CoV-2活动(图2 b)。总的来说,这些结果证实pcr阳性参与者已被感染SARS-CoV-2和安装病毒的免疫反应。对于其他参与者,很难确定它们SARS-CoV-2感染状态。一方面,缺乏抗体反应和中和活动可能表明他们没有SARS-CoV-2-infected。另一方面,由于其高水平的SARS-CoV-2曝光,我们不能完全排除SARS-CoV-2感染,虽然少见,患者COVID-19-confirmed阴性抗体结果报告(21]。
严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)血清学评估。的)量化SARS-CoV-2 nucleocapsid-specific抗体使用Elecsys化验表示为一个截止指数(COI)(信号样本/截止)。参与者分组根据其临床特点。中位数(黑条)所示。虚线显示制造商的截止值的积极性。使用Mann-Whitney t检验进行统计比较;假定值显示。b) SARS-CoV-2 pseudovirus中和活动。案例- - -用SARS-CoV-2假病毒颗粒与连续稀释病人pre-incubated等离子体被用来感染血管紧张素转换酶2-expressing hek - 293 t细胞。荧光素酶活性作为感染的测量评估3天感染后和结果表示为感染与控制(未经处理的病毒粒子,灰色阴影区域),设定为100%。 ND: not done.
SARS-CoV-2-responding CD4 t细胞大小和功能的状况
在31日参与者测试中,58% (n = 18)有一个检测SARS-CoV-2-specific CD4 t细胞反应(产生任何测量细胞因子:IFN-γ,TNF-α或- 2)使用全血测定描述(图3一)。然后我们定义的大小和表型SARS-CoV-2-specific CD4反应根据参与者的临床特点(图3 b和c)。所有的卫生工作者自我报告的症状和SARS-CoV-2 pcr阳性测试(n = 9)被发现SARS-CoV-2-specific CD4 t细胞(中位数(差)频率0.4% (0.28 -0.65%))(图3 c)。值得注意的是,SARS-CoV-2-specific CD4 t细胞的频率没有联系的大小SARS-CoV-2 nucleocapsid-specific免疫球蛋白(p = 0.64, r =−0.18)或等离子体中和活动(p = 0.46, r = 0.28)(数据没有显示)。有趣的是,在参与者没有检测到SARS-CoV-2 nucleocapsid-specific免疫球蛋白或中和抗体活性,与自我报告的症状,3的7(43%)检测到SARS-CoV-2-responding CD4 t细胞(中位数(差)的反应者0.02%(0.019 -0.03%))和六15(40%)的自我报告的症状都没有检测到SARS-CoV-2-responding CD4 t细胞(中位数(差)的反应者0.15% (0.05 -1.47%))。此外,SARS-CoV-2-specific CD8 t细胞反应中也观察到六的九SARS-CoV-2 pcr阳性参与者(66.7%)。参与者报告没有症状(n = 15),只有一个人有一个检测CD8响应和没有PCR-negative参与者(n = 7)表现出可检测SARS-CoV-2-specific CD8 t细胞反应(数据未显示)。
大小和功能的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)特殊CD4 t细胞。比例)的参与者表现出一种检测SARS-CoV-2-specific CD4 t细胞反应。b)代表的例子肿瘤坏死因子(TNF) -α和干扰素(IFN) -γ生产SARS-CoV-2肽CD4 t细胞的反应池。c)级SARS-CoV-2-specific CD4 t细胞反应(表示为一个百分比的总CD4 t细胞)在参与者分组根据其临床特点。参与者的数量和比例的反应提出了每组底部的图。进行了统计比较利用克鲁斯卡尔-沃利斯检验;假定值显示。d)每组SARS-CoV-2-specific CD4 t细胞的多官能的档案。的x设在显示每个组合的构成与黑色圆圈表示IFN-γ的存在,白介素(IL) 2和TNF-α。中位数(黑条)所示。每个组合都是彩色编码和数据总结在饼图,其中每个饼片表示中位数每个组合总SARS-CoV-2响应的贡献。弧识别TNF-α的贡献,和IFN-γSARS-CoV-2 - 2反应。Wilcoxon等级和测试是用来比较组间响应模式和统计饼图使用排列定义测试之间的差异;假定值显示。ND:没有完成。
接下来,我们定义了多官能的形象SARS-CoV-2-responding CD4 t细胞根据其能力coexpress - 2, IFN-γ或TNF-α(图3 d)。SARS-CoV-2-specific pcr阳性细胞的整体功能概要参与者截然不同,参与者没有报道症状(p = 0.0002)。事实上,SARS-CoV-2-specific CD4反应pcr阳性参与者被IFN-γ有限表达特征,并富含细胞coexpressing和TNF-α- 2。相反,在参与者报告没有症状,大多数SARS-responding CD4细胞分布之间的三重功能细胞(2+IFN-γ+TNF-α+)和细胞合拍影片IFN-γTNF-α。总的来说,在这个分析,TNF-α主要细胞因子产生,其生产与2相比显著提高(p = 0.0026)和IFN-γ(p < 0.0001) (补充图S2)。
SARS-CoV-2-responding CD4 t细胞的表型评估
而提出的分析可以使用有限的抗体进行小组识别SARS-CoV-2-responding t细胞的频率,通过仅仅测量细胞因子的生产,使用更广泛的抗体面板还允许这些细胞的表型概要文件的定义。为此,我们包括额外的标记来评估内存分化(CD27和CD45RA),细胞毒性潜在(GrB)和激活配置文件(CD38、HLA-DR ki - 67或PD-1) SARS-CoV-2-responding CD4 t细胞。
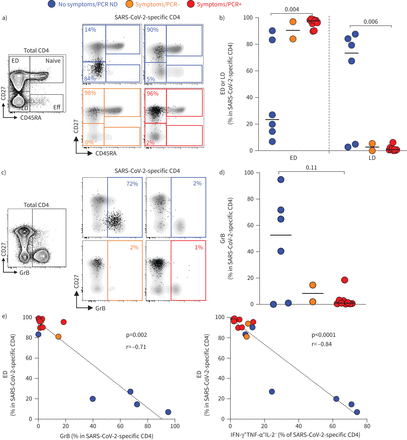
图4一和b显示在所有患者症状,SARS-CoV-2-specific CD4 t细胞显示几乎全部(平均97.7%)早期分化内存表型(艾德:CD45RA−CD27+)。相反,在四个六卫生工作者没有症状,SARS-CoV-2-specific CD4 t细胞表现出主要后期分化表型(LD: CD45RA−CD27−)。
内存分化概要和Granzyme B (GrB)表达在严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)特殊CD4 t细胞。)代表SARS-CoV-2-specific CD4 t细胞记忆差异化配置文件的例子基于CD45RA和CD27的表达。右边的流图显示了天真的分布(CD45RA+CD27+),早期分化(艾德:CD45RA−CD27+),后期分化(LD: CD45RA−CD27−)和效应(Eff: CD45RA+CD27−总CD4 t细胞)细胞。图b)总结的ED的比例和LD SARS-CoV-2-specific CD4 t细胞在每组。进行了统计比较利用克鲁斯卡尔-沃利斯检验;假定值显示。c)代表总共伽马线暴表达式的例子和SARS-CoV-2-specific CD4 t细胞。d)总结伽马线暴图表达SARS-CoV-2-specific CD4 t细胞在每组。进行了统计比较利用克鲁斯卡尔-沃利斯检验;假定值。e)的比例关系ED SARS-CoV-2-specific CD4 t细胞和伽马线暴表达式或IFN-γ的比例+TNF-α+- 2−SARS-CoV-2-specific CD4 t细胞。相关性是由双尾非参数测试的斯皮尔曼等级测试。ND:没有完成;干扰素:干扰素;肿瘤坏死因子:肿瘤坏死因子;IL:白介素。
当CD4 t细胞细胞毒性的作用仍不清楚,这些细胞的存在被描述在几个病毒感染(22]。我们因此测量伽马线暴SARS-CoV-2-responding CD4 t细胞的表达。虽然伽马线暴SARS-CoV-2-specific CD4 t细胞中几乎没有可检测pcr阳性参与者,伽马线暴表达升高4的6个参与者没有症状(图4 c和d)。此外,ED SARS-CoV-2-responding CD4 t细胞的比例负相关伽马线暴表达(p = 0.002, r =−0.71) IFN-γ的比例和TNF-αdual-producing细胞(p < 0.0001, r =−0.84) (图4 e)。的表型特征GrB-expressing SARS-CoV-2-responding CD4 t细胞(即。高度分化,产生IFN-γ和TNF-α)同意最近的一份报告中描述巨细胞病毒(CMV)特殊CD4细胞毒性t淋巴球t细胞(23]。
确定整个表型的SARS-CoV-2-responding CD4 t细胞允许歧视的参与者根据他们的临床特点,我们进行了分层聚类分析(图5一个)和主成分分析(图5 b),包括四个参数(即。的比例IFN-γ+TNF-α+- 2+和IFN-γ−TNF-α+- 2+细胞,ED的比例,和伽马线暴表达式)。分析表明,参与者报告没有症状和阴性SARS-CoV-2抗体分离显然从pcr阳性的参与者。相反,PCR和SARS-CoV-2 antibody-negative卫生工作者报告症状不能分开PCR阳性的参与者。加载图显示,伽马线暴表达式和triple-positive细胞的比例是主要的驱动程序允许参与者的隔离没有症状和负面报道SARS-CoV-2抗体(图5 c)
表型特征的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)特殊IFN-γ+CD4+根据临床特点t细胞。一)Nonsupervised双向分层聚类分析(病房方法)使用四个表型参数(即。的比例IFN-γ+TNF-α+- 2+和IFN-γ−TNF-α+- 2+细胞,ED的比例,从SARS-CoV-2-specific CD4 t细胞和伽马线暴表达式)。每一列表示一个参与者根据其临床特点,颜色由一个圆圈表示的系统树图。参与者的积极或消极SARS-CoV-2血清学试验。数据描绘成一个热图从最小到最大的为每个参数值。b)主成分分析的相关性,来自三个参数进行了研究。每个数据点代表一个参与者。两个轴代表主成分1 (PC1)和2 (PC2)。他们贡献的总方差数据显示为一个百分比。c)加载图显示每个参数如何影响PC1和PC2值。ND:没有完成; Ab: antibody; IFN: interferon; TNF: tumour necrosis factor; IL: interleukin.
最后,作为活化标志物的表达(CD38、HLA-DR ki - 67或PD-1)抗原t细胞是指示性活跃的感染(24,25),我们定义这些标记SARS-CoV-2-responding CD4 t细胞上的表达。没有观察到显著差异的测量标记在不同群体中,尽管一些异常值观察pcr阳性参与者组(图6)。有趣的是,无论参与者的临床特点,PD-1 SARS-CoV-2-responding CD4 t细胞高表达。然后我们定义SARS-CoV-2-specific CD4 t细胞的激活配置文件之间的关系和时间post-PCR-positive测试。图6 b表明,pcr阳性的参与者,CD38的表达与时间post-PCR测试相关(p < 0.0001, r =−0.91),表达CD38在前2 - 3周检测后大幅下降,表明快速清除病原体。类似的协会对所有测试激活标记,观察CD38表达式显示相关性最强的(图6 c)。
严重急性呼吸系统综合症冠状病毒2的激活配置文件(SARS-CoV-2)特殊CD4 t细胞。)CD38、HLA-DR ki - 67和PD-1表达SARS-CoV-2-specific CD4 t细胞在每组。中位数(黑条)所示。没有观察到显著差异群体之间使用克鲁斯卡尔-沃利斯检验任何标记。b)联系CD38表达SARS-CoV-2-specific CD4 t细胞和时间post-SARS-CoV-2 pcr阳性测试。每个符号代表一个参与者(n = 9)。虚线红线参与者认同纵向样本。相关性是由双尾非参数测试的斯皮尔曼等级测试。c)之间的相关性比较时间post-SARS-CoV-2 pcr阳性试验和不同的表达激活配置文件标记,根据协会的实力排名。斯皮尔曼相关热阻上绘制x设在和相应的页- - - - - -值在每个栏所示。ND:没有完成;小额信贷机构:平均荧光强度。
讨论
在这个概念分析评估的使用一个简单的全血测定测量SARS-CoV-2-specific t细胞反应在小型HCW队列中,我们表明,SARS-CoV-2-specific CD4 t细胞(表达IFN-γ,TNF-α或- 2)很容易检测到在所有测试康复的COVID-19参与者。然而,在那些没有经历任何COVID-19-related症状或测试SARS-CoV-2 PCR-negative(尽管报告症状),22(40.9%)也表现出的可检测SARS-CoV-2-specific CD4 t细胞反应。不过,中值频率SARS-CoV-2-specific CD4 t细胞相比,后者组低∼5倍SARS-CoV-2 pcr阳性的参与者。重要的是,与康复的COVID-19参与者,这些参与者没有症状或测试PCR-negative曾探测SARS-CoV-2 nucleocapsid-specific免疫球蛋白或显示强劲的中和活性。几个假说可以解释SARS-CoV-2-responding细胞的检测没有检测到的抗体反应。当参与者包括在这项研究很可能是高度暴露于SARS-CoV-2由于他们的职业,可以说任何SARS-CoV-2 CD4 t细胞反应生成1)在无症状COVID-19事件没有导致检测抗体反应,2)反映最近接触SARS-CoV-2或3)对应于SARS-CoV-2 CD4 t细胞可交叉反应的记忆。存在的许多研究已经证明SARS-CoV-2-reactive CD4 t细胞在40 - 60%的SARS-CoV-2-unexposed个人在世界各地的不同人群26- - - - - -29日]。此外,重要的是要指出,所有这些研究进行使用PBMCs和令人鼓舞的发现整个blood-based化验使用有限的血液(< 1毫升)产量可比的结果。
进一步分析了多重的和表型的SARS-CoV-2-specific CD4 t细胞显示,无论参与者的临床特点,最普遍的细胞因子检测响应SARS-CoV-2 TNF-α肽。这些观察是按照其他研究指出SARS-CoV-2适应性免疫反应的障碍的特点是低水平的I型和II型干扰素30.,31日]。然而,也有可能我们在这项研究中观察到的有限IFN-γ生产相关的刺激时间短(如。5 h)用于测定。不过,这表明TNF-α可能是一个更可靠的目标比IFN-γ检测SARS-CoV-2-specific CD4 t细胞反应。此外,SARS-CoV-2-responding CD4 t细胞在所有参与者的特点是高架PD-1表达式。这些资料已经观察到急性SARS-CoV-2感染和可能受到持续的病毒复制27,32,33]。表达PD-1抗原记忆t细胞在缺乏急性感染可能是惊人的。然而,取决于他们的特异性抗原记忆t细胞可以显示一个高度变量微分概要文件(34)和维护提升PD-1表情有些特异记忆t细胞(如巨细胞病毒或丙肝病毒)据报道甚至感染后间隙(35- - - - - -37]。此外,最近的出版物显示,PD-1-expressing SARS-CoV-2-specific CD8 t细胞不疲惫但功能康复的COVID-19患者(38]。需要进一步的实验来了解PD-1 SARS-CoV-2-responding CD4 t细胞的表达升高的影响。
最后,SARS-CoV-2-responding CD4 t细胞之间的定性不同恢复期的COVID-19参与者和参与者没有经历COVID-19-associated症状。在前者,SARS-CoV-2-specific CD4 t细胞几乎只显示一个艾德内存表型;在后者,SARS-CoV-2-responsive CD4 t细胞表现出伽马线暴LD记忆表型和丰富。
我们的研究也有一些局限性。我们的结果依赖于少量的参与者和需要在更大的群组研究中进行确认。在缺乏SARS-CoV-2照射对照组低,我们不能猜测SARS-CoV-2-responding CD4 t细胞的特异性检测serology-negative参与者。
此外,技术优化和验证的简化提出分析和测试它的性能。类似的方法使用全血IFN-γ释放试验(干扰素释放),常用的检测结核分枝杆菌感染,最近应用于检测SARS-CoV-2-specific t细胞反应(39]。虽然这两种技术有一个比较成本(∼30 - 40美元),流cytometry-based试验提出了研究低周转时间与干扰素释放(∼7与18 h),但更重要的是我们的方法更加灵活。它可以用来简单地量化SARS-CoV-2-responding CD4和CD8 t细胞(使用最少的色板)监测流行病学研究的t细胞反应的频率或疫苗试验,或被用于更多的探索性工作评估深入SARS-CoV-2-specific t细胞的表型和功能。对于每个检测的敏感性和特异性,并行分析需要的性能进行比较分析。此外,进一步优化应该执行改进的标准化和灵活性提出SARS-CoV-2-specific全血化验,包括使用管包含lyophilised试剂对细胞的刺激,预混抗体细胞染色鸡尾酒和自动控制流分析。另一种替代方法来缓解集合时间和交通的限制,对于资源有限的网站,将直接使用cryopreservative同行全血样品的解决方案,如CryoStor CS10解决方案(40),允许细胞刺激和染色在批处理执行充分装备网站。最后,在这项研究中,细胞刺激进行使用的肽覆盖SARS-CoV-2尖峰,核衣壳和膜蛋白。根据最近的出版物显示,已有的可交叉反应的反应之间的歧视和COVID-19-induced响应依赖于使用的SARS-CoV-2抗原的特异性(41),本研究中使用的肽组合不是杰出的预先存在的可交叉反应的最优从COVID-19-induced SARS-CoV-2-reactive t细胞反应。因此,该试验可能会进一步提高利用更具针对性与定义的特异性肽池SARS-CoV-2或季节性的冠状病毒。
然而,本研究的主要目的是描述的概念,一个快速和灵活的全血化验,需要一个非常有限的血液,这将是一个强大的工具来调查SARS-CoV-2-specific t细胞反应定量和定性甚至在COVID-19儿科病例。
补充材料
可共享的PDF
确认
作者感谢所有的参与者。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:c . Riou·威尔金森和R.J.威尔金森设计研究。c . Riou执行整个血液化验和流式细胞仪实验,分析和解释数据。g·谢弗中和试验实验进行。e . du Bruyn R.T.歌利亚和c Stek招募参与者。·威尔金森,h .备忘录和d提供了重要的试剂。c . Riou和·威尔金森写的手稿,与所有作者贡献提供重要的反馈。
利益冲突:c . Riou没有披露。
利益冲突:g·谢弗没有披露。
利益冲突:大肠du Bruyn没有披露。
利益冲突:R.T.歌利亚没有披露。
利益冲突:c . Stek没有披露。
利益冲突:h .备忘录没有披露。
利益冲突:d挂没有披露。
利益冲突:·威尔金森没有披露。
利益冲突:R.J.威尔金森报告从Wellcome赠款,英国癌症研究,英国研究和创新,以及欧洲和发展中国家临床试验伙伴关系,在进行这项研究的。
支持声明:这项工作是由威康(104803和203135)和克里克主意创新计划(i2i)与Rosetrees信任(2020 - 0009)。c . Riou支持欧洲和发展中国家临床试验伙伴关系EDCTP2计划支持欧盟的地平线2020计划(培训和流动性行动tma2017sf - 1951 tb -规范)和美国国家卫生研究院(NIH) (R21AI148027)。g·谢弗支持欧洲和发展中国家临床试验伙伴关系EDCTP2计划(培训和流动行为tma2018sf - 2446)。R.J.威尔金森和·威尔金森接收弗朗西斯·克里克研究所的支持,这是由英国研究和创新医学研究委员会,英国癌症研究中心和威康(FC0010218)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年1月29日。
- 接受2021年5月26日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org