文摘
全基因组测序(WGS)可用于分子类型和描述的结核分枝杆菌复杂的(MTBC)菌株。我们评估系统使用WGS-based MTBC监测方法包括所有欧盟/欧洲经济区(欧盟/ EEA)国家和突出的挑战和经验教训,被认为是未来发展的WGS-based监视系统。
WGS和流行病学数据的患者rifampicin-resistant (RR)和耐多药结核病(MDR) (TB)从欧盟/欧洲经济区国家收集2017年1月至2019年12月。WGS-based遗传相似度分析使用一个标准化的方法包括茎核心基因组序列输入(cgMLST)和单核苷酸多态性(SNP)的计算距离在所有WGS数据满足最低质量标准,以确保数据的可比性。
总共有2218 RR / MDR-MTBC隔离收集了来自25个国家。其中,56个跨境集群与最近的可能性增加传输距离(≤5个snp)由316 RR / MDR-MTBC隔离标识。跨境集群包括两个和30耐药隔离两到六个国家,展示不同的RR /耐多药结核病传播模式在西方和东方的欧盟国家。
这一初步研究表明WGS-based监测系统不仅可行,而且可以有效地阐明国内和跨境RR /耐多药结核病传播的动力学在欧盟/欧洲经济区国家。教训这个研究强调建立一个欧盟/欧洲经济区国家中央集权WGS-based结核病需要加强国家监测系统集成系统进行前瞻性WGS监测和清晰的发展过程来促进国际合作调查的跨境集群。
文摘
WGS-based监测系统监测的实现耐多药结核病疫情的出现在欧洲是可行的和有可能提供证据,以更好地阐明跨境传播模式https://bit.ly/2ZTnPjk
介绍
(MDR)耐多药和广泛耐药结核病(XDR) (TB)代表全球结核控制的一个主要威胁。共有999例耐多药结核病病例报道,2018年有一个整体较低的耐多药结核的患病率在欧盟(欧盟/欧洲经济区(EEA)(3.7%的结核病例报道),但耐多药结核病的比例仍然很高在立陶宛(17.1%)和爱沙尼亚等国(24.6%)(1]。罗马尼亚,仅2018年354例耐多药结核病病例通知报道超过三分之一(35.4%)的耐多药结核病例总数在整个欧盟/欧洲经济区(1]。
耐多药/广泛耐药结核病是困难和昂贵的治疗;2018年,耐多药结核病例的治疗成功率欧盟/ EEA仅为49.9% (1]。发展的最佳感染结核病控制和预防战略,准确跟踪国内和跨境耐多药结核病的传播和快速识别新兴耐多药/广泛耐药结核病的克隆是至关重要的。分枝杆菌点缀的重复单元的引入可变数目串联重复序列(MIRU-VNTR)基因分型的方法结核分枝杆菌复杂(MTBC)在欧盟/欧洲经济区成员国加强我们的知识的发展史和传输模式临床MTBC菌株。然而,使用MIRU-VNTR耐多药结核病的监测在欧盟/欧洲经济区受到次优覆盖(2015年是26.2%),延迟报告和缺乏流行病学数据确认的人类传播链(2,3]。此外,内在歧视性MIRU-VNTR的力量的缺乏使得这项技术不支持追踪接触者(4]。
最近,全基因组测序(WGS)已成为黄金标准分类MTBC菌株和追踪感染源和传播网络(5]。WGS还可用于抗菌药物敏感性的基因型的预测给定隔离具有足够精度的指导适当治疗(6- - - - - -8]。结核病WGS参考实验室的实现表明,这项技术可能是一个具有成本效益和节省时间的替代传统的MDR诊断和输入方法(9]。WGS检测结核传播的作用,为研究耐多药/广泛耐药结核病疫情在欧洲最近被证明(10- - - - - -13和广泛的审查14- - - - - -16]。额外的工作在基因组数据的有效翻译成有意义的信息来指导决策有关的公共卫生干预措施仍然需要跟踪疫情和监测。更具体地说,标准化方法数据分析以确保兼容性WGS数据质量评估方案、标准化的术语和先前定义的验证标准确定最近需要传输(5]。
自2015年以来,欧洲疾病预防与控制中心(ECDC)支持的研究和试点项目的应用WGS-based打字对公共卫生保护(17]。框架的一个试点研究使用分子类型的WGS MTBC菌株在欧盟/欧洲经济区,我们评估了耐多药结核病监测系统使用WGS-based方法涉及所有欧盟/欧洲经济区国家(18]。在这个项目中,我们旨在识别主要的跨境集群和提供基因来描述相关的血统和耐药性资料rifampicin-resistant (RR) / MDR-MTBC菌株在欧盟/欧洲经济区循环。我们还提出了需要解决的关键领域的未来发展在欧洲WGS-based监测系统。
方法
根据pre-analytical试点研究的实施,分析和post-analytical参数和方法约定在一个技术专家咨询召集的研究(补充表S1)。
研究参与者
所有欧盟/欧洲经济区国家被邀请参加这项研究。
数据收集和验证
WGS和流行病学数据的收集的RR /耐多药结核病患者EUSeqMyTB财团(18从2017年1月至2019年12月)(补充注意S1)。当地实验室规范pseudo-anonymised使用一个独特的欧盟测序类型样本标识符符合欧盟法规2016/679通用数据保护监管(GDPR)。WGS数据进行质量检查和只有那些满足预定义的质量标准都包括在研究(补充注意S1)。
WGS-based关联性分析
的MTBC亲缘分析使用两个连续的分析方法:1)茎核心基因组序列输入(cgMLST)和2)单核苷酸多态性(SNP)的计算距离(补充注意S2)。最初cgMLST-based分析(19)允许快速扩张的“实时”分析监测研究数据库使用大大减少计算能力相比SNP-based方法。SNP-based分析,使用MTBseq管道[20.)的数据集上执行MTBC隔离集群通过cgMLST使用的最大距离阈值≤5个snp /等位基因识别与最近的可能性增加跨境集群传输(21]。
WGS-based耐药性预测和系统分类
筛查耐药性变异和演化snp进行使用MTBseq管道(补充注意S2)[20.]。检测到变异注释与耐药性或易感性和系统发育snp根据文献[22- - - - - -27]。
跨境集群识别
SNP-based跨境集群定义为两个或两个以上的RR / MDR-MTBC隔离差≤5个snp,隔离在至少两个不同的国家。
数据报告研究的参与者
研究参与者可以评估SNP-based分析的结果通过一个外部网络服务器访问权限控制的已命名(www.euseqmytb.eu)(补充注意S3)。
结果
耐多药结核病负担在欧盟/欧洲经济区的报道
共有28个国家参加了签字的材料和数据传输协议的研究通过他们的国家结核病参考实验室,包括奥地利、比利时、保加利亚、克罗地亚、塞浦路斯、捷克共和国、丹麦、爱沙尼亚、芬兰、法国、德国、匈牙利、爱尔兰,意大利,拉脱维亚,立陶宛,卢森堡,马耳他,荷兰,挪威,波兰,葡萄牙,罗马尼亚,斯洛伐克,斯洛文尼亚,西班牙,瑞典和英国。2172名患者的研究包括2218 MTBC隔离,隔离在25的28个参与欧盟/欧洲经济区成员国(89%)(表1)。覆盖率是76.7%的耐多药结核病例报道在该地区在2018年(补充表S2)。只有立陶宛和意大利报道< 70% (图1)。

耐多药肺结核(MDR)的百分比(TB)覆盖/欧盟/欧洲经济区国家在2018年。耐多药结核病例的数量在所有实验室确诊结核病例通知欧洲疾病预防控制中心在2018年被用来作为参考。地图生成使用在线工具可用www.mapchart.net/。
基因描述提交的隔离
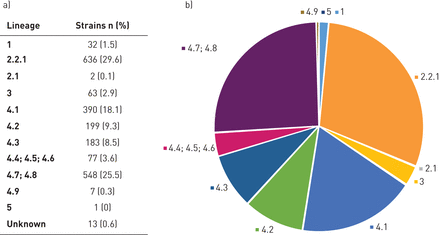
总共有2217 (99.95%)MTBC测序隔离实现最低质量标准。在RR / MDR-MTBC菌株中,最代表血统谱系4(欧美;n = 1404, 65.3%)和血统2.2.1(北京;n = 636, 29.7%),其次是血统3 (Delhi-CAS;n = 63, 2.9%)和血统1(奇印度(EAI);n = 32 1.5%) (图2和补充注意S4)。只有两个(0.1%)菌株属于血统2.1(东亚non-Beijing)和一个(0.05%)血统5(西非1)应变检测。
2151 a, b)的谱系分布rifampicin-resistant (RR) /耐多药(MDR)结核分枝杆菌复杂(MTBC)隔离EUSeqMyTB中学习。印度血统:1:奇(EAI)(包括EAI和EAI马尼拉);2:东亚(包括北京和2.1东亚non-Beijing 2.2.1);3:Delhi-CAS;4.1:欧美(包括4.1和4.1.2:欧美;以下4.4.1:交叉形;4.1.2.1:哈勒姆);4.2:欧美(包括4.2和4.2.2:欧美;4.2.1:准备乌拉尔;4.2.2.1:土耳其); 4.3: LAM; 4.4 (includes 4.4.1.1: S-type); 4.5: Euro-American; 4.6: Euro-American; 4.7: mainly T; 4.8: mainly T; 4.9: H37Rv-like; 5: West-Africa 1.
WGS透露突变预测抗利福平在2151年(97.0%)隔离;其中,1962隔离(91.2%)有额外的耐异烟肼(即。耐多药结核病例)(表2)。RR /耐多药结核病例中,耐氟喹诺酮类原料药在581年预测(27%)分离和附加阻力的二线注射代理(即。广泛耐药结核)331年(15.4%)隔离22,23]。26 (1.2%)RR / MDR-MTBC隔离进行突变预测抗bedaquiline [26]。更多细节的耐药性资料收集的隔离和基因组区域被认为是与耐药性提供了有关补充注意S5和表S3,分别。
跨境集群识别
cgMLST分析,基于≤5等位基因差异,分组1145(51.6%)隔离到307年集群,大小从2 - 36隔离,并包括244个国家和63年跨境集群。63年跨境集群由449年的隔离和的大小不等,从2 - 36隔离,与地理分布范围从2到8个国家(补充表S4)。
SNP-based分析,进行MTBC隔离集群的池cgMLST使用≤5个snp阈值,导致减少的总数集群的情况下,到1017年,隔离的数量在316年跨境集群,和跨境集群的总数56。分析了几个cgMLST-based集群(即。cgCL1 cgCL2和cgCL4)为多个SNP-based跨境和国家集群,符合SNP-based预期稍高灵敏度的方法。跨境集群,通过一个独特的识别SNP-cluster数量(snpCL) (表3),由2 - 30隔离,与地理分布从两到六个国家。只有三个国家、克罗地亚、葡萄牙和斯洛文尼亚,没有参与任何跨境集群。
所有后续分析的池316 RR / MDR-MTBC隔离包括在跨境集群SNP-based分析。
RR /耐多药结核病患者的特征包括在跨境集群
性没有聚集和非聚集RR之间的差异/耐多药结核病例。在集群RR /耐多药结核病例中,70.3% (95% CI 64.5% -75.0%)是男性与71.6%(95%可信区间69.5% -73.6%)的集群。的平均年龄是44岁(范围1 - 92年),41年在集群和集群情况下44年。
绝大多数(n = 242, 76.6%)集群RR / MDR-MTBC隔离属于家族4(欧美),其次是血统2.2.1(北京;n = 72, 22.8%)和血统3 (Delhi-CAS;)(n = 2, 0.6%补充图S1)。在天堂4,最常代表个亚系4.7 - -4.8(主要是T;n = 91, 28.8%)、4.2.1(准备乌拉尔;n = 37岁的11.7%),4.3(林;n = 30, 9.5%)和4.1.2.1(哈勒姆;n = 29, 9.2%)。
四个国家提交∼70%的集群RR / MDR-MTBC隔离:罗马尼亚、立陶宛、德国和意大利(表4)。意大利也在集群RR比例最高的国家/ MDR-MTBC提交总数之间的隔离隔离(n = 38岁的29.9%),与奥地利(n = 9, 36.0%)、瑞典(n = 8, 32.0%)和比利时(n = 5, 26.3%)。
出生国家报道了316年198年(62.7%)集群RR /耐多药结核病例。集群的外国血统的百分比在80%和100%之间在七国(比利时、芬兰、法国、爱尔兰、挪威、瑞典和英国),四个国家的50%和70%之间(匈牙利、意大利、斯洛伐克、西班牙),在20%和40%之间在两个国家(爱沙尼亚和波兰)和0%在三个国家(保加利亚,拉脱维亚和罗马尼亚)(图3)。56跨境的集群识别,34(60.7%)集群的“欧盟的起源”和由212 (67.1%)RR /耐多药结核病患者来自欧盟国家(60例起源失踪)。其中,大多数34(21)主要包括病例来自罗马尼亚和立陶宛,最高的两个欧盟国家耐多药结核病负担,以及一些情况下从意大利和波兰。剩下的13个集群在这个小组包括来自保加利亚的病例中,爱沙尼亚,波兰,意大利和匈牙利。我们还发现了15(26.8%)跨境集群,包括81 (25.6%)RR /耐多药结核病例,几乎都是外国(非欧盟国家)的起源(“非欧盟的起源”跨境集群)。在这一组,信息来源是失踪40(49.4%)的情况下。只有两个15集群包括个人出生在欧盟和非欧盟国家。从两岁EU-born案例(一个婴儿和一个蹒跚学步的孩子),我们怀疑传播发生在家庭中。的15个“非欧盟的起源”跨境集群(61 RR /耐多药结核病例),11只包括结核病患者从非洲/撒哈拉以南的非洲,和四个包括病人来自东欧地区国家(乌克兰和格鲁吉亚)。其余7(12.5%)跨境集群,包括23 (7.3%)RR /耐多药结核病例,信息来源是失踪了18(78.3%)例,因此不可能对成一个特定群体进行分类。
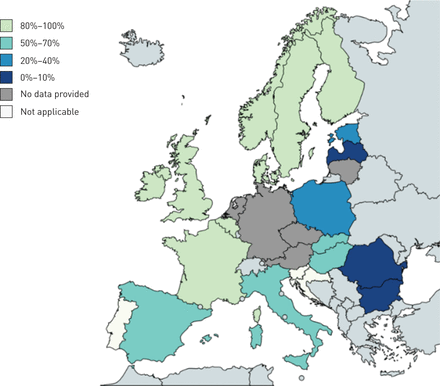
地图的比例rifampicin-resistant /耐多药结核病病例的外国血统的跨境集群/欧盟/欧洲经济区国家。地图生成使用在线工具可用www.mapchart.net/。
主要的例子跨境集群
在56跨境集群标识在这项研究中,三个(snpCL1, snpCL3和snpCL8)站在大小,相关国家和最近的可能性传播(即。低意味着每个隔离对SNP差别的集群,补充图S2)。与集群相关的主要特征成分,耐药性的耐多药结核病例的隔离和流行病学数据报告补充表S5,而相应的最小生成树所示图4。SnpCL3 snpCL8涉及四个西方欧盟国家和似乎与迁移来自撒哈拉以南非洲。从这些报道W SnpCL3隔离是没有区别的“et al。(10突变的遗传背景和模式,而且额外WGS-based亲缘分析证实这些耐多药结核病例的一部分“非洲之角”爆发。相反,突变的模式与血统的隔离属于snpCL8文献中未见报道,但是,类似于snpCL3,大多数12(7)的耐多药结核病例属于这个集群从索马里移民。
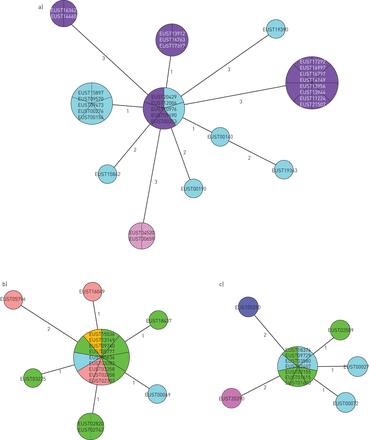
最小生成树)snpCL1, b) snpCL3 snpCL8和c)。树枝上的数字显示的遗传距离最近的单核苷酸多态性(SNP)差异分离。SNP遥远的分离株之间的差异可以重组加法的SNP数量的分支。不同的颜色表示不同的欧盟/欧洲经济区国家菌株被孤立。
不同于snpCL3 snpCL8,所涉及的耐多药结核病例snpCL1起源于欧洲,> 70%报告罗马尼亚出生的国家。值得注意的是,> 90%(11 12)耐多药结核病例属于snpCL1通知意大利耐氟喹诺酮类原料药,其中,50%也耐bedaquiline。这些包括结核病患者出生在罗马尼亚和意大利。
讨论
我们已经表明,实现WGS-based监测监测国内外耐多药结核病疫情的出现不仅是可行的,但有潜力提供证据,以更好地阐明跨境传播模式在欧洲。
总的来说,跨境本研究产生的聚类速度明显低于欧盟先前的报道之一耐多药/广泛耐药结核病的分子监测项目基于VNTR打字和覆盖了9年的时间内(3]。降低聚类速度在这项研究中观察到可能的结果,采样时间的差异之间的两项研究中,和前面的低覆盖率和选择抽样研究中,除了高分辨率的WGS MIRU-VNTR[相比3]。
大约70%的RR /耐多药结核病患者参与跨境集群出生在这个国家的通知。然而,这个比例在欧盟国家之间存在着显著的差异,在更高的在欧盟国家东部和波罗的海国家和一些西方欧盟国家不超过10%,表明不同的RR /耐多药结核病传播模式在西方和东方的欧盟国家。这是三个主要的例子所示在欧盟跨境集群循环。两个集群,snpCL3 snpCL8,显示出类似的动力学。这些集群包括患者出生在索马里和苏丹,通报了奥地利,法国,德国,意大利,荷兰和瑞典,这表明传输只发生在移民人口,可能沿途的移民进入欧盟/欧洲经济区国家之前,或在原产国。虽然出生国家没有系统的数据,我们没有确定的证据之间的耐多药结核病传播移民和人居住在欧洲,由于可能努力确定情况下进入欧盟/欧洲经济区后不久,更好的生活条件和可访问性医疗相比,通用欧洲移民在移民的条件(12),他们有限的社会融合在大多数欧盟/欧洲经济区国家。第三个集群、snpCL1传播动力学的代表一个不同的例子,其中70%的结核病患者出生或居民在国家的通知。传统独立于本研究进行的流行病学调查证实最近的传播确实发生了至少三分之一的病人。最令人担忧的是,这个集群包括耐多药结核病与额外的耐氟喹诺酮类原料药和bedaquiline隔离。虽然这些pre-XDR-TB病例诊断在意大利,到目前为止,只有这些患者具有不同的国籍并定期与同胞的联系,从而增加阻力跨境传播的机会。这个集群可能代表欧盟人口的公共卫生威胁如果不充分预防进一步传播,说明潜在WGS MTBC监测的实用程序。
这是第一个研究报道的系统使用一个欧盟MTBC WGS-based方法监测目的。确保数据可比性,我们应用一个共同的和标准化的WGS分析管道所有收集到的隔离的序列数据实现预定义的质量标准。这个WGS-based监测项目的相关性被公认在欧盟/欧洲经济区国家,让我们达到高覆盖率的耐多药结核病例ECDC的通知;因此,我们的数据是代表RR / MDR-MTBC隔离目前在欧盟/欧洲经济区循环。重要的是,这项研究允许欧盟/欧洲经济区国家缺乏WGS能力的基因型RR / MDR-MTBC菌株,从而生成一个数据库研究国家MTBC传输模式和建设WGS分析能力。
尽管成功实施的试点研究确定了一些挑战和教训学会改善进一步实现欧盟/欧洲经济区的WGS结核病。首先,尽管WGS有可能接近“实时监控”,提供数据的内在延误由于文化、配料和转诊MTBC隔离的测序实验室影响我们及时发现集群的能力,执行一种前瞻性的分析。虽然超出了研究的范围,这限制了我们的结果对公共卫生的影响,成功地显示在其他地方设置(29日,30.]。更便宜和便携式测序平台的可用性可能有助于减少这种延迟这个技术通过提高可访问性。同样,常规可行时,直接从临床样本测序结果将进一步缩短时间,从而使实时监测。
第二,完成基本的临床和流行病学数据只能来自11个国家的贡献研究;很少有国家中央集权结核病监测系统或一个系统,允许国家结核病参比实验室的工作人员直接访问这些信息。我们承认使用WGS数据就可能导致一个传输的高估,只有通过补充详细的临床和流行病学数据是否可以完全解释传播动力学。这需要连接的临床、流行病学和实验室数据。给定的数据保护的必要性,这将是未来WGS-based监测系统必须确保数据处理根据GDPR和当地法规和安全的通过一个适当的保护系统。
第三,参与国能够评估WGS试点研究数据库中的数据并主动执行额外的分析通过研究网络服务器接口。这增加平等的可访问性技术的国家卫生系统WGS国内缺乏能力。最后,跨境集群的识别,这将是重要的定义具体的标准,如抗二线和新的抗结核药物或高最近传播的可能性,来证明一个国际流行病学调查,并最有效地利用可用的资源。
初步研究的结果和经验教训将进一步直接工作建立一个操作平台结合WGS-based结核病打字和流行病学数据。目标是建立一个欧盟/欧洲经济区国家中央集权WGS-typing / epi-data数据库识别跨境结核病和耐多药结核病集群和调查有关集群同所有国家参与。飞行员学习和未来的工作将进一步促进标准化的WGS结核病,在欧盟/欧洲经济区建设能力。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
Supplementary_materialerj - 02272 - 2020 - _supplementary_material
可共享的PDF
确认
我们要感谢所有的工作人员区域参考实验室的收集和转诊RR / MDR-MTBC隔离,和操作的接触点为流行病学提供有价值的数据。
ECDC分子监测项目参与者如下。Ewa Augustynowicz-Kopeć:微生物学的部门,国家肺结核和肺部疾病研究所,华沙,波兰;Elizabeta Bachiyska:国家中心传染病和寄生虫病,索非亚,保加利亚;艾格尼丝bako: Koranyi肺学研究所,布达佩斯,匈牙利;罗克珊娜Coriu:肺学,马吕斯青年学院,布加勒斯特,罗马尼亚;分枝杆菌Věra Dvořakova:国家参考实验室,布拉格,捷克共和国;Lanfranco Fattorini:传染病部门,国家卫生研究所,罗马,意大利;玛格丽特·菲茨吉本:爱尔兰分枝杆菌参考实验室,圣詹姆斯医院,都柏林,爱尔兰;阿格涅斯卡Głogowska:微生物学的部门,国家肺结核和肺部疾病研究所,华沙,波兰;雷蒙娜Groenheit:公共卫生机构的瑞典索尔纳、瑞典; Marjo Haanperä: Dept of Health Security, Finnish Institute for Health and Welfare (THL), Helsinki, Finland; Laura Herrera León: Instituto de Salud Carlos III, Madrid, Spain; Daniela Homorodean: Clinical Hospital of Pneumology, Cluj-Napoca, Romania; Alexander Indra: Austrian Reference Laboratory for Mycobacteria, Austrian Agency for Health and Food Safety, Vienna, Austria; Sarah Jackson: Health Protection Surveillance Centre, Dublin, Ireland; Tiina Kummik: Dept of Mycobacteriology, Tartu University Hospital, Tartu, Estonia; Troels Lillebaek: International Reference Laboratory of Mycobacteriology, Statens Serum Institut, Copenhagen, Denmark; Rita Macedo: Tuberculosis National Reference Laboratory, Portuguese National Institute of Health, Lisbon, Portugal; Vanessa Mathys: Unit Bacterial Diseases Service, Infectious Diseases in Humans, Sciensano, Brussels, Belgium; Anne Torunn Mengshoel: National Reference Laboratory for Mycobacteria, Dept of Bacteriology, Norwegian Institute of Public Health, Oslo, Norway; Matthias Merker: German Center for Infection Research, partner site Borstel-Hamburg-Lübeck-Riems, Borstel, Germany; Molecular and Experimental Mycobacteriology, National Reference Center for Mycobacteria, Research Center Borstel, Borstel, Germany; Darshaalini Nadarajan: National and WHO Supranational Reference Center for Mycobacteria, Research Center Borstel, Borstel, Germany; Anders Norman: International Reference Laboratory of Mycobacteriology, Statens Serum Institut, Copenhagen, Denmark; Ilva Pole: Dept of Mycobacteriology, Center of Tuberculosis and Lung Diseases, Riga East University Hospital, Riga, Latvia; Igor Porvaznik: Clinical Microbiology Dept, National Institute for Tuberculosis, Lung Diseases and Thoracic Surgery, Vyšné Hágy, Slovakia; Wladimir Sougakoff: Laboratory of Bacteriology, National Reference Centre for Mycobacteria (CNR-MyRMA), AP-HP, Paris, France; Andrea Spitaleri: Emerging Bacterial Pathogens Unit, Division of Immunology, Transplantation and Infectious Diseases, IRCCS San Raffaele Scientific Institute, Milan, Italy; Sara Truden: National Reference Laboratory for Mycobacteria, University Clinic for Respiratory and Allergic Diseases, Golnik, Slovenia; Laima Vasiliauskaitė: Dept of Physiology, Biochemistry, Microbiology and Laboratory Medicine, Institute of Biomedical Sciences, Faculty of Medicine, Vilnius University, Vilnius, Lithuania; Centre of Laboratory Medicine, Tuberculosis Laboratory, Vilnius University Hospital Santaros Klinikos, Vilnius, Lithuania; Ljiljana Žmak: National Reference Laboratory for Tuberculosis, Croatian Institute of Public Health, Zagreb, Croatia.
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:所有研究参与者在很大程度上造成了结果提出了手稿。
利益冲突:r·安东尼报告赠款ECDC公开招标橙汁/ 2017 /商务/ 7766,在进行这项研究的。
利益冲突:助教科尔没有披露。
利益冲突:a . de奈尔报告赠款ECDC公开招标橙汁/ 2017 /商务/ 7766,在进行这项研究的。
利益冲突:诉Nikolayevskyy报告从ECDC赠款,在进行这项研究的。
利益冲突:c . Kodmon没有披露。
利益冲突:F.P.毛雷尔没有披露。
利益冲突:美国Niemann报道德国感染研究中心的资助,2167年慢性炎症EXC Excellenz集群精密医学,莱布尼茨科学校园进化医学的肺(EvoLUNG)和ECDC公开招标橙汁/ 2017 /商务/ 7766,在进行这项研究的。
利益冲突:d . van Soolingen没有披露。
利益冲突:M.J. van der Werf没有披露。
利益冲突:D.M. Cirillo报告赠款ECDC公开招标橙汁/ 2017 /商务/ 7766,在进行这项研究的。
利益冲突:大肠Tagliani报告赠款ECDC公开招标橙汁/ 2017 /商务/ 7766,在本研究的进行。
支持声明:这个项目是由欧洲疾病预防与控制中心(框架接触ECDC / 2017/012)。这项研究的资助者参与修订的手稿。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2020年6月11日。
- 接受2020年7月17日。
- 版权©2021人队
这个版本分布在创作共用署名非商业性许可证的条款4.0。