摘要
通过过早对COVID-19患者进行表型分析,我们和我们的患者暴露在相当大的、可预防的风险中。如果不坚持数据驱动的表现型,我们的认知偏见就会保证我们最终得到表现型驱动的数据。https://bit.ly/2ZM8wZV
严重急性呼吸系统综合征冠状病毒2给全球卫生保健带来了前所未有的挑战。严重冠状病毒病2019 (COVID-19)肺炎常导致低氧血症性呼吸衰竭,表现为急性呼吸窘迫综合征(ARDS)。最近,作者在几篇有影响力、知名度高的论文中提出了COVID-19肺炎的不同临床表型[1- - - - - -3.].例如,在本杂志最近的一个观点[3.,作者推测,COVID-19有五种表型表现:基于低氧血症严重程度和需要支持治疗的三种表型(无低氧血症、轻度低氧血症和中度低氧血症),以及基于其他生理和临床特征的严重低氧血症患者的两种表型。与近期其他对COVID-19患者进行显型的努力一致[1,2],作者将患者分型为一种普遍的表型,具有正常的顺应性、低肺重量和主要的灌注异常(“L”型),和一种不普遍的表型,具有更典型的ARDS特征,如深度实变和低顺应性(“H”型)。作者主张对这些所谓的表型采取不同的管理策略,包括允许增加潮气量和限制“L”表型患者的呼气末正压。
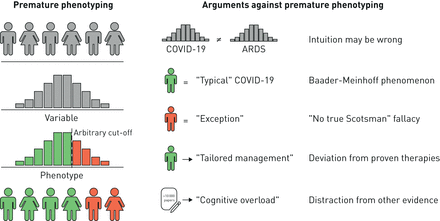
让COVID-19肺炎患者显型的冲动是可以理解的,也是可以理解的。在重症监护医学之外,过去十年的特点是精准医学的重大进展,基于个体患者的生理和生物学特征的有前景的定制疗法。如果一种新疾病的出现没有有效的治疗激励,基于启发式的识别可能对特定干预反应相似的患者子集。然而,应该抵制这种基于早期临床经验来定义表型的诱惑。过早地对患者进行表型,我们可能会造成相当大的伤害,产生更多的静态而不是信号。在这篇社论中,我们提供了反对过早表型的四个论点,讨论了负责任表型的特点,并建议了一条前进的道路,以促进我们对COVID-19患者潜在的真正异质性的理解(图1).
过早表型的危险。通过关注正态分布连续体的极端,我们有可能创造出任意的“表型”,这些表型不能代表病理生理学中有意义的潜在差异。过早的表型往往基于错误的初始印象,并导致认知偏差,包括巴德尔-迈因霍夫现象(“频率偏差”)和“不是真正的苏格兰人”谬论(排除不相容的观察)通过一个特别的纯度测试)。过早的表型可能会导致对循证实践的偏离,并对临床医生的认知负荷造成不必要的影响,从而危及护理的提供。
反对过早表型的第一个也是最简单的论据是,我们最初的直觉往往是错误的。作为一个生动的例子,一篇著名的文章[2]最近不加限定地宣称,“在COVID-19发生呼吸窘迫后不久,尽管氧合非常差,患者最初仍保持相对良好的依从性。”这一说法,虽然没有被引用的参考文献支持,但构成了对所谓的COVID-19“L表型”患者的病理生理学和定制管理的扩展讨论的基础(上文已讨论)。然而,随后的队列研究表明,COVID-19患者的肺顺应性实际上相当低[4,5],完全符合非covid -19急性呼吸窘迫综合征队列[6- - - - - -8,并且正态分布在一个连续体上,而不是作为离散的表型存在。此外,这些表型的放射学和生理特征(如。计算机断层扫描上密集的空域填充与“H”表型顺应性的降低配对)随后被证明彼此完全不相关[9].临床表型的识别,以及对其潜在生物学特性的推测,应该推迟到仔细、客观地对足够规模的队列进行检查之后。人类的直觉太容易出错,临床经验太偶然和异质性,在没有足够数据的情况下,无法可靠地识别表型。
反对过早表型的一个相关论点是,它加剧了我们对认知偏见的固有易感性。一旦我们被告知临床类别(无论它们可能是错误的),我们的大脑就会将它们视为真实的,并开始选择性地过滤我们的观察结果。例如,自被证明不正确的COVID-19患者保持了肺顺应性的说法传播后,常见的认知陷阱加强了这一神话。Baader-Meinhof现象(也称为“频率错觉”)确保了一旦临床医生被提示注意到COVID-19患者肺部顺应性接近正常,他们就开始在任何地方注意到这些患者(实际上,他们的频率并不高于非covid - ard) [6- - - - - -8].类似地,临床医生可以通过无意中犯“没有真正的苏格兰人”谬论来驳回低依从性的COVID-19病例:通过驳回声称的例外特别的“真正的COVID-19”呼吸力学基本正常。如果我们不坚持数据驱动的表现型,我们的认知偏差就会保证我们最终会得到表现型驱动的数据。
反对过早表型的第三个理由是,它分散了我们对合理的、有证据的实践的注意力。近几十年来,ARDS的临床结局有了明显改善[10并不是受重大药物发现的推动,而是受提供支持性护理的渐进改进的推动。这些缓慢但累积的进展是建立在从严格的随机对照试验中得来的来之不易的教训之上的。根据他们的设计,这些试验在基于综合征的定义下将异质性ARDS患者“集中”在一起。尽管如此,这些试验为该领域提供了大量的文献,提供了有证据支持的疗法。通过武断地将COVID-19患者划分为虚假的表型,并根据未经测试的生理直觉建议“量身定制的管理”,作者主张放弃仍然是我们抗击COVID-19最有效的工具:细致、循证驱动的重症护理提供。
反对过早表型的最后一个论点是,它恶化了ICU中本已不利的信号和噪声的比例。在病床边,重症监护医生必须过滤、处理和解释每个病人产生的海量数据流:生理、生化、放射学、等。临床医生必须将这些发现与已发表的文献综合起来,这同样令人生畏:在2020年前4个月发表了1万多份关于COVID-19的pubmed索引手稿。这种信息洪流威胁着ICU中最被忽视和最宝贵的资源:临床医生的注意力、时间和带宽。通过不必要地模糊临床图像,虚假表现型占用了我们的时间,分散了我们对更直接问题的关注。作为一个领域,我们的研究优先次序也同样模糊不清:研究人员的时间和资源被浪费在试图解释临床现象背后的生物学上,而在检查患者数据时,这些临床现象根本不存在。
那么责任表现型是什么样的呢?与任何科学实验一样,我们需要一个明确的目的来解释为什么我们要寻找表型(表1).在医学科学中,这一任务最终集中在改善病人的结果(尽管收集新的生物学和临床见解是一个同样重要的激励因素,因为它们可能是实现这一目标的关键)。为此,我们的领域有最近的例子,已成功地用于识别治疗反应和/或生物学上不同的亚群的经验衍生表型。例如,在哮喘中,使用数据驱动的无偏聚类方法,基于白介素-13诱导基因表达确定了两种不同的哮喘表型[11].后来在一项随机对照试验中发现,这种基因高表达的表型特征对一种特异性抑制白介素-13活性的单克隆抗体具有响应性[12].在ARDS中,再次使用无偏聚类方法,两种表型已被识别出具有不同的生物学和临床特征,在5个随机对照试验中一致,且具有明显不同的临床结果[13].重要的是,在三个随机对照试验中,观察到随机干预的不同治疗反应。此外,最近描述了更简单的模型,为这些表型的临床应用提供了潜力[14].
这些数据驱动的聚类方法并非不受错误和误用的影响。这些都是强有力的工具,并且独立于研究问题或研究设计的有效性,集群将不可避免地出现。因此,研究人员有责任证明已识别表型的有效性和实用性。在缺乏基本真理的情况下,最能替代有效性的条件是:1)稳健性,2)一致性和3)数据的可重现性。在几乎所有的算法中,被识别的表型高度受预测变量的影响。以COVID-19重症患者为例,我们必须承认,我们正在研究复杂的生物系统,其中相互关联的通路具有非线性关联。因此,在此类人群中寻找单变量解决方案,除了用于预测外,似乎不太可能产生有意义的亚组[15].此外,单变量解,特别是在过早地寻求时,更容易受到中心极限定理的影响。这个数学定理表明,给定足够大的样本容量,变量的均值分布将收敛于正态分布,这意味着连续变量在有限的数据下出现双峰,随着时间的推移将成为正态分布。因此,无论是生物学上的合理性还是数学上的原则,我们都不太可能得出有用的表型,如果我们把重点放在简单的、一维的疾病特征上。
为了避免这些陷阱,在选择多元模型中的预测变量时,应该考虑到研究问题,并在有效分割人口方面提供大量信息。此外,这些旨在克服认知偏差的复杂数据科学算法的使用将仅限于理论化,除非它们伴随着能够迅速和一致地识别表型的测量系统。不管使用的动机或方法是什么,重症监护中的表型通常是一项需要大量数据的工作,而在目前声称COVID-19表型的研究中,令人遗憾的是,缺乏必要的数据数量和质量。然而,最终,疾病表型的真正成功将取决于可采取的干预措施的确定。在重症监护中,虽然在二次分析中描述了许多表型异质治疗效果的例子,但它们的有效性还需要测试通过随机对照试验。仅仅是对疾病表型的识别,无论是过早的还是负责任的,本身不应该改变临床实践,而应该为前瞻性的“表型意识”试验提供信息。
总而言之,COVID-19大流行给临床医生和研究人员带来了新的挑战。虽然我们的最终目标是根据每个患者的具体病理生理情况定制治疗方案,但我们首先必须客观地收集、整理和解释足够的数据,以“分类”和全面了解疾病。通过过早对COVID-19患者进行表型分析,我们将自己和患者暴露在相当大的、可预防的风险之中。
可共享的PDF
脚注
利益冲突:L.D.J. Bos报告了荷兰肺脏基金会(青年研究基金)、荷兰肺脏基金会(公私合作基金)、荷兰肺脏基金会(Dirkje Postma奖)的拨款,以及拜耳的个人费用(咨询费)。
利益冲突:P.辛哈没有什么可披露的。
利益冲突:R.P.迪克森没什么可披露的。
- 收到了2020年5月13日。
- 接受5月23日,2020年。
- 版权©2020人队
这个版本是在知识共享署名非商业许可4.0的条款下发布的。