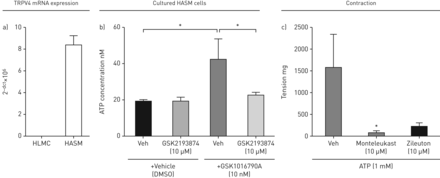
摘要
肥大细胞 - 气道平滑肌(ASM)相互作用在免疫球蛋白(IG)在哮喘中看到的I-依赖性支气管中发挥着重要作用,但较少是较少的肥大细胞活化机制。瞬态受体潜在阳离子通道,亚家族V,成员4(TRPV4)活化导致人ASM的收缩通过释放Cysteinyl白三烯(Cyslts),但机制是未知的。本研究的目的是探讨IgE的诱导支气管痉挛中IgE的肥大肥大细胞 - ASM相互作用的作用。
在麻醉的豚鼠中测量支气管内猪和使用等距张力测量评估的人和豚鼠气道组织的收缩。增加在细胞内[ca.2+使用CA成像2+- 敏感染料Fura2,延时PTychography用作ASM细胞收缩的替代物。
TRPV4激动剂GSK1016790A导致收缩在活的有机体内TRPV4拮抗剂GSK2193874对豚鼠和人及豚鼠气管组织均有抑制作用。GSK1016790A增加(Ca2+]一世并在人体ASM细胞中释放ATP而不会引起收缩。TRPV4和ATP在分离的气管组织中诱发收缩,但共培养实验表明了人肺肥大细胞的要求。表达分析和药理学研究表明,肥大细胞活化依赖于ATP激活P2X4受体。显示胰蛋白酶唤起气管组织的收缩通过PAR-2-TRPV4-ATP-CYSLT轴的激活表明该信号传导途径的潜在疾病相关性。
TRPV4活化增加[Ca2+]一世并从ASM细胞释放ATP,触发肥大细胞p2x4依赖的cylts释放,导致ASM收缩。本研究描述了一种新的肥大细胞- asm相互作用和TRPV4作为ige不依赖肥大细胞依赖支气管痉挛的驱动因子。
摘要
一项以前未应用于呼吸研究的技术现在发现了重要的ige独立机制,该机制涉及人类肥大细胞-气道平滑肌相互作用,可能与非特应性哮喘相关的支气管痉挛有关http://bit.ly/2U1n5nT
介绍
哮喘是一种慢性气道炎症疾病,其特征在于气流阻塞和症状,如胸闷,喘息和咳嗽[1那2].大多数早期发病的哮喘患者是特应性的,并表现出过敏性炎症反应。这被称为T2哮喘,由CD4+ T-helper (Th) 2淋巴细胞、肥大细胞和可能的先天淋巴细胞(ILC2)驱动,ILC2分泌白介素(IL)-4、IL-5和IL-13,导致嗜酸性炎症和B细胞产生免疫球蛋白(Ig)E [3.那4.].在特征性哮喘中,肥大细胞通过IgE与高亲和力IgE受体的结合而敏感(FcεR1)。当过敏原特异性的IgE通过相关过敏原相关联,受体聚集触发肥大细胞介质释放,释放预成型的颗粒衍生的介质,前列腺素,半胱氨酸白酮(Cyslt)和细胞因子思想,对所见的早期和后期支气管痉挛负责过敏原暴露[4.].虽然Atopic哮喘和T2炎症反应通常抑制吸入皮质类固醇(ICS)患者的患者患者的患者,但尽管有高剂量的IC,但仍然具有持续症状的患者[5.因此需要新的治疗方法。
肥大细胞可能通过与气道平滑肌(ASM)的关联哮喘发病机制中的关键效应。在哮喘中,肥大细胞渗透ASM捆绑包[6.那7.],它们与ASM细胞相互作用[8.-11].人肺肥大细胞,原位当与人ASM细胞(HASMC)共同培养时,持续的“激活”状态,具有持续较令的证据[7.那9.那11和T2细胞因子的表达[12]这可能导致增加的炎症和支气管混凝土。然而,人们认识到,肥大细胞活化的多种IgE - 独立机制也可能在哮喘中发挥作用,尽管关于所涉及的机制较少。在这里,我们研究了涉及瞬态受体潜在阳离子通道,亚家族V,成员4(TRPV4)和疾病相关介质引起的IgE离Cell-asm相互作用,例如疾病相关的介质,例如可以引起收缩的胰蛋白酶通过蛋白酶活性受体-2(PAR2)诱导TRPV4的栅极。
TRPV4是CA2+-可渗透的多模门控离子通道[13-15]表达并导致CA2+hasmc的通量[16].最近,TRPV4显示出造成分离的豚鼠和人气管组织的收缩通过释放Cyslts [17].在肺部的其他细胞系统中,TRPV4激活引起ATP释放并启动下游功能后果通过激活p2x受体[18那19].在哮喘的支气管肺泡灌洗液(BALF)和哮喘的小鼠模型中增加了ATP水平[20.].此外,ATP独立于IGE诱导啮齿动物肥大细胞中的介质释放[21那22],而啮齿类肥大细胞嘌呤受体的激活可导致脱颗粒、细胞因子分泌、趋化和细胞凋亡[22].几个P2X受体在人肺肥大细胞(HLMCs)上表达[23[所以我们假设TRPV4-ATP轴在人ASM-HLMC串扰中发挥作用,唤起肥大细胞依赖性支气管痉挛,这可能在哮喘病理生理学中发挥关键作用。
方法
使用的方法的进一步细节可以在其中找到补充材料。
动物
雄性Dunkin-Hartley豚鼠(300-800g)购自B&K(英国)购买,并在开工试验前至少1周,在温度控制(21°C)客房内,在开始实验前至少提供1周。基于1986年的动物(科学程序)法案和到达指南,根据英国家庭办公指南进行实验24].
在活的有机体内支气管中的测量
豚鼠用聚氨酯麻醉(1.5g·kg-1)和如前所述的具有短长度的Perspex管道和动物的气管夹紧,如前所述[18].
人类组织
从国际医学促进研究所(IAM,Edison,New Jersey,USA)获得人类气道样品(气管,主要支气管,二次支气管)剩余盈余。我们接受不适合移植的人气管和肺样本,因此我们经常接受不定义为“正常”的供体组织。这是本研究的局限性之一,而是避免使用13个捐赠者和一系列技术的错误结果证实了所提出的假设。通过注意到肺部疾病和捐赠者的吸烟历史,我们对组织的出处一直透明表1.在所有案件中,授予科学研究的同意,并从Royal Brompton&Harefield Trust获得道德批准(道德号码:REC 09 / H0708 / 72,从2009年12月开始)。看表1提供给我们的患者人口统计资料。
细胞培养
hasmc的收获如前所述[25].来自莱切斯特大学的人肺肥大细胞(HLMCS)从宏观正常的肺切除术中纯化来自三名患者,如前所述[26最终纯度大于99%。纯化的HLMC在含有谷氨酸I和10%热灭活胎牛血清(FCS)的DMEM / HEPES中培养,100ng·mL-150 ng·mL-1IL-6和10 ng·mL-1IL-10,每7天更换一半培养基[27].
体外收缩测量:器官浴
人类气管和支气管组织(约3 - 4毫米宽)和豚鼠气管(约两个软骨环宽)是减少纵向通过削减通过软骨对面平滑肌层和横向部分削减生产带,连接到力传感器(如前所述)(28].
HASMCs中的钙成像
从供体组织收获的Hasmcs在补充有10%Fcs的DMEM中的35mm玻璃底氟孔中生长,并且在实验使用之前血清饥饿。在实验的当天,从细胞中除去DMEM并用无菌细胞外溶液(ECS)替换,并在37℃下使其平衡30分钟。然后用细胞内钙染料Fura-2-am(12μm加载细胞,为1小时和[CA)加载1%Powerlable + Probenicid(1mm))。2+]一世使用宽地倒置显微镜监测的响应。
单次散列细胞收缩评估:ptychography
一种新的成像技术,ptychography,被用来代替HASMCs的细胞收缩[29].Ptychography是一种无标记、高对比度的显微镜技术,其产生的对比度类似于荧光成像,只需要最小的细胞操作。装有电池和低强度近红外激光(635 nm)的培养皿相互移动,以创建一个连续的重叠照明区域阵列,在这里光线散射被探测器捕捉成衍射图案阵列。这种衍射模式数组使用虚拟镜头处理算法来计算一个定量测量的光吸收,散射和相位延迟引入照明穿过样品,使样品的三维特征的分析(29].这项技术在HASMCs中产生了收缩反应(例如,在乙酰胆碱(ACh))匹配[Ca2+]一世在同一细胞中记录的升高,类似于使用整个组织发现的收缩响应[30.].
数据分析
数据表示为平均值±SEM.n的观察。采用学生t检验或单因素方差分析确定统计学显著性事后测试。统计学意义设置为p<0.05,所有处理与适当的对照对照进行比较,n个数字是指使用的不同供体组织/细胞的数量。
结果
TRPV4对收缩的影响在活的有机体内
雾化GSK1016790A 100 ng·mL-1(153nm 15s)导致麻醉的豚鼠气管压力显着且持续增加(图1A- c)。在所有病例中,两条迷走神经都被切断,因此这种影响是由于平滑肌的直接影响,而不是副交感神经反射。亚最大浓度100 ng·mL引起的气管压力增加-1(153nm持续15秒)TRPV4激动剂GSK1016790A显着抑制了1 H以下腹膜内给予TRPV4拮抗剂GSK2193874 (300 mg·/kg)-1;盐水中6%环糊精)(图1C.)但在车辆中仍未受到影响(图1B.).
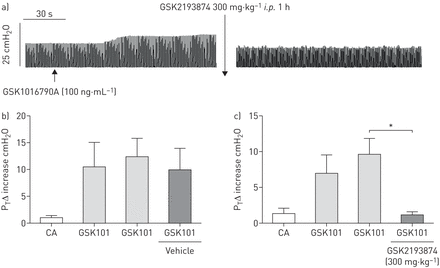
a)GSK1016790A 100 NG·mL的示例迹线-1(153nm持续15秒)介导的反应。在载体(盐水中6%环糊精)给药后(B)施用,但在GSK2193874施用后(300mg·kg-1(c)数据以平均值±表示SEM.(n = 3。*: p < 0.05,配对T.-试验比较同一动物给药前后的反应。
TRPV4激动剂对孤立气道组织的影响体外
GSK1016790A在分离的豚鼠气管中引起浓度依赖性收缩。由于激动剂诱导的持久收缩,在每块组织上仅测试一种浓度(图2A).在30分钟的预孵育后,与GSK2193874(10μm)进行显着抑制收缩(图2B.).人体组织中可以看到类似的效果(图2C和d)。最近的出版物表明,TRPV4诱导的ASM收缩依赖于Cyslts的释放[17].与此观察一致,GSK1016790A (100 nM)诱导的收缩在与cylt1拮抗剂(孟卢司特10 μ M)和5-LO抑制剂(zileuton 10 μ M)预孵育人类组织后被抑制,证实cylts是由TRPV4激动剂诱导的人类ASM (图2E.和f)。单独单独的蒙特利亚斯特(10μm)和齐丽顿(10μm)对气道调节没有影响本身.
GSK1016790A引起豚鼠离体气管收缩(a), GSK2193874(10µM) (n= 4-6) (b). c)对人体组织中GSK1016790A (100 nM)加载体(上壁)或GSK2193874(10µM)(下壁)的反应。d) GSK2193874(10µM)抑制人体组织的反应(n=3)。(f)孟鲁司特(10µM)(例trace (e),中间板)或zileuton(10µM)(例trace (e),底部板)预孵育显著抑制GSK1016790A诱导的人体组织收缩(n=3)。数据显示为平均值±SEM.*: p<0.05,使用单向单因素方差分析和Dunnett的多重比较试验比较对药物的反应(a, f)或t检验比较与拮抗剂对药物的反应(b, d)。
肥大细胞在TRPV4诱导收缩中的作用
TRPV4激动剂GSK1016790A导致[Ca2+]一世通过荧光FURA2成像评估HASMCs (图3Ab)。为了评估GSK1016790A对初级HASMC的收缩的影响,我们使用了称为PTYCHOGUCH的新型成像技术。使用这种技术,单独与HASMC孵育的GSK1016790A没有引起收缩;然而,正对照ACH(10μm)确实如,光学密度的增加所示(图3C.肥大细胞是囊性淋巴细胞的主要来源,在HASMCs与原代HLMCs共培养时,GSK1016790A引起HASMCs收缩,ptychography证实了这一点。然而,肥大细胞游离培养基没有效果,提示HLMCs需要TRPV4介导的HASMCs收缩(图3E., f和g;在补充材料中可以找到HASM细胞在HLMCs和GSK1016790A存在时收缩的视频)。
A和B)GSK1016790A的示例图像,痕迹和图表诱导人气道平滑肌细胞(HASMC)中钙的增加。示例PTYCHOGUCT重构的图像(顶部面板)和来自(C)GSK1016790A(100nM)处理的迹线(底板)和(D)乙酰胆碱(ACH)(10μM)处理的HASMC(n = 2供体)。e)PTYChoge数据单独为人类HASMC中的GSK1016790A没有收缩效应。ACH被用作阳性控制(n = 2个捐赠者)。f)重构的pychrapue图像;两大面板单独显示Hasmcs。底部两面板显示哈姆族与桅杆细胞培养,其中GSK1016790A(100nm)的添加导致光密度的增加。g)在肥大细胞存在下,GSK1016790A(100nM)引起HASMC的收缩(N = 2个供体用于HASMC,N = 3种适用于人肺肥大细胞(HLMC)的供体)。数据显示为平均值±SEM.(n = 8-56读数;)。标尺为100µm。*: p<0.05使用Kruskall Wallis检验和Dunn后比较检验比较对载具(b)或a的反应T.- 最低比较车辆控制的响应(g)。
ATP在TRPV4诱导收缩中的作用
数据表明,TRPV4激动剂激活HASMC上的TRPV4离子频道以增加[CA.2+]一世导致未知介质的释放会导致肥大细胞释放Cyslts。HASM细胞,但不是HLMC,在mRNA水平上表达TRPV4(图4A),提示TRPV4的激活对肥大细胞没有直接影响。之前的研究表明,巨噬细胞和气道感觉神经上TRPV4的激活会诱导ATP的释放[18那19],建议ATP可以是先前未知的介体。GSK1016790A引起培养的人ASM细胞ATP释放,其抑制GSK2193874(10μM)后抑制图4B.).ATP (1 mM)被证明能引起人体器官浴中离体平滑肌的收缩,孟鲁司特和zileuton均能抑制这种收缩,表明其与GSK1016790A (图4C.).此外,ATP引起了从人体供体肺肥大细胞中释放的Cyslts,但没有单独培养和在没有HLMC(补充图E1a和b).
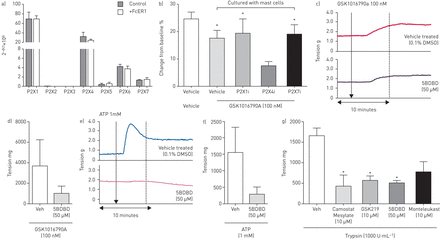
a)TRPV4 mRNA在人类气道平滑肌细胞(HASMC)上表达,但不在人肺部肥大细胞(HLMC)上。b)GSK1016790A(100nm)诱导由GSK2193874(10μM)抑制的HASMC的ATP释放。c)蒙特洛斯特和齐丽顿(10μm)抑制了分离的人气管条的ATP收缩。数据显示为平均值±SEM..从4名患者中分离出HASMC,来自3名供体肺的气管条。*:统计显着性(P <0.05);T-Test比较对相关控制(B)的响应或使用Dunnett的多种比较测试的单向ANOVA比较对车辆(C)的反应进行比较。
TRPV4诱导人ASM收缩的机制
ATP激活ICOTROPIC P2X嘌呤受体和代谢性P2Y受体。已显示肥大细胞表达了许多丙基普遍离子通道[23那31[p2x1,p2x4,p2x5,p2x6和p2x7显示在原发性HLMC上的mRNA水平上表达(图5一个).使用ptychography,在HLMC存在下,GSK1016790A(100nm)诱导的人ASM细胞的收缩仅在与P2X4拮抗剂5bdbd(50μm)孵育后显着抑制,但不孵育p2x1(IP5i10μm)或aP2x7拮抗剂(AZ1164537310μm)(图5 b).该结果在人体气道组织中翻译,其中GSK1016790A(100nm)引起的收缩。图5 c和d)和ATP(1 mm;图5 e培养5bdbd(50μm)后抑制f)。
a) P2X受体mRNA在人肺肥大细胞(HLMCs)上的表达(n=3个供体)。b) P2X受体拮抗剂P2X1 (Ip51, 10µM)、P2X4 (5BDBD, 50µM)和P2X7 (AZ11645373, 10µM)对GSK101679A (100 nM)处理的人气道平滑肌细胞(HASMCs)收缩的影响。P2X4抑制剂(5BDBD, 50µM)对GSK101679A (100 nM) (c和d)和ATP (1 mM) (e和f)诱导的人体组织收缩的影响(n=3)。g)胰酶诱导的人类气管条收缩被甲磺酸卡莫司他、GSK2193874、孟鲁司特和5BDBD抑制(n= 2-3)。数据显示为平均值±SEM..*: p<0.05 t检验与相关对照(b)或使用单向方差分析与Dunnett后检验(p<0.05)比较拮抗剂与对照剂(g)。
在寻找内源性TRPV4配体的过程中,我们推测PAR2的活化可能起到一定作用。G蛋白偶联受体(GPCR) PAR2已被证明与TRPV4功能偶联,并引起离子通道的激活[32那33].使用rtPCR,与TRPV4类似,PAR2在hasm上一致表达,但在HLMCs上不一致,只有三分之一的患者表达PAR2 (补充图E2A.).然后我们利用内源性par2配体胰蛋白酶(1000 u·ml-1),导致孤立的人体气管条收缩(图5克)如前所述[34].这种收缩受到阻断TRPV4诱导的收缩的相同拮抗剂,包括GSK2193874,MONTELUKAST和5BDBD,以及丝氨酸蛋白酶抑制剂CANOSTAT甲磺酸盐(图5克).这些数据表明,哮喘“疾病相关”的介质,如肥大细胞蛋白酶(例如PAR2等激活剂如胰蛋白酶)可以激活此途径。该机制被证明是TRPV4收缩特异性,既不是GSK2193874(10μm),蒙特洛特(10μm)也没有5bdbd(50μm)对普通收缩刺激组胺和ACH引起的收缩有任何影响(补充图E2B和C.).
在这一系列的实验中,我们已经证明TRPV4在人类ASM上的激活诱导ATP的释放,ATP激活靠近ASM的HLMCs上的P2X4受体,进而诱导cylts的释放,导致cylt1依赖的ASM收缩。这一机制在图6..
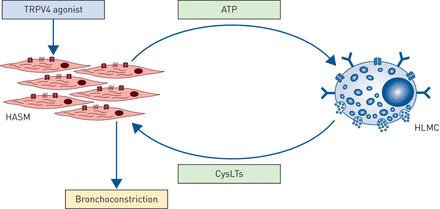
TRPV4诱发人气道平滑肌细胞(HASM)肥大细胞依赖性收缩的示意图。在这一系列的实验中,我们已经证明TRPV4在HASM上的激活诱导ATP的释放,ATP激活ASM束附近和内部的肥大细胞上的P2X4受体,从而诱导半胱氨酸酰白三烯的释放,从而导致cystlt1依赖性的ASM收缩。
讨论
由于支气管电池介导剂和细胞因子的IgE依赖性释放,旨在在特应性哮喘的发病机制中发挥基本作用,这有助于过敏原在过敏原暴露后的早期和后期反应有助于早期和后期反应的特征哮喘的发病机制中发挥着基本作用。然而,现在认识到,肥大细胞活化有许多IgE的独立机制,其在特征和非特征性哮喘和其他慢性肺病中可能发挥作用[4.].在这里,我们调查ASM-MAST细胞相互作用和非IgE依赖机制在收缩反应中发挥的作用,对“相关”哮喘介质的收缩反应。
肥大细胞蛋白酶被认为在哮喘的发展和持续性疾病的持续症状中发挥重要作用[4.].许多与过敏原相关的蛋白酶或从肥大细胞释放的蛋白酶是丝氨酸蛋白酶(胰蛋白酶样、糜蛋白酶样或中性粒细胞弹性蛋白酶样),可以激活GPCR PAR2。据报道,PAR2在过敏性和非过敏性哮喘中的作用是复杂的,与N奥奇斯等等。[34展示PAR2可以采取行动通过几种独立的信号通路;认为促炎效果是通过β-arrierin介导的介导,并且通过GPCR活化介导的保护作用并增加细胞内钙。但是,目前尚不清楚par2激活如何导致功能性后果,例如支气管痉挛[35].源自GPCR超家族激活的信号,包括PAR2,已经显示在某些瞬态受体潜在的家庭成员(包括TRPV4)上收敛,导致通道激活和敏化,其扩增疼痛,瘙痒和神经源性炎症[32那36].TRPV4激活有助于肺内的各种影响,包括感官神经激活,细胞内Ca2+ASM中的助焊剂[16-18]和Cyslt.1- 豚鼠和人气道组织的依赖性收缩[17].
在这里,我们首次展示了TRPV4激动剂GSK1016790A引起缓慢发作的能力,持续的ASM收缩在活的有机体内在TRPV4拮抗剂存在的情况下被消除。体外这种收缩也在发作和长期持续缓慢,并且由TRPV4抑制剂GSK2193874抑制。如前所述,我们证实,Cyslt抑制了这种收缩1受体拮抗剂孟鲁司特和5-LO抑制剂zileuton在豚鼠和人组织中的作用[17].由于已知Cyslts通过活化的肥大细胞合成[17那37[假设肥大细胞-ASM相互作用是该过程的核心。
为了进一步研究这种相互作用,我们初步研究了TRPV4激活是否能引起[Ca2+]一世在孤立的HASMCs中,这种评估经常被用作收缩的替代测量[38].TRPV4激动剂GSK1016790A诱导[Ca2+]一世在以前所示的Hasmcs中[16那17]但由于新颖技术评估,没有引起培养中的ASM细胞的收缩;ptychography [30.],利用光学密度的变化作为替代因子的收缩状态的变化。钙的增加通常是ASM细胞收缩的暗示;然而,已显示其他刺激在ASM中细胞内钙的强烈增加,但不引起收缩,包括苦味受体(TASR)激动剂[39,这反而会导致放松。肥大细胞已知存在于健康和非特应性患者的ASM束中[40]并且那些有哮喘的人,他们通过释放包括Cyslts(包括Cyslts)的各种调解器在收缩中发挥着关键作用[6.].因此,用原发性HLMC共同培养HASMC,以评估TRPV4诱导的收缩的肥大细胞依赖性。使用PTYChoguce,我们证明GSK1016790A只能在HASMC在HLMC存在下增加指示性收缩的光学密度。这对HLMC而言不太可能直接影响,RT-PCR表明TRPV4 mRNA在HASMC上表达但不在HLMC上。
由于TRPV4在HASMC上表达,但不在HLMC上,并且由于延迟的收缩响应,我们假设次要信使的参与。TRPV4在几种不同的细胞系统中诱导ATP释放,这可以采用肺部中具有各种下游效应的许多嘌呤菌株[18那19].类似地,我们发现添加TRPV4激动剂到分离的HASMC诱导ATP释放。ATP是在身体的每个细胞中发现的普遍存在的分子,并直接激活动物肥大细胞[20.-22].我们证明,与先前的研究一致,在HLMC的细胞表面上表达了许多丙基因符[23].此外,我们已经证明,在P2X4抑制剂存在的情况下,气道组织对ATP的收缩可以被消除,这表明可能是存在于HLMCs上的P2X4受体被ATP激活,并诱导囊性淋巴细胞的释放。P2X4是嘌呤能P2X受体中表达最广泛的一种[41],之前的工作已经将P2X4与哮喘联系起来,因为P2X4抑制剂5BDBD减弱了BALBc小鼠卵清蛋白“哮喘”模型中对抗原的反应[42那43].P2X4是Ca2+可渗透离子通道2+信号在调节hlmc分泌中起着重要作用[44].该机制也与P2X7激活有关,这可能导致LAD2人肥大细胞的脱升[31].在哮喘患者的BAL液中发现ATP及其分解产物水平升高[20.], ATP可引起支气管收缩和呼吸困难[45提示这可能是哮喘肺肥大细胞激活和囊性lt释放的相关途径。
在唤起支气管痉挛时识别PAR2-TRPV4-ATP轴的鉴定说明了肥大细胞可能在促使结构细胞的病理生理学和非特应性哮喘中的症状的致病生理学中的复杂作用。这些和类似的机制在响应于各种刺激的哮喘症状产生哮喘症状可能是重要的,所述刺激包括例如运动诱导的支气管痉挛(EIB)。Cyslts被认为是EIB的关键调解员;它们被从活性肥大细胞中释放,并且已经显示出Eib的哮喘学,痰液中的囊泡水平增加,并且呼出的呼吸冷凝物[46].此外,我们证明我们证明了抑制TRPV4介导的收缩的单一口服剂量的蒙特利亚斯特,其在运动后2,12和24小时施加显着的防护局部保护[47].认为EIB的症状被呼吸增加的渗透性和热效应引起了[46]已知激活TRPV4 [48].此外,在患有EIB的哮喘患者中,tryptase也被证明升高[49[在运动诱导的支气管痉挛中提供该轴的作用的进一步证据。
肥大细胞与哮喘ASM密切相关,可能是哮喘发病的关键效应细胞。然而,这种密切联系的功能后果尚不完全清楚。在这项研究中,我们发现了PAR2-TRPV4-ATP-cysLT轴在肥大细胞依赖性支气管痉挛中起作用。TRPV4的激活与GPCR PAR2有关,PAR2的激活已经被证明可以使两者变得敏感[36还是直接门TRPV4 [32那50].为了支持这一假设,我们已经表明胰蛋白酶会导致人体气管条的收缩通过PAR2-TRPV4-ATP-CYSLT轴的激活,因为丝氨酸蛋白酶抑制剂CANOSTAT甲磺酸盐抑制了收缩[51],TRPV4拮抗剂GSK2193874,P2X4抑制剂5BDBD和孟鲁司斯特。
总之,我们描述了一种涉及离子通道TRPV4的新型肥大细胞- asm相互作用。我们认为TRPV4在ASM上被内源性配体如花生四烯酸衍生物或蛋白酶激活,导致ATP的释放,可能通过pannexin离子孔激活P2X4。这一机制可能在哮喘中ige独立的肥大细胞介质释放中发挥重要作用,例如在EIB期间,以及在非特应性哮喘中,常见的空气变应原似乎没有发挥作用,但内源性的TRPV4间接激活因子(如胰蛋白酶)水平升高[49]还有Cyslt的地方1已显示蒙特洛斯特等受体拮抗剂是有效的[52].此外,这种机制也可能在其他肺部疾病中相关,其中已经鉴定出增加的肺组织肥大细胞和与疾病病理生理学相关[53].
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充图E1。a)ATP单独对初级HASM细胞收缩的影响。在0.3,1或3mm处的ATP没有引起使用PTYCHOGUCH分析的细胞收缩,在某些情况下有松弛。收缩刺激ACH(10μm)按预期引起细胞的收缩。数据显示为百分比从基线(休息状态)的变化,n = 2名患者,n = 17-27个细胞。b)载体,ATP在1mm和3mm和PMA(10nm)离子霉素(1μm)的效果从原发性人肥大细胞上释放到总胱抑素上释放。与载体对照相比,添加ATP(1或3nm)引起浓度依赖性浓度依赖性全囊性二硫代脲释放。所示的数据来自肥大单元中分离出1(73岁女性捐赠者)。ERJ-01458-2019.figure_e1.
补充图E2。a) PAR2 mRNA在6例患者的HASMCs中表达,2例患者的HLMCs中不表达,第三例患者PAR2 mRNA表达极低。GSK2193874、孟鲁司特和5BDBD对豚鼠离体气管常见收缩刺激组胺(b)和乙酰胆碱(c)收缩的影响。没有拮抗剂对不同于载体的收缩有任何影响。n=6 (HASMs), 3 (HLMCs), 3 - 4(气管)。erj-01458-2019.figure_e2.
可分享的PDF.
致谢
我们愿意为詹姆斯博拉基,薛辰和朝鲜大学(帝国学院)提供帮助,以协助一些器官浴,RTPCR和PTychography实验。
脚注
本文提供了补充材料www.qdcxjkg.com.
作者贡献:概念和设计:M.A. Birrell,M.G。Belvisi和S.J.Bonvini;数据分析和解释:M.G.Belvisi,M.A. Birrell,S.J.Bonvini,E. Dubuis,J.J.Adcock,M.A. Wortley和P. Bradding;写论文:S.J.Bonvini,M.A. Birrell和M.G.Belvisi。
利益冲突:S.J.Bonvini是由Astrazeneca雇用的。
利益冲突:M.A. Birrell由AstraZeneca雇用,是一名帝国学院纺场合约研究公司的非执行董事,从事呼吸前工作。
兴趣冲突:E. Dubuis无需披露。
利益冲突:J.J.Astazeneca采用Adcock。
利益冲突:M.A. Wortley无需披露。
利益冲突:P. Flajolet无需披露。
利益冲突:P. Bradding没有什么可披露的。
利益冲突:M.G.在研究期间,Belvisi报道了惠康信托和医学研究委员会的赠款;是由Astrazeneca雇用的,是一名董事学院纺丝合同研究公司的非执行董事,从事呼吸前工作,并为Ario Pharma,Aboca,Patara,Nerre,Medimmune和Boehringer Igelheim成为顾问。
支持声明:S.J.Bonvini和E. Dubuis由医学研究委员会(英国MRC)云母奖(MR / K020293 / 1)和Wellcome Trust(207504 / B / 17 / z)资助。M.A. Wortley由西北肺中心慈善机构提供资金。本研究中的人迷宫实验是在皇家Brompton和Harefield NHS基金会信托中的NIHR呼吸疾病生物医学研究单位的支持下进行了支持。莱斯特的工作得到了国家卫生研究所的支持莱斯特生物医学研究中心 - 呼吸道。表达的观点是作者的观点,而不是NHS,NIHR或健康部的观点。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2019年7月22日。
- 公认2020年2月27日。
- 版权©2020人队
此版本在Creative Commons归因许可证4.0的条款下分发。