摘要
动物模型可以为肺部感染的发病机制和免疫学提供非常详细的数据,对于开发新的治疗/预防策略以降低肺炎的发病率和死亡率是至关重要的http://bit.ly/2pdCzcH
介绍
尽管非常有效的抗生素和重症监护支持,与肺炎相关的死亡率没有显着自1960年代以来[减小1]。因此,仍需要改进的治疗和预防战略的一个主要要求,这将需要对肺炎的发病机制的新认识。动物模型研究参与性肺炎发病的分子机制时,有明显的高值,但他们也为面向临床研究新的治疗方法和疫苗,肺炎并发症直接相关的,并确定高危人群。在这篇文章中我们将介绍使用动物模型研究如何将是至关重要的,如果我们要减少与肺炎有关的巨大的发病率和死亡率。
背景上的动物模型
动物模型是低成本,广泛可用,可用于侵入性的协议,促进机制的详细研究,以告知临床方法。涉及与动物工作的问题归纳如下,并通过M在详细讨论izgerd和Skerrett(2],并在欧洲呼吸学会声188bet官网地址明“优化呼吸系统疾病实验研究” [3.]。存在各种各样的肺炎动物模型,哪种模型是最合适的将取决于正在解决的研究问题。非哺乳动物物种(昆虫、蛔虫和斑马鱼)是一种廉价而强大的工具,它概括了人类先天免疫和宿主细胞信号的许多方面。它们已被用来确定毒性决定因素[4- - - - - -9,他们缺乏高阶的感知力,这使他们从伦理的角度上具有吸引力。然而,它们受到缺乏哺乳动物呼吸系统或适应性免疫反应的限制。非人类的灵长类动物则是相反的极端,它们紧密地概括了人类的生理、免疫学和病理学,而且通常容易受到人类病原体的影响,但它们的使用引起了人们的主要伦理关注。因此,非人类灵长类动物模型通常局限于测试疫苗或潜在疗法的药代动力学、毒理学和有效性[10]之前在人类中测试,或关键结果与其他动物模型[得到的验证11,12]。啮齿动物模型是人类的先天免疫和适应性免疫的大多数方面精确的模拟一种妥协,并且也容易受到大多数人的肺炎病原体[13- - - - - -16]。有啮齿动物和人之间。一些重要的解剖学上的差异17,18肺炎]和动物模型中经常需要强制高数量的细菌(通常> 10的心愿6)19],而不是吸入[20,21],或者从上气道抽吸(图1a)。此外,多数研究者用健康的年轻成人的啮齿动物,而在人类中,肺炎很大程度上影响婴儿,免疫缺陷或老人。尽管存在这些问题的解剖,生理,免疫学和细胞生物学手段动物模型的重叠仍然复制人类感染的许多重要参数。
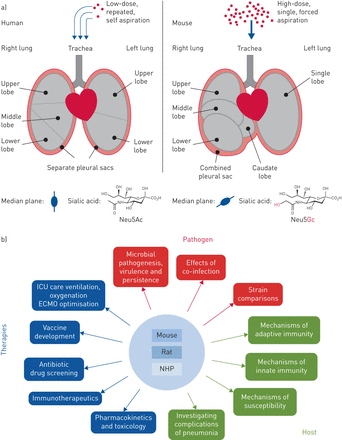
一)在人类和小鼠的肺之间的解剖和生化特性的主要不同点在于影响解释和使用肺炎包括感染的模式,小鼠肺的水平位置,肺解剖学的动物模型,和不同的细胞表面glyconjugates由于突变在CMAH基因在人类。b)该肺炎的动物模型中可以显影在人类中针对肺炎新颖预防性和治疗性干预时要使用的不同的角色。NHP:非人类灵长类动物。
动物模型的主要优点是可以通过多种方式来回答非常精确的研究问题。感染模型可与病原体的遗传操作相结合,以确定肺炎发展所需的特定微生物过程[22,23]。比较同一病原体的不同菌株可以说明为什么某些菌株在临床中占主导地位[24,25]和双重感染模型提供了重要的见解为什么呼吸道病毒感染常导致继发性细菌感染[26- - - - - -28]。主机可以使用免疫效应的治疗性或遗传耗尽[被操纵29],包括组织特异性靶向精确地定义如何宿主因素影响疾病的发展[三十]。感染模型中的宿主和病原体反应可以使用所有的“基因组”技术(包括单细胞测序和双物种RNA seq)、流式细胞术和在活的有机体内成像,共同提供的信息的详细级别是不可能的人类研究中复制,并在相当大的成本更低。因此,动物模型的巨大益处为免疫调节剂,抗生素,通风/氧合方案,疫苗接种,或对抗免疫衰老的治疗性测试(图1b)。因此,动物模型可以识别新的干预措施是否有可能在一段时间更短的时间取得成功,以相当低的成本,并与比人类研究的风险降低。
替代动物模型
有关实验替代动物模型,如组织培养模型,类器官是什么,离体人力物力模型和人类志愿者的病原体的挑战?可以将这些替代动物模型?最简洁的答案是不;肺炎的发展通过涉及肺驻留和招募免疫细胞,迅速变化的微生物群体,不同解剖隔室之间的复杂的相互作用,并且需要的细胞类型之间的广泛的串扰感染的多个阶段。这是远太复杂,通过组织培养系统或甚至类器官模型被充分取代。体外精确切割肺切片或全肺灌注/通气模型[31]通过它们的费用和小数量的可能的生物学重复的限制。感染的人体模型在很大程度上局限于在较温和的感染调查粘膜主机/病原体相互作用[32,33,34],而不是肺泡感染过程中所涉及的机制。
其中动物模型作出了重要贡献研究领域
其中动物模型已经产生了不可能容易地用其它方法获得的对肺炎重要数据中的特定区域在下面(中列出实施例所讨论的表1和说明图2)。

如何最新发现利用动物模型的例子可能会导致在不久的将来新的治疗和预防策略。iPSC细胞:人类多能干细胞。
定义谁是肺炎的风险
谁是在肺炎的风险有清晰的理解是必需的,但只能通过流行病学研究获得,如果风险因素是常见的(例如年龄,吸烟,合并症),或具有特别强的影响(例如补体缺陷)。相反,动物研究可以识别较弱或较不常见的诱因肺炎,并且还定义所涉及的分子机制。例如,指数上升的风险链球菌引起的肺炎长者肺炎[35,36]具有多因素的原因,都难以单独使用流行病学来定义。动物模型研究已经挂在DNA的完整性与年龄有关的变化和肠道微生物增加的背景炎症,其损害免疫力肺炎链球菌通过增加对细菌粘附上皮配体的表达,从而损害单核细胞功能,并减少TLR2表达[37- - - - - -39]。如果没有动物模型,我们就无法确定这些机制和调节肠道微生物群以预防肺炎的潜力。动物模型数据可以识别肺炎易感亚群之间的机制联系;例如,暴露于焊接烟雾、香烟烟雾、空气污染和老化都增加了患心脏病的风险肺炎链球菌肺炎,部分是通过血小板活化因子受体的增加的上皮表达[40- - - - - -42]。动物模型的数据也可以预测,可能易感性升高,然后可以在临床实践中寻找特定的感染群体,例如酪氨酸激酶抑制剂被证明削弱免疫烟曲霉在小鼠和临床资料已经证实这是患者的情况[43,44]。
潜在的病原体毒性电位差定义机制
由于病原体和宿主既可以是克隆的,动物模型的研究能帮助研究者排除未选中的病原体和宿主变化,以确定疾病表型的分子解释。例如,使用缺失突变体,被确定为肺炎球菌的毒力决定网站特定的角色,这有助于解释为什么肺炎球菌菌株在他们在不同的解剖部位的能力引发疾病而改变[45,46]。同样,双重感染动物模型有特点宿主与病原体因素如何影响流感引起的传输肺炎链球菌和疫苗接种的在阻止该键事件[功效47,48]。
肺炎的并发症发病机制
肺炎的并发症如积脓症、菌血症、败血症的影响上气道免疫力,感染扩散到心脏和中枢神经系统,以及inflammation-mediated肺损伤包括alveolar-capillary屏障崩溃,所有涉及多种细胞类型与进步的细菌侵入,交互和受到多个主机的影响因素包括性别、年龄、潜在的并发症,遗传和环境因素。动物模型已经帮助我们理解为什么这些并发症会发展,包括识别肺炎链球菌肺炎心肌侵袭[49],细菌易位通过间皮细胞如何使脓胸[50],以及为什么金黄色葡萄球菌引致过度的发炎反应,引致具破坏性的肺炎[51]。
确定新的治疗方法
微生物挑战的肺部炎症反应是在动物模型和人类,包括早期招募嗜中性粒细胞对病原体清除,然后渗出巨噬招募,以促进肺部炎症的分辨率模式类似。生长因子,例如粒细胞 - 巨噬细胞集落刺激因子(GM-CSF),G-CSF和M-CSF也表现出高度的啮齿动物和人类[之间的结构和功能相似性的52,53]。这使得这些常见的分子特征在动物肺炎模型中的作用得以描述,从而为肺炎的辅助治疗提供信息。例如,GM-CSF调节巨噬细胞的终末分化[54,55]在小鼠模型抵御肺炎[56,57],而GM-CSF缺乏是细菌性肺炎的重要危险因素[58]。GM-CSF的过表达肺内从提供高程度的保护小鼠肺炎链球菌肺炎,表明GM-CSF可以是未来的辅助治疗。事实上,吸入重组GM-CSF(沙格司亭,LEUKINE)改善患者的肺炎相关急性呼吸窘迫综合征氧合和结果[59],表明临床前动物模型帮助针对感染性肺部疾病的辅助治疗的发展。人类多能干细胞 - 巨噬细胞早期预防铜绿假单胞菌在小鼠呼吸道感染[60];这个和其他例子[61,62]可以帮助开发的人用抗生素无关的细胞免疫疗法。在动物模型中筛选抗生素化合物可以识别用于人肺炎新型抗菌疗法,以及诸如生物发光和细菌病原体生物光子成像更新的技术用于监测肺炎的实时进展和评估药效[提供强大的工具63- - - - - -68]。
新型预防方法
有没有可用于大多数呼吸道病原体,包括大多数呼吸道病毒的疫苗,金黄色葡萄球菌,革兰氏阴性肺炎的病原体,卡氏肺囊虫和烟曲霉.此外,现有的疫苗都有很大的局限性;的嗜血杆菌流感疫苗不能预防导致成人感染的非类型毒株和现有的流感病毒肺炎链球菌疫苗有限制的应变覆盖和最需要的老人,正是人口降低药效。因此,需要针对肺炎的病原体新的疫苗,但诱导保护肺免疫是更难实现比免疫力菌血症[69,70]。动物模型将是必不可少的用于定义防止肺部感染获得性免疫机制,确定最保护性抗原,和提高佐剂和抗原递送方法[71]。动物模型确定在保护呼吸道黏膜病原体如CD4 Th17细胞反应的关键作用肺炎克雷伯氏菌和肺炎链球菌(70,72]是依赖于特定的树突状细胞亚群[73],并在防止对调节性T细胞意想不到的作用肺炎链球菌(74]。这些数据表明,针对细胞外病原体的疫苗方法可诱导细胞免疫而非体液免疫。利用动物模型开发的新型疫苗递送系统和佐剂现已进入临床应用[75],而且会提高疫苗诱导的免疫靶向在未来肺。动物模型还可以通过筛选感染过程中高表达的基因,或通过识别天然获得保护性免疫反应所识别的抗原识别新的疫苗抗原候选[76,77]。总的来说,这是很难看到的新疫苗临床前研究可以在不使用动物模型来进行。
策略减少动物模型的数据的弱点
尽管它们的力量,动物模型不能完全概括人类的条件。这可以通过与组织培养、类器官或离体肺癌的实验数据。如何准确地对炎性刺激鼠类看法反映了人类的反应进行辩论[78- - - - - -80],但实验小鼠暴露于PETSHOP或野生型小鼠更紧密地确保了小鼠炎症反应模仿人类反应[81,82]。这提供了用于改善感染的小鼠模型中的效用潜在简单方法。动物模型的遗传修饰也可以提高其实用性。例如,删除任一胞苷酸N-乙酰羟化酶(CMAH,转换N-乙酰神经氨酸以N-羟酸对气道上皮细胞的唾液酸化glyconjugates)或载脂蛋白B-100脂蛋白(的有效抑制剂肺炎链球菌毒素肺溶菌素)增加小鼠的易感性肺炎链球菌感染 [83,84]。
结束语
只有动物模型本质上让复杂的多细胞系统的解剖情况下随时间变化的研究。鼠标遗传操作的易处理性,与新的“组学技术和应用组合在活的有机体内成像增强了我们确定宿主或病原体因素对肺炎易感性、发病机制和分辨率的影响的能力。动物模型仍然是检验新疫苗或抗菌素方法有效性的唯一方法。因此,动物模型可能仍然是成功开发新的肺炎治疗进展的关键。
脚注
利益冲突:C.J.奥利维拉有没有透露。
利益冲突:Maus没有什么要披露的。
利益冲突:J.S.布朗有没有透露。
- 收到2019年8月2日。
- 接受2019年10月3日。
- 版权所有©ERS 2020