摘要
右心室射血分数可由压力曲线计算http://bit.ly/2tjE37Q
在目前的问题欧洲呼吸杂志Heerdtet al。[1]关于验证从心导管插入术压力曲线计算的右心室射血分数(RVEF)的报告。这是非常有趣的,因为右心室(RV)功能是肺动脉高压症状学和结局的主要决定因素[2], RVEF相应地显著增加了这些患者的风险分层[3.].然而,射血分数(EF)是冲程容积(SV)与舒张末期容积(EDV)的比值,方程中没有压力。那么,如何从压力测量中计算出体积比呢?
正如最近所回顾的[4- - - - - -6]时,右心室功能与肺循环耦合的充分性由收缩末期与动脉弹性的比值(Ees/Ea)来定义。收缩末期弹性是收缩末期压力(ESP)与收缩末期容积(ESV)的比值。动脉弹性是ESP与SV的比值。Ees和Ea都有共同的压力或体积项,因此弹性比实际上可以简化为压力或体积比[7,8]: 其中Pmax是由RV压力曲线等体积部分的非线性外推计算得出的非弹射拍的最大压力[9].
其中Pmax是由RV压力曲线等体积部分的非线性外推计算得出的非弹射拍的最大压力[9].
仅用压力(Pmax/ESP)−1和仅用体积(SV/ESV)估计Ees/Ea比已被证明与金标准多拍或单拍方法很好地吻合[10],如Bland-Altman分析所示,没有(仅压力)或最小(仅体积)偏差。然而,同样的分析显示出相当广泛的一致性限制,特别是对于只计算体积的方法。在Bland-Altman分析中,偏差是准确度的衡量标准,而一致限度是精确度的衡量标准[11].需要注意的是,如前所述,用更容易测量的平均肺动脉压(mPAP)取代ESP [7],并应用于肺动脉高压患者运动引起的rv -肺动脉(PA)解耦[12],引入了一个与压力相关的偏置,可以近似地用公式[13]: 由于ESV等于EDV - SV,所以SV/ESV比值与EF [14]:
由于ESV等于EDV - SV,所以SV/ESV比值与EF [14]: EF则由H计算eerdtet al。[1]实际上等于:
EF则由H计算eerdtet al。[1]实际上等于: Heerdtet al。[1]通过后负荷操作或药物干预,在15只RVEF在18 - 59%之间的麻醉猪和6名患者(3名心力衰竭患者和3名RVEF在30 - 70%之间的肺动脉高压患者)中验证了这种仅通过压力测量EF的方法,这些患者接受了标准的诊断性右心导管和磁共振成像[1].根据实验动物数据,从RV压力曲线中预测EF的效果非常好,(EF绝对值)有−2%的小偏差,一致性范围为−9至+13%,在重复测量校正后降低到−3至+7%。测量的总体误差估计为12.5%。然而,临床数据在样本量小和不均匀以及三尖瓣反流对成像的影响方面不太有说服力,但压力衍生EF则没有。正如作者所承认的那样,在进一步的临床验证之前,从压力曲线估计体积的概念可能是正确的。
Heerdtet al。[1]通过后负荷操作或药物干预,在15只RVEF在18 - 59%之间的麻醉猪和6名患者(3名心力衰竭患者和3名RVEF在30 - 70%之间的肺动脉高压患者)中验证了这种仅通过压力测量EF的方法,这些患者接受了标准的诊断性右心导管和磁共振成像[1].根据实验动物数据,从RV压力曲线中预测EF的效果非常好,(EF绝对值)有−2%的小偏差,一致性范围为−9至+13%,在重复测量校正后降低到−3至+7%。测量的总体误差估计为12.5%。然而,临床数据在样本量小和不均匀以及三尖瓣反流对成像的影响方面不太有说服力,但压力衍生EF则没有。正如作者所承认的那样,在进一步的临床验证之前,从压力曲线估计体积的概念可能是正确的。
这种方法本身可能比看起来要复杂得多。一个关键步骤是离线检查压力曲线,以确定等体积部分,以确定Pmax [9].为此目的,大多数研究依赖于dP/dt的一阶导数和人工识别舒张期结束和开始[9,10,13].一种新引入的依赖于dP/dt二阶导数的自动化方法降低了测量的可变性,但将Pmax平均低估了13% [15].这种低估必然与ESP的高估有关,因此可能导致Ees/Ea的低估[16,17].Heerdtet al。[1]开发了一种基于dP/dt二阶导数的替代自动化方法,但使用了细化的分布函数(所谓的“4参数威布尔峰拟合”)取代了更传统的正弦函数。此外,作者严格地确定ESP为最大弹性点,这优于mPAP的重新计算[13]或用压力-体积曲线Pmax到收缩部分的切线来图形化确定[9].所有这些改进可能改善了EF的预测,但并没有完全纠正负偏倚,其仍保持在6-8%。
右心室通过收缩力的相应增加来适应肺动脉高压后负荷的增加,这最初保持了流量输出、尺寸,从而也保持了EF。这种同量适应最终失败,因此RV然后依赖于异质维度的增加来维持流量输出(即.但代价是充盈压力增加、全身充血、心室负相互作用和心排血量不可挽回的下降[4- - - - - -6].研究表明,RV - pa耦合有很大的储备,Ees/Ea比值必须从正常值1.5-2.0降低到0.8-0.9,RV体积才会高于正常值,生存期才会下降[18].同一研究表明,随着Ees/Ea降低至35%,RVEF降低,低于35%,必然与保留SV时EDV和ESV增加有关[18].在肺动脉高压患者中,理论的EF双曲线下降伴随Ees/Ea下降以及从适应不良到衰竭的进展图1.考虑到H确定的估计误差eerdtet al。[1]从动物实验中,存在一个解耦区,实际上对应于先前直接测量肺动脉高压患者的EF较高或Ees/Ea较低[18].这可能是由于ESP/ESV关系的线性假设导致了不现实的非应力体积外推[7].心室-血管耦合不仅仅是“伪装的EF”,正如曾经有人提出的那样[19],并仍然是评估RV功能适应负载条件的金标准[4- - - - - -6].然而,在临床实践中,不可能常规获得Ees和Ea,临床医生必须对替代EF感到满意。
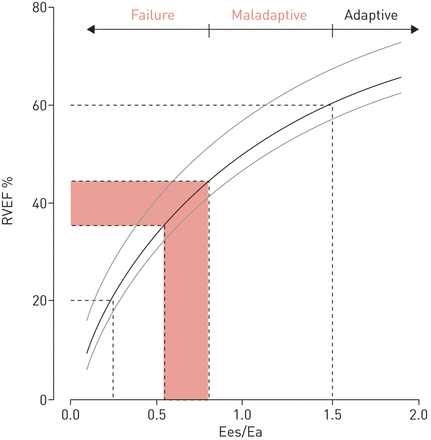
由方程Ees/Ea=EF/(1 - EF)预测的右心室射血分数(RVEF)与收缩末期动脉弹性比值(Ees/Ea)之间的关系,重新排列为EF=Ees/(Ees+Ea),在从正常到适应不良和衰竭的进展过程中。阴影区域定义了一个解耦区,在此区域下,右心室尺寸比正常增大,右心衰症状出现。
RVEF的降低,无论如何测量,都是心力衰竭生存率降低的独立预测因素[20.]和多环芳烃[21- - - - - -24].EF的临界值为35%,与右心室体积增加有关[14]也是roc推导出的good的行列式与初诊断和随访时PAH生存率低[23,24].EF的降低与RV尺寸的增加有关[14],因此,是RV重塑的综合措施。治疗诱导的右心室重塑逆转(在该研究中通过超声心动图评估)已被证明可显著改善PAH患者的预后[25].然而,在针对肺循环的单一药物治疗下,逆转右心室重塑和充分改善EF在PAH中并不常见[26,27].结合两种靶向治疗,最好是静脉注射前列环素类似物,更有可能有效,与肺血管阻力(PVR)更重要的降低成比例[28,29].最近有研究表明,在血管扩张剂挑战评估的初始不可逆疾病的PAH患者中,前期三次靶向治疗组合可使PVR降低50%以上[30.,31].这种效应与显著的临床改善和死亡率降低有关,可能与RVEF的充分增加和右心扩张的完全逆转有关[31].
总之,测量RVEF对指导肺动脉高压的治疗至关重要。Heerdtet al。[1]值得称赞的是,这一信息可以通过右心导管插管时的右心室压力分析获得。该方法将需要自动化,以便在导管实验室常规应用,并需要进一步验证与核磁共振成像的金标准。然而,这一令人振奋的想法可能会在认识和治疗严重肺动脉高压的病理生理学方面带来临床有用的进展。
可共享的PDF
脚注
利益冲突:R. Naeije没有什么可透露的。
利益冲突:M.J. Richter没有什么可透露的。
利益冲突:r·范德普尔没什么可透露的。
利益冲突:K. Tello没有什么可透露的。
- 收到了2019年12月6日。
- 接受2019年12月10日。
- 版权所有©ERS 2020















