抽象的
呼吸困难是插管患者的常见和强烈症状,但在重症监护单元(ICU)中的非侵入机械通气期间,呼吸困难的注意力很少。
本研究的目标是量化呼吸困难对急性呼吸衰竭(ARF)接受非血栓性衰竭(ARF)的患者的患病率,强度和预后对急性呼吸衰竭(ARF)的二级分析,该患者接受ARF的通风支持的患者的前瞻性观察队列研究在法国和比利时的54个icus。呼吸困难通过修改的Borg规模测量。
426例患者中位(四分位数范围)呼吸困难评分在入院时为4(3 - 5),在第一次NIV治疗后为3 (2-4)(p=0.001)。第一次NIV治疗后呼吸困难强度≥4与顺序器官衰竭评估评分(OR) 1.12, p=0.001)、呼吸频率(OR 1.03, p=0.032)、焦虑(OR 1.92, p=0.006)、渗漏(OR 2.5, p=0.002)和动脉二氧化碳张力(OR 0.98, p=0.025)相关。呼吸困难强度≥4与NIV失败(OR 2.41, p=0.001)和死亡率(OR 2.11, p=0.009)独立相关,但与较高的icu后负担和生活质量改变无关。
在接受NIV治疗的ARF患者中,呼吸困难是频繁和强烈的,与NIV失败和较差的预后风险相关。
抽象的
在ICU接受NIV治疗的患者中,呼吸困难是常见的,与较差的预后相关http:///wly/sh3z30kaieo.
介绍
呼吸困难是一种威胁性感觉,与疼痛具有共同的神经网络和临床特征[1,2].与疼痛相比,疼痛在重症监护室(ICU)受到了主要关注[3.,4,很少有人注意呼吸困难[5].然而,几乎一半的插管患者体验了呼吸困难,他们将其形容为激烈,作为其ICU的最糟糕的经历之一[6,7].呼吸困难也与延迟拔管有关[6].最后,有一体的文献表明,负呼吸道相关的经验可能在ICU相关的后创伤后应力综合征的发病机制中发挥重要作用,从而改变了生活质量(QOL)[8].
关于ICU中呼吸困难的大多数数据来自预热患者中进行的研究[5,6].然而,由于不断使用非侵入性通风(NIV)而导致急性呼吸衰竭(ARF)的越来越多的患者现在进行管理,而不会被提交[9]高流量氧气的潜在益处[10].
虽然Dyspnoea是对稳态威胁的警告标志[1[接受NIV作为ARF的一线治疗,尚未系统地评估其对结果的患病率,强度和影响。在这些患者中,呼吸困难是ARF的关键症状之一,也可以通过NIV调节。一些数据间接暗示呼吸困难可能在接受NIV的患者中经常和严重,并且可以响应NIV [11- - - - - -15].
对法国和比利时54例ICU患者机械通气(MV)的前瞻性队列进行二次分析的主要目的是量化因急性呼吸综合征(ARF)接受无创通气的患者在ICU入院时和第一次无创通气治疗后的呼吸困难发生率和强度。我们也检查了与呼吸困难相关的因素。最后,我们研究了呼吸困难对NIV成功或失败、结局、生活质量和icu后负担的影响。
患者和方法
本研究的人群来自54例法国和比利时icu患者的前瞻性观察研究,REVA的成员的网络(在机械通风研究网络)或FAMIREA研究小组(提高沟通的有效性与ICU病人的家属),最初是用来评估和合使用的频率和适应症和评估和合ICU生存的影响。
参与中心和合作者列于“致谢”部分。该研究经法国语言学会的机构审查委员会批准了呼吸学医学(Sociétédepneumologiede languefrançaise)并在公开的数据库上注册(ClinicalTrials.gov,标识符:nct01449331.).所有患者或其亲属均获得书面知情同意。另外两项基于该队列的研究也发表在其他地方[9,16].
研究人群
在2010年11月和2011年4月之间的2个月入学期间,每个参与的ICU包括在预期队列连续成年人中,需要呼吸率的呼吸率(侵袭性MV或NIV),如呼吸率> 30次循环所定义·Min−1或者通过脉冲血氧血管测量的呼吸窘迫的迹象或呼吸窘迫症状(年代阿宝2房间空气上的<90%。出于现在的目的后HOC.研究,只有收到尼弗作为ARF的一线治疗的患者。仅排除了接受核心舒适性护理的患者,并排除了患有缺失数据或呼吸困难数据的患者。
数据采集
每天在ICU,医院出院和ICU后90天遵循患者,在ICU排放后90天(第90天)。在每个时间点,研究调查人员完成了标准化的电子案例报告表格。收集的人口数据和病史包括:年龄,性别,简化急性生理学评分(SAPS)II [17],顺序器官失败评估得分(沙发)[18]、基础疾病,如慢性呼吸系统疾病(慢性阻塞性或限制性肺病、肥胖、神经肌肉疾病、等等。)、家庭氧疗的需要、慢性心力衰竭(纽约心脏协会(NYHA) III或IV级)和免疫抑制(定义为中性粒细胞计数低于1000 / mm3.,通过癌症化疗治疗的恶性肿瘤,免疫抑制治疗用于固体器官移植,皮质类固醇治疗,每日剂量为20毫克或更高至少3周或艾滋病)。ARF的原因是急性慢性呼吸衰竭(定义为预先存在的呼吸道疾病患者的呼吸衰竭),心形成肺水肿或新创ARF(定义为呼吸衰竭而没有加剧慢性肺病或心力衰竭,也称为低血量症)。
记录呼吸频率、呼吸困难强度和动脉血气值(1)在ICU开始呼吸支持前和2)在第一次NIV治疗后。为了评估呼吸困难的强度,患者被要求评价他们的呼吸不适(用法语“不幸的呼吸们)的分类比例(1-10)[19由与特定数字相联系的语言描述符组成,其中数字和相应描述符的间距本质上提供了具有比例属性的类别规模。这个量表的范围从0到10不等,0表示无呼吸困难,10表示最大的呼吸困难。它被用来识别两组患者根据呼吸困难强度为4,符合“有点严重的呼吸困难”。这种划分是基于呼吸困难和疼痛的许多相似特征(有害感觉、共同通路、涉及的相似皮层区域和情感维度)。疼痛评分为4分或4分以上被认为是镇痛的明确指征[20.].在本研究中,呼吸困难强度小于4被定义为“轻度或无呼吸困难”,而呼吸困难强度大于或等于4被定义为“中度至重度呼吸困难”[19,21].还记录了空气泄漏和焦虑,以及镇痛药(包括阿片类药物)的处方,因此需要侵入式MV,ICU和医院住院时间,ICU死亡率,住院医院死亡率和日90日死亡率.
对NIV成功或失败的定义如下:需要气管插管或停药24小时内死亡的患者归类为NIV失败。使用NIV治疗直到不再需要呼吸支持的患者被归类为NIV成功患者。ICU出院后90天(第90天),在FAMIREA研究小组的心理学家和社会学家的指导下,经过培训的社会工作者通过电话采访了幸存者。患者被要求完成36项简表健康调查(SF-36)以评估与健康相关的生活质量(HRQoL),以及事件影响量表修订(IES-R)以评估创伤后应激障碍(PTSD)相关症状[22,23]医院焦虑和抑郁症(曾经)量化焦虑和抑郁症的症状[24(按顺序)。HADS和IES-R评分越低,icu后负担越轻,SF-36评分越低,HRQoL越差。
数据质量
一名没有参与研究的ICU医生通过研究病例报告表格与病历表的比较,解决了调查者输入数据的不一致。数据库通过对所有ICU变量的独立检查,随机抽取10%的患者进行审计。
统计分析
定量变量描述为中位数(四分位范围(IQR)),组间比较采用非参数Wilcoxon秩和检验或配对Wilcoxon秩和检验。定性变量用n(%)描述,组间比较采用Fisher精确检验。使用Kaplan-Meier估计法估算ICU中位数和住院时间,关注的事件是活着出院,审查事件是死亡。
采用多因素logistic回归分析,研究ICU入院或首次NIV治疗后中至重度呼吸困难的相关因素以及NIV失效和医院死亡率的相关因素。多变量模型是用单变量分析中p值小于0.05和/或被认为与临床相关的变量建立的。以p值小于0.05为基础进行的消除过程进行逆向逐步选择程序。最终模型中变量的调整优势比(ORs)以其95%的CIs呈现。对连续变量进行对数线性检验,对非对数线性变量进行分类。对最终模型进行了Hosmer-Lemeshow拟合优度检验。最后,采用单因素分析(Fisher确切检验或Wilcoxon检验)评估呼吸困难对ICU死亡率、HRQoL (SF-36)、ptsd相关症状(ires -r)和焦虑和抑郁症状(HADS)的影响。使用log-rank检验比较住院或ICU的中位数住院时间。
所有测试均为双面,P值小于0.05被认为是统计学意义的。所有统计分析都与R统计软件,版本3.2.0(R项目进行统计计算;www.r-project.org/).
结果
研究人口和呼吸困难的患病率
在研究期间,2367名需要通风支持的患者被录取为ICU(图1).其中1799种,接受了侵袭性通气支持,1203例,非归因状况,596例作为ARF的一线治疗。剩余的568名患者接受了NIV作为ARF的一线治疗。其中61名接受舒适性NIV和81名患有呼吸困难或不完全数据的81名患者的患者被排除在研究之外。在第一次NIV会议上,总共对呼吸困难和第一次NIV会议进行了呼吸困难和第一次核糖会议后,共分配了426名患者。表格1在ICU入学时表明患者特征。NIV接口和呼吸机模式和设置在别处描述[9].
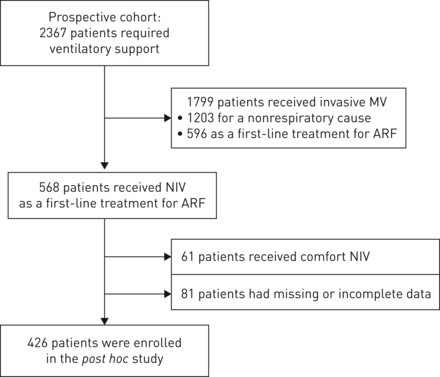
研究流程图。MV:机械通气;箴:无创性通气;ARF:急性呼吸衰竭。
在入学ICU之前,在启动NIV之前,中位呼吸困难评分在改良的Borg规模上是4(3-5),并且在234名患者中得分为4或更多(中度至严重的呼吸困难)(55%).在第一个NIV会议之后,中位呼吸困难评分降至3(2-4)(P <0.001),分数为166名患者(39%)。呼吸困难的中位绝对变异为1(0-2),219名患者(51%)中是一个或多个点。
ICU入院时和第一次NIV治疗后中至重度呼吸困难的相关因素
多变量逻辑回归分析表明,关于ICU入院,呼吸率(循环·MIN)−1)是与中度至严重的呼吸困难独立相关的唯一因素(见表格1对于与ICU入院中适度至严重的呼吸困难相关的因素)。多变量逻辑回归分析还表明,在第一个NIV会议之后,五种因素与呼吸困难独立相关。四种因素(沙发,ICU入院,焦虑和泄漏的呼吸率)与中度至严重的呼吸困难有关。但是,患者具有高动脉二氧化碳张力(P华2)发生中度至重度呼吸困难的可能性较低(见表2.第一次NIV治疗后与中度至重度呼吸困难相关的因素)。
呼吸困难与核心失败之间的关联
NIV失败率为31% (n=133)。在多因素logistic回归分析(在选择过程后),3个因素独立地与NIV的失败或成功相关(见表3对于与NIV失败相关的因素)。在第一个NIV会话与NIV衰竭相关后,高沙发评分和中度至严重的呼吸困难,而急性慢性呼吸衰竭作为沉淀因子与NIV成功相关。与患者相比,患有急性慢性呼吸衰竭的患者不太可能经历NIV失效新创ARF(或0.40(95%CI 0.23-0.70),P = 0.001)。然而,在第一个NIV会议后,患有中度至严重的呼吸困难的患者更可能经历NIV衰竭(或2.41(95%CI 1.49-3.91),P <0.0001)。
呼吸困难与结局、生活质量和icu后负担的关系
ICU入院的中度至严重的呼吸困难与任何结果更改无关(见表4.有关死亡率,住院时间的数据,生活质量和后ICU的负担)。此外,SF-36和焦虑和抑郁子分数,IES-R得分并未表明在ICU入院或第一次NIV会议上的中度至严重的呼吸困难患者中的患者造成更大的负担。
相反,在单因素分析中,第一次NIV治疗后的中度至重度呼吸困难与较高的ICU、住院和90天死亡率相关,也与较长的住院时间相关。多因素logistic回归分析表明,三个因素对住院死亡率有独立的预测作用。其中两个因素(第一次NIV治疗后的中度至重度呼吸困难和入院时的SOFA评分)显示出正相关,而一个因素,P华2关于ICU入学,展示了负关联(见表5.对于与住院医生有关的因素)。
讨论
本研究的主要和主要结果可以如下综述。在患有疾病的ICU的患者人口中:1)在第一个NIV会议与焦虑相关后,呼吸困难水平高,中度至严重的呼吸困难;2)第一个NIV会议后的中度至严重的呼吸困难与NIV衰竭和随后的插管独立相关;3)在第一个尼弗会议后,中度至严重的呼吸困难持续存在于历史较长的住宿和医院死亡率之后,但与ICU后负担或受损的QOL无关。据我们所知,这是探讨患有ARF的非加管患者患有呼吸困难并用NIV治疗的最大研究。呼吸困难已被测量为许多试验中的次要结果,评估NIV在急性对慢性呼吸衰竭和急性心胸性肺水肿中的益处[11- - - - - -14],作为终身患者核育效果的初级结果[15].然而,在如此大的人群中,呼吸困难的患病率及其危险因素和预后影响尚未进行研究。
呼吸困难的患病率和强度
ICU入院(在NIV发酵之前)时,中度至严重的呼吸困难的患病率为55%,在第一次核育第一个核育次数后39%。这种患病率类似于先前研究中报告的。50%的插管患者一旦他们能够回答有关的症状相关的问题,视觉模拟规模的中位数呼吸困难评分是五个[6].在包括呼吸困难评分在内的关于NIV治疗ARF疗效的试验中,呼吸困难评分在视觉模拟量表上从3到6 [11- - - - - -14所有研究中有高水平的呼吸困难。类似的疼痛评分需要立即治疗,并构成镇痛的明确迹象[20.].之前的报告表明,修改的Borg规模的最小临床重要差异(MCID)是一个点[25- - - - - -27].值得注意的是,第一次NIV治疗对呼吸困难有中等程度的影响,只有一半的患者呼吸困难评分下降1分或1分以上。
虽然在患有ARF的患者的患者开始之前观察呼吸困难在患有疾病之前并不令人惊讶的是,因为呼吸困难是ARF的主要临床特征之一,但即使在第一个NIV会议之后,我们患有该人群中观察到的呼吸困难严重程度的惊讶.这些研究结果表明,应在为ARF承认的ICU患者中积极调查呼吸困难,以与疼痛相同。必须强调的是,呼吸困难的救济是一个基本的临床使命,就像在痛苦的情况下,目前被一些作者认为是一个基本的人权[28,29].
从理论上讲,NIV可以缓解呼吸肌肉卸载引起的呼吸困难[30.由于患者呼吸机相互作用差,加剧了呼吸困难。在本研究中,我们观察到中位呼吸困难评分响应NIV而降低。
呼吸困难相关因素
焦虑与第一次NIV治疗后的呼吸困难独立相关,如先前在机械通气患者中的报道[6].焦虑和呼吸困难之间的相互作用在两个方向上具有因果关系复杂。焦虑,如疼痛,可以通过刺激通风驱动并因此通风来增加呼吸困难[31].相互作用,呼吸困难产生焦虑,并且已经清楚地证明了呼吸困难的缓解减少了焦虑[32].现在有一个越来越多的证据来支持焦虑和呼吸困难之间重叠的概念,并且应该改善另一个救济[31,33].
泄漏也与呼吸困难无关。在NIV患者中,泄漏是一个明确证明的呼吸模式和患者通风机异步的改变原因[34,35].在稳定的慢性阻塞性肺疾病(COPD)患者家中接受无创通气治疗时,调整呼吸机设置可减少不同步和漏气,改善晨间呼吸困难[36].因此,调整呼吸机的设置可能有助于缓解患者明显的呼吸困难。在插管患者中也有类似的观察报告[6].
值得注意的是,虽然中度至严重的呼吸困难的患者更有可能接受镇痛药,包括阿片类药物,但只有小比例(16%)患者接受此类药剂,这可能与对呼吸抑郁症的恐惧有关。然而,一些患者可能被剥夺了呼吸困难缓解治疗。这些药物在ARF患者中的受益风险平衡仍然未知。
新和合本失败
本研究的主要发现之一是呼吸困难,ARF的关键症状,与NIV失败相关。更具体地说,第一个和合会话后呼吸困难,但不是在入住ICU呼吸困难或呼吸困难的绝对变化,与和合失败,表明改进后的呼吸困难首先和合会议旨在治疗ARF可能构成有用的标志回应你们的质量。在COPD急性加重期,呼吸困难没有改善也与治疗失败相关[37].
临床结果
呼吸困难显示与较高的短期和长期死亡率相关。以前的研究已经建立了类似的联系在非批评患者中,呼吸困难是患有死亡率的患者,并构成了潜在疾病的代理,特别是心脏和肺病[38].例如,单独的呼吸困难是稳定COPD患者存活的预测因子[39]和患者提到心脏压力测试[40,41].在更急剧的环境中,呼吸困难是患者入院治疗的预测因子,患者患有COPD的急性加剧[42[疑似患者[43]或确认[44] 急性心肌梗塞。最后,即使在没有先前诊断的心肺疾病的患者中,呼吸困难也与心房颤动和心肌梗死的风险较高相关[45是全因死亡率的预测因子[45,46].据我们所知,这是第一次在第一次NIV会议后报告呼吸困难之间关联的研究以及ICU患者的死亡率较高。
而呼吸困难与icu后负担和生活质量无相关性。这一阴性结果更加令人惊讶,因为众所周知,呼吸困难与疼痛和口渴一样是ICU的压力源[3.,7]最近的数据表明,负呼吸学相关的经验可以在ICU相关的后创伤后应激综合征的发病机制中发挥重要作用[47,48].
限制
本研究提出了许多需要承认的局限性。首先,我们选择通过Borg Scale而不是视觉模拟量表量化Dyspnoea。这两个尺度是最常用于测量ICU中呼吸困难的两种仪器[49,50.].两种尺度与其有效性之间存在强烈的相关性,并且在危重病人中验证了可靠性和可靠性[51.,52.].不幸的是,这些工具的使用需要患者保持警觉和定位,而每一种工具都只是一维的,只能测量呼吸困难的强度。其次,我们只对两种情况下的呼吸困难进行了量化,一种是在ICU住院时,另一种是在第一次NIV治疗后。基于多次重复测量的纵向分析将提供额外的结果[37].第三,患者没有系统地评估谵妄,尽管谵妄可能对呼吸困难评估产生影响。然而,无法提供明确和连贯的答案的患者并不包括在研究中(那些被排除在不完整或缺少数据的人图1).最后,该研究是对预期队列的额外分析,其中第一个目标不是接受NIV患者呼吸困难的研究。
脚注
这项研究是注册ClinicalTrials.gov与标识符nct01449331..
作者贡献:L.危险,E.Azoulay和A. Demoule设计了这项研究。A. Demoule和E. Azoulay协调了这项研究。A. Kouatchet,S.Jaber,F. Meziani,S. Perbet和A. Demoule负责患者筛查,入学和随访。L.危险,C.Montlahuc,M. Resche-Rigon,E.Azoulay和A. Demoule分析了数据。L.危险,C.Montlahuc,T. Similowski,E.Azoulay和A. Demoule写了稿件。所有作者都有完全访问所有研究数据,有助于起草稿件或批判性地修改它以进行重要的知识分子,批准了稿件的最终版本,并对数据的完整性以及数据分析的准确性负责。
包括研究患者的贡献者名单:昂热大学医院,法国昂热:A.Kouatchet,A. Mercat,S. Mortaza;Pellegrin Hospital,Bordeaux,法国:F. Vargas;圣安德烈医院,波尔多,法国:O. Guisset;AmbroiseParé大学医院,Boulogne Billancourt,法国:L. Bodson,C.Charon;Bourg-en-Bresse医院,Bourg-en-Bresse,法国:X. Tchenio;Bligny Medical Center,Briis-Sous-Forges,法国:P. Andrivet;Louis Pasteur医院,Chartres,法国:M. Hamrouni,P. Kalfon;AntoineBéclère大学医院,克拉姆特,法国:O. Jacobs;加布里埃尔·蒙特里普大学医院,法国克莱蒙 - 法兰兰:B. SouWeine;米德大学医院酒店,克莱蒙 - 法兰德,法国:S.Perbet,J.M康宁; Sud Francilien Hospital, Corbeil, France: C. Clergue; Louis Pasteur Hospital, Dôle, France: D. Perez; Raymond Poincaré University Hospital, Garches, France: J. Aboab, G. Miloud; Bicêtre University Hospital, Le Kremlin-Bicêtre, France: L. Camous, D. Osman; Bretagne Sud Hospital, Lorient, France: P. Quinio, S. Kilani; La Croix Rousse University Hospital, Lyon, France: G. Bourdin, C. Guerin; North University Hospital, Marseille, France: M. Castanier, L. Papazian; La Timone University Hospital, Marseille, France: B. Eon, M. Gainnier, D. Lambert; Sambre-Avesnois Hospital, Maubeuge, France: W. Joos; Meaux Hospital, Meaux, France: X. Forceville, J. Martin; Marc Jacquet Hospital, Melun, France: S. Jochmans; Guy de Chauliac University Hospital, Montpellier, France: P. Corne; Saint-Eloi University Hospital, Montpellier, France: J. Carr, M. Conseil, S. Jaber; André Grégoire Hospital, Montreuil, France: V. Das; Central University Hospital, Nancy, France: M. Conrad; Hôtel Dieu University Hospital, Nantes, France: N. Brule; L'Archet University Hospital, Nice, France: J. Dellamonica; La Pitié-Salpêtrière University Hospital, Paris, France: A. Demoule, M. Schmidt; University Hospital, Nîmes, France: J.Y. Lefrant; Hôtel Dieu University Hospital, Paris, France: A. Rabbat; Cochin University Hospital, Paris, France: B. Zuber, J.P. Mira; Georges Pompidou University Hospital, Paris, France: E. Guerot; Lariboisière University Hospital, Paris, France: F. Bart, M. Legrand; René Dubos Hospital, Pontoise, France: J. Richecoeur; Reims University Hospital, Reims, France: J. Cousson; Poitiers University Hospital, Poitiers, France: D. Chatellier; Pau Hospital, Pau, France: J.N. Drault, W. Picard; Tenon University Hospital, Paris, France: M. Fartoukh, J. Messika; Saint-Louis University Hospital, Paris, France: E. Azoulay, D. Schnell; Saint-Antoine University Hospital, Paris, France: E. Maury, M. Alves; Saint-Joseph Hospital, Paris, France: M. Garrouste-Orgeas, B. Misset, S. Touati; Roanne Hospital, Roanne, France: P. Beuret, X. Fabre; Roubaix Hospital, Roubaix, France: P. Herbecq; Saint-Malo Hospital, Saint-Malo, France: V. Botoc, S. Chevalier, F. Collet; Hautepierre University Hospital, Strasbourg, France: V. Castelain, R. Janssen-Langenstein; Central University Hospital, Strasbourg, France: F. Meziani, N. Dumoussaud, H. Rahmani; Versailles Hospital, Versailles, France: S. Legriel; Bretonneau University Hospital, Tours, France: E. Massere; Tourcoing Hospital, Tourcoing, France: H. Georges; Toulon Hospital, Toulon, France: J.M. Arnal; Jules Bordet Institute, Brussels, Belgium: A.P. Meert; Brugmann University Hospital, Brussels, Belgium: J. Devriendt; Saint-Pierre University Hospital, Brussels, Belgium: P. Deschamps; Ghent University Hospital, Ghent, Belgium: P. Depuyt, D. Benoit.
利益冲突:S. Jaber报告了来自提交的工作之外的Fisher和Paykel,Dreter,Medtronic和Xenios的个人费用。
利益冲突:T. Similowski报告Astrazeneca,Boehringer Ingelheim France,GSK,Lungpacer Inc,Teva,Chiesi,Pierre Fabre和Invacare的个人费用,在提交的工作之外,诺瓦斯的个人费用和非财政支持。此外,T. Similowski还具有专利的“脑通风机界面,以改善呼吸困难检测”许可的空气液化物医疗系统和敏感。
兴趣冲突:E. Azoulay报告法国卫生部的补助金,从富裕的公司讲授的亚克斯翁,MSD和百乐仪,赠款和非财政支持(旅行费用)的个人费用,以及来自Gilead的个人费用和董事会参与的个人费用,在研究期间。
A. Demoule报告在提交的工作之外,来自美敦力的个人费用和非财政支持、来自飞利浦的拨款、个人费用和非财政支持、来自Resmed和Fisher and Paykel的拨款和个人费用、来自百特和汉密尔顿的个人费用以及来自法国卫生部的拨款。
支持声明:该工作得到了法国卫生部的授予,援助 - QualiqueHôpitauxdeAris(AOM 09006)和法国重症监护社会。本文的资金信息已存入CrossRef Resder注册表.
- 已收到2017年12月18日。
- 接受5月21日,2018年。
- 版权所有©ers 2018















