摘要
不可逆转的肺血管病变的存在解释了为什么达斯替尼诱导的PAH可能经常持续存在http:////wly/mkwi30hrwfc.
编辑器:
我们饶有兴趣地阅读了W先驱报等等。[1]对达沙替尼致肺动脉高压(PAH)远期预后的影响。作者报告了21例经右心导管(RHC)证实的肺动脉高压病例,并与达沙替尼有关。尽管停用达沙替尼后,大多数患者病情改善,但在长期随访中,三分之一以上的患者仍存在肺动脉高压,另外两名患者在静息血流动力学指标恢复正常后仍存在持续性运动性肺动脉高压。同样,年代哈等等。[2]报告了41例达沙替尼诱导的肺动脉高压经RHC证实,只有58%的患者肺动脉高压完全缓解,但随访的RHC或超声心动图通常没有记录。如W所述先驱报等等。[1,这些数据提示达沙替尼可能导致不可逆的肺血管功能障碍和重构。大鼠和人肺内皮细胞的实验模型支持这一假设,因为它表明达沙替尼通过产生线粒体活性氧引起剂量依赖的肺内皮功能障碍和凋亡,而伊马替尼没有观察到这种现象[3.].到目前为止,还没有公开的证据表明人类肺中存在这种病理异常。我们报告了一例达沙替尼引起的严重PAH患者,尽管药物停止和积极的多环芳烃特异性治疗进展,并最终接受肺移植。
32岁的男性被诊断为慢性髓性白血病(BCR-ABL1 +),用伊马替尼,尼洛替尼和达斯替尼依次对待。36个月后达斯替尼开始,他开发了毛细血管前肺动脉高压,rhc通过平均肺动脉压(MPAP)为57mmHg,肺动脉楔压9mmHg,心脏指数为1.4升·分钟−1·米−2肺血管阻力(PVR)为18.5个木单位(WU),对吸入伊洛前列素无反应。除上述酪氨酸激酶抑制剂(TKIs)外,患者之前未接触过任何化疗药物或厌食药。包括超声心动图、胸部对比增强计算机断层扫描(CT)、通气/灌注肺扫描、腹部超声、自身免疫筛查和HIV血清学在内的综合检查排除了达沙替尼引起肺动脉高压的其他原因。在PAH诊断时,患者表现为纽约心脏协会(NYHA)功能III级,6分钟步行距离(6MWD)为340 M胸部CT和超声心动图显示明显的双侧胸腔积液和少量心包积液。在停止达沙替尼和引入PAH治疗(5型磷酸二酯酶(PDE-5)抑制剂和内皮素受体拮抗剂(ERA)的组合)后,NYHA功能等级提高至I/II级,6MWD增加至610 我12岁以内 月。随访的RHC进行了10次 PAH诊断数月后,mPAP降至38,血流动力学明显改善 毫米汞柱,心脏指数增加到5.8 L·min−1·米−2PVR接近正常化至2.8 吴。
由于慢性髓系白血病的分子复发,考虑到与达沙替尼相比,尼洛替尼诱导PAH的可能性更小,因此减少了剂量(400 mg / d)再次使用尼洛替尼。在恢复nilo替尼后的3年中,尽管进一步减少剂量至200mg / d,我们观察到临床和功能逐渐恶化,提示肺动脉高压进展。重复RHC,肺动脉高压明显加重,mPAP升高至70 mmHg,心脏指数下降至2.2 L·min−1·米−2,PVR至11.8Wu的严重升高,以及右心房压高于14 mmHg,低静脉氧饱和度,作为预后差的因素。Pah治疗加剧,连续静脉抗生素输液,高达40 ng·kg−1·敏−1,此外,最大剂量口服PDE-5抑制剂(西地那非)和ERA(安必生坦)。然而,PAH在接下来的6年中进一步发展 6个月后,患者出现症状性右心衰,NYHA功能分级为IV级,用力性先兆症状,难治性水钠潴留和严重低氧血症,最终需要持续静脉注射利尿剂,反复胸腔穿刺,使用去甲肾上腺素和左西孟旦输注进行高流量氧疗和血流动力学支持。体外膜肺氧合支持术后,由于多环芳烃的长期预后,在多环下进行了多学科讨论,决定了慢性肺髓白血病的预后,这是成功的。20岁以后 等待名单上的天数。患者迅速脱离血流动力学支持,3小时后拔管 天。经食管超声心动图检查24小时 术后h,PAP恢复正常,右心室扩张消失,仅有轻微残余功能障碍。在支气管吻合口愈合良好且无伊马替尼耐药性的情况下,伊马替尼400 每天补充毫克。肺移植后6个月,慢性髓系白血病目前通过伊马替尼控制,BCR-ABL转录水平无法检测(主要分子反应)。未发现BMPR2基因突变。
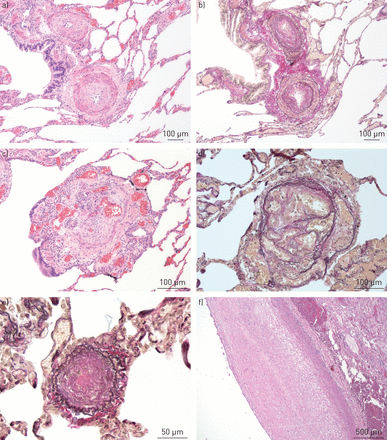
外植肺分析显示慢性PAH的动脉粥样硬化和典型的组织病理学特征[4].肺动脉病变的特征是大血管壁重塑,伴有内侧肥大和同心层状内膜增厚,以及网状病变(图1),无肺静脉阻塞或血栓栓塞疾病的证据。
达斯替尼诱导的肺动脉病变的组织病理学特征在外植入肺部观察到:a)中间肥大和同心非层状增稠,血红素氧基嗜酸盐(HE)染色的小肺动脉。b)与van Gieson弹性蛋白(VGE)染色的相同的病变,用于弹性蛋白的弹性蛋白突出动脉壁的内部和外部弹性薄片。c)对应于源自改造肺动脉并通过内皮细胞的局灶性增殖形成的复杂血管结构对应的复合状病变,他染色。d)与VGE污染相同的病变,显示出与部分破坏和动脉壁进行重塑相关的弹性薄片的破坏。e)70μm下面的肺动脉,显示通过主要是内膜增厚,VGE污渍完全湮灭。注意:在整个肺中,小型动脉瘤的变化是异质的分布。f)近端肺动脉显示重要的动脉粥样硬化,他染色。注意:既不观察到支气管动脉重塑(肥大/扩张)也不是肺静脉重塑(平滑肌增生和/或内膜纤维化)。
在我们看来,这个病例值得关注,因为它表明,尽管过渡到尼洛替尼和最大的PAH特异性治疗,达沙替尼诱导的PAH可能发生严重的进化。据我们所知,在这种情况下,没有发表过关于肺移植的数据。此外,这是首个提供达沙替尼诱导的人类特征性肺动脉重构证据的病例,与其他PAH病因一样。这似乎证实了W先驱报等等。[1达茨涅替尼证实,持久性PAH患者不可逆的肺血管疾病。它还可以解释原因,即使在治疗停止后最常观察到临床和功能性改善,血液中动力学的异常持续存在。在我们的情况下,有趣的是,PAH最初改善了Dasatinib停止后和双PAH治疗,近乎标准化PVR,只有在NILOTINIB重新引入后才会恶化,提高了关于NILOTINIB在PAH进展中的作用的问题。但是,除了疑似尼洛尼诱导的PAH的病例外,没有通过RHC确认诊断[5],目前尚无尼洛替尼引起PAH事件的确诊病例,也无尼洛替尼替代达沙替尼后PAH恶化或复发的报道,尽管尼洛替尼是达沙替尼停药后最常用的TKI [6].另一方面,已经发表了与先前记录的达塞替尼诱导的胸膜生效或PAH的患者有关的事件或与Ponatinib或Bosutinib相关的事件或恶化的PAH病例[7- - - - - -9].因此,我们不能排除尼洛尼布,类似于Ponatinib和Bosutinib,在达斯替尼损伤后在PAH进展中发挥了一些作用和导致肺血管毒性。或者,尽管达斯替尼戒断和瞬态改善PAH治疗,但这种疾病可能不可避免地进展,如其他形式的PAH。
肺移植后PAH复发的风险尚不清楚,但似乎一方面似乎不太可能取决于肺移植到PAH的易感性,另一方面,没有知道用伊马替尼治疗导致PAH,甚至对PAH的患者表现出一些有益的效果[10].在对伊马替尼的抗性或不耐受的情况下,与Dasatinib的重新检查将被禁忌。在没有先前的移植物暴露于Dasatinib的情况下,尼洛涅米的替代伊替尼可以是谨慎且密切监测的选择。
总之,这一极端病例说明了不可逆肺血管重构的可能发生,并提示达沙替尼诱导PAH。在本病例或其他报告中,很难确定达沙替尼是PAH发展的唯一负责人。然而,考虑到与达沙替尼相关的病例数量,它应被视为慢性髓系白血病患者发生PAH的主要因素。
脚注
利益冲突:无声明。
- 收到2017年8月19日。
- 接受2017年12月31日。
- 版权所有©ERS 2018