抽象的gydF4y2Ba
我们在1817名来自ECLIPSE慢性阻塞性肺疾病(COPD)队列的患者中测试了肺气肿进展是否伴随着其他体室组织损失的增强。gydF4y2Ba
临床和选定的全身生物标记测量,使用低衰减区(LAA%)的百分比通过定量断层摄影扫描肺气肿四分位数的受试者分组进行比较。最低和最高的四分位患者氨基酸代谢谱。We related LAA% to 3 years decline in lung function (forced expiratory volume in 1 s (FEV1gydF4y2Ba)),体重指数(BMI),无脂肪块指数(FFMI)和恶化,住院和死亡率。gydF4y2Ba
具有更多基线肺气肿的参与者较低的FEVgydF4y2Ba1gydF4y2Ba例如,BMI和FFMI,功能能力较差,心血管疾病较少,但骨质疏松症较多。各组间全身c反应蛋白和白细胞介素-6水平相似,但俱乐部细胞蛋白16水平较高,白细胞介素-8、表面活性蛋白D和晚期糖基化终末产物可溶性受体水平较低,且肺气肿增多。极端肺气肿四分之一患者的代谢组学不同。肺气肿较多的患者FEV加速gydF4y2Ba1gydF4y2Ba,BMI和FFMI下降,更加恶化,住院和死亡率。gydF4y2Ba
COPD患者更肺气肿发生的肺和肺外组织,这可能与异常组织维护的过度流失。由于较差的临床结果,我们提出这个小组被命名组织(MOLT)COPD表型的多器官损失。gydF4y2Ba
抽象的gydF4y2Ba
COPD患者更严重的肺气肿失去过多的肺和肺外组织gydF4y2Bahttp://ow.ly/rbnw30hFwEtgydF4y2Ba
介绍gydF4y2Ba
慢性阻塞性肺疾病(COPD)的特征在于持续的呼吸道症状和气流限制,因为气道重塑和/或肺泡肺气肿[gydF4y2Ba1gydF4y2Ba].对于尚不清楚的原因,肺气肿的存在和严重性COPD患者[之间显着变化gydF4y2Ba2gydF4y2Ba].gydF4y2Ba
肺气肿的病理标志是肺组织的丧失。横截面分析表明,肺气肿通常与其他体舱(BMI)的其他体积(BMI),测量的骨肌肉(FFMI)测量的骨骼肌较少相关[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba]以及骨密度(骨质核鸟和骨质疏松症)[gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba].同样,纵向研究发现,肺气肿患者具有加速肺功能的丧失[gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba,身体质量指数较低的患者也是如此[gydF4y2Ba9gydF4y2Ba].随着时间的推移,肺部的进展,如计算机断层扫描(CT)扫描中的肺密度降低,与晚期糖糖末端产物(SRAGE)和表面活性剂蛋白D(SP-D)的较低水平的可溶受体相关联与肺组织损伤和再生相关的分子生物标志物[gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba].然而,这些观察结果从未在概念上相互关联。gydF4y2Ba
我们假设肺气肿所特有的肺组织的渐进性损失确实与其他几个身体部位的组织块的同步和增强损失有关,这是由于普遍异常的组织维护和修复,而不仅仅是炎症[gydF4y2Ba12gydF4y2Ba].We explored this hypothesis in the ECLIPSE study (a large cohort of COPD patients that was monitored over 3 years with clinical, functional and imaging variables) in combination with high-throughput technology assessment of blood biomarkers.
方法gydF4y2Ba
学习规划gydF4y2Ba
ECLIPSE研究的详情(gydF4y2BaClinicalTrials.govgydF4y2Ba标识号:gydF4y2Banct00292552.gydF4y2Ba;GSK研究代码:SCO104960)已于此前发表[gydF4y2Ba2gydF4y2Ba,gydF4y2Ba13gydF4y2Ba].简单地说,ECLIPSE是一项观察性、控制性、纵向研究,在基线随访后,参与者分别在3个月、6个月和每6个月进行评估,持续3年。直到研究的第1060天死亡才确定。ECLIPSE符合《赫尔辛基宣言》,并已得到参与中心伦理委员会的批准。所有参与者签署知情同意书。gydF4y2Ba
参与者gydF4y2Ba
ECLIPSE研究了2164名COPD患者(Global Initiative for Chronic Obstructive Lung Disease (GOLD)分级II-IV),但目前的分析仅包括那些具有完整CT数据的患者(n=1817)。入选标准:年龄40-75岁,男女,支气管扩张剂后1秒用力呼气量(FEV)gydF4y2Ba1gydF4y2Ba)<80%的预测和FEVgydF4y2Ba1gydF4y2Ba/强迫肺活量(FVC)≤0.7;吸烟史≥10包年。主要排除标准是在入组4周内存在除COPD以外的呼吸系统疾病、其他重大炎症疾病或报告的COPD加重。gydF4y2Ba
测量gydF4y2Ba
临床表征gydF4y2Ba
采用改良医学研究委员会(mMRC)评分对呼吸困难进行分级[gydF4y2Ba14gydF4y2Ba];健康状况采用COPD-specific St George's Respiratory Questionnaire (SGRQ-C)进行测量[gydF4y2Ba15gydF4y2Ba].还记录了在研究前一年中患有抗生素,口服皮质类固醇和/或住院治疗的加剧。使用ATS-DLD-78调查问卷进行自我报告和注册。通过使用BMI评估和纠正营养状况并纠正(kg·mgydF4y2Ba−2gydF4y2Ba)和ffmi(kg·mgydF4y2Ba−2gydF4y2Ba),通过生物电阻抗测量。gydF4y2Ba
功能测量gydF4y2Ba
肺活量测量[gydF4y2Ba16gydF4y2Ba] 6分钟的步行距离(6MWD)测试[gydF4y2Ba17gydF4y2Ba]根据国际指南进行。如前所述计算BMI,气流梗阻,呼吸困难和运动能力(BODE)指数[gydF4y2Ba18gydF4y2Ba].gydF4y2Ba
CT扫描量化肺气肿gydF4y2Ba
所有受试者使用多排扫描仪(GE Healthcare, Chicago, IL, USA或Siemens Healthcare GmbH, Erlangen, Germany)进行低剂量胸部CT扫描[gydF4y2Ba10gydF4y2Ba].所有扫描都在加拿大不列颠哥伦比亚省大学中心评估。使用软件肺部工作站2.0(VIDA诊断,爱荷华州,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国,美国),被量化为低于-950 Hounsfield单位的肺CT体素的百分比。在队列的大多数患者中,CT扫描在群体的大多数患者中重复两次,并且纵向随访表现出恶化的肺气肿是先前出版物的结果[gydF4y2Ba10gydF4y2Ba].gydF4y2Ba
循环蛋白质生物标志物gydF4y2Ba
的用于检测和定量循环蛋白生物标志物的浓度的方法的细节已经发表[gydF4y2Ba19gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba].简单地说,全血收集到试管中,在室温下使血液凝固,然后在1500×离心gydF4y2BaggydF4y2Ba.通过在2000×以2000×以真空管离心,获得血浆(乙二胺四乙酸(EDTA)抗凝剂)gydF4y2BaggydF4y2Ba10-15分钟。血清和血浆储存在-80℃。在血清中测量趋化因子配体18(CCL-18),SP-D,白细胞介素(IL)-8,IL-6,俱乐部细胞分泌蛋白16(CC-16),肿瘤坏死因子(TNF)-α和SRAGE。在血浆中测量纤维蛋白原和高敏感性C-反应性蛋白(CRP)。通过验证的免疫测定法测量所有蛋白质生物标志物。通过自动临床实验室方法确定总白细胞(WBC)和中性粒细胞数。所有生物标志物在基线访问中评估,除了SRAGE之外,其中在1年级访问中的样品中测量。gydF4y2Ba
代谢组学分析gydF4y2Ba
在111-7-100-7-7-7-7-7-7-7-1-7-19-59-48例确定的41个受试者的样品中进行探索性氨基酸代谢物谱(41个,如CT扫描测定)和68岁和性别匹配的对照[gydF4y2Ba20.gydF4y2Ba].我们将15个属于最低和32的结果进行比较了最高肺气肿四分位数。gydF4y2Ba
统计分析gydF4y2Ba
结果以平均值±表示gydF4y2BaSD.gydF4y2Ba、绝对值(%)或中位数(四分位数范围(IQR))。患者在招募时按四分位数的CT肺气肿程度进行分层。连续变量采用方差分析,分类变量采用卡方检验,分类变量采用非参数Kruskal-Wallis检验。使用PROC LIFETEST计算三年产品极限生存估计。由于这些分析是探索性的,p值在名义显著性水平0.05下进行评估,不需要对多样性进行调整。所有测试都使用SAS版本9.1.3执行。gydF4y2Ba
结果gydF4y2Ba
基线特征gydF4y2Ba
临床数据gydF4y2Ba
图1gydF4y2Ba介绍了研究的CONSORT图。的2164例患者入选ECLIPSE,347被排除在这一分析,因为缺乏CT扫描。因此,我们在这里报告的1817例(84%)的基准结果;他们(9.5%)的172随访期间死亡。的347例患者,因为不完全的CT数据的分析中排除具有相似的人口统计,肺功能和相对行走能力的那些包括在研究中,但有稍微差BODE,SGRQ分数和氧饱和度(数据未示出)。在招聘的代谢轮廓在47例患者可从极端四分位数分析(gydF4y2Ba图1gydF4y2Ba).gydF4y2Ba
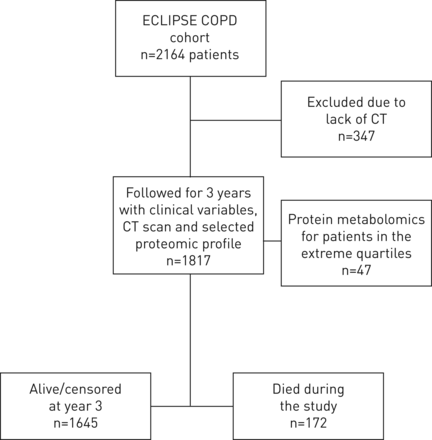
研究中包括的患者的联合图。COPD:慢性阻塞性肺病;CT:计算断层扫描。gydF4y2Ba
表格1gydF4y2Ba显示纳入研究的患者的主要基线特征,通过CT肺气肿四分位数分层。重度肺气肿患者BMI较轻,FEV较差gydF4y2Ba1gydF4y2Ba、6MWD、氧饱和度、呼吸困难、健康状况和BODE指数。在肺活量、血压和血红蛋白水平方面没有差异。有较多肺气肿的受试者报告了较高的吸烟暴露趋势,但更有可能是前吸烟者。他们也不太可能报告患有心血管疾病或糖尿病,或接受他汀类药物治疗,而报告骨质疏松症和吸入皮质类固醇的比例较高。在所有四分之一的受试者中,只有不到2%的人接受了口服皮质类固醇。gydF4y2Ba
患者的基线特征通过计算机断层扫描肺气肿严重的分层四分gydF4y2Ba
蛋白质生物标记概况gydF4y2Ba
白细胞计数和全身炎症细胞因子CRP和IL-6在各组之间没有差异。在较多的肺气肿患者中,纤维蛋白原最低程度升高,而IL-8水平显著降低(gydF4y2Ba表格1gydF4y2Ba).与此相反,与组织损伤和修复相关生物标志物组间显著不同,所以患者更严重的肺气肿显示出更高的CC-16和CCL-18值和较低的SP-d和的sRAGE的水平。gydF4y2Ba
代谢物简介gydF4y2Ba
在与肺气肿程度相关的其他变化中,最低肺气肿四分位(Q1)患者的代谢组学谱显示血清肌酸、甘氨酸和N,N-二甲基甘氨酸(gydF4y2Ba表2.gydF4y2Ba).gydF4y2Ba
计算机断层扫描肺气肿最低四分位数(Q1)和最高四分位数(Q4)患者的氨基酸代谢组特征比较gydF4y2Ba
结果随访中gydF4y2Ba
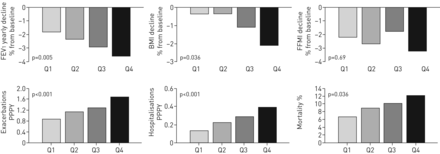
详细介绍gydF4y2Ba表3gydF4y2Ba(以图形方式描绘gydF4y2Ba图2.gydF4y2Ba),患有更多肺气肿的患者在两个FEV的绝对值下都有加速的下降速度gydF4y2Ba1gydF4y2Ba和BMI,即使他们在基线的值明显较低(gydF4y2Ba表格1gydF4y2Ba).gydF4y2Ba表4.gydF4y2Ba和gydF4y2Ba图2.gydF4y2Ba表明,在随访期间,更多的肺气肿病患者也具有更高的恶化,住院和死亡率和死亡率。gydF4y2Ba
均值±gydF4y2BaSD.gydF4y2Ba在FEV变化gydF4y2Ba1gydF4y2Ba,BMI与FFMI在患者分为肺气肿的严重性的四分gydF4y2Ba
纵向结果的四分之一的计算机断层摄影肺气肿范围在基线gydF4y2Ba
根据计算机断层扫描(CT)肺气肿的基线四分位数的纵向结果。使用低衰减区域四分位数的百分比,Q1(最低)至Q4(最高)分具有肺气肿严重程度。上限面:1 S中的强制呼气量(FEVgydF4y2Ba1gydF4y2Ba),身体质量指数(BMI)和无脂肪体重指数(FFMI)的所有跌幅为从基线的变化百分比。Lower panel: Exacerbations and hospitalisations per patient per year (PPPY) and mortality (%) over the 3 years. For further explanations, see text.
讨论gydF4y2Ba
ECLIPSE队列的这一综合分析结果支持了一个工作假设,即重度肺气肿患者构成了一个特定的COPD亚组,其特征是随着时间的推移,多个身体器官的组织质量损失增强,可能与异常的组织损失/修复能力有关,如下所示。基线时,较严重肺气肿患者的气流受限程度更高,BODE指数更差,健康状况更差,但也存在以下情况:1)BMI较低,FFMI较低(gydF4y2BaIE。gydF4y2Ba较少的肌肉质量;2)自我报告的骨质疏松症的患病率较高(gydF4y2BaIE。gydF4y2Ba较少的骨质量),但较少的心血管疾病和糖尿病(两种与低级全身炎症有关的合并症);3)与肺损伤和修复相关的细胞因子的特异性改变,例如CC-16,CCL-18,SP-D和SRAGE,以及不同的代谢型剖面。此外,在随访期间,这些患者显示:4)加速损失FEVgydF4y2Ba1gydF4y2Ba尽管入学时的价值显着较低,但BMI和FFMI仍然存在;并且,最后,5)更加恶化,住院和更高的死亡率。总而言之,这些观察结果的整合支持严重肺气肿患者的肺和肺肺组织维护和修复缺陷,直接影响临床相关结果,例如加剧和死亡。我们提出该亚组“夸大”COPD患者被命名为组织或蜕皮表型的多器官丧失。gydF4y2Ba
以往的研究和观察的新奇gydF4y2Ba
对肺气肿患者的最初描述是在近50年前作出的,其特征是消瘦和粗胸[gydF4y2Ba21.gydF4y2Ba,gydF4y2Ba22.gydF4y2Ba].以往的横断面研究已经表明,肺气肿通常与较低的BMI、FFMI和骨质疏松症有关[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba23.gydF4y2Ba],而少数纵向研究报道,这些患者的肺密度和功能加速下降[gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba,gydF4y2Ba10gydF4y2Ba].因此,我们承认,这里报告的一些观察结果并不新鲜。然而,创新之处在于,随着时间的推移,对这些发现进行了综合分析,并将其纳入了组织损伤和修复的生物标志物分析中。这种综合分析方法支持以下假设:在严重肺气肿患者中,其他肺外器官(gydF4y2Ba例如gydF4y2Ba脂肪组织、骨骼肌、骨骼)同时遭受同样的“内爆或消耗”现象(gydF4y2BaIE。gydF4y2Ba组织质量损失)作为肺一样。gydF4y2Ba
解释研究结果gydF4y2Ba
该假设得到了以下观察结果。gydF4y2Ba
肺生理gydF4y2Ba
更多的肺气肿患者有一个更低的FEVgydF4y2Ba1gydF4y2Ba在基线(gydF4y2Ba表格1gydF4y2Ba但是,尽管如此,以更快的速度丢失肺组织(gydF4y2Ba表3gydF4y2Ba,gydF4y2Ba图2.gydF4y2Ba).此观察结果与先前的报告不同,表明FEV更高的患者gydF4y2Ba1gydF4y2Ba在基线失去比较低的FEV患者更大的肺功能gydF4y2Ba1gydF4y2Ba[gydF4y2Ba24.gydF4y2Ba,gydF4y2Ba25.gydF4y2Ba].这些差异可能与这些研究中的事实有关,患者被基线FEV分组gydF4y2Ba1gydF4y2Ba级别只而不是通过他们的肺气肿程度,因为我们已经做了。事实上,在我们的分析结果相一致,最近的研究还表明,FEV率gydF4y2Ba1gydF4y2Ba在COPD下降是异质的,并且较低的BMI和CT肺气肿存在与加速FEV相关联gydF4y2Ba1gydF4y2Ba损失(gydF4y2Ba7gydF4y2Ba- - - - - -gydF4y2Ba9gydF4y2Ba].gydF4y2Ba
疾病模式gydF4y2Ba
心血管疾病、糖尿病、骨质疏松症、肺癌和贫血等合并症在COPD中非常普遍[gydF4y2Ba26.gydF4y2Ba,gydF4y2Ba27.gydF4y2Ba]并促成糟糕的结果[gydF4y2Ba28.gydF4y2Ba,gydF4y2Ba29.gydF4y2Ba].在基线时,我们观察到肺气肿严重程度存在于肺气肿的严重程度的显着差异,具有较为顽固的患者,报告较少的心血管疾病和糖尿病(通常被认为是“炎症”羟基),但更骨质疏松症和较低的BMI和FFMI(临床表达)分别丧失骨,脂肪和骨骼肌肿块)。此外,患有更多肺气肿的患者以较高的速率和相似的速度丢失BMI(gydF4y2Ba表3gydF4y2Ba,gydF4y2Ba图2.gydF4y2Ba),尽管基线值较低(gydF4y2Ba表格1gydF4y2Ba).gydF4y2Ba
全身性炎症类型gydF4y2Ba
全身性炎症常被引用为COPD共病的重要致病机制[gydF4y2Ba26.gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba].然而,先前对ECLIPSE队列的分析表明,并非所有COPD患者都有全身炎症的证据,患有这种疾病的患者BMI较高,CT肺气肿评分较低[gydF4y2Ba31.gydF4y2Ba].在这里,我们扩展了之前的分析,包括肺组织保护的标志物,如CC-16和CCL-18(在严重肺气肿患者中较高)和SP-D和sRAGE(在这些患者中较低)。相比之下,这些患者中SP-D水平的降低可以反映肺组织的损失,而sRAGE水平的降低可以作为这些患者中系统性炎症水平降低的替代标志(gydF4y2Ba表格1gydF4y2Ba)以来的sRAGE充当保护诱饵通过缓冲炎性配体,从而降低炎性损伤[gydF4y2Ba32.gydF4y2Ba].gydF4y2Ba
代谢组学模式gydF4y2Ba
虽然样品的特征在于代谢物质较小,但结果清楚地表明,更严重的肺气肿患者的模式显着不同于肺气肿的患者(gydF4y2Ba表2.gydF4y2Ba).这些观察结果与之前的研究一致,这些研究表明肺气肿患者血清中支链氨基酸(以及肌肉活检中所有氨基酸)减少[gydF4y2Ba20.gydF4y2Ba].同样,他们与之前的报道一致,肺气肿患者在低强度运动后全身蛋白和尿素代谢被抑制,而在非肺气肿性COPD患者和对照组中运动诱导的合成代谢反应得以维持[gydF4y2Ba33.gydF4y2Ba].gydF4y2Ba
与结果的关系gydF4y2Ba
该分析的一个重要和新颖的组成部分是对随访期间发生变化的基线观察进行调查。我们注意到,与非肺气肿患者相比,严重肺气肿患者更容易出现病情加重,更容易住院并在3年内死亡(gydF4y2Ba表3gydF4y2Ba,gydF4y2Ba图2.gydF4y2Ba).这些观察结果与先前的一项研究一致,该研究描述了恶化风险的双峰模式。虽然CT确定的气道增厚的患者加重了病情,但它也表明,与气道厚度和肺气肿都在中间的患者相比,肺气肿更多的患者也增加了病情加重的风险[gydF4y2Ba34.gydF4y2Ba].无论是病情加重的原因或类型是两组相似还不清楚。gydF4y2Ba
我们的观察结果一起支持严重肺气肿的关联,具有过度的外肺组织丧失。然而,从我们的数据中不可能确定对该COPD表型负责的确切病理能力机制,并且需要进一步的研究来提供对治理肺和外肺组织逐渐丧失的生物机制的洞察力。但是,值得注意的是,我们没有发现血红蛋白水平或白细胞之间的差异,呼气群体中的血液细胞计数,这表明浪费现象不影响所有器官系统,而是一些含有间充质源性的器官体系共同[gydF4y2Ba35.gydF4y2Ba].同样,肺气肿患者肺组织中最近的B细胞签名可能有助于照亮组织损失的潜在机制,因为浪费也是B细胞驱动的全身疾病中的常见特征[gydF4y2Ba36.gydF4y2Ba,gydF4y2Ba37.gydF4y2Ba].gydF4y2Ba
潜在的限制gydF4y2Ba
我们的研究有一些潜在的局限性。首先,研究结果只显示了相关性,并没有证明因果关系。因此,研究结果需要在一项验证这些假设的研究中进行前瞻性的重复。其次,我们只研究了一组有限的生物标志物。但是,我们是根据以往的报道来选择它们的,它们都是可以在临床实践中测量的。第三,ECLIPSE研究中的共病是自我报告的,没有进行客观评估;然而,自我报告和客观评估的共病之间有很好的相关性。最后,死亡率数据是指全因死亡率,因为研究中没有记录特定原因的死亡率。gydF4y2Ba
结论gydF4y2Ba
该研究的结果表明,具有严重肺气肿的COPD患者在几个器官中随着时间的推移,包括肺,骨骼,骨骼肌和脂肪组织的时间过度丧失组织。适当的鉴定这些患者在临床上是相关的,因为它们具有更加恶化,并且更有可能在3年内住院和死亡而不在没有这种表型的患者。我们建议将该亚组命名为组织(或蜕皮)COPD表型的多器官丧失。gydF4y2Ba
补充材料gydF4y2Ba
补充材料gydF4y2Ba
请注意:gydF4y2Ba编辑部没有编辑补充材料,并随着作者提供的,上传。gydF4y2Ba
表S1:女性和男性的基线特征分别,按计算机体层摄影肺气肿严重程度的四分之一分层gydF4y2Baerj - 02146 - 2017 - _supplementary_table_s1gydF4y2Ba
披露gydF4y2Ba
补充材料gydF4y2Ba
A. Agusti.gydF4y2BaERJ-02146-2017_AgustigydF4y2Ba
B.R.切利gydF4y2Baerj - 02146 - 2017 - _celligydF4y2Ba
r·凡尔服饰gydF4y2BaERJ-02146-2017_Faner.gydF4y2Ba
N. Locanore.gydF4y2BaERJ-02146-2017_Locanore.gydF4y2Ba
b·米勒gydF4y2Baerj - 02146 - 2017 - _millergydF4y2Ba
诉Pinto-PlatagydF4y2BaERJ-02146-2017_PINTO-PLATAgydF4y2Ba
j·莱利gydF4y2BaERJ-02146-2017_RILEY.gydF4y2Ba
E.K.西尔弗曼gydF4y2BaERJ-02146-2017_SilvermangydF4y2Ba
r. tal-singergydF4y2BaERJ-02146-2017_tal-singergydF4y2Ba
J. VestbogydF4y2Baerj-02146-2017_vestbo.gydF4y2Ba
E.F.M.武泰gydF4y2Baerj - 02146 - 2017 - _woutersgydF4y2Ba
J.C. Yates.gydF4y2BaERJ-02146-2017_yates.gydF4y2Ba
致谢gydF4y2Ba
作者感谢所有参与ECLIPSE的受试者、调查者和研究现场工作人员。gydF4y2Ba
参加Eclipse的主要调查员和中心(gydF4y2Banct00292552.gydF4y2Ba, SCO104960)。保加利亚:Y. Ivanov,普莱芬;k . Kostov索非亚。加拿大:J. Bourbeau,蒙特利尔;m·菲茨杰拉德温哥华;哈利法克斯·埃尔南德斯;k·基利安,汉密尔顿;r·利维,温哥华;f . Maltais蒙特利尔;d O ' donnell,金斯顿。 Czech Republic: J. Krepelka, Praha. Denmark: J. Vestbo, Hvidovre. The Netherlands: E. Wouters, Horn. New Zealand: D. Quinn, Wellington. Norway: P. Bakke, Bergen. Slovenia: M. Kosnik, Golnik. Spain: A. Agusti, Palma de Mallorca; Jaume Sauleda, Palma de Mallorca. UK: L. Yashina, Edinburgh; W. MacNee, Edinburgh; D. Singh, Manchester; J. Wedzicha, London. Ukraine: Y. Feschenko, Kiev; V. Gavrisyuk, Kiev. USA: A. Anzueto, San Antonio, TX; S. Braman, Providence, RI; R. Casaburi, Torrance, CA; B. Celli, Boston, MA; G. Giessel, Richmond, VA; M. Gotfried, Phoenix, AZ; G. Greenwald, Rancho Mirage, CA; N. Hanania, Houston, TX; D. Mahler, Lebanon, NH; B. Make, Denver, CO; S. Rennard, Omaha, NE; C. Rochester, New Haven, CT; P. Scanlon, Rochester, MN; D. Schuller, Omaha, NE; F. Sciurba, Pittsburgh, PA; A. Sharafkhaneh, Houston, TX; T. Siler, St Charles, MO; E. Silverman, Boston, MA; A. Wanner, Miami, FL; R. Wise, Baltimore, MD; R. ZuWallack, Hartford, CT. Steering Committee: H. Coxson (Canada), L. Edwards (GSK, USA), R. Tal-Singer (Co-chair, GSK, USA), D. Lomas (UK), W. MacNee (UK), E. Silverman (USA), C. Crim (GSK, USA), J. Vestbo (Co-chair, Denmark), J. Yates (GSK, USA). Scientific Committee: A. Agusti (Spain), P. Calverley (UK), B. Celli (USA), C. Crim (GSK, USA), B. Miller (GSK, USA), W. MacNee (Chair, UK), S. Rennard (USA), R. Tal-Singer (GSK, USA), E. Wouters (The Netherlands), J. Yates (GSK, USA).
脚注gydF4y2Ba
本文提供了补充材料gydF4y2Bawww.qdcxjkg.com.gydF4y2Ba
支持声明:Eclipse学习由GSK资助。本文的资金信息已存入gydF4y2BaCrossRef Resder注册表gydF4y2Ba.gydF4y2Ba
临床试验:本研究注册于gydF4y2BaClinicalTrials.govgydF4y2Ba使用标识符号码gydF4y2Banct00292552.gydF4y2Ba.gydF4y2Ba
利益冲突:可以在本文旁边找到披露gydF4y2Bawww.qdcxjkg.com.gydF4y2Ba
- 收到了gydF4y2Ba2017年10月17日。gydF4y2Ba
- 接受gydF4y2Ba2017年11月20日。gydF4y2Ba
- 版权©2018人队gydF4y2Ba
参考gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba