摘要
咳嗽是去看初级保健医生的最常见原因,但它仍然是一种未被满足的医疗需求。脂肪酸酰胺水解酶(FAAH)是一种分解内源性大麻素的酶,抑制FAAH产生镇痛和抗炎作用。大麻素抑制迷走感觉神经激活和咳嗽反射,因此假设抑制FAAH会产生镇咳活性通过内源性大麻素的升高。
原代迷走神经节神经元,组织生物测定,在活的有机体内电生理学和有意识的豚鼠咳嗽模型被用来研究脂肪酸酰胺在迷走传入神经中调节感觉神经激活的作用。
FAAH抑制产生的抗咳活性的豚鼠伴随血浆脂肪酸酰胺的升高N-花生烯酰乙醇酰胺(anandamide),棕榈酰乙醇酰胺,N-油基乙醇酰胺和亚油基乙醇酰胺。棕榈酰乙醇酰胺抑制了咳嗽刺激诱导的豚鼠气道迷走神经节神经元的激活,豚鼠和人迷走神经的去极化和c纤维传入神经的放电。这些影响是被调节的通过大麻素CB2/ Gi / o-偶联通路和蛋白磷酸酶2A的激活,导致钙活化钾通道的钙敏感性增加。
这些发现确定FAAH抑制作为开发新型的、没有直接大麻素受体激动剂不良副作用的镇痛剂的靶点。
摘要
以脂肪酸酰胺水解酶抑制为靶点,开发新型安全的镇咳疗法http://ow.ly/l4ZE30dbbB1
介绍
慢性咳嗽严重到足以干扰正常的日常生活活动,据认为影响了约7%的人口[1].它常与炎症性气道疾病有关,包括慢性阻塞性肺病、哮喘、特发性肺纤维化、肺癌或肺外疾病,如胃食管反流和鼻鼻窦炎,也是药物治疗的副作用,如血管紧张素转换酶抑制剂[2].难治性咳嗽也可能是特发性的,可占专科咳嗽诊所患者的18-42% [3.].尽管它很重要,但治疗咳嗽的选择有限,最近的证据表明,非处方咳嗽药物无效。4].
咳嗽反射是由迷走神经和支配气道的感觉传入神经调节的。2,5].气道感觉神经的细胞体主要分布在鼻神经节和颈静脉神经节。肺中存在几种已知的感觉神经亚型:有些更机械敏感,如。快速适应受体和缓慢适应受体以及被称为“咳嗽”受体的亚型,还有一些对化学更敏感,如。c纤维和Aδ痛觉感受器。存在于这些迷走神经末梢的离子通道可以被各种各样的刺激激活,引起咳嗽和其他反射。瞬时受体电位(TRP)通道是涉及启动感觉反射的离子通道的主要家族。
之前的研究强调了大麻素CB的作用2调节气道感觉神经活动和咳嗽反射的感受器[6,7].然而,直接施用大麻素并非没有不良副作用[8].脂肪酸酰胺水解酶(FAAH)是神经系统内发现的一种完整的膜蛋白,负责内源性大麻素的水解N-arachidonoylethanolamide (AEA;和其他相关的酰胺化信号脂质,如棕榈酰乙醇酰胺(PEA),N-油酰乙醇酰胺(OEA)和亚油酰乙醇酰胺(LEA)。这些信号脂质通过各种不同的受体发挥作用,如大麻素CB1/ CB2还有受体通过非大麻素受体,包括TRPV1、过氧化物酶体增殖物激活受体(PPARs)和阿片受体[9- - - - - -11].通过基因缺失或FAAH的药理抑制来提高AEA和其他生物活性脂肪酸酰胺(FAAs)的内源性水平,可在疼痛和炎症的临床前模型中引起镇痛作用[12].这些脂质信号分子根据需要合成和释放,并在局部起作用,因为它们很快就被灭活了。这表明,调节这些配体的水平可能具有治疗潜力,从而减少由广泛的系统性大麻素受体激活引起的潜在副作用。
鉴于CB2受体激动剂已被证明在临床前咳嗽模型中产生镇咳活性[6,7],我们假设FAAH的抑制可能是开发新型止咳药的一个靶点。在这些研究中,我们使用了临床咳嗽挑战研究中常用的咳药,即。辣椒素和柠檬酸(代表低pH值溶液)[2].
材料与方法
动物
在活的有机体内而且体外实验采用雄性Dunkin-Hartley豚鼠(300-500 g;单纤维400-800克在活的有机体内(哈兰,比斯特,英国和B&K Universal,赫尔,英国)放置在一个温度控制(21°C)的房间里,免费提供食物和水,在开始实验前至少一周。这些实验是根据英国内政部1986年颁布的《动物(科学程序)法》和《英国动物保护法》的动物福利准则进行的[13].
测量PF-04862853和FAA水平
在独立的药代动力学特征研究中,在口服药物后0、30、60、120、180、240、300和360分钟采集血液样本(隐静脉出血)。如前所述,采用液相色谱-质谱(LC-MS)在血浆中测量新型FAAH抑制剂PF-04862853的血浆水平[14,15].等离子体的制备方法如上所述[14,15],以评估AEA、PEA、OEA和LEA水平,也通过LC-MS测量。
清醒的豚鼠在咳嗽
PF-04862853 (1 mg·kg−1)或载液(0.5%甲基纤维素/0.1%吐温80盐水)每个操作系统咳嗽记录前4小时。研究采用盲法,并由独立操作人员进行口服给药。在所有的实验中,操作员都不知道治疗组的情况。意识清醒的豚鼠被放置在单独的双室容积描记箱中(Buxco, Wilmington, NC, USA),用柠檬酸气雾剂(0.3 M气雾剂在生理盐水中,持续10分钟)评估咳嗽情况,如前所述[7,16].实验结束时动物被处死。
豚鼠与人离体迷走神经的记录
分离的豚鼠和人迷走神经去极化的记录如前所述进行[2,6,7,16].简单地说,用辣椒素(1µM)或低pH值(ph5)灌注2分钟(内部控制)两次刺激神经,然后再灌注10分钟。然后在车辆或FAA在场的情况下重新评估刺激效果。清洗5-10分钟后,在每次实验结束时刺激神经以确认生存能力。在相关实验中,载药/拮抗剂/钾通道阻滞剂在载药/FAA存在之前灌注10分钟。用于实验检验Gi / o亚单位、载液(生理盐水)或百日咳毒素(PTX)在迷走神经切除前3天腹腔注射(25µg,腹腔注射),用于离体迷走神经记录实验。
迷走神经是从捐献者身上解剖出来的全体不适合移植的肺(来自美国新泽西州爱迪生的国际医学进步研究所),除了一个从肺移植受者的肺组织中解剖迷走神经的病例(来自英国伦敦的皇家布朗普顿和海尔菲尔德NHS基金会信托)。样本来自9名患者(7名男性,2名女性;中位年龄(范围)51岁(27-67岁),无呼吸道疾病史,除受体样本来自囊性纤维化患者外。在所有情况下,组织都同意用于科学研究。获得了皇家布朗普顿和哈里菲尔德NHS基金会信托的伦理批准。
在活的有机体内单纤维记录
豚鼠用脲烷(1.5 g·kg)麻醉−1,i.p。),根据需要添加额外的聚氨酯。气管插管,人工通气,使血气和pH维持在生理水平,潮气量10 mL·kg−1每次呼吸50-60次·min1实验室的空气。套管连接到气压传感器(SenSym 647;法内尔,利兹,英国)用侧臂对着监视器测量气管压力。分别在右颈静脉和颈动脉插管注射药物和测量全身动脉血压。通过(静脉)给药维库溴铵使动物瘫痪;初始浓度为100 μg·kg−1,注射。,维持在50 μg·kg−1每20分钟。在颈部做了一个切口,以定位两个迷走神经,从颈动脉清除,并在中央端进行切割。对左侧迷走神经进行梳理,直到可以用铂电极记录单纤维单元的放电。用于这些实验的c纤维被确定为缺乏自发放电和对恶性通货膨胀和通货紧缩的反应性,对辣椒素/柠檬酸的反应性,并且具有< 1m·s的传导速度−1[2,17].在确定c纤维后,实验方案如下:刺激(辣椒素100 μM,持续15秒或柠檬酸300 mM,持续60秒)以气溶胶的形式刺激动作电位放电,刺激间隔时间使其恢复到基线活动水平。PEA (10 mg·kg−1,i.p。), 30分钟后再进行同样的刺激,以评估PEA对动作电位激发的影响。
离体气道神经元细胞内钙的成像
解剖颈静脉神经节,从组织中分离神经元,识别气道末端神经元和评估细胞内游离钙[Ca2 +]我使用荧光团Fura-2 AM进行水平测定,如前所述[2,18].在每个实验开始和结束时分别使用50mm氯化钾溶液10 s,以评估细胞活力和正常反应。用低pH值(pH 6)或辣椒素(100 nM)刺激神经元2次1分钟,然后用载体或PEA (1 nM)刺激10分钟。然后在载体或PEA存在的情况下重新评估刺激。“反应性细胞”的标准是[Ca2 +]我≥10%对50mm氯化钾溶液的反应。
化合物、材料和溶液
PF-04862853(7-氮杂螺[3.5]壬烷尿素)[14]由辉瑞全球研发中心(英国剑桥)提供。SR141716A和SR144528购自Tocris Bioscience (Bristol, UK), LEA购自Cambridge Bioscience (Cambridge, UK)。Fura-2 AM购自Invitrogen (Paisley, UK)。L-15和Hanks的平衡盐溶液购自Gibco/Invitrogen (Carlsbad, CA, USA)。上述未提及的所有试剂均购自Sigma-Aldrich (St Louis, MO, USA)。
在钙成像实验中,50mm钾溶液中含有50mm KCl, 91.4 mM NaCl, 1mm MgCl2, 2.5 mM CaCl2, 0.33 mM NaH2阿宝4, 10 mM葡萄糖,10 mM HEPES;在37°C使用KOH调整pH值为7.4。为在体外将整个迷走神经和钙成像实验、辣椒素和PEA溶解于100%二甲亚砜(DMSO)中,并在灌注液中按1:1000稀释。这是Krebs-Henseleit解[16]用于迷走神经实验和细胞外溶液(5.4 mM KCl, 136 mM NaCl, 1 mM MgCl2, 2.5 mM CaCl2, 0.33 mM NaH2阿宝4, 10 mM葡萄糖,10 mM HEPES;pH调整为7.4,在37°C使用NaOH)用于钙成像实验。单个药物的最终载体浓度为0.1%,当药物组合一起灌注时最高可达0.3%。
数据分析与统计
p值<0.05被认为是显著的。通过配对t检验(在药物存在的情况下进行比较,并与相同制剂的初始对照反应进行比较),或通过Mann-Whitney u检验或Kruskal-Wallis与Dunn's检验来评估显著性事后分析(取决于处理列的数量),如图例所示。
结果
PF-04862853抑制FAAH,提高FAAs并抑制清醒豚鼠模型中的咳嗽
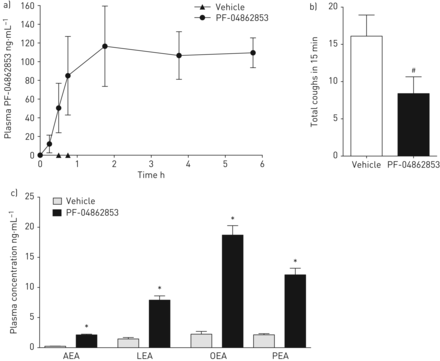
已知PF-04862853在给药后4小时达到峰值药物水平,并在大鼠和犬中表现出良好的口服生物利用度,分别为53%和33% [14,15].我们在豚鼠中的结果与这些结果相似,PF-04682853的峰值水平(1 mg·kg−1,订单。)在给药后2-4小时发生(图1一个);我们选择4 h时间点进行进一步评估。PF-04862853 (1 mg·kg−1,订单。)显著抑制柠檬酸诱发的咳嗽(图1 b).该剂量对同一动物的FAAH活性产生了强烈的抑制作用(~ 84%,与以前对大鼠和狗的研究相似[15]),同时伴有血浆AEA、PEA、OEA和LEA升高(~ 4 - 7倍;图1 c).这些数据表明FAAH抑制剂的镇咳活性与PF-04862853峰值水平、FAAH酶抑制和FAAs升高有关。
口服剂量的PF-04862853导致脂肪酸酰胺(FAAs)的升高和抑制柠檬酸诱发的咳嗽。阿肯色州教育协会:N-arachidonoylethanolamide;李:linoleoylethanolamide;OEA:N-oleoylethanolamide;豌豆:palmitoylethanolamide。a) 1 mg·kg后各时间点的PF-04862853血浆水平−1,订单。b) PF-04862853的效果(1 mg·kg−1,订单。0.3 M柠檬酸诱发咳嗽次数的影响。c) PF-04862853 (1 mg·kg)给药后FAAs AEA、LEA、OEA和PEA的血浆水平−1,订单。,给药后4小时)。载体:0.5%甲基纤维素/0.1%吐温80盐水。数据以均数±表示扫描电镜,每组n=8只。与车辆对照组比较:#: p<0.05 (Mann-Whitney U-test);*: p<0.05(配对t检验)。
FAAs抑制豚鼠离体迷走神经去极化通过CB的2受体
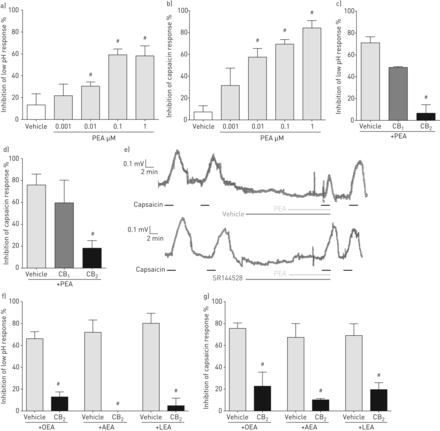
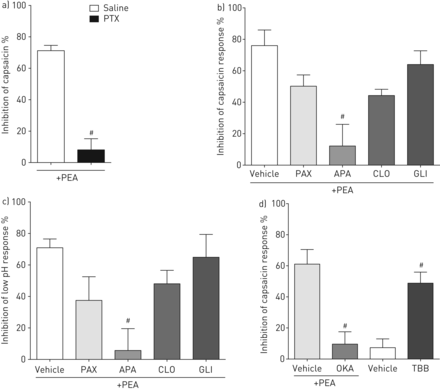
我们研究了PEA、AEA、OEA和LEA对咳激诱导豚鼠离体迷走神经去极化的影响。PEA (1 nM至1µM)对低pH值和辣椒素诱导的离体豚鼠迷走神经去极化(图2一个b).在100 nM的浓度(PEA的次最大浓度)下,所有四种FAAs都对低pH和辣椒素诱导的去极化产生了显著的抑制作用(60-80%),而CB则显著逆转了这一抑制作用2受体拮抗剂SR144528,但没有被CB1受体拮抗剂SR141716A (图2 c- g)。
棕榈酰乙醇酰胺(PEA)和其他脂肪酸酰胺抑制低pH值和辣椒素诱导的迷走神经去极化通过大麻素CB的激活2受体。OEA:N-oleoylethanolamide;阿肯色州教育协会:N-arachidonoylethanolamide;李:linoleoylethanolamide。a, b) PEA对a)低pH (pH 5)或b)辣椒素(1 μM)诱导的离体豚鼠迷走神经去极化的浓度相关抑制。c-e) CB的作用1(SR141716A;10nm)和CB2(SR144528;10 nM)对PEA的受体拮抗剂(100 nM)对c)低pH (pH 5)-或d)辣椒素(1 μM)诱导豚鼠迷走神经去极化的抑制作用,e)显示有代表性的载体或CB实验痕迹2PEA抑制辣椒素反应的拮抗作用。f, g) CB的作用2(SR144528;10 nM) OEA、AEA或LEA受体拮抗剂(100 nM)对f)低pH (ph5)-或g)辣椒素(1 μM)诱导豚鼠离体迷走神经去极化的抑制作用。载体:0.1% v/v二甲亚砜。数据以均数±表示扫描电镜, n=每组4条单个动物神经。与车辆对照组比较:#: p<0.05 (Mann-Whitney U-test或Kruskal-Wallis with Dunn’s事后分析)。
PEA抑制单纤维燃烧在活的有机体内钙的流入在体外在气道中支配神经/神经元
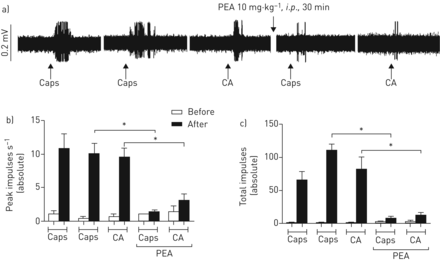
PEA (10 mg·kg−1,i.p。)在柠檬酸(0.3 M)或辣椒素(100µM)气雾剂的激活下,显著降低了c纤维单气道的总动作电位激发和激发频率(图3一- c)。
棕榈酰乙醇酰胺(PEA)抑制柠檬酸(CA)和辣椒素(Caps)诱发的c纤维放电在活的有机体内.a)在PEA (10 mg·kg)存在之前,在辣椒素(100 μ M)或柠檬酸(0.3 M)气溶胶中分别激发单个c纤维动作电位15和60秒的代表性痕量−1,i.p。,辣椒素激发前30分钟)。b)在气管内喷入柠檬酸(0.3 M)或辣椒素(100µM)时,评估豚鼠气道神经c纤维的峰值放电频率和c)总脉冲。面板显示了在使用柠檬酸或辣椒素之前的自发放电水平和在使用柠檬酸或辣椒素之后的自发放电水平。对照反应之前已经在每条神经上建立i.p。PEA (10 mg·kg−10.5%甲基纤维素/0.1%吐温80盐水10 mL·kg−1).数据以均数±表示扫描电镜, n=3条神经纤维在单个动物。与各对照组比较:*:p<0.05(配对t检验)。
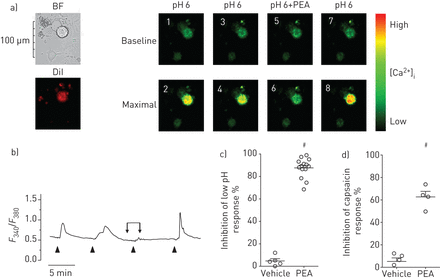
我们还使用了在体外因此,我们检查了经鼻内给药的逆行示踪剂DiI染色的孤立颈静脉神经节神经元的细胞内钙通量在活的有机体内,以识别气道终止中子在体外.PEA (1 nM)显著地消除了低外部pH (pH 6)或辣椒素(1µM)诱导的细胞内钙信号。在体外经DiI染色的颈静脉神经节神经元(指示气道支配神经元)(图4一- d)。
Palmitoylethanolamide(豌豆;1 nM)抑制低pH和辣椒素诱导的气道神经元细胞内钙的增加。a)具有代表性的图像,显示具有DiI发射的神经元的亮场(BF)图像,指示气道终止神经元。图1-8显示ph6刺激前后细胞内钙水平。b)同一神经元/实验中定量细胞内钙水平的痕量,箭头(pH 6)和大括号/箭头(PEA;1海里)。F340/F380:在340和380 nm激发下的荧光强度之比。c, d) PEA (1 nM)抑制c)低pH (pH 6)-或d)辣椒素(100 nM)诱导豚鼠离体气道颈静脉神经元细胞内钙的增加。数据以均数±表示扫描电镜,每组n= 4-14个细胞,n= 3-4只动物。载体:0.1% v/v二甲亚砜。与车辆对照组比较:#: p<0.05 (Mann-Whitney U-test)。
PEA抑制豚鼠离体迷走神经去极化通过Gi / o信号通路及其对钙活化钾通道的影响
利用PTX阻断信号转导通过Gi / o子单元。在PTX剂量的豚鼠中,PEA对辣椒素诱导的去极化的抑制作用与车辆剂量对照动物的PEA对迷走神经的抑制作用相比大大减弱,表明Gi / o信号(图5一个).大麻素效应通常被认为至少部分是由钾通道的影响介导的;因此,我们检测了各种钾通道阻滞剂对PEA抑制迷走神经去极化的影响。克霉唑,帕罗西林和格列本脲,中间体阻滞剂(IKCa)和大号(BKCa钙活化和atp敏感(K三磷酸腺苷)钾通道对PEA对豚鼠迷走神经去极化的抑制作用无显著影响。相比之下,apamin(1µM),一种小电导阻断剂(SKCa)钙活化钾通道,几乎取消了PEA对辣椒素和低ph诱导的去极化抑制(约85-90%)(图5 b和c).与SK上的活动一致Ca通道,PEA抑制了被检测的多个兴奋性离子通道激动剂引起的豚鼠迷走神经去极化(补充图S1),即。TRPA1激动剂丙烯醛(300 μM)、合成TRPV4激动剂GSK1016790A (300 nM)或内源性TRPV4激动剂低渗透溶液(−80 mOsm)。
棕榈酰乙醇酰胺(PEA)通过CB抑制孤立的迷走神经去极化2/ Gi / o小电导钙活化钾通道和磷酸酶2A的活化。PTX:百日咳毒素;罗马帝国:paxilline;APA: apamin;CLO:克霉唑;GLI:格列本脲;OKA:冈田酸;7-tetrabromobenzotriazole TBB: 4、5、6日。a) PTX作用(剂量25 μg,i.p。在去除神经组织前3天)对PEA (100 nM)抑制辣椒素(1 μM)诱导的豚鼠迷走神经去极化。b, c) PAX (1 μM)、APA (1 μM)、CLO (10 μM)或GLI (10 μM)对PEA (100 nM)抑制b)辣椒素(1 μM)-和c)低pH (ph5)诱导豚鼠迷走神经去极化的影响。d) OKA (1 nM)对PEA (100 nM)抑制辣椒素(1 μM)诱导离体豚鼠迷走神经去极化的影响及TBB (10 μM)对辣椒素(1 μM)诱导离体豚鼠迷走神经去极化的影响。载体:0.1% v/v二甲亚砜。数据以均数±表示扫描电镜, n=每组3-4条来自单个动物的神经。与相关车辆对照组比较:#: p<0.05 (Mann-Whitney U-test或Kruskal-Wallis with Dunn’s事后分析)。
作为SKCa我们检测了蛋白磷酸酶2A (PP2A)的可能参与,PP2A是SK的调节部分Ca通道多蛋白复合物以及酪蛋白激酶II (CKII)和钙调蛋白(CaM)。CaM被绑定到SK上Ca将钙结合转化为通道开口;CKII磷酸化CaM降低SKCa钙敏感性(因此开放概率),而PP2A去磷酸化CaM增加钙敏感性[19].PP2A抑制剂(冈田酸;1 nM)阻断了PEA对迷走神经去极化的抑制作用,而CKII抑制剂(4,5,6,7-四溴苯并三唑;10µM)抑制去极化本身(图5 d).这些结果表明PEA激活了SKCa通过激活PP2A,使SK脱磷酸化Ca结合CaM以增加通道的钙敏感性。
PEA抑制人迷走神经去极化通过一个CB2-PP2A-SKCa通道机制
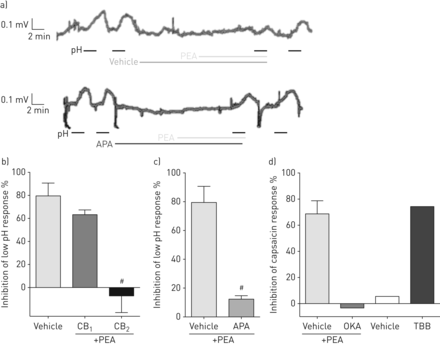
为了增加本研究的转译性质,我们在独特的人类迷走感觉神经测定中进行了关键实验,以类似于豚鼠的方式评估去极化。PEA (100 nM)对低pH和辣椒素诱导的迷走神经去极化均有抑制~ 70-80% (图6).此外,PEA对去极化的抑制作用被CB完全逆转2受体拮抗剂,而不是CB1受体拮抗剂(图6 b),而SK则大幅逆转(~ 85%)Ca通道阻滞剂;1 μm) (图6 c).在初步实验(n=2)中,PP2A抑制剂阻断了PEA的作用,CKII抑制剂模拟了PEA的作用(图6 d),表明PEA对人迷走神经去极化的抑制也是由CB介导的2-PP2A-SKCa渠道通路。
棕榈酰乙醇酰胺(PEA)抑制迷走神经去极化通过CB2-磷酸酶2a -小导钙活化钾通道。APA: apamin;OKA:冈田酸;7-tetrabromobenzotriazole TBB: 4、5、6日。a)在(上)载体或(下)APA (1 μM)存在时,PEA抑制低pH响应的代表性痕迹。b) CB的作用1(SR141716A, 10 nM)和CB2(SR144528, 10 nM) PEA受体拮抗剂(100 nM)抑制低pH (ph5)诱导的人离体迷走神经去极化。c) APA (1 μM)对PEA (100 nM)抑制低pH (ph5)诱导的人离体迷走神经去极化的影响。d) OKA (1 nM)对PEA (100 nM)抑制辣椒素(1 μM)诱导的人离体迷走神经去极化的影响以及TBB对辣椒素(1 μM)诱导的人离体迷走神经去极化的影响。载体:0.1% v/v二甲亚砜。数据以均数±表示扫描电镜, n=每组4条来自单个动物的神经扫描电镜如图所示,n=2条来自单个动物的神经。与相关车辆对照组比较:#: p<0.05 (Mann-Whitney U-test或Kruskal-Wallis with Dunn’s事后分析)。
讨论
最近的证据表明,CB2受体在动物模型中介导气道感觉神经活动和咳嗽的抑制,突出显示CB2受体是治疗咳嗽的潜在靶点[6,7].然而,大麻素与镇静、恶心和成瘾等多种中枢效应有关,这限制了它们作为治疗手段的使用[20.,21].FAAH的药理阻断已经成为一种潜在的有吸引力的策略,通过这种策略,内源性大麻素水平升高,并保留大麻素受体激活的有益作用,以缓解疼痛[22],同时避免了全球大麻素受体激活的不良影响。
在过去的十年中,FAAH抑制剂的开发取得了进展,最初的兴趣集中在开发FAAH抑制剂以增强FAAs的作用并减轻疼痛。最近,新兴的文献表明,这些FAAs通过与各种受体(细胞外和细胞内)的相互作用,可以诱导一系列不同的效应,包括食欲抑制、脂质和葡萄糖代谢的调节、血管舒张、心功能和炎症[22].然而,据我们所知,FAAH抑制剂的作用还没有在气道中进行过研究。我们假设通过选择性抑制剂抑制FAAH可能具有镇咳作用。本研究中使用的FAAH抑制剂(即。PF-04862853)是一种新近开发的化合物,具有优良的效价、选择性、药代动力学特性和活性在活的有机体内炎症性疼痛模型的疗效[15].
PF-04862853,在给药4小时后,抑制了豚鼠的咳嗽,并与血浆中FAAs (PEA, AEA, OEA和LEA)水平的升高有关。虽然FAAs有几个子类,但本研究中确定的内生FAAs属于N-酰基乙醇酰胺亚类,并已在哺乳动物大脑组织和外周组织中发现[23- - - - - -25].这些FAAs被称为“内源性大麻素”,因为它们可以作为CB的激动剂1和CB2受体。鉴于外源性大麻素具有镇咳作用通过CB作用2感觉神经的感受器[6,7],我们假设这些FAAs通过同样抑制感觉神经激活来介导FAAH抑制的镇咳作用通过CB的2受体。
所有被检测的FAAs都抑制了低pH和辣椒素诱发的豚鼠离体迷走神经去极化,这一效应被选择性CB逆转2受体拮抗剂,而不是CB1受体拮抗剂[26,27].此外,PEA(用作样本)还抑制了辣椒素和柠檬酸诱发的豚鼠气道神经c纤维的动作电位激发在活的有机体内,辣椒素或低pH诱导豚鼠离体气道终端颈静脉神经元细胞内钙含量升高在体外.这些实验的结合有力地表明,抑制FAAH升高的FAAs对CB起作用2感觉神经上的受体介导PF-04862853的镇咳作用。此外,在ptx处理过的动物迷走神经组织中,PEA抑制消失,提示Gi / oCB下游的亚单元信令2受体。虽然我们利用迷走神经准备的数据表明了一种外周作用机制,但FAAs的中心效应不能被忽视。
尽管经检测的FAAs可激活CB2受体(28- - - - - -31],以前的出版物也提出了对CB的影响1受体(29], PPAR (PPAR-α, -β和-γ)受体[10,31- - - - - -33],和TRPV1 [9,34,35]及TRPM8 [36离子通道。然而,一个角色为CB2受体已在这些研究中明确确定,这些研究使用了高度选择性的药理学工具[26,27],这与以往的研究结果一致[6,7].然而,仍然不可能完全排除非大麻素受体对大麻的作用在活的有机体内FAAs的活性。
Apamin, SK的抑制剂Ca通道,阻断了PEA对豚鼠离体迷走神经去极化的抑制,证实了之前的报道,CB1和CB2受体激动剂可激活钾通道[37].SKCa通道是钙激活钾通道家族之一,其激活导致钾从神经元流出,从而降低其兴奋性。SK的Ca通道与CaM、PP2A和CKII一起是多蛋白复合物的一部分。CaM被绑定到SK上Ca钙通道在钙结合转化为通道打开的过程中起着关键作用。CaM的灵敏度,因此SK的灵敏度Ca钙离子通道通过磷酸化/去磷酸化调控,CKII磷酸化导致钙敏感性降低,PP2A去磷酸化导致钙敏感性增加[19].我们发现冈田酸,一种PP2A抑制剂,阻断了PEA在迷走神经上的抑制活性,这表明PEA的作用是增加对钙的敏感性(因此增加了SK的活性)Ca通道通过激活PP2A。关键数据集在人迷走神经制剂中重复,结果与豚鼠相似。
总之,抑制FAAH可在清醒的豚鼠体内产生镇咳活性。我们的数据表明,这种影响可能是由升高的FAAs介导的,作用于大麻素(CB2)迷走感觉神经上的受体,导致SK的激活Ca通道,一种转化为人类迷走神经的效应。迄今为止,对这一领域的兴趣集中在开发FAAH抑制剂以减轻疼痛,早期临床研究表明,一种密切相关的类似物(即。PF-04457845)对所研究化合物的耐受性良好,在超过最大抑制FAAH活性和提高FAAs所需剂量时,对认知功能没有影响[38].这些数据表明,抑制FAAH导致FAAs升高可能是治疗慢性咳嗽的一种有趣和新颖的治疗方法。虽然临床前和临床辣椒素挑战研究的疗效(如。使用TRPV1拮抗剂)并没有转化为慢性咳嗽患者的疗效,FAA配体抑制多兴奋性离子通道激动剂引起的迷走神经去极化的事实赋予了更大的成功机会[39- - - - - -41].有了临床可用的化合物,可以通过采用重新定位的方法和利用疼痛治疗领域的化合物来进行概念验证临床研究。最近,P2X3抑制剂AF-219在治疗耐药患者的慢性咳嗽中表现出前所未有的疗效,这一策略获得了成功[42].
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
图S1。棕榈酰乙醇酰胺(PEA)通过激活CB2受体抑制丙烯醛-,GSK1017690A-或低渗诱导的迷走神经去极化。PEA (100 nM)抑制TRPA1激动剂丙烯醛(300 μM)、合成TRPV4激动剂GSK1016790A (300 nM)或内源性TRPV4激动剂低渗透溶液(-80 mOsm)诱导的离体豚鼠迷走神经去极化。数据以均数±SEM表示,每组n=3-4。erj - 00782 - 2017 - _figure_s1
披露的信息
补充材料
M.G. Belvisierj - 00782 - 2017 - _belvisi
硕士博雷尔erj - 00782 - 2017 - _birrell
c . Perros-Hugueterj - 00782 - 2017 - _perros女人
m . Papakostaerj - 00782 - 2017 - _papakosta
确认
作者贡献:M.A. Wortley, J.J. Adcock, R. Kinloch, G. McMurray, C. Perros-Huguet, M. Papakosta, M.A. Birrell和M.G. Belvisi对作品的概念或设计做出了重大贡献。M.A. Wortley, J.J. Adcock, E.D. Dubuis, S.A. Maher, S.J. Bonvini, I. Delescluse, M.A. Birrell和M.G. Belvisi对数据的获取、分析或解释做出了贡献。所有作者都参与了作品的起草或对重要知识内容的批判性修改,并最终批准了即将出版的版本,并同意对工作的各个方面负责,以确保与工作任何部分的准确性或完整性有关的问题得到适当的调查和解决。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:S.A. Maher和E.D. Dubuis由医学研究理事会的项目赠款资助(MR/K020293/1)。M.A.沃特利也得到了西北肺脏中心慈善机构的资助。本研究中的人类迷走神经实验是在皇家布朗普顿和海尔菲尔德NHS基金会信托基金和伦敦帝国理工学院的NIHR呼吸疾病生物医学研究部门的支持下进行的。本文的资助信息已存入交叉参考基金注册.
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2017年4月13日。
- 接受2017年6月21日。
- 版权所有©ERS 2017