文摘
咳嗽反射变得反应在急性和慢性呼吸道疾病,但理解底层机制受到困难获得人体组织包含的神经末梢和神经细胞体。我们精制成年干细胞感觉神经元模型来克服人类神经元的有限的可用性,并将该模型应用于研究瞬时受体电位锚蛋白1 (TRPA1)通道表达和激活。
人牙髓干细胞向神经元分化表型(hDPSCs),称为外围神经等价物(pn)。通过分子和免疫组织化学技术,结合Ca2 +microfluorimetry和全细胞块夹紧,我们调查了角色的神经生长因子(神经生长因子)和病毒模拟聚我:C TRPA1激活。
pn展出形态学、分子和感觉神经元的功能特征和表达功能TRPA1频道。PNE与神经生长因子治疗20分钟生成明显增大出入口电流比未经处理的pn的TRPA1兴奋剂肉桂醛(p < 0.05)。PNE治疗聚我:C引起类似的瞬态反应加剧TRPA1比未经处理的细胞活化。
使用PNE神经元模型我们观察到神经生长因子和聚我:C介导的感觉神经元的高反应性,代表与疼痛的加剧反应相关的潜在neuro-inflammatory机制认可在过敏性咳嗽综合症。
文摘
开发小说成人干细胞的神经元模型研究神经高反应性的咳嗽http://ow.ly/Ilvb30eokUC
介绍
气道感觉神经控制咳嗽和代表是肺部清除分泌物,保护自己免受吸入异物和刺激1]。条件如哮喘和慢性咳嗽这个神经反射变得反应过度,引起麻烦的咳嗽通常由低电平触发物理和化学刺激(2,3]。这些异常的感官反应通常在呼吸道病毒感染恶化,虽然病毒在呼吸道上皮细胞和免疫细胞的影响已被广泛研究,有关机制所知甚少负责气道神经高反应性(4- - - - - -6]。伴随的症状是最打扰病人气道高反应条件,没有目前的治疗,充分缓解和“重置”这种状态(7]。潜在的治疗目标包括瞬时受体电位(TRP)阳离子通道负责感应化学和物理刺激和表达在许多细胞类型包括气道感觉神经8]。我们曾表明,人类鼻病毒上调表达的锚蛋白1 (TRPA1)和TRP辣椒1 (TRPV1)通道在神经分化使人类神经母细胞瘤细胞系(9];然而,参与神经高反应性的机制仍有待调查。
许多刺激神经组织的分子释放到呼吸道病毒感染后气道,包括神经生长因子(神经生长因子),改变TRP通道功能(10),可能在调节气道感觉神经响应性很重要。此外,众所周知,感觉神经元表达toll样受体(通常)在宿主防御中发挥关键作用的微生物感染(11]。toll样受体3 (TLR 3)是特别感兴趣的,因为它对病毒双链RNA(极),病毒复制的副产品,包括鼻病毒(12,代表一个潜在的路线通过病毒感染可能引起咳嗽反射高反应性。
调查TRP通道在人类感觉神经元表达和调控是具有挑战性的,因为周围神经元的细胞体被安置在神经元ganglia无法访问的活检。尽管TRP通道的研究一直在进行动物模型(13- - - - - -15TRP)有认可的种间差异函数和表达式(16- - - - - -18]。此外,在欧盟(EU)的立法保护动物为科学目的有迫切需要新一代的发展在体外模型基于人类生物学(19]。因此,人工神经元模型可能补充或取代目前用于呼吸研究一些动物模型并提供人体生理学相关的数据。
牙髓组织来源于神经嵴细胞迁移在开发过程中(20.,21),是一个multipotential干/祖细胞的来源。倾向的人牙髓干细胞向神经细胞表型(hDPSCs)来区分,以前称为外围神经等价物(pn),据报道(22- - - - - -24),可能会解释他们的神经嵴来源。神经嵴干细胞的主要贡献者是周围神经纤维的发展,其中包括三叉神经(三叉神经节的25,26)和颈静脉神经节的迷走神经27]。颈静脉神经节C-fibres终止在肺外的航空公司和直接回应咳嗽引起的刺激,如辣椒素和血管舒缓激肽,表达神经肽和速激肽,因此被认为是重要的在痛觉气道反应如咳嗽。在这里,我们描述的发展功能的人类在体外从hDPSCs分化神经元模型,适用于研究神经炎症因子的作用TRPA1 channel-mediated神经高反应性。
方法
详情可在网上补充。
细胞培养和hDPSC浓缩
人牙髓细胞从成熟收获永久第三磨牙依照法国道德立法(28)和维护基本medium-alpha (MEM-alpha)补充10%胎牛血清的边后卫,UI·100毫升−1青霉素和100µg·毫升−1链霉素、谷酰胺和200年µM抗坏血酸。hDPSCs在牙髓细胞培养丰富优惠粘附纤连蛋白(10µg·毫升−1一夜之间在4°C)涂布six-well盘子和孵化20分钟的37°C。Non-adherent细胞被丢弃。hDPSCs维持在MEM-alpha纤连蛋白2天。
神经诱导
hDPSCs是从fibronectin-coated板使用胰蛋白酶和播种到收获塑料/玻璃器皿涂poly-l-ornithine(0.01%)和层粘连蛋白(5µg·毫升−1)和孵化neurobasal B27的补充,ng glutaMAX,人类基本成纤维细胞生长因子(40毫升−1ng)和上皮生长因子(40毫升−1为7天)。
免疫荧光
pn是分化从hDPSCs如上所述圆形盖玻片(16毫米,厚度1)。在PBS和固定细胞被洗淹没在冰冷的丙酮8分钟然后风干。细胞被洗在PBS和阻塞孵化10%正常山羊血清非特异性结合。
细胞治疗与特定主要抗体山羊血清(10%)在一夜之间在4°C(表S1)。适当anti-species Alexa萤石二级抗体轭合物在PBS稀释含0.1% Triton X 100和应用于细胞在室温下1 h。样本安装使用延长黄金(热费希尔科学,佩斯利,英国)与DAPI和使用荧光显微镜观察。
中存在
神经诱导hDPSCs朝着实现pn正如上面列出的,除了细胞生长在96 -孔板。总RNA提取使用PicoPure RNA隔离设备(热费希尔科学)和量化使用Take3板块和板块读者(BioTek、斯文顿、英国)。RNA样本使用上标很cDNA反向转录合成装备(热费希尔科学)根据制造商的指示。qPCR反应是建立用TaqMan普遍mastermix)(热费希尔科学)根据制造商的指示使用预先设计TaqMan引物(热费希尔科学;表S2和S3)。使用Stratagene qPCR进行PCR仪器(安捷伦,斯托克波特,英国)和分析使用Mx3005P软件(安捷伦)。
全细胞膜片钳
pn分化所描述在盖玻片(厚度0)。全细胞电流记录使用硼硅酸盐片吸量管(2 - 5 MΩ阻力),b Axopatch 200放大器(英国分子器件、Workingham)和pClamp9软件(分子设备)。
测量电压门控钠+氯化钠通道活动,中海浴(150毫米,6毫米中海,MgCl 1毫米2,1.5毫米CaCl25毫米葡萄糖和10毫米dH的玫瑰2O;使用三羟甲基氨基甲烷)和液吸管pH值变化到7.4(120毫米中海,MgCl 1毫米2,4毫米Na2ATP, 10毫米BAPTA和10毫米dH的玫瑰2O;pH值变化到7.2使用三)解决方案。1µM河豚毒素(TTX)是由中海浴的解决方案。实验在室温下进行。持有的潜在−120 mV。电流−电压(我−V)关系协议是使用电压测量的步骤。
TRP通道活动记录使用中海浴溶液和Cs-aspartate(100毫米CsOH.2H吸管的解决方案2啊,100毫米天冬氨酸,20毫米中海,MgCl 1毫米2,4毫米Na2ATP, 0.08毫米CaCl210毫米BAPTA和10毫米dH的玫瑰2O;pH值变化到7.2使用三)。100年µM肉桂醛,10µM HC030031 10µM辣椒素和20µM capsazepine在中海浴组成的解决方案。实验在37°C。控股可能是0 mV。我−V关系记录使用电压斜坡的协议。所有数据分析使用Clampfit9软件(分子设备)。
Microfluorimetric钙成像
microfluorimetric钙成像,pn分化所描述在盖玻片(厚度0),pn装满Fura-2AM(5µM) 40分钟在37°C,放入一个记录室安装在倒置显微镜和过冷的阶段汉克斯(140毫米氯化钠,氯化钾5毫米,2毫米CaCl2.2H2啊,1毫米MgCl210毫米,消息灵通的自由酸和5毫米dH的葡萄糖2O;pH值变化到7.4使用氢氧化钠)。所有的解决方案都保持在37°C使用水浴和灌注系统。(Ca2 +]我测量(细节补充材料)和观察TRP通道活动(Ca的变化2 +)我与10µM辣椒素刺激后和10µM capsazepine稀释汉克斯。
共焦Ca2 +成像
pn装满0.4µM fluo-4 / AM 6分钟在室温和成像使用iXon887 EMCCD相机(和或技术、贝尔法斯特、英国)耦合到Nipkow旋转磁盘共焦头(CSU22、日本横河、日本)。氪氩激光(干预流浪英国、伊利、英国)在fluo-4 488海里被用来激发,和发现发射光波长510纳米。实验使用×60目的(奥林巴斯)和图像获得15帧每秒。背景荧光的相机,获得使用一个空框架,从每一帧减去获得“F”。F0确定最低控制条件下荧光。伪扫描图像和相应的强度剖面情节获得使用图像J软件(贝塞斯达国立卫生研究院,医学博士,美国)。ΔF / F0指的是测量的变化2 +从基础到峰值水平。
ELISA
pn分化在96 -孔板。上层清液收集后治疗方法(如下面所列)和白介素8 (IL)使用人类引发和IL - 6和IL - 6水平测量DuoSet ELISA试剂盒(研发系统,阿宾顿,英国)根据制造商的指示。
pn的治疗
pn服用促炎细胞因子(神经生长因子,100 ng·毫升−1;ng IL-1β5毫升−1;肿瘤坏死factor-α(TNF-α),10 ng·毫升−1;C(2)和聚我:µg·毫升−1)20分钟,6小时或24小时(表S4)。控制细胞培养介质。
结果
丰富hDPSCs接受神经元分化成为功能性pn
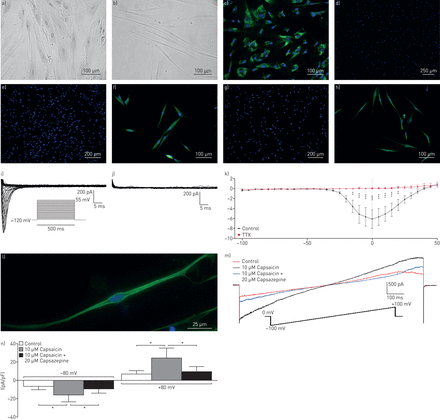
hDPSCs表达神经嵴蛋白标记,我,AP2αHNK1(图S1)和显示组成的成纤维细胞的形态学多极伸长(图1一个)。后7天内神经元分化,细胞获得了一个典型的双极神经元形态与集中位于胞体肿胀和axon-like预测(图1 b)。免疫荧光证实从hDPSC PNE在分化表型的改变,体现纤维母细胞标记FSP损失的表达式(图1 c和d),获得特定的成熟神经元标记PGP9.5 (图1 e和f)和synaptophysin (图1 g和h)。pn也表达了神经肽P物质和CGRP怎样符合感官神经表型(图S2)。
人牙髓干细胞(hDPSCs)进行形态和表型的变化在神经元分化成为功能性外围神经等价物(pn)。hDPSCs成纤维细胞的形态组成的舒展多极伸长(a)。神经元分化后细胞失去这形状和承担一个典型的双极神经元形态由胞体肿胀和axon-like预测(b)。未分化hDPSCs表达成纤维细胞标记FSP (c),这FSP表达式是失去了在神经元分化,不再用pn (d)。在神经元分化之前,hDPSCs不表达特定的神经元标记PGP9.5 (e)或synaptophysin (g),它们存在于PNE文化(f和h,分别)。pn展览voltage-activated Na+电流后7天内分化。家庭的内向电流记录PNE遵循一系列500 ms消除电压的步骤从最初持有潜在−120 mV 55个mV 5 mV增量(i)。这个反应,在相同的细胞,完全被抑制的TTX(1µM) (j)。目前−TTX的缺失和存在的电压关系正常化对细胞电容(n = 7;意味着细胞电容38 pF,扫描电镜2.85(测量使用pClamp软件)(k),误差表示扫描电镜。TRPV1的表达在pn是免疫荧光(左)所示。完整的细胞片夹紧进行录音pn调查TRPV1通道的功能表达。除了TRPV1受体激动剂的辣椒素在电压斜坡协议两个出入口膜电流增加。这种反应被抑制的存在TRPV1拮抗剂capsazepine (m),峰值电流测量80−80 mV和统计分析(n)。* mV: p < 0.05;* *:p < 0.01;* * *:p < 0.001。
使用完整的细胞片夹紧pn的神经细胞表型是进一步证实了通过展示功能的电压门控钠+(NaV)通道。使用基于cs浴和吸管块向外K的解决方案+电流,一个家庭迅速灭活的内向电流都时生成一系列500 ms消除电压措施应用于5 mV的增量从最初持有的潜在−120 mV (图1我)最后一个测试55 mV的潜力。电流完全抑制Na+通道抑制剂,TTX(1µM) (图1 j)。正常细胞对电容电流,绘制显示我−V的关系(图1 k)。
TRPV1以来一直与神经细胞表型相关,基因和蛋白质表达的pn是由qPCR表(S5)和immunofluorescene (图1 l)。确认在pn TRPV1功能,使用c执行完整的细胞片夹紧+的浴和吸管的解决方案。使用电压斜坡的协议,在出入口电流显著增加后观察TRPV1受体激动剂的应用辣椒素(10µM),由capsazepine显著抑制(20µM) (图1米和n)车辆只有控制响应(图S3)。进一步功能研究证实pn的适用性microfluorimetric (Ca2 +]我成像TRPV1活动执行。Fura-loaded pn被证明证明自发活动(图S4),神经元功能的特点,辣椒素应用瞬时增加PNE (Ca2 +]我观察(图S5a),与(Ca2 +]我立刻水平下降。TRPV1对手的存在,capsazepine PNE (Ca2 +)我没有增加基底以上水平(图S5b)。比例的变化与辣椒素capsazepine画了统计分析的缺失和存在(图S5c)。
pn表达TRPA1功能
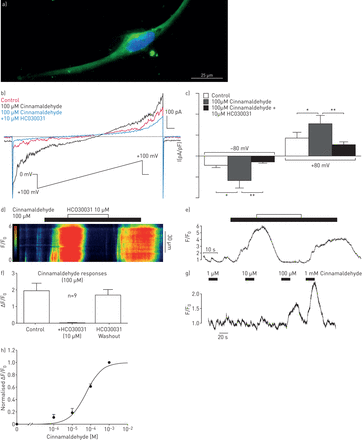
建立了pn的神经细胞表型(图1 gydF4y2Ba他们研究TRPA1渠道研究的适用性。证实了基因表达TRPA1 qPCR(表S5)以及通过免疫荧光蛋白表达(图2一个)。研究功能性TRPA1 pn,全细胞膜片钳实验使用Cs+的浴和吸管的解决方案。使用电压斜坡的协议,在出入口电流显著增加观察在pn肉桂醛的应用(100µM)都被HC030031(10µM) (图2 b和c)。汽车只有控制响应(图S3)。进一步证实pn是否适合功能TRPA1研究我们对肉桂醛的影响(100µM)在Ca2 +水平单pn使用共焦Ca2 +成像。肉桂醛诱导强劲上涨(Ca2 +)我是可逆抑制后续HC030031应用程序(代表图2 d和e和总结情节图2 f;n = 9)。肉桂醛的反应被证明是浓度依赖(图2 g和h),电子商务5054µM。使用microfluorimetric [Ca2 +]我成像fura-loaded pn显示自发活动(图S4),和肉桂醛的应用(Ca的PNE瞬间上升2 +]我观察(图S6a),其次是下降(Ca2 +我水平之后立即。在HC030031面前,PNE (Ca2 +)我没有增加基底以上水平(图S6b)。均值的变化比例画了统计分析(图S6c)。
TRPA1通道蛋白的存在外围神经等价物(pn)被证实使用免疫荧光(a)。完整的细胞片夹紧进行录音pn调查的功能表达TRPA1频道。TRPA1受体激动剂的肉桂醛在电压斜坡协议两个出入口膜电流增加。这种反应被抑制的TRPA1拮抗剂HC030031 (b),峰值电流测量80−80 mV和统计分析(c)的mV。*: p < 0.05;* *:p < 0.01。肉桂醛的应用程序隔离pn诱导(Ca强劲上涨2 +]我被后续的应用可逆地抑制HC030031 9细胞(d和e)。肉桂醛的平均振幅响应从1.96ΔF / F显著降低0在控制条件下到0.02ΔF / F0在HC030031的存在;p < 0.01,配对t检验(f),误差表示扫描电镜。Cinnamaldehyde-induced海拔(Ca2 +)我是浓度依赖、EC的意思50值这一效应是54µM(95%置信区间38 - 79µM, n = 4;分别为g和h)。
神经生长因子诱导TRPA1 pn的高反应性
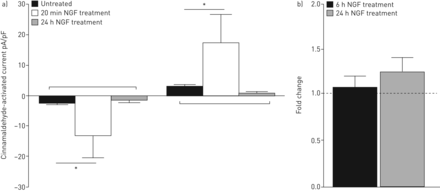
神经生长因子是在感觉神经元诱导高反应性10,29日,30.),因此神经性值得调查的细胞因子在体外模型。pn治疗神经生长因子对膜片钳实验前20分钟立即产生显著(p < 0.05)更大的出入口电流刺激时肉桂醛(图3一),证明PNE TRPA1通道高反应性神经生长因子的存在。这个反应状态没有持续,pn治疗24小时不产生较大的电流观测之前(图3一)。
外围神经等效(PNE) TRPA1渠道成为反应20分钟后孵化与促炎介质神经生长因子(神经生长因子)(100 ng·毫升−1),但这种影响并不明显pn孵化24小时与神经生长因子;他们没有显示高度对肉桂醛的反应(100µM) (a)。*: p < 0.05。这种高反应性也似乎是独立的基因表达无显著变化中的基因表达TRPA1 pn 6 h和24小时后观察神经生长因子(100 ng·毫升−1)治疗(b)。
研究基因表达TRPA1是否改变神经生长因子治疗后我们进行了存在pn孵化与神经生长因子6 h和24 h。在基因表达TRPA1观察(没有显著的变化图3 b)。确定这是一个NGF-specific效果,我们与促炎细胞因子治疗pn TNF-α(10 ng·毫升−1ng)和IL-1β(5毫升−1),并观察TRPA1基因表达无显著变化(图七)。
我们也调查了类似的效果是否回应神经生长因子治疗观察pn与辣椒素刺激。无显著变化capsaicin-induced电流被认为在治疗和神经生长因子治疗细胞(图S8a)。同样,确定任何更改TRPV1基因表达后神经生长因子治疗(图S8b)。
病毒模拟聚我:C诱导引发释放和TRPA1 pn的高反应性
多聚肌苷酸是用来证明模型的有效性探讨病毒感染对感觉神经元的影响。细胞上清液从pn孵化与保利我:C进行分析引发和il - 6。上层清液从控制细胞,这些孵化与保利我:C 6 h引发水平没有显著变化,也没有可检测il - 6在控件(图4一从细胞和b)。然而,上层的孵化与保利我:C 24 h的水平明显高于有引发(2140.8 pg·毫升−1)和il - 6 (246.5 pg·毫升−1)(图4一和b)。额外的浓度和时间的影响聚我:C在图S9报告引发的水平。
多聚肌苷酸诱发白介素8 (IL)和IL - 6分泌外围神经等效(PNE)文化。上层清液从pn孵化与保利我:C(2µg·毫升−1)24小时显示增加引发了未经处理的pn和il - 6水平比或pn孵化与保利我:只C 6 h (a和b分别)。PNE TRPA1渠道成为反应20分钟后孵化与病毒模拟聚我:C(2µg·毫升−1)。pn处理聚我:C证明反应加剧TRPA1兴奋剂肉桂醛(100µM)相比,在未经处理的pn这种高反应性(C)。似乎是独立的基因表达无显著变化中的基因表达TRPA1 pn观察后6 h和24 h聚我:C治疗(d)条代表扫描电镜。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
多聚肌苷酸也在pn诱导TRPA1高反应性。治疗pn聚我:C片夹紧前20分钟立即生成明显增大出入口电流肉桂醛,而未经处理的pn (图4 c)。pn孵化与保利我:C 24 h不容易适合膜片箝记录,表明在质膜发生了变化。没有显著变化观察6小时或24小时后基因表达TRPA1聚我:C治疗(图4 d)。
讨论
在这项研究中,我们成功地分化从人类牙髓干细胞对pn的形态学、分子和感觉神经元的功能特征。我们观察到TRPA1通道高反应性刺激后神经生长因子和病毒模拟聚我:C。反应在发病迅速,和独立的TRPA1基因表达。综上所述,我们的数据表明,pn代表小说特有的在体外TRPA1通道功能的调查模型对人类感觉神经元和监管。我们相信这个模型有潜力提供洞察过敏性咳嗽的潜在机制。
的重要改进我们的方法的浓缩hDPSCs使用微分纤连蛋白粘附,从牙髓文化允许表型从hDPSC PNE相比,7天21天之前报道使用牙髓细胞培养(22]。功能性神经分化的细胞,所述活动应该考虑神经性格化的先决条件,特别是在发现压敏电阻器的钠离子通道hDPSCs(不存在31日]。
为pn的适用性作为提供证据在体外研究模型的炎性TRP通道调节我们调查神经营养细胞因子神经生长因子的影响。神经生长因子水平升高在哮喘患者的气道32),与流感感染的儿童气道神经生长因子水平增加,与疾病严重程度和咳嗽持续时间(33我们观察到神经生长因子诱导迅速增加TRPA1激活符合报告之前在鼠标感觉神经元的主要文化28]。如此快速的影响可能是由于细胞内激活细胞信号通路导致磷酸化TRP通道与随后的通道的高反应性(9]。我们数据显示神经生长因子可迅速诱导TRPA1通道高反应性,支持角色transcription-independent机制在调节TRP反应(10]。有趣的是,我们没有看到对辣椒素的反应增加NGF-treated细胞,之前报道的豚鼠模型在活的有机体内(34]。这种差异可以强调动物和人类组织和之间的差异可能会增加临床相关性PNE模型。同样值得注意的是,积极的临床前动物模型中的数据的TRPV1拮抗剂XEN-D0501形成鲜明对比:缺乏疗效的报道在慢性咳嗽的安慰剂对照试验(35]。
PNE治疗后病毒模拟聚我:C,大幅增加在引发和il - 6的分泌和增加电流响应肉桂醛比未经处理的pn观察。这是第一个报告显示功能TRPA1和多边形之间的关系我:C。众所周知,病毒模拟聚我:C模拟病原体相关分子模式(PAMP时)dsRNA,并激活三个模式识别受体(PRRs) TLR3,视黄acid-inducible基因1 (rig - I)和黑色素瘤differentiation-associated蛋白5 (MDA5) [36]。TRPA1的功能交互和保利我:C因此可以介导通过一个或多个受体。
总之,pn代表小说特有的在体外模型适用于研究人类感觉神经元的通道功能和监管是符合当前欧盟和英国的指令来代替,减少和优化使用动物研究[19]。使用这个模型,我们表明,神经生长因子和病毒模拟聚我:C直接和快速诱导TRP通道高反应性在人类感觉神经细胞膜的代表可能neuro-inflammatory过程负责咳嗽反射高反应性。我们已经仔细区分神经元的实验发现高反应性和神经过敏症。实验neuro-inflammatory条件下我们观察到神经反应增加对于一个给定的刺激可能临床并行的形式“hypertussia”在过敏性咳嗽综合症患者(CHS) [37]。我们还没有确定PNE模型可以对低水平刺激呈现“高度敏感”。CHS是在呼吸障碍获得越来越多的认可,过敏,胃肠病学、语音/语音和耳鼻喉科医疗专家(37]。需要提高我们理解神经生物学的这个条件,我们相信我们报告在这个手稿小说技术和临床相关性的实验研究结果感兴趣的那些在这个领域工作。
补充材料
披露的信息
确认
我们承认凯瑟琳·富尔顿的娴熟的技术援助。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:这项工作由国家中心更换,细化和减少动物研究(NC3Rs)和缓解疼痛基金会(英国)。资金信息,本文已沉积的Crossref资助者注册表。
利益冲突:披露可以找到与这篇文章www.qdcxjkg.com
- 收到了2017年5月15日。
- 接受2017年7月16日。
- 版权©2017人队