摘要
基质金属蛋白酶9 (Matrix metalloprotease-9, MMP-9)在囊性纤维化的进展中发挥作用,强力霉素可降低MMP-9体外在此,我们探讨囊性纤维化加重治疗期间强力霉素对MMP-9相关读数和临床终点的影响。
这项随机、双盲、安慰剂对照研究纳入了正在加重的囊性纤维化住院患者。在8天的住院期间,总共有20名参与者服用多西环素,19名参与者服用安慰剂。在研究开始和结束时采集生物标本。主要终点为痰液中MMP-9总水平和安全性/耐受性。次要终点包括肺功能的改变、下一次恶化的时间和MMP-9相关蛋白酶活性(活性MMP-9和TIMP-1)的标志物。非参数检验用于组内和组间分析。
强力霉素耐受性良好,无治疗中断或严重不良事件。强力霉素使总痰MMP-9水平降低63.2%(p<0.05),并与活性MMP-9水平降低56.5%(p<0.05)、痰TIMP-1增加1.6倍(p<0.05)、1例患者用力呼气量改善相关 s(p<0.05),以及下一次加重的时间增加(p<0.01)。
多西环素的辅助使用改善了痰液中失调的MMP-9水平,以及与蛋白水解肺环境减少相一致的生物标志物。临床结果指标的改善表明强力霉素对囊性纤维化患者有重要的治疗益处。
摘要
强力霉素改善CF急性肺加重期间蛋白酶/抗蛋白酶失衡和临床终点http://ow.ly/lF9p308Ov6i
介绍
囊性纤维化(CF)是全世界白种人中最常见的遗传性遗传病[1].这是由于囊性纤维化跨膜电导调节因子(雌性生殖道),从而破坏正常的上皮细胞功能[2]最突出的表现是在肺部,呼吸道中粘液纤毛清除的丧失导致粘液停滞、感染和持续炎症[3.].最终,这种持续的炎症会促进CF气道的细胞外基质重塑和支气管扩张,导致气体交换受损,细菌定植增加,疾病相关死亡率增加[4].CF肺疾病中观察到的进行性肺重塑在生命早期就开始了[4,最近的动物研究表明,这些变化对大小呼吸道都很重要[5].尽管这种气道重塑对疾病结局有直接影响,但目前在CF基金会的药物开发流水线中,没有特异性的抗纤维化治疗,只有一种抗蛋白酶治疗(https://tools.cff.org/research/drugdevelopmentpipeline).事实上,细胞外基质产物如胶原蛋白和弹性蛋白的肺重塑会导致气道和实质结缔组织完整性的丧失,并导致肺弹性后坐力的丧失[6].这些影响导致CF肺通气/灌注不匹配的逐渐恶化[7,导致低氧血症和肺功能丧失。
除了肺健康状况的稳步下降外,病程的特点是肺功能进行性下降,肺部症状恶化和间歇性气流丧失[8].这些间歇性发作被称为CF急性肺加重(APE),它们强烈导致疾病相关的发病率和死亡率[9].在APE发作期间,CF气道表现出增加的细菌负担和中性粒细胞炎症反应,并伴有显著的蛋白酶激活[10].目前治疗类人猿的方法是通过静脉注射抗生素提高粘液清除率和治疗呼吸道感染[9].
许多蛋白酶已经成为CF气道中肺重塑和相关炎症的重要贡献者,大多数注意力集中在人中性粒细胞弹性蛋白酶(NE)的水平和活性的升高[11].最近,一种不同的蛋白酶,基质金属蛋白酶-9 (MMP-9),已被证明在CF肺疾病患者的气道分泌物中有差异的升高[12].MMP-9是一种金属蛋白酶,由中性粒细胞、巨噬细胞和气道上皮细胞释放[13]作为一种前酶,随后由于其前结构域的丧失而被激活,从而产生一种活性酶和一种单独的前酶库。我们的研究表明,在急性CF住院患者急性加重期间,相对于自然发生的MMP抑制剂、金属蛋白酶组织抑制剂1 (TIMP-1),气道MMP-9水平和活性均显著增加,这种失衡相对于临床稳定的CF患者增加了3倍[12]因此,这种蛋白酶-抗蛋白酶失衡可增强气道重塑,影响气道免疫力,并在围加重期调节气道-宿主-病原体的相互作用[14].例如,最近我们的小组描述了CF气道中mmp -9生成的细胞外基质片段乙酰化脯氨酸-甘氨酸-脯氨酸(Ac-PGP)的水平升高,这是中性粒细胞炎症的关键调节因子[15].由于这种蛋白酶失效的潜在下游影响,虽然这些努力在很大程度上是不成功的,但由于副作用曲线差,主要是由于宽容较差的副作用曲线(而主要是持久的抗MMP治疗)即使用羟肟酸抑制剂的关节痛)或肺内缺乏适当的药物输送[16].
强霉素是一种四环素抗生素,广泛用于治疗革兰氏生物体引起的感染。以前的研究表明,十二胞环素的抗MMP活性,初步报告表明它可以用作MMP-9的小分子抑制剂[17,18].然而,随后的文献表明强力霉素也影响MMP-9的转录[19,20.].这些结果为强力霉素作为治疗CF肺疾病中MMP-9失调提供了科学依据。因此,我们进行了一项随机、双盲、安慰剂对照试验,以确定多西环素是否具有良好的耐受性,并能改变CF患者在住院CF APE治疗期间痰液中的MMP-9活性。除了这些主要目标,次要终点还包括与蛋白水解环境、炎症和临床参数(肺功能、住院时间和下一次加重时间)相关的生物标志物。因此,本研究设计为强力霉素对气道生物学的影响提供了机制上的见解,并提供了证据,表明该药物有可能用于治疗蛋白酶抗蛋白酶失衡的慢性肺病。
方法
病人
根据常规诊断标准,所有参与者均被诊断为CF,其中包括2个汗液Cl−值>60 mM,且至少有两个符合诊断的临床特征[2].入选标准包括CF诊断,年龄>19岁,与铜绿假单胞菌,并正在进行需要住院治疗的APE。显著的排除标准包括对强力霉素或四环素过敏或敏感;同时或近期(28天内)使用皮质类固醇(强的松>5 mg·天)−1);不能自动产生痰;需要有创或无创通气的急性呼吸衰竭、慢性肝或肾疾病;怀孕,殖民洋葱种和分枝杆菌种的活跃定植。患者在入院时进行筛选,并获得研究中所有参与者的知情书面同意。在研究过程中,每季度召开一次数据安全监测委员会会议,以评估任何安全考虑,并就研究进行向首席研究员提供反馈。
学习规划
该研究是一项针对成年CF患者的单中心、随机、双盲、安慰剂对照试验,在美国阿拉巴马大学伯明翰医院(UAB)进行。ClinicalTrials.govNCT01112059).研究对象由首席研究员或研究协调员从2010年6月至2012年6月的CF住院患者人群中招募。所有参加者均符合富克斯的标准[8]参加研究。同意接受强力霉素100治疗的患者随机分为相同数量 每日两次口服mg,或服用外观相同的安慰剂,持续8小时 APE治疗住院期间的天数。在整个研究过程中,受试者继续服用所有CF慢性护理药物和标准的住院患者加重治疗(静脉注射抗生素和增加气道清除率)。研究药剂师通过计算机生成的随机分配,以四名参与者为一组,填写处方,并且只能访问随机代码。所有参与者均由CF住院服务的护理人员给予强力霉素或安慰剂。这些药物是泡罩包装的,研究协调员和研究药剂师每天都会验证它们的正确使用。在整个研究过程中未报告与方案的差异。
值得注意的是,标准的患者护理和出院决定是由CF护理医生进行的,他们对研究任务是盲目的。在住院开始和结束时使用美国胸科协会指南进行肺活量测定[21].作为标准护理的一部分,在住院初期收集痰细菌学和血清c反应蛋白(CRP)。所有参与者在入院开始、住院第8天和出院时都进行了简短的病史和体格检查。在治疗前基线和患者出院时采集额外的痰液和血液以进行试验特异性读数(图1a).值得注意的是,39名可分析的参与者中只有36人能够在两个时间点提供痰液,39名可分析的参与者中有38人能够在两个时间点提供血液。只有拥有完整数据集的参与者才会被分析以获得一个给定的结果。所有39名参与者都进行了临床分析,如肺功能、住院时间和下一次病情加重的时间。对于下一个加重指标,我们前瞻性地跟踪了在UAB的CF提供者的研究参与者的临床访问,根据记录的Fuchs标准确定这些访问后第一次加重的任何点。只有在符合合适的Fuchs标准并采用亲代抗生素时,我们才保守地确定病情加重。
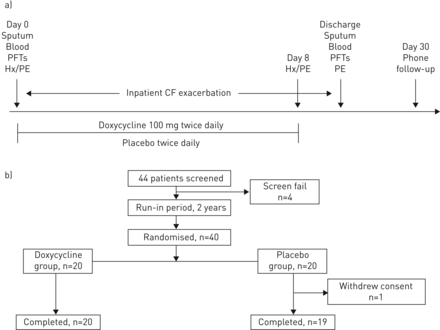
临床试验设计配偶图。a)强力霉素作为一项住院囊性纤维化(CF)加重试验设计的辅助治疗:所有CF加重的住院患者在入院24小时内询问同意,治疗8天。在药物治疗和出院前收集生物标志物信息和患者的身体状况。主要终点包括安全性/耐受性和总基质金属蛋白酶(MMP)-9活性。次要终点包括炎症标志物和肺功能的改变。所有患者出院后30天进行电话随访。Hx:病史;体育:体格检查;pft:肺功能检查b)本临床试验的CONSORT图:筛选44例患者进行研究; of these, 40 participants were deemed eligible and were randomised to one of two study groups. One subject withdrew consent during the course of the study, thus 39 participants (n=20 in the doxycycline group and n=19 in the placebo group) underwent complete follow-up and were included in the analyses.
主要研究终点为痰液中MMP-9的总水平和治疗的安全性/耐受性。次要研究终点包括活性MMP-9、肺功能、住院时间、下一次加重时间、MMP-9相关蛋白酶活性标志物和炎症标志物(即NE, CRP,促炎细胞因子)。所有患者出院后均进行1个月的随访。
生化分析
血清和痰的处理如在线数据补充中所述。MMP-9特异性ELISA和活性、TIMP-1 ELISA、NE ELISA分析、细胞因子分析和Ac-PGP肽检测如在线数据补充中所述进行。
统计测试
基于我们之前的工作[12,我们估计,每组20例患者的样本量为80%,α=0.05,表明强力霉素治疗组在治疗8天后总MMP-9降低了45%。描述性统计包括平均值±sd为所有定量测量计算,并以图表显示(除非图例中另有说明)。使用稳健非参数统计检验对强力霉素治疗组和安慰剂对照组进行人口统计学和诊断比较,以避免因违反终点正态假设而产生的潜在偏差。治疗前和治疗后生物标志物和肺功能的比较采用Wilcoxon秩和检验进行治疗内组分析,各组间的变化程度采用Mann-Whitney统计方法进行比较。使用Kaplan-Meier分析和log-rank检验来确定强力霉素和安慰剂治疗的患者在下一次病情加重的时间上是否存在显著差异。治疗效果进一步估计为风险比(HR), 95%置信区间由Cox比例风险模型计算,并校正种族、性别和年龄作为协变量。显示与1秒内用力呼气量(FEV)变化的单变量关联的变量1) (p<0.05),采用逐步回归的多元线性回归模型确定临床因素、痰生物标志物和FEV百分比变化之间的独立相关性1在研究期间。统计学检验为双侧,p<0.05为差异有统计学意义。计算使用Instat软件(GraphPad, 5.0版)、SPSS统计软件(20.0版,IBM公司)或SAS(9.4版,SAS Institute)。
研究批准
人类参与者提供书面知情同意书。研究方案由UAB机构审查委员会批准(方案F081024004)。
结果
患者的人口特征和安全性
参与者的基本特征在表1,这两组人都非常接近。总体而言,两组患者均表现为基线中至重度气道阻塞,门诊FEV稳定1安慰剂组为45.8±16.3%,强力霉素组为50.2±17.7% (p=0.58)。此外,两组患者在住院前一年的平均病情加重频率相似(安慰剂组为2.9次相对强力霉素组出现2.8次加重;p = 0.61)。
两组的痰细菌学具有可比性(甲氧西林敏感金黄色葡萄球菌(MSSA)和铜绿假单胞菌),尽管安慰剂组的甲氧西林耐药发生率没有显著提高金黄色葡萄球菌(耐甲氧西林金黄色葡萄球菌)。值得注意的是,强力霉素组和安慰剂组各有一名患者的培养呈阳性嗜麦芽窄食单胞菌,两者均对强力霉素敏感。图1a用痰液和采血符号描述临床试验的模式。在住院期间,两组患者均接受标准护理,包括静脉注射氨基糖苷和-内酰胺抗菌剂,以及加强气道清除通过每天两次胸部打击疗法。MRSA患者同时接受静脉注射万古霉素或口服利奈唑胺治疗。所有参与者在住院期间继续基线CF药物治疗。
本试验的配偶图如所示图1b.总的来说,4人被认为筛查失败(2人由于缺乏痰,1人由于活动性咯血,1人由于开始咳痰注射。剩余的40名参与者采用区块随机模式随机分为两组,每组一组通过UAB研究药房。安慰剂集团的一个主题在研究过程中撤回了同意。完成该研究的所有39名参与者在医院排放后30天内活着。值得注意的是,在研究期间没有注意到显着的不良事件,观察到10例不良事件(每组五个),所有这些都是自我限制的。只有十二胞菌素组的不良事件中的一个不良事件被判断为可能与研究药物(嘴唇刺痛1天,自我解剖)。
强力霉素可降低气道MMP-9水平和活性
在基线时,每个研究人群的MMP-9总水平(前MMP-9 +活性MMP-9)均有类似的升高,超过90%的可测MMP-9处于活性状态。住院治疗结束时,强力霉素组MMP-9总活性显著降低(p=0.01) (图2a),而安慰剂组则没有(图2b)此外,强力霉素组的活性MMP-9水平降低了56.5%(p<0.05)(图2c),提示强力霉素影响气道MMP-9蛋白和酶活性。两组患者血清MMP-9水平也低于痰液水平,住院治疗后相对不变(图S1)。
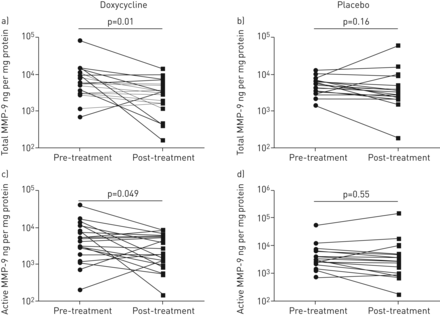
强力霉素治疗对气道基质金属蛋白酶(MMP)-9的中和作用:痰液中总MMP-9 (a, b)和活性MMP-9 (c, d)被量化和标准化为总蛋白,强力霉素组n=19,安慰剂组n=17。数据显示为每个样品前相对治疗后。
doxycycline衰减Pro-proteolytic CF环境
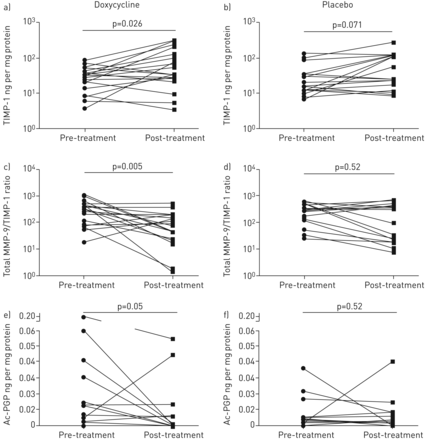
先前的研究强调,CF气道中的促蛋白水解环境对正在进行的蛋白酶-抗蛋白酶失衡、细胞外基质重塑和气道炎症有重大影响[11,14].为了解决这一平衡,我们量化了痰液TIMP-1水平,并观察到尽管两组之间的基线水平具有可比性,但与安慰剂组相比,多西环素治疗组在治疗过程中增加了1.6倍(p<0.05,图3a).当相对于TIMP-1检测总水平时,强力霉素治疗组>降低70% (图3c),表明CF气道中这种关键蛋白酶-抗蛋白酶复合物之间的平衡得到了改善。
多西环素治疗恢复蛋白酶 - 抗滴发酶的平衡和细胞外基质分解标志物的细胞外基质分解标志物:量化金属蛋白酶(TIMP)-1(A,B)的痰组织抑制剂与总基质金属蛋白酶(mm)P-9进行比较(c,d);通过电喷雾电离 - 液相色谱串联质谱法测量细胞外基质击穿标记痰乙酰化脯氨酸 - 甘氨酸 - 脯氨酸(AC-PGP)(E,F)并标准化为总蛋白质。n = 19 on for doxycycline,n = 17用于安慰剂。数据显示为每个样品前相对治疗后。
强力霉素治疗组的痰Ac-PGP水平降低(图3e),而安慰剂组则没有(图3f),加强对蛋白水解环境的观察。在研究过程中,两组间NE水平没有观察到差异(图S2a),表明这种抗蛋白酶作用对MMP活性是特异性的。两组患者CRP水平均有所下降,但安慰剂或强力霉素治疗后没有观察到差异(图S2b)。此外,安慰剂组和多西环素组在经典早期反应前炎症细胞因子(表2).
强力霉素可改善CF住院患者病情加重期间的临床预后指标
结合强力霉素治疗过程中观察到的生化变化,我们还检测了强力霉素对CF APE临床结果的影响。在加重过程中,两组患者的强迫肺活量(FVC)总容积和预测的%均得到改善,但两组之间无统计学差异(图S3a和b)。这些结果与FVC (FEF)的25-75%时强迫呼气流量的变化相一致25 - 75)(图S3c)。虽然FEV1在两个治疗组中均得到改善(图4a和b),两者的总体积变化(图4c)和% pred (图4d)在强力霉素治疗组中明显高于安慰剂组。与安慰剂组相比,多西环素治疗组的总住院天数减少了12.7天相对分别为14.2天;p = 0.17)。我们还观察到强力霉素组的总数更少注射。相对于安慰剂组(13.4相对15.3天;p = 0.064)。最后,我们发现强力霉素组与安慰剂组相比,在下一次病情加重的时间上有显著改善(图5) (log-rank检验p<0.01),调整HR为0.289 (95% CI 0.128-0.633;p < 0.01)。mrsa阳性组没有观察到差异相对mrsa阴性参与者(图S3d)。
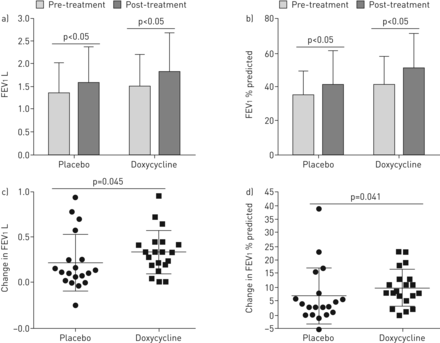
在囊性纤维化纤维化期间改善临床参数:1 s(fev1)(a)和fev中的绝对强制呼气量1%预测(b)恶化前后,以及每个个体的差异(c和d,分别),显示在每个治疗组。多西环素组20例,安慰剂组19例。
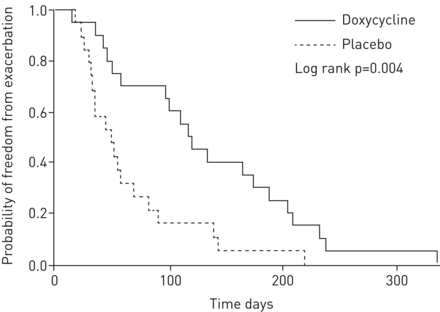
在囊性纤维化期间改善了下一步加剧的时间:与安慰剂(虚线)相关的时间差,显示具有对数秩检验的Kaplan-Meier非激增曲线。多西环素组20例,安慰剂组19例。
强力霉素治疗与肺功能改善独立相关
年龄,种族,性别,基因型,体重指数,铜绿假单胞菌(粘液类和非粘液类菌株)和葡萄球菌(MRSA和MSSA)感染与FEV改善无关1% pred在单变量分析中。在研究的生物标志物中,FEV的变化1% pred与与TIMP-1标准化的痰中MMP-9活性的%变化相关(ρ=−0.34,p<0.05),但与血液或痰中其他生物标志物的变化无关。在多元线性回归模型调整基线FEV1(%)、治疗分配和MMP-9活性/TIMP-1的%变化,只有强力霉素治疗与FEV的变化独立相关1%研究期间(标准化β=0.34,p<0.05)。
讨论
CF的治疗在过去20年有了显著的发展,随着新型抗菌、抗炎、气道水化和最近CFTR调节疗法的发展[1].然而,尽管有这些显著的治疗成果,持续的气道重塑伴支气管扩张仍然是治疗进展性CF肺疾病的关键挑战,这一过程在APE期间得到增强。目前的研究是过去20年来针对CF APE的最大的介入临床试验之一[9,说明有必要在这一人群中进行额外的随机对照研究。肺加重是CF病程中的关键时期,与肺功能丧失、未来APE和死亡率具有很强的预测关系[2,5,6].我们的研究强调使用一种耐受性很好的药物,作为针对CF肺疾病中升高的蛋白酶活性的潜在益处的概念证明。
这两个研究队列在CF疾病的人口统计学和临床特征方面非常匹配。两个人群之间的一个显著差异是同时发病率的差异金黄色葡萄球菌定植,所有MRSA和MSSA定植的参与者都对脱氧土霉素敏感金黄色葡萄球菌通过体外测试。MRSA与较差的生存率有关[22],建议这可能是目前研究的重要困境。然而,随着MRSA的所有参与者用MRSA特异性治疗(LINEZOLID和VINCOMYCIN)治疗,由于毒素对MRSA的潜在影响似乎最小。此外,单变量分析没有证明肺功能变化与MRSA定植状态之间的关联。类似地,亚组分析下一次恶化的时间没有表现出与MRSA定植身份的差异。总的来说,这些研究结果强烈表明,十氧环素的有益结果与抗微生物效应无关金黄色葡萄球菌. 然而,未来的研究应包括MSSA和MRSA区块随机化以及基于金黄色葡萄球菌抗菌药物的敏感性。
我们之前的数据表明,在CF气道中MMP-9水平不成比例地增加(与循环水平相比),大多数痰中MMP-9处于活跃状态,APE期间作为前酶的很少[12].这些发现强调了系统用药必须达到足够的水平以在气道分泌物中检测到的重要性。最近的一项研究表明,每天200毫克口服强力霉素可使CF患者痰液中有一定浓度的强力霉素[23]能够中和MMP-9活性[24].
我们的结果清楚地表明,强力霉素治疗组在接受各种慢性护理药物(包括阿奇霉素,一种具有潜在抗炎活性的药物)的情况下,痰中MMP-9的中和作用[25].根据多西环素治疗人群中MMP-9水平和活性的变化,我们观察到痰液中TIMP-1和Ac-PGP水平均有改善。此前有报道称,在小鼠炎症模型中,多西环素可增加TIMP-1 [26但我们的研究首次在人类疾病中证明了这一点。这些结果表明,单一药物可能通过降低MMP-9负担和增加内源性TIMP-1水平来影响MMP-9/TIMP-1平衡的恢复。此外,Ac-PGP是CF肺疾病中与MMP-9活性直接相关的细胞外基质分解产物[27,28]因此,CF肺中MMP-9的减弱可能会影响气道重塑[29].
尽管强力霉素对MMP-9有强大的作用,但强力霉素并没有改变血清中CRP的水平或痰中炎症细胞因子的水平。虽然以前的文献使用体外和在活的有机体内模型显示强力霉素对炎症细胞因子表达有影响[30.,31,临床试验也未能观察到这些发现[32,33].循环MMP-9的变化在安慰剂组和强力霉素组之间也没有差异,可能反映了与肺室相比,全身MMP-9水平较低。
该研究显示强力霉素治疗组患者住院天数减少,尽管这一结果可能受到非临床因素的影响,如患者在家完成治疗的能力相对医院。也许这项研究中最令人鼓舞的发现是FEV的改善1多西环素组相对于安慰剂组和下一次恶化的时间变化。气流阻塞的相对改善程度强调了蛋白酶失衡在CF肺疾病中的重要性。FEV的改善程度1与安慰剂组相比,强力霉素组(约110 mL,预计FEV1%的绝对增加4.1%)与用于CF慢性管理的其他肺部治疗,包括多纳斯- α、高渗盐水、阿奇霉素[34- - - - - -36]最近,ivacaftor/lumacaftor在CF患者中的delta F508突变为纯合[37].尽管由于这些不同药物的研究设计的差异,很难得出相对疗效的结论,但它们为我们的结果的临床影响提供了背景。同样,强力霉素调节的蛋白酶-抗蛋白酶失衡的改善治疗可能正影响APE的分辨率,提供了一个更安静的恶化后基线,并延长了到后续恶化的时间。尽管我们的单中心研究跟踪了在我们机构接受治疗的CF患者群体,但未来的多中心试验将必须捕捉所有的恶化事件(包括CF中心以外的那些),以验证我们下一次恶化结果的时间。
考虑本研究有几个有限的局限性。虽然该研究具有相对大量的参与者,但它是一个单一的审判。此外,尽管通过调节气道中的缺乏测定蛋白酶活性很可能是介导的,但是可以通过其他潜在的生物效应来介导这些读出,例如气道粘膜的变化,肺细胞的变化在这个短处理窗口上的气道微生物组中的信号传导或改变。最后,我们没有评估寿命质量措施的改变,并在这项研究中得到了良好的问卷。无论如何,这些发现存在一项批判性研究,为多期式,随机,双盲,安慰剂对照试验提供了责任,该试验可以设计和供电,以检查这些额外的生物机制以及验证该单中心研究的结果。
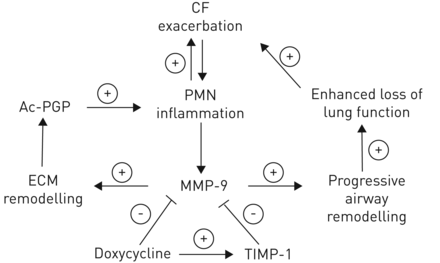
总之,我们的研究证明了MMP-9的中和作用、强力霉素的耐受性以及APE期间和之后有意义的临床改善(图6).这些结果,再加上良好的安全性、最小的经济负担和肺蛋白水解特征的改善,证明强力霉素作为一种治疗CF肺疾病APE的独特疗法的强大潜力。
强力霉素作为囊性纤维化(CF)加重期新辅助治疗的模型CF急性肺加重表现为细菌负荷增加和中性粒细胞炎症反应。基质金属蛋白酶(MMP)-9是由多形核(PMN)白细胞释放的,同时释放的还有其他蛋白酶,如中性粒细胞弹性蛋白酶。除了增加对肺实质的蛋白水解损伤外,调控异常的MMP-9活性还可以破坏细胞外基质(ECM),增强乙酰化脯氨酸-甘氨酸-脯氨酸(Ac-PGP),增加中性粒细胞流入气道。强力霉素通过降低MMP-9负荷和增加内源性TIMP-1水平,减轻气道重塑,改善临床结果(如1秒内的用力呼气量和延长下一次急性加重时间),对恢复MMP-9/金属蛋白酶组织抑制剂(TIMP)-1平衡有影响。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充方法erj - 01102 - 2016 - _supplement
图S1。血清中总MMP-9水平(a)、活性MMP-9水平(b)、TIMP-1水平(c)和总MMP-9/TIMP-1水平(d)的变化以治疗后和治疗前水平的差异表示,平均±SD;强力霉素组20例,安慰剂组18例。ERJ-01102-2016图1
图S2。强力霉素治疗不影响气道炎症标志物。痰中性粒细胞弹性酶(NE)采用ELISA定量(a)并标准化为总蛋白,强力霉素组为19例,安慰剂组为17例。定量测定血c反应蛋白变化(b),均值±SD;多西环素组16例,安慰剂组17例。面板(a)和(b)显示的数据是每个个体的读数(治疗前减去治疗后)的差异。ERJ-01102-2016_图_S2
图S3。强力霉素治疗并没有改变FVC和FEF (25-75%), MRSA也没有影响强力霉素治疗下一个加重期。每个个体的绝对FVC (a)、预测FVC百分比(b)和FEF 25-75% (c)在读出(治疗后减去治疗前)的差异中显示。多西环素组20例,安慰剂组19例。(平均数±标准差)。(d)多西环素治疗后,与无MRSA患者(实线)相比,MRSA患者下一次加重时间(点线)的Kaplan-Meier曲线与Log-rank检验。ERJ-01102-2016\u图\u S3
披露的信息
确认
作者要感谢George (Marty) Solomon和Steven Rowe在组织本手稿方面的帮助,感谢UAB的CF临床研究团队成员和Nathaniel Weathington在患者招募方面的指导。我们也要感谢Anuj Gaggar和Eric Sorscher对这份手稿的批判性阅读。最重要的是,作者想要感谢同意参加这项临床研究的患者。
作者贡献:概念和设计:徐星,G. Sabbatini, R. Quinn, J.E. Blalock, J.P. Clancy, A. Gaggar;分析与解释:徐旭,T. Abdalla, P.E. Bratcher, P.L. Jackson, J.M. Wells, X-Y。路;为重要的知识分子内容起草手稿:徐旭、徐旭。卢,j·e·巴洛克,j·p·克兰西,a·加格。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:这些研究部分由NIH资助(HL07783, HL090999和HL087824至J.E. Blalock;HL102371 to A. Gaggar;K08HL123940给J.M. Wells)、囊性纤维化基金会治疗(GAGGARA0给A. Gaggar)、退伍军人管理局(1 I01 BX001756给A. Gaggar)和Ismail Moustapha学者基金(A. Gaggar)。发表在本杂志上的这项研究得到了美国国立卫生研究院和家庭吸烟预防和烟草控制法案的支持。内容完全是作者的责任,并不一定代表国家卫生研究院或食品和药物管理局的官方观点。本文的资金信息已存入资助者打开注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
本研究注册于ClinicalTrials.gov标识号NCT01112059.
- 收到了2016年6月1日。
- 接受2016年12月19日。
- 版权©2017人队