抽象
前列腺素d2(PGD2)导致咳嗽和哮喘水平升高,表明它可能有助于症状。尽管前列腺素D2受体2(DP2)是知之甚少PGD的行动,众多的药物开发目标2对感觉神经和咳嗽。
我们使用人和豚鼠的生物测定,体内电生理和豚鼠有意识咳嗽模型评估前列腺素D的作用2受体(DP1),DP2和PGD血栓素受体拮抗剂2响应。
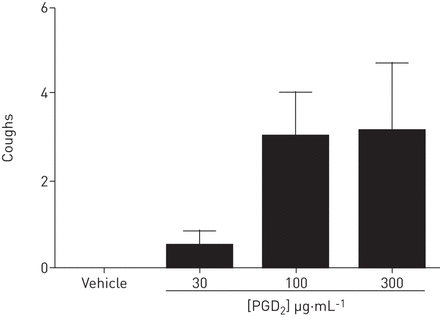
PGD2在清醒的豚鼠模型中引起咳嗽和气道颈静脉神经节钙的增加。利用药理学和受体缺陷小鼠,我们证明了DP1受体介导小鼠、豚鼠和人迷走神经传入的感觉神经激活。体内,PGD2和DP1受体激动剂,但不是DP2受体激动剂,激活单气道c纤维。有趣的是,DP的激活2抑制感觉神经射击辣椒素体外和体内。
该DP1受体可以是用于与哮喘有关的症状的治疗靶标。其中内源性PGD2水平升高,DP消失2感觉神经受体介导的抑制会导致增加迷走神经有关的症状,这种负面影响,应与DP临床研究进行调查2拮抗剂。
抽象
前列腺素d2激活感觉神经和经由DP唤起咳嗽1受体http://ow.ly/BR1kp
介绍
前列腺素d2(PGD2)是由肥大细胞产生的主要环氧合酶产物,与由其它细胞如T辅助(TH)2个细胞,肺泡巨噬细胞,树突状细胞和血小板[产生较低水平1- - - - - -4]。PGD水平的提高2哮喘[已发现5,6]及哮喘病人接受变应原刺激后[7,8]。PGD2对气道有许多影响,可能有助于哮喘的病理生理学,包括增加粘液的产生[9],血管舒张[10]和毛细血管通透性[11]。PGD的吸入2诱导正常人支气管收缩,这是患者更深刻哮喘[12,13]。最近PGD2已被证明具有对嗜酸性粒细胞,嗜碱性粒细胞和Th2淋巴细胞[趋化特性14]。
PGD2由花生四烯酸代谢通过环氧合酶途径产生的,然后通过PGD合酶。PGD2通过药理学上不同的G蛋白偶联受体(GPCR)来诱导其生物活性。最初,它的大部分作用被认为是前列腺素D的激活2受体(DP1)并且在血栓素(TP)受体高浓度的活性。然而,最近PGD2被确定为同源配体为孤儿GPCR(GPR44),其已被确定对炎性细胞。这种受体最初被命名为CRTH2(表达于Th2细胞趋化因子受体 - 同源分子),但现在被称为DP2受体与前列腺素类受体的命名法线[15]。近年来,人们对PGD的促炎作用进行了大量的研究2有证据表明PGD2,通过在DP2受体募集炎性细胞向气道[14]。与这些观察结果相一致的是,现在有几个DP2拮抗剂正在试用用于治疗哮喘和过敏性疾病[16]。
PGD2已在临床前研究及鼻腔刺激后的临床研究中显示会引致咳嗽[17,18]。此外,增加了PGD的水平2在哮喘患者的气道[发现5,7和慢性咳嗽[19],并且应当认识到,等过度咳嗽感觉神经相关的症状是哮喘表型的一部分。然而,没有人知道关于PGD的活动2关于气道感觉神经。我们第一次证明了PGD2在豚鼠中引起剂量相关的咳嗽,并激活单一的c纤维气道传入体内通过DP1受体激活。这一发现得到了人类、豚鼠和基因缺陷小鼠迷走神经组织药理学数据的支持,证实了DP的作用1受体,并建议在该受体拮抗剂可以是用于的症状的治疗有用,如哮喘患者咳嗽。已经发现,两个DP1和DP2我们进一步研究了DP受体对迷走神经活动的调节作用。有趣的是,我们发现DP的激活2受体实际上抑制迷走神经的活动。因此,在条件其中内源性PGD2水平升高,DP消失2感觉神经的受体介导的抑制可导致增加迷走神经有关的症状如咳嗽,因此应该与新颖DP临床研究进行研究2拮抗剂。
方法
动物
雄性C57BL/6和BALB/c小鼠(18-20 g)和Dunkin Hartley豚鼠(250-350 g)购自Harlan(比斯特,英国)。培育缺乏下列基因之一的老鼠对Ptgdr(DP1)GPR44(DP2)Tbxa2r(TP),TRPA1和TRPV1至少8次被反交叉到各自的背景上(DP1,TP,TRPA1和TRPV1在C57BL / 6背景;DP2在BALB/c背景上)。实验根据英国内政部项目许可证(PPL 70/7212)进行,实验程序严格遵守1986年《动物(科学程序)法》。
气道颈神经节细胞,对钙运动
豚鼠,气道特定,颈神经元标记,提取并如先前所述解离[21],并在网上补充材料。对于钙成像的细胞负载6μM的Fura-2乙酰氧基甲基酯(的Fura-2 AM)。细胞的生存力通过施加在实验的开始和结束的50mM钾溶液进行评估。PGD2(1μM)或辣椒素(0.1μM)施加70秒。对于抑制实验,抑制剂施加10分钟,在抑制剂的存在下激动剂重新施加。后的洗涤周期,所述激动剂被重新应用。细胞内钙变化记录并使用Image J(卫生,贝塞斯达,MD,USA的美国国立卫生研究院分析,http://imagej.nih.gov/ij/)。
在迷走神经节基因表达
豚鼠颈神经节的前一节和补充材料中描述的解剖。RNA提取和样品逆转录[23]。引物和探针豚鼠DP1和DP2受体由Applied Biosystems (Life Technologies Ltd, Paisley, UK)设计和生产。数据表示为2-Δct×106其中Δct表示目标的差异表达与18 s rRNA。
从单个c纤维传入体内记录
用氨基甲酸乙酯(1.5 g·kg)麻醉豚鼠−1)腹膜内使用维库溴铵的神经肌肉阻滞(0.10毫克·千克−1静脉内,接着每20分钟与0.05毫克·千克−1注射)。气管插管,肺通气。切断双侧迷走神经,用左侧迷走神经记录。对迷走神经进行戏弄,直到获得一个单独的活动单元,并如前所述记录动作电位[24]。控制基线记录2分钟后,辣椒素(100μM)是由气溶胶15年代和纤维的变化活动,气管内的压力和血压记录。在记录变量的同时,以10分钟为间隔喷雾激动剂60秒。在实验结束时,通过测定传导速度确认了c纤维的验证。所有的动物随后都被过量的戊巴比妥杀死。
体外迷走神经的准备
豚鼠,小鼠和人迷走神经解剖,置于Krebs-Henseleit溶液,并安装在一个“润滑脂隙”如先前所描述(进一步的细节可以在在线补充材料中找到)[记录室21]。使用激动剂2 min,然后使用Krebs-Henseleit溶液。在拮抗剂实验中,获得了两种可重复的激动剂反应。将拮抗剂或载体灌流10分钟,然后在拮抗剂存在并记录抑制程度的情况下,即刻再次使用激动剂2分钟。拮抗药物浓度为pA的100倍2值(拮抗剂亲和力的度量)。
化合物和材料
PGD2,前列腺素E2(PGE2),15 (R) 15-methyl-pgd2其中,BW245C、BWA868C、CAY10471、SQ29548购自开曼欧洲(爱沙尼亚塔林)。辣椒素和JNJ17203212购自Sigma-Aldrich (Poole UK)。HC-030031购自Chembridge(美国加州圣地亚哥)。所有的盐类都来自BDH (VWR国际有限公司,普尔,英国)和Sigma-Aldrich公司。关于准备解决方案的细节可以在网上的补充材料中找到。
数据分析和统计
数据以均数±表示扫描电镜和统计学显着性表示为p <0.05。配对t检验,Mann-Whitney U检验,Kruskal-Wallis检验和重复测量方差分析被用作适合于数据集和使用GraphPad Prism 5(格拉夫派得软件公司,拉霍亚,CA,USA)来计算。
结果
PGD的影响2气道颈神经节细胞
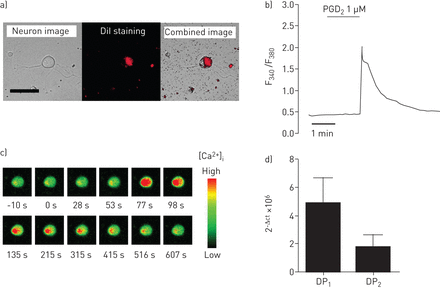
PGD2可激活初级气道特异性颈静脉神经节(即。根据细胞内钙含量的增加(图2 a - c)。实时荧光定量PCR分析表明,两者均具有良好的分离效果1和DP2受体存在于整个豚鼠颈静脉神经节(图。2D)。然而,表达数据对整个神经节进行,其结果应谨慎给予迷走神经节解释还含有微血管,神经胶质细胞和雪旺氏细胞,以及该项目遍布内脏神经元。因此,mRNA的来源可能不是神经元。
前列腺素d2(PGD2)在气道颈静脉神经节细胞中的反应。a)逆行标记(DiI)的存在表明细胞正在支配气道。酒吧= 50μm规模。b)对PGD的响应2表示为荧光的比值(F340/F380)。灰色条表示时的PGD2应用。c)如钙的变化,其描绘通过随着时间的推移细胞应答的快照。d)中的表达Ptgdr(DP1)和GPR44(DP2)在整个豚鼠颈神经节,数据表示为平均值±扫描电镜中,n = 8。
豚鼠体内单传入纤维记录
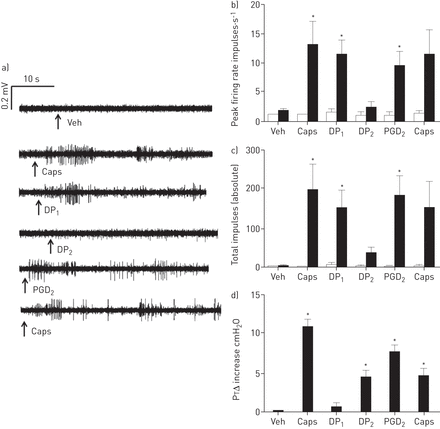
TRPV1激动剂吸入辣椒素被用于识别单一气道c纤维[24(图。3A)。可以通过响应性气溶胶化辣椒素及其传导速度C-纤维进行了表征。在此研究中使用的C-纤维具有平均值±扫描电镜的0.72±0.07米传导速度·s的−1(范围:0.6-0.85米·秒−1)。该DP1受体激动剂(BW245C)和PGD2引起了一阵射击,而DP2受体激动剂(15(R)-15-甲基PGD2)没有任何影响(图。3B和c)。有趣的是,PGD2和DP2受体激动剂(但不包括DP1受体激动剂诱导支气管收缩(图。3D)。利用豚鼠离体气管平滑肌我们证实,PGD2-诱导的收缩是由TP受体介导的(图S1)。在这个系统中,DP1受体激动剂对色调,而DP没有影响2受体激动剂引起的收缩,这是由TP(而不是抑制DP2)受体拮抗剂(图S1b和c)。
前列腺素d的效果2(PGD2)和前列腺素D2受体(DP)上气道单传入神经纤维激动剂体内。a)所述C-纤维烧制PBS(辆的以下雾化),辣椒素(CAPS)(100μM,15秒),BW245C的实施例的痕迹(DP1)(100年μg·毫升−1,60秒),15(R)-15-甲基PGD2(DP2)(100年μg·毫升−1, 60秒)或PGD2(100微克·毫升−1,60秒)。b)中每前(白色条)和之后(黑色条从单个迷走神经C-纤维记录的第二和c)的总脉冲)辣椒素雾化,BW245C,15(R)-15-甲基PGD脉冲的平均峰值频率2或PGD2。d)的支气管痉挛评估通过在气管压力的增加(PtΔ增加)。数据以均数±表示扫描电镜,n = 3。*:P <0.05。
初步数据还表明,PGD2和DP1激动剂可以唤起在机械性刺激感受器(中档,辣椒素敏感性Aδ纤维传导速度(CV)4.9米·s的动作电位放电−1;和辣椒素敏感性,古典迅速适应受体(RAR)CV14.7米·s的−1)。至少对民主党来说是这样1激动剂此不伴随支气管痉挛和在这两种情况下这个限制为辣椒素敏感的纤维,这表明这种情况通过辣椒素敏感性纤维的直接活化和通过在DP1受体/ TRPV1-TRPA1轴。
PGD2-诱导豚鼠和小鼠离体迷走神经去极化
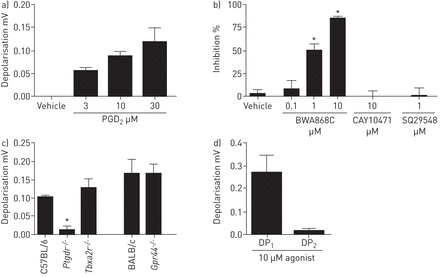
许多止咳剂[25,26]如辣椒辣素,低pH溶液和PGE2,目前已知的迷走神经感觉神经兴奋剂和豚鼠,小鼠和人类迷走神经分离制剂已被证明会引起类似的神经去极化反应跨物种对这些兴奋剂[20- - - - - -22]。这些数据表明,分离的迷走神经是用于进行可激活或抑制的感觉神经功能的剂全面药理评价的有用和预测准备,因此,咳嗽反射未被的药代动力学和其它考虑,限制的解释复杂化的体内学习。利用这个系统,我们发现,PGD2引起的浓度相关性增加在去极化在豚鼠分离的迷走神经(图。4A)。在豚鼠分离的迷走神经,BWA868C(DP1受体拮抗剂)抑制PGD2以浓度依赖性方式诱导的去极化(图。4B),但不是PGE2(类似的PG知激发感觉神经驱动响应22)(数据未显示)。此外,CAY10471 (DP)2受体拮抗剂)和SQ29548(TP受体拮抗剂)对响应于PGD没有影响2(图。4B)。此外,BW245C (DP1受体激动剂)在豚鼠迷走神经的去极化引起的,但15(R)-15-甲基PGD2(DP2受体激动剂)没有作用(图。4D)。从基因缺陷小鼠利用迷走神经组织证实了这些结果,我们发现,应对PGD2(10μM)在从所述迷走神经组织实际上被取消Ptgdr- / -(DP1受体缺陷)小鼠中,与野生型(C57BL / 6和BALB / c相比),GPR44- / -(DP2受体缺陷),Tbxa2r- / -(TP受体缺陷)小鼠(图。4C)。
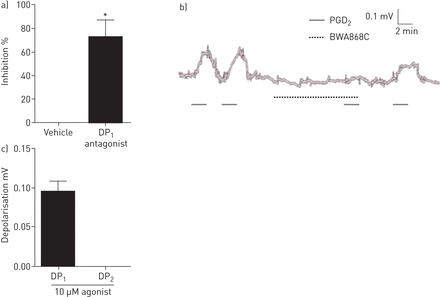
参与前列腺素d受体的鉴定2(PGD2-诱导豚鼠和小鼠离体迷走神经的激活。a) PGD的浓度反应2诱导去极化在离体豚鼠迷走神经。数据以均数±表示扫描电镜,n = 4。b)在豚鼠百分抑制率分离PGD的迷走神经2(10μM)通过载体(0.1%DMSO),前列腺素d2受体(DP1)(BWA868C)(0.1,1,10μM),10μMDP2受体拮抗剂(CAY10471)和1μM凝血恶烷受体拮抗剂(SQ29548)。数据以均数±表示扫描电镜中,n = 4-6。*:P <使用配对t检验拮抗剂之前和之后比较0.05响应。C)PGD的影响2(10μM)在前列腺素受体缺陷小鼠。在去极化神经分离的野生型C57BL / 6进行比较来Ptgdr- / -和Tbxa2r- / -小鼠和野生型BALB / c键GPR44- / -老鼠。数据以均数±表示扫描电镜中,n = 4-6。*:P <0.05在受体缺乏组织使用秩和检验或Mann-Whitney U检验相应的野生型比较的响应。d)在豚鼠选择性DP受体激动剂响应分离迷走神经。去极化到BW245C(DP1,10μM)和15 15-methyl-pgd (R)2(DP2,10μM)。数据以均数±表示扫描电镜,n = 4。
DP1受体介导的去极化诱发PGD2在人类迷走神经组织
该DP1受体拮抗剂BWA868C显著抑制PGD2全身的两极化的(图。5Ab)和DP1,但没有DP2受体激动剂,人类迷走引起去极化(图。5C)。BWA868C抑制作用的一个例子是在图5b。
参与前列腺素d受体的鉴定2(PGD2)人的诱导去极化分离迷走神经。一)PGD的百分抑制率2诱导人的(10μM)的去极化用载体(0.1%DMSO)或10μM前列腺素d分离迷走神经2受体(DP1)拮抗剂(BWA868C)。数据以均数±表示扫描电镜,n = 4 - 5。*: p<0.05,配对t检验。b)一个显示PGD抑制的例子2- BWA868C诱导的人迷走神经去极化。c)人离体迷走神经选择性DP激动剂的反应。两极化的10μM BW245C (DP)115-methyl-pgd)和10μM 15 (R)2(DP2)。数据以均数±表示扫描电镜,n = 3。
参与DP信号通路1受体介导的神经激活
该DP1受体是GPCR和很可能是在配体结合它调节参与受体后的信号传导途径来唤起去极化离子通道。TRPV1和TRPA1是已知的感觉神经中表达,并且这些激活被称为唤起咳嗽豚鼠意识咳嗽模型和人类离子通道[20,26]。去极化到PGD2在豚鼠分离的迷走神经由TRPV1(JNJ17203212)和TRPA1被部分抑制(HC030031)在浓度拮抗剂先前显示最大限度抑制TRPV1和TRPA1激动剂,分别(图。6A)21]。此外,在从分离的神经的响应TRPV1- / -和TRPA1- / -小鼠野生型相比被降低显著(图。6B)。这表明两个TRPV1和TRPA1的去极化通过PGD诱导作用2。
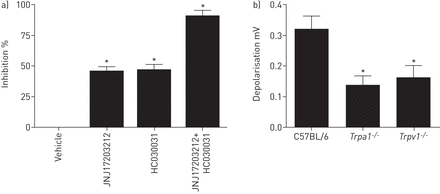
前列腺素D的受体后信号通路2(PGD2全身的神经两极化。a) PGD的抑制2通过TRPV1拮抗剂(100μMJNJ17203212)或TRPA1拮抗剂(10μMHC030031) - 诱导的豚鼠迷走神经的去极化。数据以均数±表示扫描电镜,n = 4。*: p<0.05,配对t检验。b)中的去极化幅度PGD2(10μM)在来自野生型C57BL / 6小鼠分离的迷走神经,TRPV1- / -要么TRPA1- / -老鼠。数据以均数±表示扫描电镜中,n = 6。*:P <0.05,Kruskal-Wallis检验。
在DP的作用2受体在迷走神经激活的调制
到目前为止给出的数据提供了强有力的证据表明PGD2激活气道感觉神经通过在DP1而不是DP2受体。然而,这两种受体在迷走神经颈神经节表示。虽然DP2受体不激活迷走神经,受体仍有可能调节感觉神经活动。利用豚鼠离体迷走神经和气道特异性颈神经节细胞,我们发现DP2受体激动剂抑制对感觉c纤维兴奋剂辣椒素的反应(图。7A这种效应转化为人的DP2激动剂在人类也抑制辣椒素诱导的去极化分离迷走神经(图。7C)。此外,利用豚鼠离体迷走神经,我们发现DP阻断了对辣椒素信号的抑制作用2受体拮抗剂(图。7D)。最后,我们已经说明了DP的抑制作用2接收器体内作为DP2受体激动剂显著降低辣椒素诱导的C-纤维传入单击发(图8)。
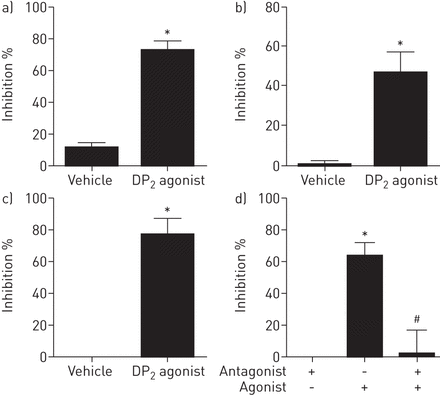
前列腺素d2受体2(DP2激动剂诱导的迷走神经激活抑制体外。a)用载体(0.1%乙醇)或15(R)-15-甲基前列腺素D抑制辣椒素诱导的去极化2(PGD2)(DP2激动剂,0.1μM)在分离的豚鼠迷走神经。数据以均数±表示扫描电镜,n = 4。b) 15(R)-15-甲基pgd对辣椒素诱导的气道颈静脉细胞钙离子运动的抑制作用2(DP2激动剂,0.01μM)。数据以均数±表示扫描电镜中,n = 5只豚鼠,由14个气道细胞车辆和17个的气道细胞DP的2激动剂。C)辣椒素诱导的去极化的抑制车辆(乙醇,0.1%)或15(R)-15-甲基PGD2(DP2受体激动剂,0.1μM)在人类孤立迷走神经的神经。数据以均数±表示扫描电镜,n = 3。d)15(R)-15-甲基PGD的拮抗作用2神经去极化的介导的抑制具有选择性DP2在分离的豚鼠迷走神经拮抗剂(CAY10471,10μM)。数据以均数±表示扫描电镜,n = 4。*:配对t检验激动剂效果p<0.05;#:P <0.05为拮抗剂通过非配对t检验的效果。
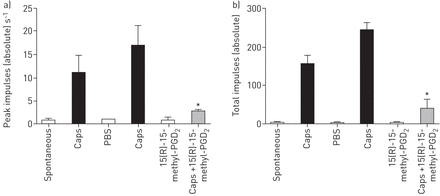
前列腺素d2受体2(DP2)激动剂诱导的抑制辣椒素诱导的气道单c纤维传入神经冲动体内。辣椒素(CAPS)中的溶液雾化入麻醉豚鼠的气道和从单个传入C纤维记录击发。PBS被雾化继之以第二辣椒素反应。10分钟,15(R)-15-甲基 - 前列腺素d后2(PGD2)(100年μg·毫升−1)给药,在45分钟10分钟,并再次后辣椒素重新应用。数据表达为每第二和b)的总脉冲A)峰的冲动。数据以均数±表示扫描电镜,n = 3。*:P <0.05在单向ANOVA重复测量试验前后15(R)-15-甲基PGD比较辣椒素的响应2。
讨论
PGD2从肥大细胞,Th2细胞和树突状细胞[释放1- - - - - -4],它是在气道哮喘增加的患者[5,6]和有强有力的证据表明,它可能在表征哮喘和过敏性鼻炎的过敏性炎症反应有关。支持这一论点的是数据,表明在该DP缺陷小鼠1受体不卵清蛋白诱导的哮喘模型开发的哮喘表型27]。此外,在过敏性气道炎症豚鼠模型中,选择性DP1受体拮抗剂,S-5751,减少抗原引起的鼻塞、结膜血浆渗出、炎性细胞浸润上呼吸道和下呼吸道[28]。前列腺素d受体基因(PTGDR)也已在哮喘表型暗示为在人受试者中连锁和关联分析[结果29],并报告具体的变种PTGDR启动子与哮喘相关[三十]。
PGD2也被认为有助于症状如咳嗽过度[17,18]。哮喘和非哮喘性嗜酸性支气管炎是慢性咳嗽最常见的原因。有趣的是,肥大细胞介质如组胺和PGD2非哮喘性嗜酸性支气管炎的痰中肥大细胞的激活是其特有的特征,肥大细胞介质可能是引起咳嗽的原因[31]。然而,我们的机制的理解参与PGD2诱导的咳嗽是有限的。PGD2激活DP1,DP2和TP受体,但尚不清楚哪种受体和受体后信号通路参与了气道感觉神经的激活和咳嗽反射。为了进一步研究这个问题,我们想确定一个合适的临床前模型系统。我们决定使用豚鼠,因为豚鼠常被用于研究气道感觉神经生物学,豚鼠对一系列的止咳药的反应与人类相似[20,21,26]。PGD2在有意识的豚鼠诱发咳嗽。这被证明是对由观察结果证实气道特定传入的效果PGD2诱发钙流入呼吸道具体颈细胞。此外,PGD2和选择性DP1受体激动剂,但不是DP2在受体激动剂,引起C-纤维击发体内电模型[32]。利用一系列的药理学工具和受体缺陷小鼠的迷走神经组织(虽然小鼠不咳嗽,但它们的迷走神经传入反应在许多情况下与豚鼠和人类相似和可比较),我们已经提供了重要的证据,表明PGD2诱导的感觉神经激活由DP介导1(而不是DP2或TP)受体。与DP一起研究TP受体1和DP2,虽然TP受体激动剂被认为不会引起咳嗽[33),因为PGD2已知通过TP受体介导气道平滑肌收缩[32,34这一发现在本研究中得到了证实。不能排除的一种可能性是PGD2诱导支气管收缩(通过TP激活可间接引起咳嗽通过机械敏感性维甲酸受体的激活。然而,DP的选择性激活1受体能唤起动作电位发放独立的支气管痉挛有利于理论的,它是呼吸道传入直接激活导致胚胎植入前诊断2诱发咳嗽。临床相关数据还介绍证实了上述调查结果和证明,首次为DP作用1受体激活通过PGD2在人类的迷走神经组织。
该DP1受体通常被认为是与G蛋白G结合的年代,提示DP的活化1受体将导致的cAMP [增加35,36]。然而,这是相对于我们以前的研究类似的生物系统,这表明cAMP的升高对气道感觉神经激活的抑制作用[37]。有趣的是,更符合这里显示的数据,细胞表达DP1受体也已显示以引起细胞内钙的增加在由PGD刺激2或选择性DP1激动剂BW245C [35]。此细胞内钙增加似乎是依赖于cAMP的,并可能导致从蛋白的活化激酶A(PKA)和Ca L型的随后参与2+通道和兰诺定受体[38]。GPCR偶联下游导致离子通道激活的机制尚不完全清楚,但磷脂酶C (PLC)和PKA通路被认为在许多TRP通道的信号转导中很重要[39- - - - - -41]。GPCR结合至G问- 偶联受体可导致PLC,磷脂酰肌醇的水解(4,5)-bisphosphate的激活(PIP2),得到肌醇(1,4,5)-trisphosphate(IP3.),二酰基甘油生产(DAG)和蛋白质的活化的激酶C(PKC)。PKC和DAG已经被发现直接绑定TRPV1受体和IP3.胞内钙库的释放诱导的可能参与TRPA1的活化。此外,PIP2被认为是组成型地抑制TRP受体。因此,它的水解通过PLC可以disinhibit这些离子通道,他们认识到随后的刺激[41]。另外,依赖pka的磷酸化可以通过G的激活发生年代-偶联受体,从而增强离子通道的兴奋性[41]。的TRPV1和TRPA1离子通道是已知的对气道感觉神经和激动剂待表达在这些受体导致咳嗽[20,21,25]。在本研究中,我们发现TRPV1和TRPA1都介导了下游对PGD的响应2以下DP1受体激活。TRPV1和TRPA1拮抗剂均可部分抑制PGD的去极化反应2。另外,在迷走神经从组织TRPV1- / -和TRPA1- / -小鼠中响应于PGD2显著降低。这些通道也与PGE诱发的咳嗽有关2演戏通过的前列腺素E受体3 [22]。
整个机身,DP1受体是要么不可检测或以低水平组织中表达[35,36,而DP2受体广泛分布[42]。在豚鼠迷走神经节中,我们同时检测到了DP1和DP2mRNA的表达。然而,整个迷走神经节还含有其他细胞类型,包括施万细胞,胶质细胞和微血管以及神经元的项目到内脏等这些样品中DP受体识别并没有提供确凿的证据。因此,在本研究中,我们已经阐明功能的DP1受体激活气道感觉神经和诱发反射事件,如咳嗽。然而,选择性DP2受体激动剂没有引起去极化和一个DP2拮抗剂对PGD无明显抑制作用2。除能引起去极化剂外,还能使神经对其他刺激物的作用变得敏感[43,44或抑制神经活动[37]。我们进一步研究发现,一个DP2受体激动剂抑制辣椒素诱导的气道神经节颈细胞的活化,并从两个豚鼠和人分离的迷走神经,并且这种作用可被一个DP2受体拮抗剂。此外,这是证实了体内在单纤维记录模型中,辣椒素诱导的动作电位放电在给药后降低2受体激动剂。事实上,适度的咳嗽反应诱发的PGD2在这项研究和有趣的观察是DP2受体的激活可能抑制c纤维的排出,提示DP2受体拮抗剂可增强PGD诱发的咳嗽反应2。因为发现DP2受体拮抗剂可抑制由过敏原引起的炎症反应近年来,哮喘领域的药物发现一直是人们关注的焦点,临床试验中出现了几种化合物[16]。然而,这个数据将表明应谨慎制定DP时,应小心2拮抗剂用于治疗哮喘,作为防止DP2受体激活(特别是内源性PGD2生产是高是可能的过敏性疾病)可能是有害的,并导致气道反射的不适当的刺激。
总之,有强有力的证据表明肥大细胞介质如PGD2可能参与与表征哮喘和过敏性鼻炎的过敏性炎症反应相关的症状。也有证据表明,这涉及到,至少部分,DP1受体激活。然而,尽管哮喘的遗传相关性研究,临床前研究的数据,鼓励使用药物干预和DP1受体在哮喘模型中,DP基因敲除小鼠1受体拮抗剂却令人失望,在临床研究目前尚未用于治疗。特别是,DP1在1秒拮抗剂拉罗匹仑曾在过敏性鼻炎患者和哮喘没有功效被迫其中呼气容积是主要的终点〔45]。我们在这里提出的证据表明PGD2激活气道感觉神经唤起咳嗽,并提供明确的证据DP的参与1气道反射事件中的受体。这些数据表明,在专门针对症状进行的临床试验中,应利用客观咳嗽测量等新的临床工具重新审视这一目标[46,47]。
确认
Ptgdr- / -,Tbxa2r- / -小鼠承蒙Shuh Narumiya(京都大学,日本)和丸山隆行(ONO制药,日本大阪)提供。GPR44- / -小鼠承蒙平井裕之(BML公司,日本东京)和中村正孝(东京医科齿科大学,东京,日本)提供。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
支持声明:S.A.马赫和M.S.格雷斯是由医学研究理事会(MRC,UK)项目的资助(G0800195; MR / K020293 / 1)。S.J.Bonvini和文学硕士沃特利分别支持国家心肺研究所信托MRC助学金。E.D.爵是由威康信托项目赠款(089301 / Z / 09 / Z)和勃林格殷格翰资助。在这项研究中人体组织的实验与在皇家布朗普顿和哈尔菲尔德NHS信托基金会和英国伦敦帝国学院的支持下,NIHR呼吸系统疾病的生物医学研究单位开展了。
利益冲突:披露能够随本文的在线版本中找到www.qdcxjkg.com
- 收到2014年4月1日。
- 接受2014年8月26号。
- 版权所有©ERS 2015年