摘要
我们的目的是研究吸烟习惯和环境烟草烟雾(ETS)暴露与支气管高反应性(BHR)的关系。
随机抽取292名成人,采用结构化访谈、肺活量测定、皮肤点刺试验、呼出一氧化氮含量(Feno.)支气管组胺激发。
BHR的大多数受试者都是吸烟者或出吸烟者。在20岁之前开始吸烟与BHR显着相关,因为目前的吸烟,吸烟量和ETS暴露会如此。随着含量的暴露量增加(P <0.001),BHR的严重程度显着增加(P <0.001)。目前肺功能下降的吸烟者特别高的BHR风险。无论年龄大小,1 s中的强制呼气量有损到期呼气量和平均最大呼气流量是更严重的BHR的独立决定因素。在多变量分析中,吸烟仍然是BHR后的独立决定因子,后肺功能和其他协变量的调整后:≥15包 - 多年的比率为3.00(95%CI 1.33-6.76)。BHR和B之间的关联Feno.依赖于吸烟习惯。
结果表明,吸烟是BHR的显着风险因素,具有剂量依赖性模式,并且BHR的严重程度随着包装的增加而增加。调查结果强烈建议对受试者的吸烟习惯进行评估。
摘要
支气管高反应性与吸烟呈剂量依赖关系;严重程度随包装年限的增加而增加http:///wly/pad0h.
介绍
吸烟会导致慢性气道阻塞,主要由周围气道向大气道逐渐发展[1那2]. 大规模的国际研究表明,吸烟是支气管高反应性(BHR)的危险因素[3.-5.]但是吸烟曝光的数量是否与BHR的严重程度相关联。尚未详细探讨作为BHR严重程度可能的独立触发因素的剂量依赖的吸烟和小气道阻塞。
只有少数最近的流行病学研究评估了BHR的各种可能决定因素[6.那7.].BHR的大多数流行病学研究是描述性的,并报告了它们的BHR结果作为剂量反应坡或剂量 - 反应率[8.]. 将这些BHR指标转化为临床实践是一项艰巨的工作,因此它们仅用于研究[5.那7.]. BHR测试是诊断哮喘的常用工具,但在解释BHR的原因时,吸烟的影响尚不清楚[9.]. BHR与吸烟的关系主要在特定人群中进行研究[10-12].
我们的目的是研究吸烟、环境烟草烟雾(ETS)暴露和呼出的一氧化氮含量(Feno.)在芬兰首都赫尔辛基的成人受试者中的BHR。通过与组胺的剂量方法评估支气管反应性[13],在芬兰临床使用已超过三十年。吸烟暴露量对BHR严重程度的影响,定义为组胺的激发剂量导致1s内用力呼气量减少15%(FEV1)在两个临床验证的截止级别(PD151.6毫克和0.4毫克[13]),通过多元回归分析计算。在计算当前吸烟状态的影响时,PACK-yoct和BHR上的ETS,通气功能和小气道阻塞的变量被用作共变量。
对象和方法
研究队列
该研究样本由292名随机选择的受试者组成,他于1996年在赫尔辛基举行邮政调查问卷调查[14]. FinEsS I邮政调查的人口(n=8000)是从芬兰人口登记册中随机选择的,旨在与一般人口的年龄和性别相对应。FinEsS I研究的参与率为76%(n=6062)。在参与者中,1200人被随机邀请参加FinEsS II临床研究,其中一半(n=600)被随机选择参加BHR研究。FinEsS II临床研究的参与率为54%(n=643)[15而BHR研究的45.4% (n = 292)。
此BHR研究样本代表了1996年的原始研究队列,哮喘,呼吸系统症状和吸烟习惯的年龄,性和患病率[15].年龄范围为26-66岁(平均47岁),58%是女性。基线fev.1研究的受试者的范围从预测的芬兰参考值的60%到136%16].赫尔辛基大学中央医院道德委员会批准了这项研究,所有科目都签署了知情同意。人口统计数据呈现表1和2。
临床检查
BHR挑战测试在初步临床访问的2周内进行,包括结构化面试,肺动料试验和皮肤刺测试(SPTS)[17]. 访谈由一名医生进行,一名训练有素的护士进行肺活量测定和SPT。对年龄<61岁的受试者和两个对照组(阳性对照组:组胺10mg·mL)进行SPT-1;阴性对照:甘油溶剂)和15例过敏原[15]. 访谈内容包括呼吸系统症状、哮喘和过敏家族史、生活条件、职业、吸烟习惯和ETS暴露等问题。
BHR试验
BHR试验的纳入标准为试验前FEV1≥60%的值预测或≥1.5升,在测试前4周内没有呼吸道感染,没有明显的心脏病(3个月内心肌梗塞,不稳定的冠状动脉疾病,功能障碍或心律失常),没有中风。允许受试者使用其正规用药,除β外2-激动剂和抗组胺药物(检测前12小时不使用短效β激动剂,48小时不使用长效β激动剂,5天不使用抗组胺药物)。18名受试者因FEV基线较低而被排除1。
通过使用Spira Electro 2喷射雾化器(芬兰Hämeenlinna Spira呼吸护理中心有限公司),通过控制潮气呼吸的剂量学方法,使用组胺进行支气管激发[13]. 受试者吸入缓冲二磷酸组胺气雾剂的剂量增加四倍。终点是一场失败≥含铁量为15%1或使用的最大非升压剂量为1.6mg。组胺挑战后,支气管后核糖(0.4毫克Salbutamol(Ventoline,Glaxosmithkline,Brentford,英国)通过Volumatic®(英国伦敦葛兰素史克公司))钒铁1被测量了。PD.15由内插计算[18].
根据1994年美国胸部社会(ATS)的标准,使用VMAX22肺活量计(Sensormedics,Yorba Linda,CA)进行流量肺活量测定量。19].我们录制了最大的FEV1以及至少三条可接受曲线的用力肺活量(FVC)和流量参数,如50%FVC时的平均最大呼气流量(MEF50.),由FEV之和最大的曲线得出1和FVC。组胺试验后测量支气管舒张反应。所有肺活量检查均使用鼻夹。在95%的受试者中Feno.在50 mL·s下测量-1流量符合1999年ATS标准[20.].的Feno.在BHR测试前进行测量。
统计分析
与BHR相关的BHR严重程度,危险因素和症状在PD的两个不同截止水平下确定15. 通过多元logistic回归分析计算BHR的危险因素,包括独立变量年龄、性别、哮喘家族史和单变量分析中显著的决定因素。在分析中,使用了年龄(47岁)和包装年份(8.5岁)的平均值。结果以优势比(95%CI)表示。卡方检验和Fisher精确检验用于评估各组之间的差异。此外,p<0.05被认为具有统计学意义。对年龄小于45岁的个体重复分析≥45岁,将吸烟暴露的影响定义为两个年龄组测量的BHR的潜在起始。
社会科学统计包(Windows的SPSS版本15.0; IBM,Chicago,IL,USA)和STATACT 8_2007(Cytel Inc.,Cambridge,Ma,USA)用于统计分析。
结果
抽烟
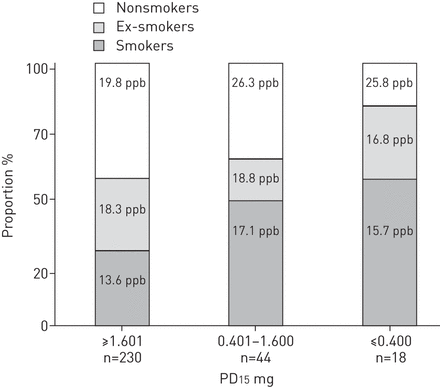
吸烟增加患BHR的风险(表2.). BHR严重程度与包装年数的增加平行增加(p<0.001)(图1)。标记为BHR的受试者,56%是吸烟者和28%的射击者相对28%的吸烟者和27%的免疫吸烟者,没有BHR。在20岁时(n = 129)之前的吸烟开始产生4.03(95%CI 1.11-14.67)的赔率比为标记的BHR,并且在15年前开始吸烟的相应值为5.38(95%CI 1.14-25.37),非闻名者作为参考。在26岁后,没有人开始吸烟,标志着BHR。
支气管高光反应性(BHR)的严重程度和吸烟历史(包装历史)。BHR根据诱导的组胺的挑衅剂量分类,诱导15%在1 s中的强制呼气量下降(PD)15) [13] AS:NO BHR(> 1.6mg),温和(0.401-1.6mg),中等(0.101-0.4mg)和赫尔辛基成年人一般人群样品中的温和(≤0.1mg)(n = 292)。p值代表趋势的测试。***:P <0.001。
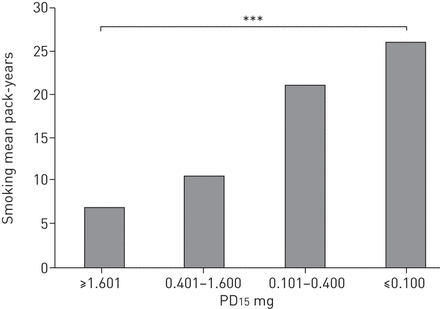
Pack-yoct与BHR和标记的BHR的关联在仅1+包(或1.91,95%CI 1.05-3.49和4.07,95%CI 1.15-14.39)中变得显着。≥8.5包的吸烟历史为BHR和5.99(95%CI 1.67-21.45)的2.65(95%CI 1.40-5.00)的差距为2.65(95%CI 1.67-21.45)。患有> 15包的吸烟历史导致标记为BHR的差距为8.00(95%CI 2.17-29.45),并与梗阻相结合,为12.85(95%CI 3.36-49.09)。目前的吸烟者具有损坏的通气功能被定义为FEV1小于80%pred,FEV1/FVC <0.7和MEF50.<63%的pred,BHR(分别为10.17,8.37和6.85的风险很高)(表4.)。
在多变量分析中,吸烟仍然是BHR的独立决定因素,并且当协同变化时,包括肺功量受损的肺功能和在单变量分析中具有重要的BHR的其他决定因素时(表5.). 在调整年龄、女性性别、儿童期喘息或哮喘、FEV后,吸烟>15包年仍与BHR和显著BHR显著相关1<80%pred和mef50.<63%pred(表4.). 在多变量分析中,除了通气功能变量外,儿童期哮喘或喘息也是BHR的重要危险因素。
环境烟草烟雾
标记为BHR的受试者,33%报告的ETS在研究时暴露相对17%的人没有BHR。家庭和工作中的ETS与标记的BHR相关(OR 3.73,95%可信区间1.05–13.17和OR 4.65,95%可信区间1.32–16.42)。然而,仅非吸烟者接触烟草烟雾与BHR无显著相关性。
通气功能
低基线FEV1值与低PD相关联15值(P <0.001)。
基线FEV1<80%pred与阻塞一起(FEV1/FVC <0.7)增加了BHR的风险,比值比为5.73 (95% CI 1.75-18.73) (表4.). 在肺功能变量的单变量分析中,MEF50.低于正常下限(LLN)是BHR和标记BHR的强决定因素。当MEF50.
Feno.与BHR相关
之间的联系Feno.BHR强烈依赖于吸烟习惯(图2). 在不吸烟的BHR患者中,Feno.与剩余的受试者相比,> 25ppb和明显更高(p = 0.008)。电流暴露于ETS与较低的相关联Feno.(13.2 ppb)与非缺乏受试者(19.3 ppb)(p = 0.002)。
具有平均呼出一氧化氮分数的吸烟类别(Feno.),按支气管高反应性(BHR)的严重程度分组[13](无(激发剂量导致1s内用力呼气量下降15%(PD15) ≥1.601毫克),轻度(PD150.401-1.600 mg),并标记(PD15≤0.400mg))在芬兰赫尔辛基的成年人口样本中。非闻人:意思Feno.20.8 PPB;出吸烟者:意思Feno.18.3 ppb;吸烟者:我的意思是Feno.十亿分之14.6。n = 292。p值表示对趋势的检验。均值±sdFeno.是18.1±13.47 ppb(范围2.13-95.60 ppb)。p = 0.004。
年龄的影响
用BHR吸烟协会在两年龄段中检查:那些<45岁(第1组:平均36岁; N = 126)和≥45岁(第2组:平均年龄54岁; n =166)。BHR的患病率在1和2组之间没有区别(19.8%)相对分别为22.3%),而标记BHR在第2组中更为常见(4.8%相对7.2%). 第一组包括更多的非吸烟者(46.8%)相对37.3%)和包数量低于2组(平均5.6相对10.8)。具有障碍物被定义为FEV的受试者的比例1/ FVC <88%的pred在1和2组中相同(30.4%相对分别为30.1%)但障碍被定义为FEV1/FVC<0.7在第2组更常见(1.6%)相对第1组和第2组分别为12.0%)。
在第1组,吸烟和LLN的FEV1与BHR(或1.78,95%CI 0.68-4.46和或1.93,95%CI 0.54-6.86分别没有显着相关),但这两种因素都增加了第2组(或3.55,95%CI 1.42中BHR的风险-8.91和11.10,95%CI 3.84-32.10)。在多变量分析中,BHR的年龄调整后的决定簇与模型中没有年龄的分析没有不同的分析(表4和5.)。肺功能参数,MEF50.<63%的性能提高了风险,无论年龄较小如何1.20-9.55)和13.60(95%CI 1.88-98.23)。
讨论
在这项研究中,我们在普通人群的成人样本中发现了吸烟与BHR严重程度的剂量依赖性关联。目前的研究表明,增加吸烟暴露(以包年定义)与更严重的BHR相关。即使在调整肺功能降低(FEV)对BHR的影响后,这种相关性仍然显著1),气道阻塞和基线外围气流限制。在多变量模型中,儿童和女性性别哮喘或喘息的历史也是BHR的独立决定因素。
一般来说,危险因素在≥45岁的主题中最强烈相关,而在<45年龄与BHR的重要协会中,稀释了,除MEF外50.<63%pred。
我们发现,目前的大多数吸烟者已经开始在15-19岁时吸烟。开始吸烟7 - 20年增加了BHR的风险增加了标记的BHR四倍的风险。在7-14岁时开始吸烟,年龄在7-14岁,在成年多于五倍以上的已标记BHR的风险增加。通过包装的曝光对吸烟曝光的分类显示比当前吸烟状况的一般条款更重要的关联,IE。非吸烟者或目前的吸烟者。没有研究暴露于烟草烟雾的急性效应。
我们的结果表明,ETS暴露和吸烟干扰Feno.在一般人群中检测气道炎症的价值,类似于n的结果adif.等等。[22]. 吸烟暴露在评估健康方面起着不可估量的作用Feno.这可能解释了先前关于BHR与其他气道调节和炎症测量方法之间关系的研究中发现的一些矛盾结果[23那24].不进行暴露于烟雾烟雾的生物测量,这导致ETS暴露的稍微不完全定量。
参与BHR研究的纳入标准对最终结果产生了影响。在这一普遍的人口队列中,BHR的患病率为21%,严重或中等BHR的患者构成了6%的研究[17]后者的结果与芬兰成人哮喘患病率的最新数据相当一致[14那15].
然而,在我们的研究中,与所有BHR研究一样,一些最严重的患者由于基线FEV较低而被排除在外1价值因此,在计算BHR增加的危险因素或决定因素时,不能考虑严重降低的通气功能。气道口径大小效应假说和性别差异都是BHR的重要决定因素[25],如多变量模型所示。流行病学研究中BHR测试和结果比较的方法学考虑缺乏这一部分的批判性评估[26]. 在大多数BHR研究中,只有肺功能预测值用于评估危险因素。这可能排除了通气储备减少对BHR的最终影响,尤其是在老年受试者中。
作为周围气道阻塞的替代变量,我们使用MEF50.从基线肺活量测定法调查流动限制典型的吸烟史作用。众所周知,措施的可重复性和可靠性越来越少于FEV1[27].但是,在我们的研究队列中,已经评估了肌肌测量测量的质量和代表性[28],平均fev1本研究样本中预测值的FVC符合电流芬兰参考值。
我们发现MEF受损50.与BHR密切相关。此外,在调整MEF后,>15包年吸烟作为BHR的独立危险因素保持稳定50.和FEV.1
<45岁和≥45年的个体分析结果表明,暴露于烟草烟雾是中年后BHR的潜在成立。在终身暴露之后出现病理定义的BHR,例如烟草烟雾曝光。这符合从较大流行病学BHR研究中获得的结果,其中已经提出由烟草引起的重塑变化导致纵向设置中增加的BHR [7.].据报道范书B.erge等等。[12],炎性细胞的关键作用,例如中性粒细胞,巨噬细胞和淋巴细胞,以及与BHR相关的空气俘获用作慢性气道疾病表型的表型。在戒烟后,前瞻性研究表明哮喘吸烟者中的BHR显着降低;因此,吸烟者应该有助于戒烟[10那11].
目前一般人群研究的局限性是显而易见的,因为样本量略少于300名受试者。然而,我们可以在选定的患者群体中显示出类似的BHR与吸烟的相关性,如哮喘患者、过敏患者和慢性阻塞性肺疾病患者[10-12那31].
目前的研究是在2006年之前进行的,当时芬兰禁止在公共场所和餐馆吸烟。随着公共场所禁烟,芬兰的吸烟习惯也开始减少。32].呼吸症状和肺功能紊乱的患病率降低可能是吸烟减少的结果,如戒烟后哮喘吸烟者的前瞻性研究中发现[10那11那31那33].
总之,即使在纠正了肺功能受损、女性和儿童哮喘或喘息史的影响后,吸烟和BHR仍具有剂量依赖性。BHR的严重程度随着包年的增加而增加,并且在20岁之前开始吸烟的显著BHR的风险超过4倍,因此表明吸烟暴露是中老年BHR的触发因素。MEF低50.作为一种单一的肺活量测量,呈现了BHR的最高比率比,表明使用BHR的气流限制受损的显着关联。吸烟和ETS曝光混淆了协会Feno.和BHR。我们的结果支持在工作和家庭中采取禁烟行动和立法限制ETS暴露。评估BHR患者的吸烟习惯很重要。
致谢
特别感谢研究助理K. Ahlskog和M. Veneranta, I. Sippo-Tujunen就技术问题提供的咨询和支持,肺功能和临床生理学实验室的工作人员,以及赫尔辛基大学医院Meilahti医院肺病研究中心的工作人员。
脚注
支持声明:这部分款项研究得到了支持赫尔辛基大学医院(项目TYH1235),芬兰肺病的IDA MONTIN基金会基金会和研究基金会的补助金。
利益冲突:没有宣布。
- 收到2012年5月8日。
- 公认2013年4月18日。
- ©ERS 2013