文摘
唐氏综合症儿童高危急性呼吸窘迫综合征。在唐氏综合症,调节炎症和细胞凋亡,重要的急性呼吸窘迫综合征病理生理学,是不正常的。这是与自由基拾荒者的不平衡。我们调查的表达自由激进的食腐动物和氧化应激的影响在呼吸道上皮细胞凋亡和炎症方面从唐氏综合症儿童与对照组相比。
我们从唐氏综合症儿童培养初级鼻上皮细胞(n = 12)和控制(n = 17),然后把它们暴露于氧化应激通过补充超氧化物。
首先我们表明,自由基拾荒者的表达CuZn-superoxide歧化酶高出28% (p = 0.06),过氧化氢酶降低了36% (p = 0.04),谷胱甘肽过氧化物酶降低了73% (p = 0.004)在唐氏综合症儿童与控制。我们发现在细胞凋亡没有显著差异,唐氏综合症和对照组之间在暴露于氧化应激。我们也没有发现显著差异水平的白介素(IL) 1β,IL - 6,引发、血管内皮生长因子和粒细胞集落刺激因子在初级鼻上皮细胞暴露于氧化应激后上层清液唐氏综合症和对照组之间。
我们发现了一个不平衡在呼吸道上皮细胞的自由基拾荒者从唐氏综合症的孩子,但这并没有导致增加水平的细胞凋亡或暴露于氧化应激炎症。
文摘
自由基清除剂不平衡:呼吸道细胞凋亡或炎症不增加唐氏综合症的孩子http://ow.ly/mxypE
介绍
急性呼吸窘迫综合征(ARDS)是一种严重危及生命的肺部疾病的一个主要挑战现代重症监护医学(1]。在ARDS,肺泡上皮和内皮细胞障碍的渗透率增加,由于炎症和细胞凋亡2]。这将导致严重的低氧血和呼吸衰竭。2012年,国际共识定义ARDS已经更新(3]。术语的急性肺损伤轻微ARDS现在过时了,因此我们只指在这个手稿ARDS。肺和肺外触发,例如肺炎和愿望或脓毒症和创伤,可以诱导ARDS。病人的特点,如慢性疾病或遗传结构的存在,可以调节发展ARDS的风险4]。
我们最近发现唐氏综合症儿童有显著的风险增加发展中ARDS [5]。在唐氏综合症,调节炎症和细胞凋亡异常,导致传染病的风险增加和阿尔茨海默病(6,7]。ARDS的风险增加唐氏综合症是否与炎症和细胞凋亡的异常调节呼吸道上皮细胞并没有被调查。
在唐氏综合症,它已经表明,一些细胞类型,如神经元和粒细胞增加内在的细胞凋亡水平与高氧化应激(8,9]。这种氧化应激增加已经导致了过度的CuZn-superoxide歧化酶(SOD1),胞质自由氧游离基清除剂,是21号染色体上编码。SOD1降低过氧化氢过氧化物(H2O2),它可以转化为过氧化氢酶、谷胱甘肽过氧化物酶(GPX)水。SOD1的失衡和H2O2减少酶可能导致积累H2O2和羟基自由基。这增加氧化应激和通过增加炎症和细胞凋亡可能是有害的。这种不平衡已被证明在唐氏综合症中性粒细胞,红细胞和唐氏综合症胎儿大脑皮层(10- - - - - -12]。SOD1的表达和H2O2减少酶和氧化应激的反应尚未进行唐氏综合症呼吸道上皮细胞。
我们假定,自由基拾荒者的不平衡会导致增加氧化应激导致呼吸道上皮细胞的凋亡和炎症水平增加,可能导致ARDS的风险增加孩子患有唐氏综合症。在这项研究中,我们使用鼻上皮细胞为肺泡上皮细胞模型。这个模型使用过另一种为下呼吸道上皮细胞,原因很明显,很难获得。有证据表明,炎症的刺激的反应是类似于鼻和降低气道上皮细胞(13]。
如果我们能显示增加易受氧化stress-driven损伤呼吸道上皮细胞从孩子患有唐氏综合症,可能有抗氧化剂治疗的作用为防止发展为ARDS的生命垂危的孩子患有唐氏综合症。这可能会降低发病率在这些儿童和可能提供线索的重要性氧化应激在ARDS一般儿科人口的发展。
本研究的目的是调查在一个在体外设置容易氧化stress-driven受伤唐氏综合症患儿的呼吸道上皮细胞凋亡和炎症,并链接到一个潜在的失衡在唐氏综合症的自由基拾荒者与对照组相比。
材料和方法
采样和培养初级鼻呼吸道上皮细胞
主鼻上皮细胞(PNECs)获得来自患有唐氏综合症的孩子参观了门诊或日托中心的艾玛儿童医院/学术医学中心(AMC)(阿姆斯特丹,荷兰)nonpulmonary紊乱。儿童与正常染色体组型作为控制。患儿并发呼吸道感染被排除在外。
细胞学刷(Cytobrush +;介绍了美国——贝瑟尔CooperSurgical,特兰伯尔——,CT) 1 - 2厘米到鼻子和旋转沿鼻腔。这些细胞被培养在环境空气的37°C,补充5%的二氧化碳,BEGM-Bulletkit支气管上皮中(Cambrex合作,东卢瑟福,新泽西,美国)(图1)。细节在网上所描述的补充材料。∼2周后培养1 - 2通道,PNECs被用于实验的confluency∼90%。
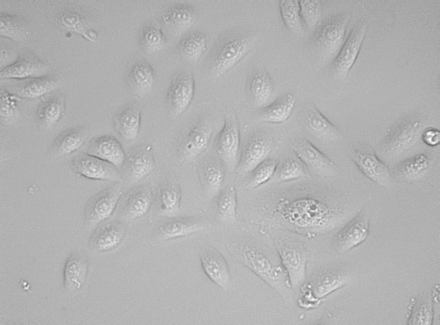
原发性鼻上皮细胞单层培养。
蛋白表达
SOD1,过氧化氢酶GPX表达测量在sds - page分离蛋白免疫印迹紧随其后。细节在网上所描述的补充材料。加载的变化被相关肌动蛋白或tubulin-content正常化。绑定主要抗体被IRDye视觉效果(美国东北LI-COR生物科学,林肯)共轭二次抗体。量化是由红外荧光检测使用的奥德赛成像仪和软件(LI-COR生物科学)。
接触氧化应激
两种方法诱导氧化应激在PNEC文化。分析细胞凋亡在氧化应激,PNECs受到3 h为0 - 0.2 - 0.5毫米黄嘌呤及黄嘌呤氧化酶0-16-40μ·毫升−1(Sigma-Aldrich,圣路易斯,密苏里州,美国)生成外源性超氧化物(14]。接触的PNECs随后被分离胰蛋白酶/ EDTA 5 - 10分钟(Lonza、巴塞尔、瑞士)。细胞悬液立即用于流式细胞术。
细胞因子反应是检测不到3 h后暴露于黄嘌呤/黄嘌呤氧化酶,此时已经停止生产超氧化物。因此,我们使用了一个替代方法来产生超氧化物的检测对氧化应激炎症反应。PNECs暴露了24 h 0-6-25-100μM羰基氰化物m-chlorophenyl腙(CCCP Sigma-Aldrich)生成内源性过氧化物(15]。浮在表面的删除和存储在-80°C。细胞内氧化应激测量通过测量2 ',7 ' -dichlorodihydrofluorescein二乙酸(DCFDA)荧光。细节在网上所描述的补充材料。
检测细胞凋亡
细胞凋亡和细胞死亡后接触黄嘌呤及黄嘌呤氧化酶通过流式细胞仪测定。这些细胞被孵化与APC-labelled annexin-V(美国表达载体,卡尔斯巴德,CA)和propidium碘(Sigma-Aldrich)。的FACSCanto流式细胞分析仪(BD生物科学,富兰克林湖,新泽西,美国)和FlowJo软件(树星公司,亚什兰,或者美国)被用于分析。
炎症反应
上层清液中细胞因子,趋化因子,生长因子含量经过24小时的接触挺多路复用荧光珠试验测定的白介素(IL) 1β,IL - 6,引发、血管内皮生长因子和粒细胞集落刺激因子(进一步被称为“细胞因子”)(Luminex;研发系统,明尼阿波利斯,美国)。这些细胞因子选择基于两步选择过程。首先,我们进行了文献检索识别表达的细胞因子在不同水平与对照组相比,唐氏综合症。其次,在研究中,我们使用一个30-plex小组,调查哪些细胞因子表达在人类细胞因子PNEC上层清液。
细胞损伤的标志,乳酸脱氢酶活性测定采用比色测定来确定NADH生产(8000年Cobas,罗氏诊断,曼海姆,德国)。
统计分析
比例的患者团体使用双面确切概率法进行了比较。对于正态分布数据,t是用来比较的意思。不是正态分布数据,Mann-Whitney U-tests被用来比较中位数。重复措施的分析,数据的对数转换获得正常,允许一般线性重复度量模型。斯皮尔曼相关系数的计算评估蛋白表达之间的联系和流式细胞分析仪和Luminex数据。一个双边的假定值< 0.05被认为是具有统计学意义。
在线存款
在网上补充材料,我们描述细节细胞培养,细胞内氧化应激测量,免疫印迹和mRNA的测量。
道德的考虑
PNEC抽样程序是通过学术医学中心(阿姆斯特丹,荷兰)伦理委员会和知情同意了父母的所有参与者。
结果
鼻刷子进行共有34个孩子。五毛刷样品(所有从唐氏综合症儿童)并没有贴壁细胞(n = 2),或细胞被感染(n = 3)。我们能够文化PNECs实验条件的剩余的29个孩子患有唐氏综合症的12和17对照组。因此,鼻刷技术被证明是适合收获PNECs,很少有文化的失败。病人特点所示表1。细胞培养生产足够的材料来执行所有分析在大多数,但不是所有的实验。为每个分析,给出n在图标题。
自由基拾荒者的表达在PNECs唐氏综合症的儿童不同于控制
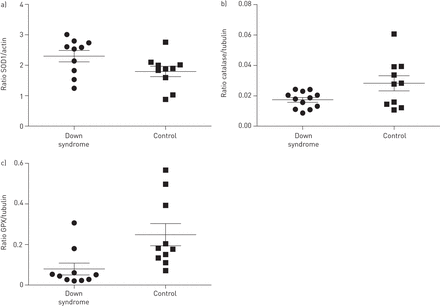
SOD1,过氧化氢酶GPX表达式给出图2。SOD1表达式提出了比SOD1 /肌动蛋白。均值±sd表达SOD1的唐氏综合症主题为2.30±0.59与在控制1.80±0.54 (p = 0.06)。过氧化氢酶及GPX表达式被视为与微管蛋白的比例。均值±sd过氧化氢酶的表达在唐氏综合症主题为0.018±0.006与在控制0.028±0.016 (p = 0.04)。中位数(四分位范围)的表达GPX唐氏综合症学科是0.048 (0.026 - -0.060)与0.179(0.128 - -0.418)在控制(p = 0.004)。
蛋白表达的)CuZn-superoxide歧化酶(SOD1), b)过氧化氢酶和c)谷胱甘肽过氧化物酶(GPX)在原发性鼻上皮细胞。行代表均值和酒吧扫描电镜。唐氏综合症:n = 10(过氧化氢酶n = 12);控制:n = 10。
细胞内氧化应激增加黄嘌呤/黄嘌呤氧化酶和挺
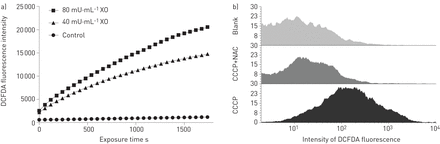
黄嘌呤/黄嘌呤氧化酶系统生成过氧化物,在浓度低得多,一些H2O2(14]。通过孵化细胞与细胞外接触之前DCFDA黄嘌呤/黄嘌呤氧化酶,我们显示在NCI-H292细胞,这种细胞外代的过氧化物的方法导致了细胞内氧化应激增加(图3)。CCCP诱发超氧化物的形成通过解偶联线粒体蛋白梯度,从而防止ATP合成。细胞内氧化应激的生产挺在我们的模型中所示图3 b。
一)细胞内氧化应激以5 - (6)-chloromethyl-2 ', 7 ' -dichlorodihydrofluorescein二醋酸盐(DCFDA)荧光增加H292细胞接触后0 - 0.5 - 1.0 mM的黄嘌呤和0-40-80亩·毫升−1黄嘌呤氧化酶(XO)。b)细胞内氧化应激以DCFDA H292细胞荧光增加3 h后暴露在200μM羰基氰化物m-chlorophenyl腙(CCCP)。没有增加DCFDA荧光当细胞同时孵化2毫米的抗氧化剂N乙酰-l半胱氨酸(NAC)。
氧化应激的细胞凋亡PNECs PNECs之间没有显著不同的孩子患有唐氏综合症和对照组
坏死和凋亡细胞死亡,增加模式存在剂量依赖的相关性在暴露于黄嘌呤及黄嘌呤氧化酶PNECs唐氏综合症儿童和对照组。我们没有发现差异表达annexin-V和/或propidium碘后既不暴露剂量之间的黄嘌呤/黄嘌呤氧化酶PNECs唐氏综合症和对照组(图4)。转换对正态分布是不可能的,因此,全球语言监测机构重复测量分析不能被执行。
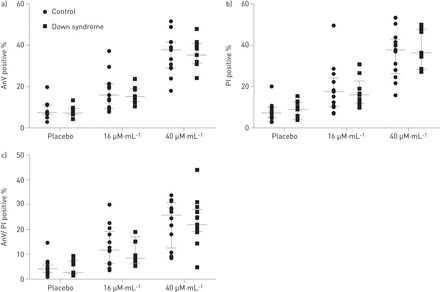
的百分比)annexin-V积极(AnV), b) propidium碘积极(π)和c) AnV和PI-positive主要鼻上皮细胞接触后0 - 0.2 - 0.5毫米黄嘌呤和0-16-40亩·毫升−1黄嘌呤氧化酶对3 h。线表示中位数和四分位范围。唐氏综合症:n = 9;控制:n = 13。
SOD1的表达和细胞死亡之间没有相关性接触过氧化物
没有明显SOD1的表达之间的相关性,过氧化氢酶GPX和流式细胞仪分析细胞死亡的结果在接触过氧化物PNECs唐氏综合症或对照组。为了调查是否失衡H2O2第和H2O2退化酶与细胞死亡,SOD1之间的比例和过氧化氢酶的表达和GPX计算和测试相关的细胞死亡在超氧化物接触。我们没有发现这样的相关性。
细胞凋亡调节基因的mRNA表达在氧化应激反应PNECs唐氏综合症的孩子不是不同于控制
多路复用ligation-dependent探针扩增的结果(MLPA)分析细胞凋亡相关的mRNA内容提出了数字S1和S2。总之,我们发现感应的病因,Nix和NIP3暴露于氧化应激。这些蛋白的表达是对氧化应激(16,17]。生存素的表达完全被抑制在接触> 6μM挺。生存素是细胞凋亡蛋白的抑制剂(IAP)家庭和功能参与有丝分裂。没有差异之间的细胞凋亡调控蛋白mRNA表达PNECs唐氏综合症和对照组。这是符合我们观察到细胞凋亡水平在暴露于氧化应激PNECs不不同的唐氏综合症和对照组之间。在基线,p21的表达,调节细胞周期的进展,较低的PNECs与对照组相比唐氏综合症。
炎症反应中氧化应激PNECs唐氏综合症的孩子不是明显不同与控制
多路复用荧光珠化验结果PNEC后上层清液提出了接触氧化应激图5。我们并没有发现任何显著性差异水平的IL-1β,il - 6,引发,血管内皮生长因子(VEGF)和粒细胞集落刺激因子(包含)之间的任何条件PNECs唐氏综合症和对照组。上层清液的水平的il - 6和GCSF PNECs唐氏综合症的主题都与对照组相比更高。这一发现并没有证实了一般线性重复措施造型(p = 0.14 GCSF il - 6和p = 0.18)。SOD1的细胞因子水平和表达之间的相关性,过氧化氢酶GPX检查。没有明显的相关性,除了SOD1和il - 6水平在100年接触μM挺(斯皮尔曼的ρ0.55,p = 0.04)。如图所示的上层清液中乳酸脱氢酶活性的增加,细胞溶菌作用明显暴露后24小时至100年μM挺。低浓度的挺(0-6-25μM)没有导致细胞裂解。
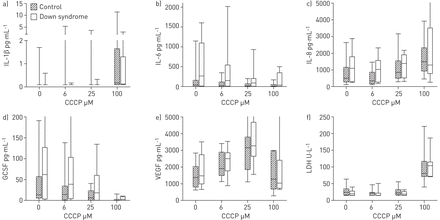
水平)白介素(IL) 1β,b) IL - 6 c)引发,d)粒细胞集落刺激因子(包含),e)血管内皮生长因子(VEGF) andf)乳酸脱氢酶(LDH)的上层清液后原发性鼻腔上皮细胞暴露于0-6-25-100μM羰基氰化物m-chlorophenyl腙(CCCP) 24 h。箱形图代表值,第一和第三个四分位数,和范围。唐氏综合症:n = 10;控制:n = 15。
讨论
我们发现了一个不平衡的H2O2第和退化酶在初级唐氏综合症儿童鼻上皮细胞与对照组相比。然而,这并没有导致敏感性改变氧化应激损伤细胞凋亡或坏死,或表达的改变促炎细胞因子,趋化因子和生长因子。
我们所知,这是第一次报告的表达SOD1,过氧化氢酶和GPX呼吸道上皮唐氏综合症的人。作为SOD1是21号染色体上编码,从理论上讲,无视基因表达调控,SOD1在称21三体综合症可能是50%。我们发现一个超表达SOD1∼28%的唐氏综合症与对照组相比。
也没有以前的报告在呼吸道上皮细胞氧化应激的影响暴露在唐氏综合症。大多数研究关于氧化应激和细胞凋亡在唐氏综合症表现在各种鼠标模型关注神经元(18]。我们最近显示,在人类胎儿呼吸道上皮细胞、凋亡细胞的比例并不是不同的唐氏综合症和对照组之间,但氧化应激的作用不是评价研究[19]。
我们提出,过度缺乏海拔SOD1的H2O2减少酶会导致增加生产的H2O2在主要呼吸道上皮细胞已被证明发生在神经元和成纤维细胞(8,20.]。然而,在一项研究中使用的数学模型,结果表明,过度的SOD1事实上会导致增加,减少,或在H没有区别2O2生产,根据超氧化物的存在的替代途径消费和负反馈调节的过氧化物生产(21]。在肺损伤的实验研究,过度SOD1似乎有益的影响占主导地位的22]。例如,过度的老鼠SOD1防止肺泡细胞凋亡后ceramide-induced氧化应激(23]。在我们的研究中,尽管SOD1的表达不利的比率,过氧化氢酶GPX,我们没有发现有害影响的增加细胞凋亡或暴露于氧化应激炎症。然而,SOD1的超表达也没有导致防止氧化应激。因此,在我们的在体外研究中,SOD1表达式在PNECs似乎并不与细胞凋亡。这可能是解释为一个产能过剩或适应其他酶的抗氧化系统,消除SOD1进行靶向治疗的效果。此外,细胞凋亡是一个高度管制的过程和其他凋亡通路可能counterregulate SOD1进行靶向治疗的影响。最后,其他细胞车厢中重要的病理生理学ARDS,如内皮细胞,可能更受氧化应激造成SOD1超表达。
我们不会减少过氧化氢酶的活性和GPX PNECs。过氧化氢酶和GPX编码染色体上3,11日,分别。虽然SOD1始终在唐氏综合症,过氧化氢酶的活性和GPX取决于组织被调查。先前的研究已经表明,他们的活动在唐氏综合症类似或增加与控制(24),但这不是一个一致的发现(25]。
我们没有调查其他蛋白质,与氧化应激在唐氏综合症和疾病有关,如ETS-2、应用和DSCR121]。然而,我们研究一个端点效应的氧化应激在PNECs(细胞凋亡和坏死),没有发现唐氏综合症与对照组之间的差异。因此不可能这些蛋白质发挥重要作用在氧化应激的影响在唐氏综合症PNECs细胞死亡。
在这项研究中我们调查的细胞因子(IL-1β,il - 6,引发,VEGF和GCSF),所有但GCSF已被证明是增加等离子体ARDS患者的26]。在支气管肺泡灌洗液,但VEGF在ARDS是升高的。在体外,我们发现IL-1β增加,引发和VEGF在PNEC上层清液接触后增加的氧化应激水平。il - 6和GCSF减少PNEC上层清液的唐氏综合症对象和控制在暴露于氧化应激水平增加。这可能是由我们的时间点取样。另外,在活的有机体内,其他在呼吸道上皮细胞il - 6可能负责增加。而VEGF的表达并不是不同的唐氏综合症和对照组之间在我们的研究中,血管生成反应VEGF可能抑制在唐氏综合症的主题,展示了最近在唐氏综合症小鼠模型(27]。
虽然不重要,但是我们发现的il - 6和GCSF水平PNEC上层清液始终高于唐氏综合症与对照组相比,无论氧化应激水平。在唐氏综合症引发并没有显著增加与对照组在最高暴露于氧化应激。这是与之前的研究一致,显示增加血浆il - 6水平,引发唐氏综合症儿童(28,29日]。在粒细胞,GCSF可以抑制细胞凋亡在唐氏综合症而不是控制(9]。在我们的研究中,在唐氏综合症和对照组中,我们没有发现GCSF水平和细胞凋亡之间的关系。
我们使用MLPA调查之间的差异调节凋亡唐氏综合症和控制对象。这些结果进行解释时应特别谨慎,由于小样本大小。不太可能,但仍然不是不可能,调节细胞凋亡是不同的两组之间,虽然最终的结果,凋亡细胞的比例,不是组织之间的不同。
我们的研究结果并不支持这一概念的高风险ARDS唐氏综合症儿童可以解释为增加肺泡上皮细胞的凋亡和炎症引起的自由基拾荒者的不平衡。从理论上讲,氧化应激可能是负责以外的其他pro-apoptotic刺激增加肺泡细胞凋亡在唐氏综合症。然而,事实上是否存在细胞凋亡增加肺在唐氏综合症ARDS与控制还有待建立。
基于我们的研究结果,它似乎不合理执行研究的能力抗氧化治疗预防ARDS重病孩子患有唐氏综合症。然而,我们也不能排除鼻腔上皮细胞用于本研究对氧化应激的反应不同于肺泡上皮细胞。此外,气道上皮细胞接触可能导致ARDS的触发,比如严重的感染,可能会有不同的反应比在这项研究中使用的健康细胞。此外,我们没有研究肺泡内皮,也在ARDS的发病机制中扮演着重要角色2]。内皮细胞可能有不同的敏感性在唐氏综合症,从而导致氧化应激ARDS的高风险唐氏综合症。最后,我们的结果不排除这种可能性,抗氧化治疗可能有利于ARDS人口作为一个整体,及其可能的影响依赖ARDS的原因和疾病进展的阶段。动物研究静脉和aerolised SOD、过氧化氢酶和他们模仿已被证明能够防止肺损伤在几个模型。治疗与细胞内SOD1以外的其他形式的SOD,如细胞外SOD和线粒体SOD,已被证明是比细胞内保护形式的SOD在唐氏综合症。然而,很少有研究在人类和执行结果是令人失望的(22,30.]。
总之,我们发现了一个不平衡的自由基在气道上皮的唐氏综合症患儿拾荒者,但这并没有导致增加水平的细胞凋亡或暴露于氧化应激炎症。
确认
作者要感谢芭芭拉Smids-Dierdorp,塔玛拉·德克尔,Annemiek Dijkhuis(实验免疫学和呼吸医学部门)和雷内·利恩(遗传代谢疾病的部门、学术医疗中心大学的阿姆斯特丹,荷兰)实验室援助;和Jan Pieter van Trotsenburg Marchal和保罗(儿童医院的儿科内分泌学的部门,艾玛/ AMC,阿姆斯特丹,荷兰)有帮助的孩子患有唐氏综合症。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
声明:支持被授予以下非营利组织:Tysfonds(Middenmeer、荷兰)Steun艾玛Kinderziekenhuis AMC的基础(阿姆斯特丹,荷兰),Janivo基金会(泽斯特、荷兰)。
利益冲突:没有宣布。
- 收到了2012年8月6日。
- 接受2012年的11月5日。
- ©2013人队