摘要
三分之一的特发性肺纤维化(IPF)患者发展为肺动脉高压(PH-IPF),这与死亡率增加有关。肺部脉管系统基因表达谱的改变是否预示着PH-IPF的临床发病尚不清楚。我们比较了有PH值和无PH值的IPF患者肺血管中的基因表达与对照组。
从16例IPF患者中使用激光捕获显微解剖分离肺小动脉:8例有PH值(PH-IPF), 8例无PH值(NPH-IPF), 7例对照组。将提取的RNA制备探针,与Affymetrix Hu133 2.0 Plus基因芯片杂交。生物计量研究分支阵列工具和匠心路径分析软件用于分析微阵列数据。
单因素分析显示255个基因将IPF小动脉与对照组区别开来(p<0.001)。血管平滑肌和内皮细胞增殖的介质、Wnt信号和凋亡在IPF小动脉中表达差异。无监督和有监督聚类分析显示PH-IPF和NPH-IPF小动脉中相似的基因表达。
IPF患者肺小动脉基因表达谱在有和没有ph共存的IPF患者中相似。参与血管增生和异常凋亡的通路在IPF患者中被激活,这些通路可能有助于肺血管重塑。
特发性肺纤维化(IPF)是一种使人虚弱且致命的弥漫性肺实质疾病,中位生存期<3年。超过三分之一的IPF患者在肺移植初始评估时已经有肺动脉高压(PH-IPF),绝大多数患者在移植时已出现临床明显的PH [1,2].目前尚不清楚IPF患者的PH亚群是否具有明显的血管分子表型,或者是否所有IPF患者与对照组相比在肺血管基因表达上都存在分子差异。IPF中肺血管功能障碍的机制有价值,因为PH-IPF与功能状态下降和死亡风险增加有关[1,3.].
PH-IPF患者的肺小动脉由于成纤维细胞堆积和细胞外基质沉积而表现出明显的内膜肥大、内侧平滑肌细胞增殖和外膜增厚[1].先前的研究利用DNA微阵列来评估特发性肺动脉高压(PAH)和PH-IPF中的基因表达。与PH-IPF患者相比,PAH患者全肺匀浆中与转化生长因子(TGF)-β、细胞外信号相关激酶(ERK)/丝裂原激活蛋白激酶(MAPK)、血小板衍生生长因子(PDGF)和cAMP信号相关的基因表达差异[4].在PH-IPF中观察到全肺匀浆中血管生成基因表达减少和与血管重塑相关的基因上调[5].考虑到肺血管在全肺匀浆中基因表达的比例相对较小,这些研究中观察到的基因表达差异可能主要反映了肺实质的变化,而不是肺血管的变化。直接确定有PH值和无PH值的IPF患者肺血管中的基因表达是否发生改变具有临床意义,因为两组之间的差异意味着不同的血管表型。IPF中血管基因表达与对照组的差异提示IPF中特定的病理过程,可能导致肺血管重塑。
因此,我们评估了无PH的IPF患者(NPH-IPF)和共存PH的IPF患者的激光捕获微解剖(LCM)肺小动脉的基因表达,并与对照组进行了比较。我们试图确定可能介导IPF血管重塑发展的基因和生物学途径。一些结果以前曾作为摘要报道过[6].
方法
研究人群
详情请参阅在线补充资料。我们通过查询哥伦比亚大学组织库数据库中的术语“肺”和“普通间质性肺炎”(UIP)和/或“肺动脉高压”来确定潜在的符合条件的研究对象。我们纳入了符合美国胸科学会诊断IPF标准(以前和现在)的IPF患者[7,8].如果IPF患者的平均肺动脉压(mPAP) >25 mmHg,且经右心导管测量肺毛细血管楔压≤15 mmHg,符合世界卫生组织(WHO)第3组标准,则将其纳入PH-IPF组[9,10].如果IPF患者mPAP≤25 mmHg,则将其纳入NPH-IPF组。
我们排除了有胶原血管疾病临床证据的患者,胶原血管疾病是肺动脉高压的另一个已知病因(如.慢性阻塞性肺疾病,阻塞性睡眠呼吸暂停和血栓栓塞性疾病),左心室功能障碍或左侧瓣膜疾病,缺少血流动力学或肺功能数据,年龄<18岁。
15个IPF样本来自肺外植体,1个来自外科肺活检。从四个未使用的供体肺刨花和三个正常肺切片中切除的肺类癌肿瘤标本作为对照。临床数据收集获得了哥伦比亚大学机构审查委员会(IRB-AAAC0695)的批准和放弃同意。
组织样品的处理和LCM
所有肺组织均于围手术期获得,快速冷冻于液氮中并保存于-80°C。在显微解剖时,将组织样本切成5 μm切片,用95%乙醇固定,并在PALM膜上风干(PALM Microlaser Technologies, Bernried, Germany)。使用LCM染色试剂盒(Ambion, Foster City, CA, USA)对切片进行染色。使用蔡司Axiovert显微镜(卡尔蔡司微成像公司,Thornwood, NY, USA)和PALM微束LCM系统(PALM微激光技术)进行血管解剖。所有在支气管维管束内可见的肺小动脉(100-450 μm)均用LCM分离。
RNA分离,微阵列处理和分析,免疫组化染色
利用RNAqueous-Micro Kit (Ambion)分离RNA。使用改进的Eberwine程序扩增和生物素化RNA,使其最低目标为15 μg RNA进行杂交。目标cRNA杂交到Affymetrix Hu133 2.0 Plus寡核苷酸阵列(Affymetrix, Santa Clara, CA, USA)。生物特征研究分支阵列工具软件v3.7.2。(Richard Simon and Amy Lam at National Cancer Institute, Bethesda, MA, USA)用于基因芯片数据的归一化、过滤和初始质量控制评估。使用单变量分析(p<0.001)对类别分配之间的差异基因表达进行监督分析。所有比较的错误发现率设置为q<10%。利用10,000个随机排列进行了排列分析,全局p<0.01。利用独创性途径分析(IPA;匠心系统,红木城,CA,美国)。
对10例IPF病例(5例PH-IPF和5例NPH-IPF)和5例正常供体肺的石蜡组织块进行切片和染色,以检测分泌卷曲相关蛋白(SFRP)-2(单克隆兔抗人)(Sigma-Aldrich Corp.圣路易斯,密苏里州,美国),sparc相关模块钙结合(SMOC)-2(多克隆兔抗人)(Lifespan Biosciences Inc.,西雅图,华盛顿州,美国)和信号传感器和转录激活因子(STAT1)(单克隆兔抗人)(Sigma)使用DAKO Envision Dual Link试剂盒(DAKO, Glostrup,丹麦)。使用Fisher精确检验(SPSS, v16.0;IBM北美,纽约,纽约,美国)。
结果
我们纳入了8例PH-IPF患者,8例NPH-IPF患者和7例对照组(表1).IPF患者年龄大于对照组,且以男性为主。PH-IPF和NPH-IPF患者在年龄、性别、种族、吸烟史和肺功能方面相似。肺功能数据显示两组患者均存在限制性损害,且无阻塞性生理障碍。1例CT显示轻度上肺气肿;组织学或胸部CT均无明显肺气肿。值得注意的是,PH- ipf组的PH存在程度较轻,mPAP为29 mmHg。
检测了四种常见的内皮细胞和上皮细胞基因的原始基因表达值,以确认肺小动脉的分离,同时尽量减少肺实质或气道的包涵。所有样本中内皮基因表达升高,而上皮基因表达极低(在线补充表E1),证实了肺小动脉的成功分离。
我们首先比较了PH-IPF小动脉和NPH-IPF小动脉。无监督层次聚类是一种根据组间内容相似性对基因微阵列数据进行分组的方法。PH-IPF和NPH-IPF小动脉无监督分层聚类分析的树突图显示两组之间没有分离(图1),单因素分析基因表达无显著差异(在线补充表E2)。
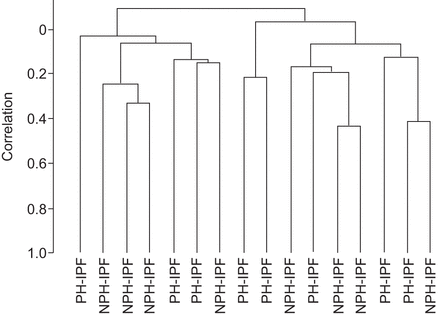
特发性肺纤维化(IPF)和肺动脉高压(PH)患者的血管与没有PH值的IPF患者的血管(NPH-IPF)。使用非中心相关和平均链接的无监督层次聚类分析。树突图显示PH-IPF和NPH-IPF样品之间的基因表达没有分离。
然后我们分析了组合IPF样本(PH-IPF + NPH-IPF)的基因表达。与控制。无监督的层次聚类表明IPF样本和对照之间存在显著的分离(图2).通过单因素分析,与对照血管相比,IPF小动脉中有255个基因表达差异(p<0.001, q<10%) (图3),所选结果载于表2(完整名单载于网上补充表格E4)。Wnt信号的两种介质SFRP2和CCND1,以及补体家族成员(C4A, C4B和CFH)在IPF小动脉中上调。与血管增生相关的转录因子和细胞外蛋白STAT1和SMOC2在IPF小动脉中的表达增加。

特发性肺纤维化血管与控制船只。无监督层次聚类分析,使用非中心相关和平均链接。树枝图显示了IPF样本的基因表达与对照分开的聚类。
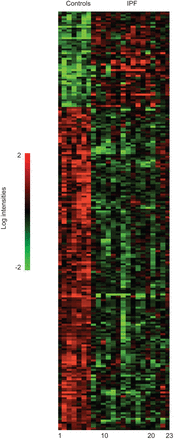
特发性肺纤维化(IPF)血管差异表达基因热图与控制。259个基因差异表达,p<0.001,错误发现率<10%。红色:上调基因;绿色:下调基因。
相反,与对照组相比,调节内皮功能的kruppel样转录因子家族成员(KLF6和10)在IPF小动脉中下调。S1PR1的配体sphingosin 1磷酸是内皮细胞屏障完整性的效应物,也被下调。一氧化氮信号传导媒介精氨酸酶II的表达[11],在IPF小动脉中减少。IPF小动脉中凋亡效应因子IGFBP3和TIMP3下调。
最后,我们分析了PH-IPF组的基因表达与对照组和NPH-IPF组与控制。PH-IPF分析与对照组没有发现有统计学意义的基因。NPH-IPF组分析结果与控件显示在联机补充表E3中。
生物途径分析
我们使用IPA软件来确定特定的生物通路和/或典型信号通路基因表达是否在IPF小动脉中更高与控制(表3).IPF小动脉的首要生物学功能是癌症,而首要的分子和细胞功能是细胞生长和增殖。最常见的信号通路包括氨基酸代谢、AMP激酶信号通路、纤毛中性营养因子信号通路和补体系统。IPF小动脉中与血管内皮生长因子(VEGF)信号相关的基因(ACTB, EIF1, PIM1和PIK3CA)和缺氧相关信号(KLF10, ARG2和ARHGAP26)下调,一氧化氮信号标记物(ITPR2, PIK3CA和IGFBP3)也下调。ERK/MAPK和TGF-β信号通路相关基因同时上调和下调。STAT1和PLAU都是平滑肌增殖的介质,在IPF小动脉中表达上调。许多影响癌症和细胞凋亡的基因在IPF小动脉中有差异表达(表3).
基因阵列数据的免疫组化染色验证
选择生物学意义的基因产物进行免疫组化染色,以确认基因表达数据(图4).与对照组相比,IPF小动脉中STAT1和SMOC2蛋白表达显著上调(p<0.05)。SFRP2蛋白表达在IPF小动脉中也趋于高表达(p=0.10)。这些结果证实了基因表达数据。
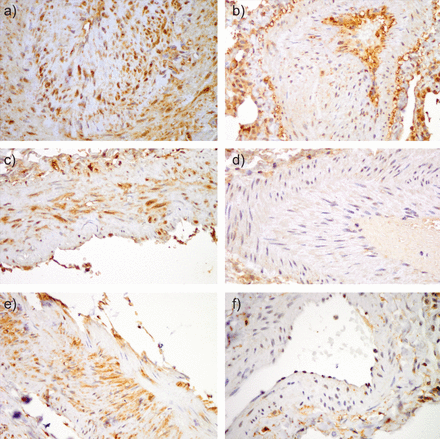
a)普通间质性肺炎(UIP)组织的血管在内皮和内侧平滑肌细胞中显示明显的信号换能器和转录激活因子1核质染色,而b)正常血管仅显示内皮染色。c) UIP组织的血管在内侧平滑肌细胞和内皮细胞中显示强烈的分泌蛋白、酸性、富半胱氨酸相关模块化钙结合(SMOC)-2的细胞质染色,而d)正常血管为阴性。e) UIP组织血管壁可见内侧平滑肌细胞分泌卷曲相关蛋白2细胞质染色,f)正常血管未见染色。a, b) Magnification×100, c-f) magnification×150。
讨论
我们的研究结果为IPF患者肺小动脉中血管增生和异常细胞凋亡相关基因的表达与对照组相比存在差异提供了直接证据。此外,无PH值的IPF患者和共存PH值的IPF患者肺小动脉中有相似的基因表达,提示血流动力学正常的IPF患者可能存在临床前肺血管疾病。
IPF中肺血管重塑的机制尚不清楚。据我们所知,这是第一个利用LCM肺小动脉的基因表达谱来检测IPF中的血管基因表达的研究,这是纤维化肺病中一个技术要求很高的过程。我们研究中的患者也经历了广泛而精确的临床表型。
之前的两项PH-IPF基因表达谱研究都使用了全肺匀浆。Gagermeier等.[5]报道了13例PH-IPF患者的基因表达数据。他们发现VEGF、内皮素(ET)-1和血小板内皮细胞粘附分子表达降低,而磷脂酶A2等炎症基因上调。我们还发现与VEGF信号通路相关的基因被下调,尽管炎症基因在我们的IPF样本中并不高。Rajkumar等.[4]比较了18名PAH患者和8名PH-IPF患者的全肺基因表达。与PH-IPF相比,PAH中rho激酶和cAMP信号传导介质上调。由于我们没有检查PAH患者,因此很难将这项研究与我们的研究进行直接比较。最近,Mura所言等.[12]检测了不同病因的肺纤维化(UIP和非UIP)患者肺基因的表达,伴有和不伴有严重PH (mPAP >40 mmHg)。PH组细胞增殖和成纤维细胞迁移途径高表达。虽然在我们的研究中,前一种途径在IPF患者的脉管系统中也有很高的代表性,但在最高上调的基因中没有重叠。本研究的患者与我们的患者之间存在显著的表型差异。结果的差异可能进一步解释为我们直接关注孤立的肺小动脉,而不是先前研究中实质、气道和血管的混合。对分离肺小动脉的研究使我们能够直接确定肺血管系统中的基因表达,而不受IPF影响的肺实质的潜在人工制品。
IPF肺小动脉中促进细胞增殖的基因上调,而不受ph共存的影响。SMOC2促进血管生成和内皮细胞增殖[13], SMOC2消融抑制暴露于PDGF-β和其他与IPF发病机制有关的生长因子的小鼠成纤维细胞的DNA合成[14].此外,SMOC2促进细胞周期进程通过cyclinD1,在我们的样本中也被上调[15].鉴于这些发现,SMOC2有助于IPF的血管重塑是合理的。此外,在IPF肺小动脉中,STAT1的基因和蛋白质表达增加,而不考虑共存ph的存在。STAT1增加血管平滑肌细胞增殖,以响应血管紧张素II和血清素,被认为是多环芳烃的介质[16,17].W食物等.[18]表明STAT1介导人血管平滑肌细胞(HVSMCs) ET-1生成的增加[18].此外,在我们的IPF样本中过表达的PLAU已被证明可以激活人血管内皮细胞和HVSMCs中的STAT1 [19,20.].这些数据表明,PLAU和其他介质可能激活IPF中的STAT1,导致血管增生。我们在IPF小动脉中发现SFRP2表达增加,这可能表明Wnt信号通路在促进PH-IPF发展中的作用。SFRP2是典型和非典型Wnt信号的中介,在实验模型中促进血管生成并抑制缺氧诱导的内皮细胞凋亡[21].此外,最近已证实非典型Wnt信号在特发性PAH的发展中起积极作用[22].最后,在有和没有ph共存的IPF患者的肺小动脉中,抑制增殖的基因下调。KLF10介导抗增殖和抗凋亡作用通过TGF -β-Smad信号[23].KLF6作为肿瘤抑制因子,在内皮细胞中表达,由缺氧和其他形式的细胞应激诱导[24].KLF10和KLF6的下调可能有助于IPF中血管细胞增殖和凋亡的解除。YY1是一种锌指转录因子,它抑制血管平滑肌细胞生长,并在血红素加氧酶(HO)-1的下游发挥作用,在我们的样本中被下调[25,26].HO-1表达降低是严重多环芳烃的特征,提示多环芳烃的病理生物学与IPF血管改变之间的潜在联系[26,27].有和没有共存PH值的IPF患者肺小动脉中促进和抑制细胞增殖的基因表达的类似改变强烈提示血管功能在IPF过程中早期发生改变。这些发现与先前的报道一致,即绝大多数IPF患者的临床PH值随着时间的推移而发展[2].另外,有或没有PH的IPF患者肺小动脉中相似的基因表达可能表明,导致IPF肺血管改变的生物学过程可能是IPF作为一种疾病的表现,而不是PH。
有趣的是,与对照组相比,IPF血管中差异表达的基因主要属于细胞增殖和癌症类别。癌症生物学和IPF之间的共同致病关系,包括异常细胞增殖和凋亡受损,已被越来越多地注意到[28].在多环芳烃中,STAT3激活有助于高增殖、抗凋亡内皮细胞的增殖[29].在我们的样本中,细胞凋亡的几种调节因子低表达。相反,增殖介质,如STAT1和SMOC2,则上调[19,20.].这些结果表明,不受控制的血管增生和凋亡受损可能也有助于IPF的血管重塑。最后,我们的样本中SFRP2表达的增加表明Wnt信号在IPF血管变化的发展中起着积极作用[22].
我们的研究有几个局限性。我们研究了少量的患者,尽管这是基因微阵列研究的典型样本量。我们使用LCM分离血管进行分析,这是一种技术复杂的方法,在IPF的血管研究中是一种新颖的方法。逆转录酶(RT)-PCR没有用于验证,因为从结构扭曲的肺小动脉组织中精确分离肺小动脉组织,纤维化实质排除了提取足够数量的组织用于表达微阵列分析和RT-PCR。PH-IPF患者肺动脉压仅轻度升高,但符合WHO标准,是典型的PH-IPF [3.,30.].与NPH-IPF组相比,更严重的PH-IPF患者可能在基因表达上有显著差异。IPF中肺纤维化合并肺气肿与PH值相关[31];然而,在我们的研究中,只有1例患者有轻度上肺气肿的证据[31].此外,肺活量和肺容积在两组之间相似。我们使用从接受类癌切除术的患者的正常肺中获得的标本作为部分对照样本,并承认虽然组织在结构上表现正常,但在分子水平上可能是异常的。最后,虽然高通量基因表达分析可能会出现I型错误,但我们限制了假阳性率,并使用免疫组织化学确认了选定的基因表达结果。
总之,肺血管基因表达特征在IPF和PH并存患者和仅IPF患者中相似,其特征是细胞生长异常和凋亡失调控。IPF临床前肺血管改变的特征可能会导致这些患者共存PH的新治疗策略的发展。
致谢
我们感谢Neil Schluger(哥伦比亚大学肺、过敏和重症监护医学部主任)在审阅手稿后提出的有益意见。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
这项工作得到了The斯托尼·沃尔德-赫伯特基金(批准号CU08-7872)。
权益声明书
利益冲突信息可以在本文的在线版本中找到www.www.qdcxjkg.com
- 收到了2012年5月29日。
- 接受2012年8月29日。
- ©2013人队