文摘
最近几乎没有性别信息社区获得性肺炎(CAP)的患者的结果。本研究的目的是确定女性是否与更好的临床结果住院患者的帽子。
二次分析是由社区获得性肺炎的组织关于男性和女性患者帽从6月1日在17个国家80家医院,2001年8月2日,2011年。结果临床稳定,停留时间和住院和28天的死亡率。Propensity-adjusted,多元回归模型来预测的发生概率研究的结果。
其中有6718名患者在这项研究中,40%是女性。调整风险比(人力资源)临床稳定时间为0.91 (95% CI 0.85 - -0.97;p = 0.005)。长度的调整人力资源保持为0.94 (95% CI 0.88 - -1.01;p = 0.089)。住院死亡率的调整风险比为1.04 (95% CI 0.86 - -1.24;p = 0.717), 28天死亡率为1.15 (95% CI 1.02 - -1.30;p = 0.018)。
这项研究表明流行病学的帽子可能会改变,而且女性比男性有更糟糕的结果帽。他们更有可能需要更长的时间达到临床稳定、再住院,15%更有可能28天后死亡。当前肺炎评分系统可能需要修订的关于女性的死亡风险。
二十年前,sex-dependent结果和护理质量的差异是由美国医学协会承认的伦理和司法事务委员会需要审慎的调查(1]。这是紧随其后的是一个重点的研究需要对呼吸道健康的女性,但是最近的数据缺乏。
社区获得性肺炎(CAP)是最常见的传染病之一,排名第四大死因的女性在美国(2]。与男性和女性结合的研究表明限制患者的死亡率与几个独立危险因素有关,如重症监护室承认,高龄,胸腔积液,增加时间第一个抗菌剂量和并发症的存在(如。贫血,慢性肾功能衰竭和充血性心力衰竭),以及性(3,4]。
第一个查询与院内肺炎性和肺炎开始(HAP)。一项研究发现,男性患者HAP发生率较高,和长度的增加保持(LOS)在重症监护室后创伤,但女性患者HAP证明更高的死亡率(5]。在另一项研究中,女性比男性三倍死与机械通气相关肺炎与[6),但不是在其他的研究7,8]。
两大研究使用信息描述1997年医疗保险和医疗补助数据帽和性结果。> 140所示000老年人,病人住院,帽,男性死亡率高于女性(11.6%与9.8%,p < 0.001) (9]。在另一项研究中,老年男性比女性更频繁地死在随后一年住院帽后,死亡的风险最高的排放(44.8%后的第一个月与36.9%,调整后的kaplan meier (p≤0.001)10]。
查询到性结果和帽开始后第一个HAP的性别差异研究解决的结果。治疗CAP患者的成本是重要的,在美国每年100亿美元,其中大约92%花在医院护理(11]。因此,使住院病人患肺炎的决定是一个重要的健康经济问题。为了提高决定住院治疗,肺炎严重程度指数(PSI)成立于1997年,是一个准确的帽子来评估患者的预后模型风险(12]。常设调查小组委员会的目的是基于21个研究群体提供数据(17 641名患者)显示,雄性比雌性更死,因此10分减去PSI的一名女病人(13]。点的差异归因于每个性使用ψ是准确的时间出版;然而,流行病学有可能随时间改变。一项新的研究评估患者的性行为和结果之间的关系帽是十分必要的。
我们评价一个大型、多中心、国际队列研究的主题与帽重新评估之间的关系性和贫穷的结果在住院患者帽。
材料和方法
研究设计和研究的病人
这是一个国际成人患者住院的回顾性研究数据收集帽子。在17个国家80家医院,6月1日之间,2001年8月2日,2011年。在每个参与中心,医疗记录的住院患者的诊断综述了帽子。图表中选择所有病人诊断为帽在每个机构。抗菌疗法并不是由随机,他们也没有记录的前瞻性。调查人员转移的病例报告的形式完成通过一个安全的网站,社区获得性肺炎的组织”研究总部在路易斯维尔大学的路易斯维尔,肯塔基州,美国。样本数据收集形式可在:www.caposite.com。验证的数据质量进行研究中心在每种情况下进入分支头目数据库。这项研究是由机构审查委员会和放弃,因为这是一个回顾,观察性研究。
记录所有患者进入研究的综述了几个因素。世界人口和疾病信息包括年龄、性别、地区、吸烟状况、养老院居住状态和并发症,包括慢性阻塞性肺疾病(COPD)、充血性心力衰竭、冠状动脉疾病、高血压、肝、肾或脑血管疾病,糖尿病,艾滋病毒感染和恶性肿瘤。在入学体检结果指出包括改变精神状态和生命体征。放射性的发现了涉及叶的数量和空泡的存在或胸腔积液。实验室值从入学的日子,包括血小板、白细胞计数、动脉血气分析(pH值、动脉氧张力(PaO2),PaO2/吸入氧气分数(FIO2)比率)、血清钠、血清肌酐、白蛋白、血尿素氮(BUN)和红细胞比容。常设调查小组委员会(12]和crb - 65(混乱、呼吸频率≥30次·分钟−1,收缩压小于90毫米汞柱,舒张压≤60毫米汞柱,年龄≥65岁)(14)计算,微生物信息,当礼物,也记录下来。
研究变量的定义
帽子被定义为一个新的肺渗透在胸部的存在相关的住院的时候至少有下列之一:1)新的或增加咳嗽;2)温度异常(< 35.6°C或> 37.8°C);3)异常血清白细胞计数(白细胞增多,左移或白血球减少症定义为当地实验室值)。
低血压是定义为一个< 90毫米汞柱的收缩压或舒张压< 60毫米汞柱。气体交换被定义为的改变PaO2< 60毫米汞柱,PaO2/FIO2比< 300或氧饱和度< 90%。五个保健测量的过程。每一个对象均为血培养24小时内承认,抗菌政府承认,8小时内的氧化状态评估和之前的流感和肺炎球菌疫苗。品柱区域指定为美国/加拿大、欧洲、南美洲和亚洲、非洲。
时间临床稳定性计算日期的天数从入学日期,病人符合临床稳定性标准。时间临床稳定的标准,定义为在美国胸科学会帽,指南如下:所有的缺乏热≥8 h,提高白细胞增多(从前一天下降≥10%),容忍口服摄入和改善临床症状(如。改善咳嗽和气短)[15]。标准临床稳定性评估期间每日住院的前7天。7天内患者达到临床稳定的入学被定义为临床改善。滞留时间(LOS)计算的天数从入学之日起(0)指定为天出院日期。住院期间死亡率被定义为死于任何原因(死亡率)和28天内死亡率(28天)。时间临床稳定,洛杉矶,住院死亡率和28天死亡率被选为结果。
统计分析
患者基线特征和临床结果的女性和男性比较使用卡方或确切概率测试分类变量和t或Mann-Whitney U-tests连续变量。性别差异在时间临床使用kaplan meier生存曲线稳定和洛进行了评估。生存曲线之间的显著差异进行分析使用生存率较。
检查性对住院和28天死亡率的影响,倾向分数调整方法是使用[16]。使用逻辑回归模型,创建了一个倾向评分包括所有患者基线特征所示表1加过程的护理和重症监护的必要性。倾向评分被用来调整差异研究人口使用泊松回归模型误差方差(强劲17]。这种方法允许我们获得调整死亡率(住院死亡率和28天死亡率)风险比率对于那些在每一个性爱。倾向分数调整也是用来控制差异之间的关系性和时间临床使用Cox比例风险回归模型稳定性和洛杉矶。
一个假定值≤0.05被认为是在所有分析具有统计学意义。SAS v9.3 (SAS公司卡里,数控,美国)和MedCalc v12.0 (MedCalc软件、Mariakerke比利时)是用于所有分析。
结果
共有6718名患者被纳入研究:2665名女性和4053名男性。均值±sd年龄为64.7±19.1年(范围18 - 104岁)和40%是女性。收集到的25个变量中,其中7人是更糟的是女性(养老院居住、脑血管意外、精神状态改变,异常温度,tachypnoea,收缩压异常和贫血),虽然其中有五个是糟糕的男性(慢性阻塞性肺病、肝病、肾病、糖尿病和异常包)(表1)。护理的过程中,血培养是从女性获得更少和更少的女性承认之前收到了肺炎球菌疫苗(表1)。疾病的严重程度在统计学上使用crb - 65相似,但更糟糕的是男性在使用PSI。雌性的意思是PSI是85.8±46.6,和男性为94.7±45.7 (p≤0.001) (表2)。意味着PSI女性没有10分从他们的得分是94.7±48.8(在线补充图E1)病原体被确认在2204年的病人。链球菌引起的肺炎在男女最常见的病原体。最常见的病原体所示表3。顺便说一下,在92患者假单胞菌从疗养院,只有11个。肺炎未经调整的结果按性别分层所示结果表4,每个女性结果更糟。女性的数量在每个地区都不同:美国/加拿大:603 (30%);欧洲:1213 (42%);南美洲:804 (46%);非洲和亚洲/:45 (61%)。
时间的临床稳定的分析显示,女性比男性更不可能达到临床稳定在任何一天后第七天。kaplan meier曲线有差异为每个性(p < 0.001) (图1)。调整风险比(人力资源)临床稳定时间为0.91 (95% CI 0.85 - -0.97;p = 0.005)。洛杉矶的未经调整的分析显示,女性比男性更不可能在任何一天从医院出院后第14天。kaplan meier曲线之间的差异被发现(p = 0.006) (图2洛杉矶),但是人力资源调整为0.94 (95% CI 0.88 - -1.01;p = 0.089)。

kaplan meier曲线时间临床稳定在2665名女性和4053名男性:社区获得性肺炎患者。p < 0.001。
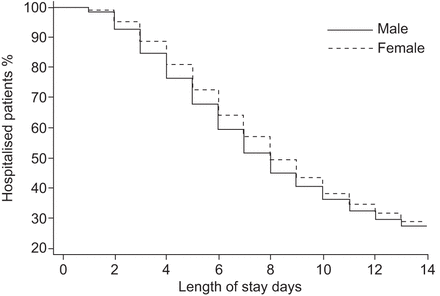
kaplan meier曲线的长度保持在2665名女性和4053名男性:社区获得性肺炎患者。p = 0.006。
在医院死亡的患者的比例高于女性(10.8%)比男性(9.3%;p = 0.041),但调整风险率(RR)住院死亡率没有统计学意义;调整RR 1.04 (95% CI 0.86 - -1.24;p = 0.717)。28天内死亡的患者的比例为26.0%,女性为21.4%,男性(p < 0.001)。这一结果在统计学上意义重大调整后的结果。28天的调整RR死亡率为1.15 (95% CI 1.02 - -1.30;p = 0.018)。
讨论
这项研究表明,女性是一个独立的预测帽当检查住院病人的临床结果。女性患者更有可能需要更长的时间来提高临床男性患者相比,女性患者和28天死亡率较高,∼5%的绝对差。调整后的结果也更糟糕的女性,除了洛(趋势走向意义)和住院死亡率。男性和女性之间的差异我们观察到病人的冲突与先前观察到帽(9,10]。我们可能见证的流行病学变化发生在近几十年来,尽管已很少关注男性和女性如何限制管理;换句话说有一个护理过程的性别差异的问题。
包括本研究过程的护理是很重要的,因为一个或更多的可能是一个重要因素来解释两性之间的差异的结果。获得血培养和有一个为每个性肺炎球菌疫苗在不同比例进行本研究。尽管这两个过程质量的护理措施在美国国立医院质量的措施,相互矛盾的文学已经发表在过去几年来支持任何一种改善患者的结果。最近的一项研究> 11 000名患者没有发现更频繁的住院或更高的死亡率受试者之前接种疫苗研究入境(18]。同样,在最近的一项研究关于质量度量的影响限制患者抗生素管理之前,没有一个被发现是重要的,包括获得血培养(19]。专业社会准则在美国现在不再推荐获得血培养与帽每个病人承认。尽管如此,本研究中发现的结果的差异进行调整后分析,包括调整护理的过程。
本研究的一个含义是,概念,女性患者比男性低风险上限可能需要修改。因为女性患者有更糟糕的结果在目前的研究中,他们可能需要住院PSI得分较低,或PSI分数需要加以修订。一定数量的点可能不需要从女性减去分数,或者甚至可能需要添加女性相比当前程序从女性10分减去分数。此外,其他目前肺炎评分系统,如crb - 65,可能需要调整性(14]。在临床研究中,女性会更准确地代表和分布式根据真正的疾病严重程度;因此将会有更少的α-和β-errors。
回顾我们的研究是有限的,这意味着可能存在选择偏倚。如果帽包括所有病人承认,那将帮助,但并非如此。此外,病人登记仅限于专业类型的病人被每个首席研究员。这项研究仅限于综述了关心的五个过程。其他进程的护理,如是否要执行一个特殊过程(如。支气管镜检查或parapneumonic积液引流)或当承认一个重症监护病房,没有可用的数据库和可能是重要的。尽管并发症的比例和疾病的严重程度统计对比分析,这将是理想的两性平等这些值,因而无需调整。未来的审判或病例对照研究设计可以使每一组疾病的严重程度。前瞻性、随机对照研究也将控制混杂因素。
尽管有这些限制,本研究演示了一些独特的优势。这是一个国际的研究包括病人从多个大洲。它突出了一个需要进一步研究,以确保女性被认为一个精确的临床疾病的严重性当照顾。排除标准是最小的,允许接近病人的表现可能会遇到在世界的许多地区,从而增加其generalisability。目前的研究包括将近7000患者诊断的帽子被证实放射学,而不是识别与诊断或计费代码。
总之,这项研究表明,女性患者有更高的风险不良帽状况比男性住院期间。他们有长时间的临床稳定,和更高的死亡率比男性28天。这还需要进一步的研究来验证我们的发现前瞻性。如果改变了和女性流行病学帽真的有更糟糕的结果与男性相比,本研究中的数据展示,那么未来的研究修改当前肺炎评分系统对更高的女性死亡率风险是必要的。
确认
作者欣然承认分支头目的工作人员在构建和维护分支头目数据集。美国:f·阿诺德·d·克里斯坦森,p . Peyrani和j·拉米雷斯(路易斯维尔大学的肯塔基州路易斯维尔市的);r . Nakamatsu(退伍军人医疗中心,肯塔基州路易斯维尔市的);k . Ayesu(奥兰多奥兰多地区医疗中心);b . Ostrowsky (Montefiore医疗中心和维勒医院,纽约,纽约);t .小文件(总结卫生系统,阿克伦,哦);美国Burdette(格林纪念医院,种子直感,哦);美国蜚蠊(好撒玛利亚人医院,辛辛那提,哦);m·雷斯特雷波(德克萨斯大学健康科学中心,圣安东尼奥,TX);j . Bordon(普罗维登斯医院,华盛顿特区);p .总值(新泽西州哈肯萨克大学医学中心,哈肯萨克市)。 Canada: T. Marrie (University of Alberta Hospital, Sturgeon Community Hospital, Grey Nuns Hospital and Royal Alexandra Hospital, Edmonton); K. Weiss (Maisonneuve-Rosemont Hospital, University of Montreal, Montreal). Puerto Rico: R. Fernandez (Hospital Municipal de San Juan, San Juan). Andorra: J. Roig (Hospital Nostra Senyora de Meritxell, Escaldes). Germany: H. Lode (City Hospital E.v.Behring/Lungenklinik Heckeshorn, Berlin); T. Welte (Medizinische Hochschule Hannover, Hanover). Italy: F. Blasi and S. Aliberti (Instituto Malattie Respirattorio, University of Milan, Instituto di Recerca e Cura a Carattere Scientifico, Policlinico, Milan); R. Cosentini (Policlinico, Milan); D. Legnani (Ospedale L. Sacco, Milan); G. Cervi (Policlinico di Modena, Modena); P. Rossi (S. Maria della Misericordia, Udine). Spain: A. Torres (Instituto de Neumonologia y Cirugia Toracica, CIBER Enfermedades Respiratorias, Barcelona); D. Portela Ojales (Hospital Xeral-Cies, Vigo); M. Bodi (Hospital Universitario Joan XXIII, Tarragona); J. Porras (Hospital Sant Pau i Santa Tecla, Tarragona); J. Rello (Critical Care Department, Joan XXIII University Hospital, CIBER Enfermedades Respiratorias, University Rovira and Virgili, Tarragona); R. Menendez (Pneumology Service, Hospital Universitario La Fe, CIBER Enfermedades Respiratorias, Valencia). Switzerland: D. Stolz (Universitatsspital Basel, Basel). UK: J. Chalmers (Royal Infirmary of Edinburgh and Western General Hospital, Edinburgh); T. Fardon (Ninewells Hospital, Dundee). Argentina: G. Benchetrit (IDIM A. Lanari, Buenos Aires); E. Rodriguez (Hospital Espanol de La Plata, La Plata); J. Corral (Hospital Dr Oscar Alende, Mar del Plata); J. Gonzalez (Hospital Enrique Tornu, Buenos Aires); L. de Vedia (Hospital Francisco J. Muniz, Buenos Aires); G. Lopardo (Profesor Bernardo Houssay Hospital, Buenos Aires); C. Luna (Hospital de Clinicas, Buenos Aires); J. Martinez (Instituto Medico Platense, La Plata); L. Marzoratti (Sanatorio 9 de Julio, Tucuman); M. Rodriguez (Hospital Rodolfo Rossi, La Plata); A. Videla (Hospital Universitario Austral, Buenos Aires); F. Saavedra (Sanatorio Otamendi Miroli, Buenos Aires); H. Lopez (Centro de Infectología, Buenos Aires); M. Gnoni (Sanatorio Central EMHSA, Bueno Aires); J. Gonzalez (Hospital Enrique Tornu, Buenos). Chile: P. Jimenez (Hospital Clinico Regional, Santiago); P. Fernandez (Instituto Nacional del Torax, Santiago); M. Parada (Clinica las Condes, Santiago); A. Díaz Fuenzalida (Pontificia Universidad Católica de Chile, Santiago); R. Riquelme (Hospital de Puerto Montt, Puerto Montt); M. Barros (Hospital Carlos van Buren Hospital, Valpraiso). Guatemala: J. Manuel Luna (Hospital Nacional Roosevelt, Guatemala City). Panama: I. Toala (Complejo Hospitalario Dr Arnulfo Arias Madrid, Panama City). Paraguay: G. Arbo Oze de Morvil (Clinica San Roque y Centro Médico La Costa, Asuncion). Uruguay: G. Aiello (Maciel Hospital, Montevideo). Venezuela: F. Arteta (Hospital Luis Gomez Lopez-Ascardio, Barquisimeto); J. Delgado (Hospital Central Dr Urquinaona, Maracaibo); G. Levy (Hospital Universitario de Caracas, Caracas); L. Rivero (Hospital Central University Antonio M. Pineda, Barquisimeto); B. Rodriguez (Hospital IVSS Dr Domingo Guzman Lander, Barquisimeto); M. Perez Mirabal (Hospital Universitario de Los Andes, Merida). Philippines: M. Mateo (University of Santo Thomas Hospital, Manila); M. Mendoza (University of the Philippines and National Kidney and Transplant Institute, Manila). South Africa: C. Feldman (Johannesburg Hospital, Johannesburg).
脚注
可以从本文的补充材料www.www.qdcxjkg.com
感兴趣的语句
没有宣布。
- 收到了2012年3月15日。
- 接受2012年6月30日。
- ©2013人队















