摘要
的QuantiFERON微管(QFT-MT)的性能,用0.9毫升的血液,和的QuantiFERON-TB金在管试验(QFT-IT)(3毫升血液),用于诊断结核病(TB)的在儿童和成人进行比较特有的设置。
在152名儿童疑似TB和87个成人确诊的TB,QFT-IT与两种QFT-MT浓度(QFT-MT A和B)进行比较。的正面和不确定的结果的比例,干扰素(IFN)-γ的响应,批间协议和灵敏度进行了评估。
我们发现了相似比例的不确定结果,IFN-γ水平和可比较的敏感性。所有儿童的分析间一致性均为中度(QFT-IT)相对QFT-MT A:85%,K = 0.44和QFT - 它相对QFT-MT B:88%,K = 0.50)和成人(QFT-它相对QFT-MT A:88%,K = 0.50和QFT-它相对QFT-MT B:89%,k = 0.49)。与成人(分别为83%,86%和88%)的儿童,敏感性低(QFT-it 23%,QFT-MT为18%和B 19%)(分别为83%,86%和88%)。
QFT-MT检测可以可靠地执行,使用少于三分之一的血容量使用QFT-IT。减少的体积可能对儿童结核病的研究和未来诊断有用。IFN-γ释放试验在地方病环境下免疫不成熟或受损的重症儿童中敏感性差和不确定率高,值得进一步研究。
据估计,儿童占TB流行区域总结核病(TB)负担的10-20%,例如坦桑尼亚和诊断儿童活性结核病的工具受到限制,这都是关于性能的限制[1]以及在大多数结核病流行地区获得工具的机会,如胸部x线摄影、结核菌素皮肤试验(TST)、显微镜检查和培养[2那3.];迫切需要新的诊断工具,特别是儿科结核病[4.].
干扰素(IFN)-γ释放试验(IGRAs)在世界范围内越来越多地被用作TST诊断感染的替代方法结核分枝杆菌[5.].这些测试检测到感染结核分枝杆菌和它们的主要用途是在诊断潜伏性结核感染。然而,IGRAs使用由临床医生在活性的TB的诊断的附加工具[6.那7.];IGRA可以是幼儿中有用的诊断工具,因为非常幼儿中的一个积极的IGRA反映了最近的暴露,从而强大的活跃结核病风险。
有两种可商购的IGRAS,Quantiferon-TB金管(QFT-it; Cellestis Ltd,Chadstone,Australia)和T-Spot-TB(T-Spot; T-Spot; Oxford Immunotec,英国)。QFT-它测量全血释放的IFN-γ的水平,以应对刺激结核分枝杆菌- 特异性早期分泌的抗原(ESAT)-6,培养滤液蛋白(CFP)-10和TB7.7抗原,而T-斑点使用ELISPOT方法鉴定对ESAT-6和CFP-10响应ESAT-6和CFP-10的纯化淋巴细胞的数量。QFT-它涉及3ml静脉血液的收集(三毫升进入三个管中的每一个),并且T-斑通常需要8毫升血液。广泛使用这些测试可能受到所需血量的限制,特别是在婴儿和幼儿中的血液[8.那9.],临床医生可能被劝阻使用这些测试[10.].
为了解决这个问题,Cellestis已经开发了一种QFT的原型版本,其总共需要0.9毫升血液(Qualliferon-MicroTube(QFT-MT))。QFT-MT的原理与QFT-IT相同。来自患者的全血液在包含的管中孵育结核分枝杆菌-特异性抗原,然后用ELISA技术检测IFN-γ水平。QFT-MT的性能和可行性尚未在临床环境中进行评估。
这项研究的目的是,IT QFT通过比较正,负比例和不确定的结果,IFN-γ,批间协议和灵敏度的水平在儿童和成年人诊断活动性结核病,以确定是否QFT-MT是适当的替代品的区域中,其中TB是特有的。此外,QFT-MT的实际执行情况进行评估。
材料和方法
研究环境和人口
研究参与者是从2008年12月至2010年5月Muheza指定的地区医院(坦加,坦桑尼亚)前瞻性招募的。该医院的集水区有277 000人,2009年该区结核病检出率为每10万人348人[11.那12.].有疑似活动性结核病症状和体征的15岁以下儿童(表1)被列为对QFT-IT的小儿诊断活动性结核病[性能更大的医院为基础的研究的一部分13.].年龄≥15岁,痰涂片阳性,经荧光显微镜或培养证实的结核病患者,根据《结核学杂志》的标准从医院结核病门诊纳入表1.作为[13.], 152名符合纳入标准并有QFT-IT和QFT-MT配对结果的儿童和87名成人连续入选。所有研究参与者提供了微生物检查样本,并进行了HIV和TST检测。
标准化的问卷,用来记录参与者的人口统计学和临床细节。孩子们在2-和6个月的随访用于诊断和分类的确认到诊断组评估。
INF-γ释放测定
在注射器中收集静脉血,并根据制造商的说明立即分配到QFT-IT和QFT-MT管中。将1mL分配到每个QFT- IT管中,并进入每个QFT-MT管中的每一根300μL。将管在4小时内取向实验室,并在37℃下孵育16-24小时。两种Igras包括预涂层管:含有盐水作为阴性对照的含氮管;含有Phytohaemaglutinin作为阳性对照的丝分裂管;和含有肽Esat-6,CFP-10和Tb7.7的Tb-抗原管。用两种不同浓度的ESAT-6,CFP-10和TB7.7测试QFT-MT原型在指定的TB-抗原(AG)A和TB-AG B中,含有1μg·mL的管中-1和3μg·ml-1每个肽分别具有QFT-MT A或B. QFT-MT A或B的测试结果。QFT-它为1μg·mL-1.对于10名患者(七个儿童和三名成人),由于TB-AG B管的短缺,仅使用TB-AG QFT-MT原型进行了测试。
孵育后立即将样品离心,上清液保存在-70℃,直到在坦桑尼亚姆贝亚NIMR-Mbeya医学研究中心使用QFT-IT ELISA检测IFN-γ。根据制造商的说明书,QFT-IT、QFT-MT A和B结果被报告为阳性、阴性或不确定,QFT-MT A和B使用相同的标准解释。并记录定量结果。
我们收获血浆样品之前使用微量离心(5418的Eppendorf),用于QFT-MT管离心3分钟,在10 000rpm下。检查技师经历没有问题而不破坏沉淀除去血浆,即使微管不包含在所用的分离胶QFT-IT管中。该微量打破了只在数据收集之前的结论。因此33个样本(22名儿童和成人11)是用标准的实验室离心机(Vulcon技术CS6C),这导致从颗粒中的等离子体的同样良好的分离离心。
结核菌素皮试
两个单位的纯化蛋白衍生物RT23从Staten血清研究所(哥本哈根,丹麦),使用制造商推荐的Mantoux技术皮内给药。经专门训练的工作人员在48-72小时后以毫米为单位记录硬化的横向直径。≥10 mm的硬化被认为是阳性的,除非HIV感染,在这种情况下≥5 mm的硬化被认为是阳性的。
结核病诊断
结核病诊断如[13.].在简短的痰样品从成人收集,收集对孩子们连续三个早晨无论是痰或胃洗样品并送了验证镜检和培养中央结核病参比实验室(CTRL)(达累斯萨拉姆,坦桑尼亚)。用于荧光显微镜和罗氏固体培养基培养金胺染色。对 - 硝基苯甲酸,其抑制结核分枝杆菌但不是非结核分枝杆菌,阳性样品中加入排除非结核分枝杆菌。
每个孩子被分为“确诊”、“极有可能”、“可能”和“非结核病”四组。根据微生物学资料、胸片结果、研究组临床检查及随访资料(表2),这符合最近关于儿童结核病分类的专家共识[17.].只包括具有完整后续数据的儿童。仅包括Ziehl-Neelsen染色的阳性显微镜诊断为TB的成年人,以及通过正荧光显微镜或阳性培养的确认。
数据管理和统计分析
对数据进行双重输入到使用MS-访问(微软,亚历山大,弗吉尼亚州,美国),包括错误,范围和一致性检查程序的数据输入数据库。统计分析采用STATA(; StataCorp,科利奇站,TX,USA释放10)进行的。对于两个比例抽样测试被用来比较的正,负和不确定结果的比例。魏氏的匹配,对符号检验被用来比较IFN-γ中位数水平,数据的对数变换后。κ统计数据被用来评估QFT-IT和QFT-MT之间的一致性。的κ值根据兰迪斯规模解释[18.].对于数据分析,以“微生物学确诊结核病”和“非常可能的TB”孩子们被分为一组。HIV状态,年龄<2年和营养不良状态,如由z得分确定≤-2或身体质量指数(BMI)<18.5公斤·米-2,对于阳性或不确定的IGRA结果,采用logistic回归分析进行危险因素分析。p值<0.05被认为是显著的。
道德
该研究方案经坦桑尼亚医学研究协调委员会(NIMR / HQ / R.8a /卷IX / 584),并得到了丹麦中央伦理委员会的评估没有任何异议。以积极的HIV测试参与者伴随着艾滋病毒诊所复诊。报告诊断准确性研究的标准(STARD)随访结果报告(www.stard-statement.org).
结果
研究人群
共有152名结核症状和体征可疑的儿童和87名确诊的结核成人符合条件(表3).两个孩子分别为阳性结核分枝杆菌25例符合高度可能结核病标准,27例为“确诊或高度可能结核病”,59例为“可能结核病”,66例为“非结核病”。在87名成年结核病患者中,68人通过荧光显微镜和阳性培养确诊,15人仅通过显微镜确诊,4人仅通过培养确诊。
qft-it和qft-mt结果
总的来说,三种测试(QFT-IT、QFT-MT A和QFT-MT B)的结果没有差异。在152名儿童中,我们发现20(13%)阳性,93(61%)阴性,39(26%)不确定QFT-IT结果(无花果。1A).QFT-MT A和QFT-MT B的结果相似,17(11%)和17(12%)阳性,100(66%)和93(64%)阴性,35(23%)和35(24%)分别不确定结果。比较QFT-IT,QFT-MT A和QFT-MT B之间的阳性,阴性和不确定的响应者的比例,儿童或成人中的任何测试之间没有显着差异,使用双样本比例测试计算。七个孩子(具有确认的TB)和三名成年人只有QFT-MT的结果,但没有QFT-MT B的结果。
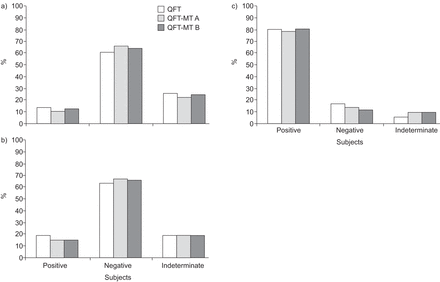
a)用抗原A(QFT-MT A)和QFT-MT中的Qualtiferon-TB金中管(QFT-IT)和QFT-MT的Qutiferon-MicroTube(QFT-MT)的比较具有疑似结核病(Tb)(n = 152),b)具有证实Tb(n = 87)的确认或高度可能的Tb(n = 27)和c)的儿童(n = 87)。
显示有确诊或高度可能的TB和成人儿童的阳性,阴性和不确定结果的比例图1b及c.在87名具有“确认的TB”的成年人中,69(79%)具有阳性,14(16%)阴性,四(5%)不确定QFT- IT结果,同时为QFT-MT A和B有68(78%)67(80%)阳性,11(13%)和九(11%)阴性和八(9%)和8(10%)不确定的结果。
批间协议
QFT-IT与QFT-MT A和B型儿童和成年人的协议的实力适中(表4).
中位数干扰素-γ的水平
QFT-IT管中IFN-γ中位水平较高结核分枝杆菌在所有152名儿童QFT-MT(p≤0.03)相比,特异性抗原(表5)在可能的Tb的59名儿童中,与QFT-IT相比,QFT-MT中的中值IFN-γ抗原反应较低(P = 0.04)(表5).QFT-MT A组和b组TB抗原涂层管中IFN-γ水平无差异。在所有儿童中,不论诊断分类分组如何,在无或有丝分裂原管中IFN-γ水平中位数均无差异(数据未显示)。
在成人中,这三个测试之间的唯一差别是与所述的管(P <0.01)相比,在抗原刺激后显著较高的平均IFN-γ水平在QFT-MT B中。
IGRAS和TST对活跃结核病诊断的敏感性
在排除不确定的结果后,具有确认或高度可能的TB的儿童和可能结核病的儿童令人惊讶地低,但三次测试之间没有显着差异(表6).在146名可用TST检测的儿童中发现了同样低的TST敏感性,在25名确诊或极有可能结核的儿童中有2名(8%)TST呈阳性,在51名可能结核的儿童中有4名(8%)(数据未显示)。在87名确诊结核病的成人中,IGRAs的敏感性在83%至88%之间(表6),两种测试的灵敏度没有差别。在71例有效TST结果的成人中,TST的敏感性为87%(71例中62例)(数据未显示)。
危险因素分析
我们发现低灵敏度和儿童高度不确定率与成年人相比。(数据未显示)既不HIV感染,年龄<2年也不营养不良被显著与QFT-IT,QFT-MT A或QFT MT乙阳性或在此亚组不确定的结果相关联。在较大的队列研究包括211名儿童,年龄<2年与增加的一个不确定的结果的可能性[相关联13.].
在成人中,在调整年龄和BMI后,HIV感染与阳性QFT-呈阳性QFT-敏感(调节或0.21,95%CI(0.06-0.71); P = 0.01)和阳性QFT-MT A(0.23(0.06-0.89); P = 0.03),但不是QFT-MT B(0.41(0.10-1.78); p = 0.24)(数据未显示)。
讨论
QFT-IT和QFT-MT A和B表现出相当的性能。TB-犯罪嫌疑人的孩子在QFT-IT有IFN-γ的较高的平均水平比QFT-MT管都抗原包被的管,但也有阳性,阴性和不确定结果的比例相似,灵敏度没有差别。试验大多有IFN-γ的类似定量水平,不同之处在于具有较高的抗原浓度(QFT-MT B)的QFT-MT管,似乎在成人比QFT-MT的管稍好执行,相对于中值抗原特异性IFN-γ,但同样的整体测试性能是相似的。
两种试验之间的测定一致性是中等的,这反映了相当大的测定间变异性。在阳性结果的临界值附近IFN-γ水平的变化可能是造成这种差异的原因,特别是在艾滋病毒感染者和幼儿中,他们对特定抗原的IFN-γ水平可能较低。来自纽约的一项研究[19.]已经表明,较低的临界值对于正QFT-IT可能是这些孩子有关,但这也将导致增加批间差异。
与QFT-IT一样,QFT-MT A和B在这一负担沉重的环境下,在识别活动性结核病儿童方面的表现似乎非常有限,敏感性低(介于18-23%之间),不确定率高(高达26%)。在成人结核病患者中,QFT-MT格式与QFT-IT测试具有高灵敏度和低不确定率。据我们所知,这是首次发表的关于QFT-MT性能的研究。我们的结果在QFT-MT(1和3 μg·mL-1)具有与QFT-IT (1 μg·mL)相当的性能-1)无论是在儿童和成人暗示有可能降低血液中不失精确度活动性结核病的诊断,可能也为潜伏性结核感染得出的体积。
IGRAs可以被认为是最准确的潜伏结核病诊断测试,并解决了TST的两个主要局限性,低特异性和逻辑挑战,测试必须在应用后2-3天阅读。尽管IGRAs比TST有所改进,但在实施IGRAs方面仍存在重大障碍,特别是在资源匮乏的环境中,需要当地的培养箱、附近的实验室或用于储存、运输和ELISA的冷冻能力。在资源高和资源低的地区都需要更简单、更安全和更灵活的解决方案。在儿童和婴儿中,血液量可能会限制QFT-IT的使用,特别是在父母/监护人不愿从孩子身上抽血或医生不愿抽血的情况下。减少血量可能有助于大规模和个别的检测。预计将对IGRAs进行许多改进,IE。使用其它生物标志物,如IFN-γ诱导蛋白(IP)-10,其可以被存储在滤纸上,护理测试点和系统中的“芯片上的实验室”测试系统[20.].我们的结果可能为基于更少量血液的改进测定方法的发展铺平道路。
我们发现低灵敏度和QFT-IT的高不确定率,如在较大的队列研究评估儿童结核病在坦桑尼亚[诊断使用QFT-IT的13.以及QFT-MT A和B在儿童中的作用。
在这一人群中的敏感性低于报道的一些研究[21.[其他研究中报道的高度不确定率[22.那23.].高不确定率和低灵敏度归因于宿主因素,如年幼[22.那24.那25.],HIV感染随CD4计数[26.-28.],营养不良和蠕虫感染[29.-31.].对这些病重儿童的误诊或过度诊断也可能是敏感性差的原因,或者是技术差。
风险因素分析表明,低敏感性和高不确定率不能用任何一个单一因素来解释,而是由导致t细胞反应受损的因素组合而成,如营养不良、疾病严重程度、艾滋病毒感染、年轻和免疫不成熟[13.].
低灵敏度表明,在这种环境中,不能推荐使用IGRAS以及TST,并且最近尚不指出,世界卫生组织最近认为IGRA和TST都应该用于诊断活性TB疾病的诊断- 以及中等收入国家[32.].然而,在高收入,低结核病国家,IGRAS在潜伏的结核病诊断和儿童活跃结合的诊断处理中发挥着重要作用,与微生物方法结合。在该设置中,QFT-MT可以是有用的低血量替代方案。
对儿童表现不佳的另一种解释可能是不充分的技术或实验室错误。但与儿童相比,所有IGRAS在成年人中表现良好,因为QFT-IT和QFT-MT样本在使用相同的实验室工作人员,设备上同时进行并加工,并在同一医院进行加工和加工和标准的操作程序,我们发现,由于技术错误,儿童的表现差不太可能。
微管格式有一些限制,但很少有限制。血浆的量是有限的,如果需要确认结果或评估试验内的可变性,可能几乎没有重新运行样本的空间。在我们的研究中,没有QFT-MT样本被重新运行,但我们预计变化类似于QFT-IT。这是一个值得关注的问题,关于如何解释逆转、转化和边缘的积极和消极结果有一个持续的辩论[33.],如果应该向前应考虑QFT-MT格式,则必须考虑。报告的一个实际问题是,在管上写识别细节的空间非常小,否则研究团队发现易于使用QFT-MT格式。
使用注射器通过瓶盖填充试管没有问题,并且有一条黑色的线清楚地标记为300 μL。尽管制造商推荐使用微离心机来分离QFT-MT管中的等离子体,但由于微离心机的故障,我们不得不使用标准实验室离心机来分离少量样品。这被发现同样适用于从球团中分离上清。因此,它应该是可能的过程的QFT-MT管与QFT-IT完全相同的设备。
结论
总体而言,使用的血0.9毫升QFT-MT测试的性能等于QFT-IT测试使用3毫升的血液。有正,负和不确定结果的比例之间没有差异,有良好批间协议。的QFT-MT试验以1μg性能·毫升-1,3μg·ml-1用在3微克朝向更高的IFN-γ水平的趋势相称·毫升-1管在成人中。从技术上讲,QFT-MT几乎不需要适应,并且没有报告显着的实际困难。
mictrotube格式有潜力作为一个低血容量测试和这些有前途的初步结果应该刺激进一步的大规模调查,而高不定率和灵敏度差的干扰素释放在重症患儿不成熟或受损免疫在高负担环境需要进一步调查。
据我们所知,这是对QFT-MT的业绩首次公布的研究报告和观点可能会进一步减少出血量,IE。在一个关心点测试。
致谢
作者要感谢Muheza指定地区医院(Muheza,坦桑尼亚)的患者和家长/监护人、工作人员和管理人员为这项研究提供了便利。还感谢B. Amos (Teule医院)和NIMR-Mbeya医学研究方案的实验室工作人员在实验室问题上提供的宝贵帮助、区域和地区结核病协调员L. Kijazi(坦桑尼亚坦加地区Bombo医院)和M. Fadhili(坦加Muheza指定地区医院,Muheza区,坦加,坦桑尼亚)的援助和支助性监督,以及疟疾联合方案的行政支助。
脚注
支持声明
这项研究是由IMPACT-TB项目资助的,作为博士论文的一部分。Reinholdt Jorck的国际卫生集群基金也提供了资金哥本哈根大学(211- 0357/07-3012),雄辩基金,丹麦研究委员会(09- 064923)、KNCV (U.07.0674)和丹麦国际发展援助(74-08-UHH DANIDA)。Cellestis接受了研究方案,并提供了QuaniFERON微管、ELISA试剂和微离心机,但Cellestis并未参与研究手稿的设计、结果分析或撰写。
感兴趣的语句
没有宣布。
- 已收到2011年11月7日。
- 公认2012年7月11日。
- ©2013年















