摘要
端粒酶逆转录酶(叔)或端粒酶RNA (, TERC)基因突变是肺纤维化的主要单基因原因。测序的叔/, TERC基因被建议用于家族性肺纤维化患者。很少有人知道这种突变的可能预测因素及其对预后的影响。
我们回顾性分析了2007-2014年间肺纤维化患者的所有遗传诊断。我们评估了叔/, TERC疾病相关变异(DAV),与DAV相关的因素,以及DAV对生存的影响。
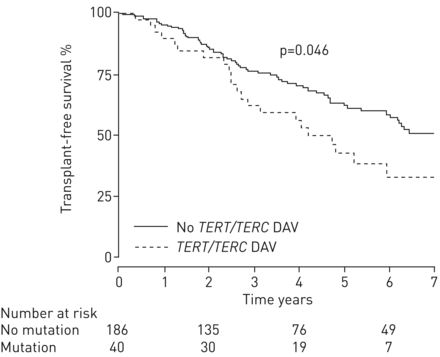
237例肺纤维化患者(153例为家族性肺纤维化,84例为端粒综合征特征,无家族性肺纤维化)进行了检测叔/, TERCDAV。40例患者(16.8%)诊断为DAV,其中5例为非特发性间质性肺炎。普遍存在的叔/, TERCDAV在家族性肺纤维化或只有端粒综合征特征的患者之间没有显著差异(18.2%)与16.4%)。年龄小、红细胞增多、血小板计数低与DAV的存在有关;40-60岁患者发生DAV的概率增加。无移植生存率与无移植生存率相比较低叔/, TERCDAV (4.2与7.2年;p = 0.046)。
叔/, TERCDAV与特定的临床和生物学特征相关,并降低无移植生存率。
摘要
肺纤维化患者叔/, TERC疾病相关变异显示无移植生存期降低http://ow.ly/EmYs304atGl
简介
间质性肺疾病(ILD)的遗传背景以特发性肺纤维化(IPF)的患病率为特征,在一般人群中为0.02%;然而,2-20%的IPF患者来自ILD家庭[1,2].家族性IPF的遗传学研究发现端粒酶逆转录酶(叔)和端粒酶RNA (, TERC),两者都是正常端粒酶活性所必需的[3.,4].杂合突变叔/, TERC在家族性ILD患者中有~ 15%被检测到,但在散发性IPF患者中很少被检测到(<3%)[3.- - - - - -5].突变叔/, TERC也与肺外异常有关,被评估为端粒综合征,涉及皮肤、肝脏和血液异常[6- - - - - -8].即使在具有相同突变的患者中,表型也可能是异质的[9].此外,多态在MUC5B与IPF密切相关,无论是散发的还是家族性的[5,10,11].
2011年IPF国际指南不建议在了解状态下进行基因检测,但2013年特发性间质性肺炎国际指南和法国实用指南建议在家族性肺纤维化(FPF)患者中搜索基因异常[12- - - - - -14].然而,叔/, TERC需要澄清突变检测的适应症,以及这些突变的临床影响。这项研究的目的是评估的患病率叔/, TERC在一个疑似ILD的国家队列中发生突变叔/, TERC在法国进行基因突变研究,以寻找预测这些突变的因素,并评估它们对生存的影响。
方法
病人
这是一项回顾性、观察性、非介入性研究。所有转介至叔/, TERC本研究筛选了2007年至2014年1月在法国巴黎Bichat医院基因实验室进行的测序。这个实验室是法国的参考设施叔/,TERC突变检测,属于一个网络,包括成人和儿科中心,对罕见肺部疾病特别感兴趣。在本研究中,我们纳入了所有ILD和疑似先证者叔/, TERC突变。所有患者均由肺科医生进行ILD的遗传诊断。转诊为先天性角化不良的患者不包括在内;然而,在回顾临床图表时,1例患者符合先天角化不良标准,未被排除[15].肝肺综合征患者不包括在这项研究中。
对患者的临床图表进行审查,并使用标准化和匿名收集表格收集数据。特别评估了个人和家族肺部疾病(特别是ILD)、血液系统疾病(包括异常血细胞计数)、肝脏异常(反复不明原因的肝酶水平升高或肝脏疾病)和个人皮肤异常(30岁前头发变白、皮肤色素沉着、口腔白斑和指甲营养不良)的病史。在ILD诊断时收集标准生物学检测结果。红细胞大细胞症定义为平均红细胞体积>100 fL,血小板减少症定义为血小板计数<150 g·L−1根据世界卫生组织的定义[16].在这项研究中,个人或家族性肝脏或血液疾病和个人皮肤症状被认为是肺外受累。
根据2011年美国胸科学会(ATS)/欧洲呼吸学会(ERS)/日本呼吸学会(JRS)/拉丁美洲胸科学会(ALAT)关于IPF的官方声明,肺部诊断基于多学科团队讨论,包括临床数据、肺高分辨率计算机断层扫描(HRCT)和病理评估[188bet官网地址14,17]及修订后的特发性间质性肺炎分类[13].在本研究中,经多学科讨论后被诊断为IPF的ct扫描可能为常规间质性肺炎,但没有可用的组织学资料的患者被归类为IPF。系统地考虑了职业或家庭接触吸入的纤维原性颗粒(如石棉)或可能与慢性超敏性肺炎相关的抗原(如慢性接触鸟类或霉菌)(见在线数据补充),以及根据公开可用的数据库使用与肺纤维化相关的药物(www.pneumotox.com).烟草烟雾暴露量被量化。收集ILD诊断时肺功能检查结果。死亡和肺移植数据收集至2015年9月1日,随访丢失的病例除外。
根据法国的国家规定,所有患者或亲属都签署了生殖细胞遗传分析的同意书。法国呼吸医学学会机构评审委员会(Société de Pneumologie de languue Française)批准了这项研究(CEPRO 2015-020)。
基因分析
测序方法在在线数据补充中介绍。患者叔而且, TERC罕见变异是根据美国遗传学和基因组学学院的指导方针和欧洲人类遗传学学会的建议分类的[18,19].简单地说,有五种头部类型的变异:致病性,可能致病性,不确定意义(VUS),可能良性和良性。在可用的情况下使用以下支持、中等或强标准:变体的性质(非常强到支持)、先前的报告(强)、种群数据(中等)、分离数据(强到支持)、作为功能数据的端粒长度(支持)、计算和预测数据,如多肽或组合注释依赖消耗(CADD)评分(支持)和特定表型(支持)。将一个中等致病性标准和四个或四个以上的支持致病性标准结合起来,可得出可能致病性的结论[18].在VUS组中,具有一个中度标准和三个支持标准的变异被认为是VUS可能与疾病相关(VUSD)。所有其他VUS均被认为是可能良性的VUS (VUSB)。被分类为致病性、可能致病性和VUSD的变异被保留为疾病相关变异(DAV)。
统计分析
连续变量用中位数(极差)表示,用t检验进行比较。分类变量用n(%)表示,采用卡方检验进行比较。患者的比较叔/, TERC由于样本量小,突变涉及非参数检验。
由于大量患者接受了肺移植,传统的生存分析中,接受肺移植的患者在移植时将被审查,这将提供有偏见的估计(信息审查)。因此,我们将死亡或移植(无移植存活)的时间作为我们的主要终点。研究的起点是ILD诊断的日期。使用单变量和多变量Cox模型评估基线协变量对无移植生存的影响。中心内观测值的相关性由分组Jackknife估计器解释[20.].
与此相关的因素叔/TERC DAV通过比较携带者和非携带者以及拟合单变量和多变量logistic回归模型进行检验。采用广义估计方程模型对中心效应进行了解释。使用具有集群选项的coxph函数(生存包)计算Cox模型,使用gee函数(gee包)计算logistic模型。所有检验均为双侧检验,p=0.05,有统计学意义。所有分析均使用R软件(2.15.2版本;www.r-project.org).
结果
病人
2014年1月1日,对237名ILD先证者(153名FPF患者和84名非FPF患者肺外受累)的DNA进行了疑似检测叔/,TERC突变,包括先前报道的11例患者[21- - - - - -23) (图1).平均年龄为61.3岁(21.4-92.6岁),男性居多(71.4%)(表1).最终肺部诊断为IPF (n=97),可能、可能IPF或IPF工作诊断(n=73),怀疑特发性非特异性间质性肺炎(n=12),慢性超敏性肺炎(n=13),药物性肺炎(n=4),脱屑性间质性肺炎(n=3),呼吸道性细支气管炎合并ILD (n=1),胶原性血管疾病相关ILD (n=17:类风湿关节炎,n=6;Sjögren氏综合征,n=5;未分化性结缔组织病,n=2;系统性硬化症,n=1;纤维化伴抗中性粒细胞细胞质自身抗体相关血管炎,n=2;系统性红斑狼疮(n=1)、尘肺病(n=3)、特发性胸膜实质纤维弹性增生(n=2)、隐源性组织性肺炎(n=1)、肺泡蛋白沉着症相关肺纤维化(n=1)、不可分类纤维化(n=10)。共纳入195例特发性ILD患者,其中IPF 170例,继发性ILD 42例。
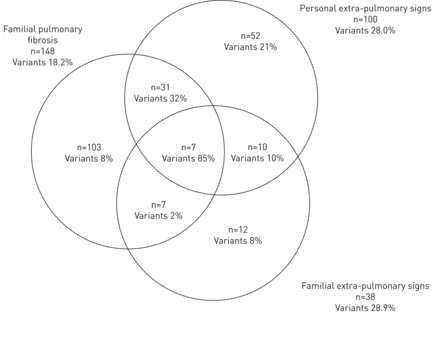
研究中的先证者包括导致怀疑突变的因素和每组中疾病相关变异患者携带者的百分比。
关于肝脏和血液疾病以及皮肤症状的详细信息在在线数据补充中。
航空公司的叔/, TERC突变
遗传学
我们鉴定出31个(13.0%)先证物具有致病性或可能致病性叔/,TERC变异,26个(10.9%)内叔5个(2.1%), TERC(表2和E1)。9个变种被归类为VUSD, 11个变种被归类为VUSB。作为致病或可能致病的患者携带者叔/,TERC变异与VUSD患者携带者组无明显差异,两组均被收集,称为患者携带叔/, TERC并与无任何变异组进行比较。VUSB内的运营商叔或, TERC未纳入进一步分析。在3、2、2和2先证物中分别发现了4个多次出现的超稀有变异(表E1)。据我们所知,他们都不是亲戚,因为他们没有相同的名字,也不是来自同一个地区。
图1显示患者的比例叔/,TERC存在FPF和/或肺外受累的DAV。在FPF患者中,突变比例为18.2%。有FPF和肺外体征的患者发生突变的比例最高(38例中有16例(42.1%))。
患者叔/,TERC对DAV进行基因分型MUC5Brs35705950多态性。小等位基因(高危)的频率MUC5B多态性在74人中占19 (25%)叔/,TERCDAV和DAV均大于对照组(n=1229, 10.8%;p = 8×10−66),但低于法国IPF队列(n=142, 41.9%;(p = 0.02)5].
端粒平均长度显著缩短, TERC与DAV载体相比叔DAV携带者或对照组分别为4.7 kb、7.1 kb和7.6 kb (p=0.01和p=0.002)(图E1a)。与正常值比较,所有患者均有, TERCDAV和11例致病性或可能致病性患者叔变体显示端粒长度缩短。在承运人内叔DAV患者自述为第二代患者,其端粒比第一代患者更短(p=0.02)(图E1b)。
肺的参与
带菌者的平均年龄(范围)叔/,TERCDAV为57岁(36-79岁)(表2).大部分(55.2%)为吸烟者,42.1%长期暴露于潜在的肺毒性粉尘(石棉、金属、木材、鸟类、霉菌、等。);73.6%为吸烟者或有慢性肺毒素接触史。最终肺部诊断为IPF (n= 24,60.0%)、不可分类的纤维化性ILD (n= 7,17.5%)、慢性超敏性肺炎(n= 3,7.5%)、疑似特发性非特异性间质性肺炎(n= 4,10.0%)、类风湿关节炎相关的ILD (n= 1,2.5%)和药物性ILD (n= 1,2.3%)。因此,5例患者(12.5%)表现为继发性ILD(过敏性肺炎、结缔组织疾病或药物诱导)。
肺外的参与
个人血液学异常有两种。共有12例患者仅出现血细胞计数异常,未发现骨髓疾病:血小板计数低(n= 6,15.0%),红细胞增多(n= 3,7.5%),或两者均有(n= 3,7.5%);在11例患者中,通过骨髓抽吸或骨髓活检确诊骨髓疾病:骨髓异常增生(n= 5,12.5%)、骨髓衰竭(n= 2,5.0%)、骨髓纤维化(n= 1,2.5%)和急性髓系白血病(n= 1,2.5%)。在随访期间,2例血小板减少症患者出现骨髓发育异常;1例患者患有急性髓系白血病和1例既往无细胞减少的骨髓增生异常。此外,JAK2的V617F突变在2例骨髓增生异常的患者中得到证实。
共有13例患者出现肝脏疾病:反复不明原因的肝酶升高(n= 5,12.5%)、非酒精性脂肪性肝炎(n= 4,10.0%)、特发性肝硬化(n= 3,7.5%)和局灶性结节性增生(n= 1,2.5%)。肝肺综合征没有明确的评估,也没有病例记录。
总体而言,11例患者出现皮肤异常:皮肤色素沉着(n= 5,12.5%)、头发过早灰白(n= 5,12.5%)、口腔白斑(n= 1,2.3%)和指甲营养不良(n= 1,2.3%)。总数大于11,因为患者可能会表现出几种症状。只有1例皮肤色素沉着、口腔白斑和指甲营养不良符合角化不良的先天标准。
的预测因素叔/,TERC突变
不同载体间差异无统计学意义叔或, TERC年龄、性别比例、吸烟、纤维性暴露、肺外体征、肺功能测试改变、组织学或HRCT模式或最终诊断的DAV。我们进一步比较了有无治疗的患者叔/, TERCDAV。
与没有的病人相比叔/, TERCDAV,那些有DAV的人更年轻,很少有IPF的诊断,更多的是有肺外体征(表2).
基于平滑样条的图支持在诊断年龄和患病概率之间的非线性关联叔/,TERCDAV;40 - 60岁患者成为携带者的概率高于年轻患者(<40岁)和老年患者(>60岁);不容易定义阈值(图2).HRCT模式、继发性ILD的存在以及肺功能测试评估的ILD严重程度与突变无关。
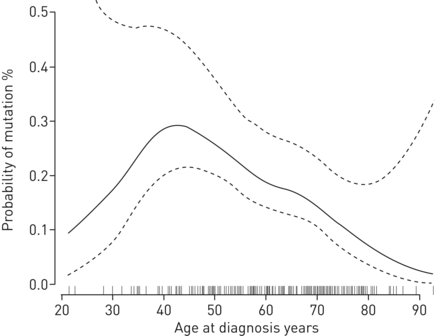
诊断年龄与端粒酶逆转录酶概率的相关性(叔)/端粒酶RNA (, TERC基因疾病相关变异(DAV)。基于平滑样条的图。年龄较小与DAV的存在显著相关,而DAV的概率与年龄之间没有线性回归。平滑样条曲线支持40 - 60岁患者DAV的可能性增加。
在多因素分析中,皮肤异常(p=0.006)、血小板计数低(p=0.05)、家族性肝脏疾病(p=0.01)和肺部疾病亲属数量(p=0.004)与发病仍有显著相关性叔/, TERCDAV。诊断时年龄与叔/, TERC该模型中的变量(p=0.21)。包括这5个变量的模型显示出公平的甄别,受试者工作特征曲线下面积(AUC)为0.74 (95% CI: 0.64-0.85)。因此,包括所有这5个变量的分数与单独的变量相比没有明显的优势。在最终模型的5个变量中,低血小板计数的鉴别能力最高(AUC为0.67(0.57-0.77))。
如果我们将分析局限于FPF患者亚组,年龄年轻(p=0.07)、肺部疾病亲属数量增加(p=0.06)、终身不吸烟(p=0.02)以及个人或家族肺外体征(p<0.0001)与肺外症状的存在相关叔/, TERCDAV。
生存
总体和无移植生存率
整个人群(n=226)的中位数(范围)随访时间为3.7年(0.1-18.4年)。随访期间,69例(30.5%)患者死亡,27例(11.9.0%)患者接受肺移植,其余130例(57.5%)患者在研究结束时仍然存活。
整个队列的中位无移植生存期(95% CI)为6.3年(5.1-8.1年)。3、5、10年无移植生存率分别为73.5%(67.4 ~ 80.0%)、58.99%(51.7 ~ 67.1%)、26.6%(17.1 ~ 41.3%)。中位数随访在带菌者和非带菌者之间无显著差异叔/, TERCDAV(3.3岁(0.4-13.8岁)与3.4年(0.1-18.4年);p = 0.90)。无移植生存率无明显差异MUC5BRs35705950多态性中的叔/,TERCDAV运营商。携带者的中位无移植生存期低于非携带者(4.2(2.9 -∞))与7.2(6.0-9.4)年;Log-rank检验p=0.046) (图3).患者移植的频率高于非移植的患者叔/, TERCDav(11人(30.2%)与16 (9.2%);p = 0.002)。移植年龄在携带者和非携带者之间没有差异(52.5岁与54.4年;p = 0.6)。
端粒酶逆转录酶携带者和非携带者无需移植(叔)/端粒酶RNA (, TERC基因疾病相关变异(DAV)。DAV携带者的中位无移植生存期降低(p=0.046)。
与无移植生存相关的因素
文中给出了基线测量变量与无移植生存之间的关系表3.的存在叔/, TERCDAV、男性、肺活量或肺对一氧化碳的扩散能力下降以及红细胞增多症和血小板减少症与无移植生存率降低显著相关。在包括年龄、性别、强迫肺活量和控制中心在内的多变量模型中,DAV的存在降低了无移植生存率(HR 1.92 (95% CI 1.15-4.13);p = 0.003)。当分析仅限于诊断为IPF的患者时,也发现了类似的结果(HR 2.36 (1.35-4.13);p = 0.003)。结果与普通间质性肺炎的ct扫描概率一致。
死亡原因
在69例死亡病例中,36例(52.1%)被认为与纤维化有关(终末期肺纤维化、急性加重或肺动脉高压),33例(47.8%)与纤维化无关(肝硬化、感染、难治性全血细胞减少、心力衰竭、中风、肺栓塞或未知)。对于顽固性全血细胞减少的患者,5个叔/, TERCDAV携带者死亡与2例非携带者(p=0.01)。两组因终末期纤维化而死亡的频率相似(17人中有5人死亡)与62人中有31人;p = 0.13)。
讨论
该系列是一个疑似单基因引起的ILD的国家队列,并对其进行了系统测序叔/,TERC以及许多参与中心(n=31)。在疑似患有叔/,TERCDAV,该系列显示:1)肺外受累和诊断时的年龄预测其存在叔/,TERCDAV, 2)叔/,TERCDAV可能与不同的肺部表型相关,包括非特发性ILD; 3) a叔/,TERCDAV与无移植生存率降低相关。
我们纳入了所有ILD和疑似患者叔/,TERC突变。特发性间质性肺炎的ATS/ERS/JRS/ALAT报告建议进行手术叔/,TERC对家族性ILD病例进行测序,不考虑肺外体征[13],而法国临床实践的国家建议也建议执行叔/,TERC肺外体征患者的测序[14,24].我们的结果支持更广泛的建议,因为FPF患者的突变率(18.2%)与没有家族性ILD发生但肺外受累提示端粒综合征的患者(16.4%)相似。这一检出率与以往FPF研究中观察到的检出率相似[3.,4].
总的来说,37.5%的患者叔/,TERCDAV有红细胞增多症,50.0%的血小板减少症和32.5%的肝脏异常,所有预测叔/, TERCDAV。叔/,TERC以往队列中DAV携带者出现肺外体征[9,25,26].例如,在同一个人或家庭中,与肺纤维化相关的骨髓衰竭被发现高度预测叔/, TERC突变(27].叔/,TERC突变与隐源性肝硬化、肝肺综合征、先天性角化不良和头发过早变白有关[7,28].先天性角化不良的典型三联征是指甲发育不良、皮肤色素沉着和口腔白斑[15].在审查图表后,一个病人符合标准,是,作为怀疑,携带者叔DAV。然而,据我们所知,ILD患者的血小板减少率或大细胞增多率叔/,TERC突变之前未见报道。端粒长度最短的受试者是, TERCDAV,提示这些患者外显率增加,端粒综合征风险增加[8].两者之间缺乏临床差异叔而且, TERC本研究中的DAV携带者可能与少量的, TERC包括DAV载体,需要进一步评估。
在目前的系列研究中,40例DAV患者中有5例被认为存在非特发性ILD,而非携带者组186例中有35例(p=0.34)。非ipf ILD可能有遗传背景。事实上,在114名诊断为慢性超敏性肺炎的患者中,17.5%的家庭成员患有肺纤维化,这一论点支持非特发性和特发性ILD之间的遗传连续统[29].此外,在29例ILD患者的手术标本中,Diaz德leon等.[9]报告了2例慢性超敏性肺炎。此外,我们和其他人最近报道RTEL1,PARN而且叔在FPF背景下,非特发性ILD(如结缔组织疾病相关的ILD、尘肺病、慢性超敏性肺炎)患者的突变[23,30.,31].这一系列证据表明,非ipf ILD和非特发性ILD应该表明,在ff或端粒综合征病例中需要进行基因检测。
近三分之二的叔/,TERC本系列DAV携带者报告吸烟或纤维性暴露。在一项美国队列研究中,来自21个家庭的134名患者叔突变,几乎所有ILD患者(96%)都是吸烟者或被宣布接触过肺毒性[9].叔/,TERC在病毒性或酒精性肝硬化系列中也报告了突变[32].此外,患有叔/,TERC在使用细胞毒性药物时,突变可在肺移植后出现严重的血液学并发症[23,33,34].总的来说,属于端粒综合征的疾病可被认为是多因素的,由强烈的遗传易感性和毒性暴露(如吸烟)导致ILD。
在目前的研究中,有移植的无移植存活率低于无移植的叔/, TERC单变量和多变量分析的DAV。在IPF的背景下,端粒长度先前与移植存活率降低有关[35].男性性别、肺功能测试结果、红细胞增多症和血小板减少症也与无移植生存率相关。评估存在竞争事件(移植)的患者的生存是棘手的。传统的方法(Kaplan-Meier估计)假设接受移植的患者的生存时间分布与未接受移植的患者的生存时间分布相同(无信息审查)。这种假设在这里显然是站不住脚的,而且这种方法高估了患者的“真实”生存率,因为随着时间的推移,病情最严重的患者会从数据库中删除。因此,我们将死亡或移植时间作为终点,并报告无移植生存期。
例如,与散发性IPF相比,整个队列的生存期似乎出乎意料地高(中位生存期7.3年),这清楚地表明人群疑似患有IPF叔/,TERCDAV是ILD患者的一个亚群体。在最大的一系列与肺纤维化相关的患者中叔迄今为止报道的突变,诊断后平均生存期为3年[9].然而,有报道称患有叔突变(一份报告27年)[36].此外,本系列中超过一半的患者没有IPF,而是有其他肺部诊断,如肺泡蛋白沉着症或超敏性肺炎,预后不太严重[37].患者可能因为有肺纤维化的家族病史而被尽早转诊,这可能会增加生存率。年龄与无移植生存期下降无显著相关性(p=0.11)。然而,相对年轻的患者经常被转诊进行肺移植,这导致该组的移植自由生存期降低。
我们的研究有几个局限性。由于研究的回顾性性质,一些数据缺失,可能存在中心偏差;然而,我们没有发现突变患病率或存活率的任何中心效应。其次,虽然端粒长度和端粒酶活性分析可能难以解释,但我们并没有通过功能分析或特异性转染来确认突变在蛋白质水平上的影响。38,39].然而,我们认为所有罕见变异都可能是致病突变,这在遗传诊断过程中是常见的,并提出了实际的建议,尽管鉴定因果变异是当前遗传学的一个挑战[18,19,40].以前有或没有功能分析或特异性转染的几个突变被报道过。尽管所有患者的Southern印迹分析中端粒长度没有减少,但预测致病评分(CADD评分和多酚)是有害的。另有四种基因被报道可导致端粒介导的肺纤维化:RTEL1,PARN,DKC1中而且TINF2[30.,31,41- - - - - -43].的确,在无移植组存活下来叔/, TERCDAV可能受到其中一个基因突变的影响[44].
总之,本系列研究表明,以FPF为特征或有提示端粒综合征的肺外体征的ILD患者,无论是特发性还是非特发性,都应该进行基因检测。然而,在没有结论性功能分析的情况下,增加患者和基因分析的数量也会导致未知意义的变异数量的增加,正如本队列中的一些患者所报道的那样。
确认
合作者:E. Magois, B. Toublanc (CHU d’Amiens, Amiens), A. Plessier(医院Beaujon, Clichy), A. Gondouin(医院Minjoz, Besancon), L. Savale(医院du kremin -Bicetre, Bicetre), d . Bouvry, B. Duchemann, A. Hervé, Y. Uzunhan, M. Zysman(医院Avicenne,博比尼),B. Gentil(医院Oudot, Bourgoin), P. Bonniaud, L. Olivier-Faivre (CHU de Dijon, Dijon), A. Mehdaoui(医院Eure Seine, Evreux), J. Le Pavec(中心外科Marie Lannelongue, Le Plessis Robinson), N. Pottier,B. Wallaert (CHRU de Lille,里尔),C. Khouatra, L. Kiakouama, J. Traclet, P-J。Souquet(里昂普拉德尔医院和南里昂医院),C. Gomez(马赛北医院),A. Bourdin, V. Moulaire (CHRU de Montpellier,蒙彼利埃),M. Aubier, O. Brugière, G. Dauriat, P. Dieudé, A. Marceau, M. Neuville, P. Pradère, C. Taillé(巴黎比哈特医院),L. Texeira(巴黎科琴医院),S. Feuillet, L. Galicier, G. Lorillon, E. Oksenhendler, R.P. de la Tour, F. Riviere, F.S. de Fontbrune . Tandjaoui(巴黎圣路易斯医院),M. Wislez, A. Olaiwan, H. Lioté(巴黎特隆医院),J.F. Boitiaux(医院Dubos, Pontoise), P. Delaval(医院Pontchaillou, Rennes), S. Dominique(医院尼科尔,鲁昂),S. Hirschi (Hôpitaux斯特拉斯堡大学,斯特拉斯堡),A. Didier, S. Ollier(医院Larrey,图卢兹),E. Manali, S. Papiris (Attikon大学医院,雅典,希腊),S. Amselem, N. Nathan, A. Clement(医院特鲁索,巴黎;所有法国)。
作者贡献如下。构思与设计:R. Borie, L. Tabèze, G. Thabut, C. Kannengiesser, B. Crestani;分析与解读:R. Borie, L. Tabèze, H. Nunes, V. Cottin, S. Marchand-Adam, G. Prevot, A. Tazi, J. Cadranel, H. Mal, L. Wemeau-Stervinou, G. Thabut, A. Bergeron Lafaurie, D.以色列- biet, C. Picard, M. Reynaud Gaubert, S. Jouneau, J. M.。纳卡切,曼基基安,C. Ménard,雷维,J. f .;科迪埃,D.瓦雷,B.格兰尚,C.坎尼吉塞尔,B.克雷斯塔尼;起草重要知识内容的手稿:R. Borie, L. Tabèze, H. Nunes, V. Cottin, S. Marchand-Adam, J. Cadranel, L. weemau - stervinou, G. Thabut, J. m .。Naccache,肯尼迪。科迪尔,D.瓦莱,C.坎尼吉塞尔,B.克雷斯塔尼。
脚注
其他合作者在致谢部分列出
编辑评论:呼吸呼吸J2016;48: 1556 - 1558。
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:这项工作得到了巴黎Universités总理府(legs Poix)和来自Université巴黎索邦大学Cité的“FPI-SPC”资助。
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2015年12月14日。
- 接受2016年9月3日。
- 版权所有©ERS 2016