文摘
肺部静脉阻塞疾病(PVOD)是一种罕见的肺动脉高压(PH)的特点是肺小静脉的优惠改造。在当前的PH值分类,PVOD和肺毛细血管haemangiomatosis (PCH)被认为是一种常见的实体和代表不同的表达式相同的疾病。最近发现的biallelic突变EIF2AK4基因是遗传的原因PVOD / PCH代表了我们的一个重要里程碑PVOD的分子发病机制的理解。尽管PVOD和肺动脉高血压(PAH)共享一个相似的临床表现,带有严重的前毛细管的PH值,重要的是要区分这两种情况PVOD携带更糟糕的预后和可能发生危及生命的肺部水肿PAH的起始治疗。PVOD基于非侵入性调查作出准确的诊断是可能的参数,利用氧气低一氧化碳扩散能力和特征信号的高分辨率计算机断层扫描胸部。不存在以证据为基础的治疗目前PVOD和肺移植仍是首选的治疗病人的资格。
文摘
最新进展,如发现的遗传基础PVOD将为未来的转化研究铺平道路http://ow.ly/YldhC
介绍
肺动脉高压(PH)是一个定义的肺循环血流动力学状态的平均肺动脉压力(肺动脉平均)≥25毫米汞柱1]。肺部静脉阻塞疾病(PVOD)是一种罕见的PH值为特征的优先参与肺静脉系统(2,3]。病理特征是闭塞的小肺静脉纤维内膜的增厚和片状毛细血管增生(4]。类似于其他类型的阻塞性肺血管疾病,PVOD导致进步的肺血管阻力增加,最终在右心衰和死亡5]。
第一次详细的临床和病理描述PVOD归功于德国医生j·赫拉80多年前(6]。然而,直到1966年,PVOD的术语是由H容易的et al。(7),他承认PVOD是一个独特的实体从所谓的“原发性肺动脉高压(现在称为特发性肺动脉高压(PAH))。最近,我们理解的一个重要里程碑PVOD实现的发现biallelic突变EIF2AK4(真核翻译起始因子2α激酶4)负责基因遗传PVOD [8]。尽管显著进步我们的知识的基因,细胞和分子基础PVOD在过去的十年中,它仍然是经典孤儿肺部疾病没有任何证明有效的药物治疗。肺移植仍然是合格的目标治疗病人。本文旨在提供一个全面PVOD先进的更新。
PVOD PH值在当前分类系统
当前分类系统从第五世界研讨会PH值(不错,2013)和2015年欧洲心脏病学会(ESC) /欧洲呼吸学会(ERS)的诊断和管理指南酸度将分为五个主要组根据共享病理生理学、临床特征和治疗方法(188bet官网地址表1)[1,5,9]。组1 PH值由多环芳烃及其各种亚型如特发性、遗传、药物引起的多环芳烃以及那些与结缔组织疾病有关,艾滋病毒感染、门脉高压、先天性心脏病和血吸虫病。尽管PVOD分类属于组1 PH值,它被一个特殊的子群指定组1′的统一实体下PVOD /肺毛细管haemangiomatosis (PCH)。以前被一些视为不同的实体,目前的证据支持这一概念,PVOD和PCH事实上不同的表达式是相同的障碍。事实上,二研究显示标记重叠PVOD和PCH的组织学研究10),他们的临床和影像学结果[相差无几11- - - - - -13]。常见疾病的概念进一步强调,最近发现突变EIF2AK4负责基因遗传病例PVOD和PCH [8,14]。
PVOD和PCH的小组指定组1′为了强调相似性和多环芳烃的重要差异。一般来说,PVOD / PCH的临床表现和血液动力学的研究结果和多环芳烃是相似的,但PVOD / PCH的临床过程通常是更积极的(15]。重要的是,PVOD / PCH通常展示一个贫穷的多环芳烃和多环芳烃的使用药物治疗反应相关的潜在风险危及生命的肺部水肿(16]。2015 ESC /人指南(1)提出了进一步细化的分类组1′PVOD / PCH展开的子分类包括特发性、遗传、药物和toxins-induced和相关形式的PVOD (表1)。PVOD和PCH目前被认为是相同的障碍,我们选择使用术语PVOD代表PVOD / PCH的实体在整个审核。
组织学特点
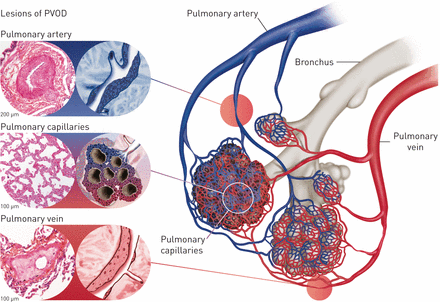
定义PVOD的病理特点是弥漫性的参与小静脉和隔静脉血管病变的特点是内层的纤维化导致腔的狭窄或闭塞(图1)[4,17]。大规模参与小pre-septal附近的小静脉闭塞的或闭塞的纤维内膜的增厚是PVOD的诊断通常被认为是必要的,因为适量的纤维变化和肺静脉的“arterialisation”中可以看到其他形式的长期肺静脉高血压如二尖瓣狭窄(17]。在PVOD,静脉和小静脉内膜的重塑可能范围从松散的纤维组织变量细胞结构致密,paucicellular,僵化的病变。可想而知,这种差异反映了血管损伤演化的不同阶段。在静脉壁弹性纤维可能显示钙水垢,显示为黑色pigment-like存款。小含巨细胞肉芽肿显示吞噬降解弹性纤维经常遇到有时在附近的小静脉和动脉。
血管病变和肺静脉阻塞疾病(PVOD)的病理特征。所有三个隔间PVOD肺微循环的影响,尽管有一个优惠肺部静脉系统的参与。小静脉的病变包括小pre-septal小静脉内膜的纤维化。毛细血管内皮细胞的病变的特点是旺盛的增殖(毛细管haemangiomatosis)。动脉病变与肺动脉高血压与内膜纤维化和中肥大,但复杂的丛状的病灶是缺席。
肺泡毛细血管PVOD通常扩张和肿胀由于下游阻塞,和弗兰克angioproliferation甚至可能产生毛细血管病变发生的PCH (图1)[18]。肺和胸膜淋巴管扩张。在一系列病理标本35例确诊为要么PVOD (n = 30)或PCH (n = 5), Lantuejoulet al。(10)表明,73%的PVOD患者显示PCH-like angioproliferative病变。阻塞静脉病变也被发现在大多数病人诊断为PCH。这些发现表明,在大多数情况下,PCH代表次要angioproliferative过程由post-capillary阻塞引起的。
尽管post-capillary和毛细管改造通常更引人注目,肺动脉病变也在PVOD遇到。动脉病变PVOD类似于多环芳烃与偏心内膜纤维化和中肥大(图1)。然而,丛状的(或复杂)多环芳烃不存在严重的病变特征。可以使血栓阻塞血管病变和随后recanalisation可能产生“colander-like”病变。神秘的肺出血常发生在PVOD,可能由于post-capillary阻塞(19]。大量haemosiderin在肺泡巨噬细胞和2型pneumocytes以及存款的间质。水肿也存在于间质,沿着小叶间septae最为突出,这可能最终发展成肝纤维化。
在一个解释性的方法中,不同形式的慢性肺血管疾病,如多环芳烃、PVOD或慢性血栓栓塞PH历来被偏爱的解剖部位贴上标签,如。肌肉肺动脉,肺小静脉或更大弹性动脉类型。然而,最近的病理研究导致了越来越认可的一个明显的动脉和静脉疾病重叠(20.]。Dorfmulleret al。(21)显示,75%的患者结缔组织疾病有关的多环芳烃显示明显的静脉阻塞性病变。这一发现或许可以解释,部分贫困对多环芳烃的临床观察治疗系统性sclerosis-associated PAH患者。同一个作者的有趣的是,最近的一项研究表明,明显的改造pre-septal小静脉,隔静脉和系统性肺血管也存在于慢性血栓栓塞患者PH值,表明post-capillary改造可能与专利的增加支气管肺的静脉吻合(22]。
遗传学的PVOD
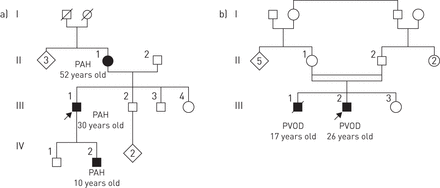
2014年,法国PH值网络报道的谱系13 PVOD家庭遗传疾病(8]。通过仔细检查这些13的家谱的家庭,我们都被这一事实只有一代受疾病和遇到高频的血缘关系,这是目前在超过一半的家庭(图2)。这些观点都是常染色体隐性传播的特征。Whole-exome测序在两个受影响的兄弟姐妹从五个家庭允许biallelic突变的示范EIF2AK4在场所有13 PVOD家庭。有趣的是,13个家庭之一EIF2AK4突变最初诊断为PCH [8]。随后,B美国东部时间et al。(14)还发现了EIF2AK4突变在另一个PCH家庭和零星的PCH情况下。最近,描述了从西班牙大吉普赛家庭有几例由于bi-allelic PVODEIF2AK4突变(23]。儿科病例PVOD biallelic突变的EIF2AK4一直还报告说,到目前为止,最年轻的患者患有遗传PVOD 11岁(8,14,23]。
说明家庭遗传树肺动脉高血压(多环芳烃)和肺静脉阻塞疾病(PVOD)。可遗传的多环芳烃因BMPR2(骨形态形成蛋白受体2型突变和b)遗传PVOD biallelic突变造成的EIF2AK4(真核翻译起始因子2α激酶4)基因。作为一个常染色体显性遗传PAH传播特征与不完全外显率;每一代可能受到疾病的影响。作为常染色体隐性遗传PVOD传播特征;只有一个一代受到疾病和血缘关系经常被报道的影响。
在法国PH值网络,遗传咨询和EIF2AK4突变筛查提供了所有PVOD有疑似或确诊的患者,有或没有一个疾病的家族史24]。尽管biallelicEIF2AK4突变被发现在所有的家族PVOD病例,亦发现了突变的9%(7 81)显然PVOD的散在病例。EIF2AK4突变携带者的特点是年轻的时候在诊断和缺乏PVOD风险因素的情况下,如烷化剂或有机溶剂(在本文的后面看到)。到目前为止,biallelic PVOD外显率的运营商EIF2AK4突变似乎很高,但外显率的精确率仍有待确定。
最后,发现EIF2AK4突变证实PVOD和PCH是两个二演讲同样的疾病实体。所有患者携带biallelic突变EIF2AK4基因被分组下的“遗传”一词,组1′。2在当前分类的PH值(表1)。尽管在骨形成受体突变类型2 (BMPR2)基因在家族已报告形式的怀疑PVOD [25),这些情况下的PVODBMPR2突变提高这些患者可能的错误分类的问题。
在PVOD风险因素和相关条件
化疗
众多的案例报告公布时间化疗药物管理和发展之间的联系PVOD [26- - - - - -35]。肝静脉阻塞病(或正弦阻塞综合症)是一种少见但高剂量化疗的并发症,尤其是在造血干细胞移植的设置(36,37]。Ranchouxet al。(38最近进行一个系统分析可能的病例化疗所致PVOD从法国PH值网络和得出结论,代表了主要的烷基化剂类药物与化疗所致PVOD。不幸的是,大多数的患者接受化疗的方案,其中包括几个同时或连续的药物,导致困难与PVOD识别特定的药物。法国PH值网络最近也报道PVOD病例患者接受mitomycin-C单独或与5 -氟尿嘧啶治疗鳞状的肛门癌(39]。使用来自法国癌症登记处的数据,估计患者PVOD肛门癌的发病率是3.9每年每1000名患者,明显高于0.5的发病率每年每百万个人特发性PVOD [39]。化疗所致PVOD据报道在儿科癌症的设置和血液学的恶性肿瘤,尤其是在骨髓移植(30.,40]。放疗PVOD被建议作为一个危险因素,但数据缺乏。值得注意的是,烷基化剂作为风险因素的识别PVOD使得小说动物模型的发展PVOD(见后)。
有机溶剂接触
职业暴露是新兴的一种潜在PVOD相关和经常遇到的风险因素。在最近的一个病例对照研究比较PVOD PAH患者(41),PVOD与职业接触有机溶剂,与三氯乙烯(氯化溶剂)的主要代理与本协会。重大的历史三氯乙烯接触在42%的PVOD患者被发现与只有3%的多环芳烃(调整或8.2,95%可信区间1.4 - -49.4)。PVOD积极接触史患者的特点是老年疾病的发病和缺乏的突变EIF2AK4基因,而那些没有接触史的通常是年轻和包庇biallelic很大一部分EIF2AK4突变(41]。
烟草暴露
累积接触烟草被报道高PVOD与特发性PAH相比,这一发现是独立的性别(25]。在最近的研究表明有机溶剂的作用PVOD的发展,重要的是要注意,所有患者重要的接触三氯乙烯并发烟草暴露38包年(平均总接触的人)41]。这可能表明一个电位器的烟草和溶剂接触效应PVOD的发展。有趣的是,一个更高频率的烟草暴露也被发现在PAH患者与健康对照组相比,或慢性血栓栓塞PH患者42]。众所周知,烟草接触可能导致内皮功能障碍(43),可以直接诱导肺血管重塑的动物模型PH值(44,45]。然而,它仍未确定为什么烟草暴露与PVOD相关似乎更强烈,有偏爱影响肺部静脉和毛细血管隔间。
自身免疫和炎症条件
越来越认可的是,明显小静脉的参与可能是相对常见的结缔组织疾病有关的多环芳烃,尤其是系统性硬化症(21,46,47]。PVOD也被报道与其他炎症性疾病,如结节病(48),朗格汉斯细胞肉芽肿病(49)和桥本甲状腺炎(50),尽管这些联系是局限于孤立的案例报告或小系列。PVOD真正的患病率在结缔组织疾病有关的多环芳烃是未知的,足够大的组织学系列是没有系统的评价。然而,最近的一项研究表明,有多达三分之二的患者前毛细管的PH值由于系统性硬化可能显示辐射的迹象PVOD在胸部的高分辨率计算机断层扫描(HRCT) (51),符合比例的估计严重静脉参与组织一系列的结缔组织疾病有关的多环芳烃(21]。
PVOD的分子发病机制和动物模型
与多环芳烃,是目前已知的关于PVOD的病理学。然而,PVOD和PAH显示一些重叠的临床和组织学特征,以及他们可能收敛的分子通路。事实上,这两种情况的特点是over-activation血小板源生长因子/血小板源生长因子受体轴(52- - - - - -55)和serotonin-induced平滑肌增生是一种常见的发病机理中看到各种形式的PH值(56]。PVOD和多环芳烃,内皮细胞增殖特性的血管病变和proangiogenic因素产生c - kit+肥大细胞也渗入血管病变(53,54,57]。虽然有争议,另一个常见的分子pathomechanism PAH和PVOD之间可能的减少生产由肺内皮一氧化氮(NO)。事实上,内皮没有合酶是降低在PVOD肺动脉高血压改造与此同时存在(58]。然而,与特发性肺动脉高压的丛状病变,血管病变PVOD保留标记的细胞生长抑制,如过氧物酶体proliferation-activated receptor-γcaveolin-1。这表明,非典型内皮细胞表型导致PVOD和特发性多环芳烃是不同的59]。
免疫介导的肺小静脉损伤和炎症条件已被建议作为一个潜在的机制与PVOD有关。细胞毒性t细胞、自然杀伤细胞和自然杀伤t细胞功能可能发挥重要作用在血管内稳态。炎症细胞的溶细胞室的分析显示重大修改循环细胞毒性t细胞的比例,自然杀伤细胞和自然杀伤t细胞数量在PVOD和多环芳烃,这是与浪费的PVOD granulysin含量(60]。这或许可以解释在PVOD granulysin血清浓度的增加与PAH患者相比。Granulysin是涉及各种各样的疾病,包括感染、癌症、自身免疫、皮肤和生殖疾病(61年),及其在PVOD放松管制也可能是疾病的发病机理的重要性。
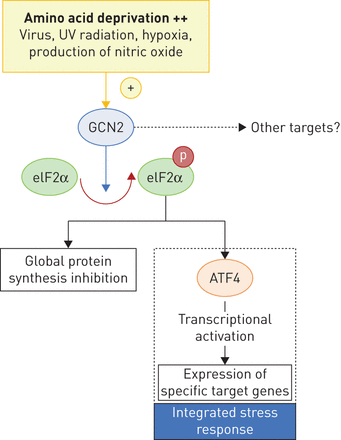
biallelic突变的发现EIF2AK4基因是遗传的原因PVOD创造了机会阐明中央分子途径参与PVOD发病机制,类似于我们理解的核心作用BMPR2 /转换增长factor-β轴多环芳烃的发现BMPR2突变。的EIF2AK4基因编码的一般控制nonderepressible 2 (GCN2),这属于一个四口之家激酶磷酸化的α-subunit真核翻译起始因子2 (eIF2α)(图3)。这四个丝氨酸/苏氨酸激酶,GCN2活跃(PKR-like内质网激酶),PKR(蛋白激酶双链依赖rna)和HRI (heme-regulated抑制剂),参与控制的一般翻译为应对各种细胞的压力。的磷酸化eIF2α保护细胞蛋白质合成减少,调节相关基因的表达变化在应激反应,定义为“综合应激反应”(62年,63年]。这些基因参与多种细胞机制,如抗氧化应激、炎症、细胞生存和血管生成。特别是GCN2被诱导基因表达的变化以应对氨基酸不足(图3)[8,62年,63年]。GCN2已经证明参与应对其他诱因,包括病毒感染、缺氧或紫外线辐射(63年]。迄今为止,eIF2αGCN2特征是唯一底物,但有证据表明,活化的影响GCN2 eIF2α磷酸化可能没有发生变化,建议其他途径可能是由GCN2控制。的角色和表达GCN2肺脉管系统在很大程度上是未知的;然而,可以假定,由于减少GCN2活动EIF2AK4突变可能导致增加易受氧化应激和炎症的增加64年]。关于小静脉的毛细管烷基化剂毒性,感兴趣的注意,在动物模型(Gcn2- / -老鼠),缺乏GCN2促进氧化应激和inflammation-mediated DNA损伤在天冬酰胺酶治疗,表明GCN2防止肝毒性天冬酰胺酶治疗期间(64年]。因此,需要进一步的调查来了解之间的联系EIF2AK4突变,GCN2表达和小静脉的的发展和人类PVOD毛细血管病变。
GCN2(一般控制nonderepressible 2)途径。可遗传的肺部静脉阻塞疾病(PVOD)是由于biallelic突变的EIF2AK4(真核翻译起始因子2α激酶4GCN2)基因编码。GCN2属于一个四口之家激酶和磷酸化α-subunit真核翻译起始因子2 (eIF2α),参与控制的一般翻译回应各种细胞压力(通过激活转录因子(ATF) 4)。GCN2激活是氨基酸的主要触发剥夺(+ +),但它已经表明GCN2可能参与应对其他诱因,如病毒感染、缺氧、生产的一氧化氮(精氨酸减少)或紫外线(UV)辐射。的磷酸化eIF2α保护细胞蛋白质合成减少,调节相关基因的表达变化在应激反应(抗氧化应激、炎症、细胞生存或血管生成),定义为“综合应激反应”。之间的联系EIF2AK4突变,GCN2表达和小静脉的的发展和毛细血管病变在人类PVOD仍然遥遥无期。
最近,我雅典et al。(65年]表明ERG-apelin受体(APLNR)轴的控制可能发挥作用在肺小静脉内皮细胞增殖。ERG是Ets转录因子家族的成员,已被确认为内皮细胞分化的调制器。这些作者表明,ERG结合并作为G-protein-coupled受体基因的转录激活因子,APLNR,淘汰赛ERG或APLNR结果肺静脉内皮细胞增殖体外。老鼠的纯合缺失ERG或ALPNR开发改建post-capillary肺小静脉。在人类PVOD肺组织,ERG蛋白质和APLNR信使rna和蛋白质水平降低与控制肺部。然而,作者并没有发现任何差异的表达GCN2从动物肺组织与纯合或杂合的删除ERG或APLNR。因此,之间的关系EIF2AK4和ERG-APLNR轴应该更好的理解PVOD的病理学特征。
烷化剂作为风险因素的识别的发展PVOD [38),化疗所致的动物模型PH值了。在实验模型中,环磷酰胺接触能引起PH值在三个不同的动物:老鼠,老鼠和兔子38]。腹腔内注射的老鼠mitomycin-C导致PVOD的发展,所展示的PH值的存在对核心catheterisation和优惠改造的小肺静脉与焦点的内皮细胞增殖的毛细血管床39]。重要的是,mitomycin-C管理导致损耗存在剂量依赖的相关性肺GCN2蛋白质含量而肺BMPR2水平在这些动物不受影响。动物模型将提供一个机会来获得进一步的洞察PVOD的分子机制,探索新的治疗目标。
流行病学
患病率和发病率PVOD只能估计由于准确诊断是挑战没有组织学(或基因)确认和许多情况下PVOD仍并被错误地归类为多环芳烃。组织病理学的高血压患者肺血管疾病表明PVOD也许占3 - 12%的病例贴上“特发性多环芳烃”经(66年- - - - - -68年]。PVOD可能更高的表示如果“治疗难治性PAH患者需要肺移植被认为是(69年]。因此,一个保守的估计是一个流行∼1 - 2例每百万居民的年发病率-0.5∼0.1 /百万特发性或遗传PVOD。然而,这个数字并不占PVOD设置的结缔组织疾病或其他相关条件/危险因素(化疗、溶剂),这表明PVOD情况下的真实数量可能更高。
PVOD据报道发生在所有年龄段从儿科到老年人口(3,19,25]。发现biallelic突变的EIF2AK4基因在13个家庭从法国PH值网络表明遗传PVOD年轻患者在诊断(±10年27日)(8]。与常染色体隐性传播,疑似性别比例的遗传PVOD是均匀分布的25,70年),这是与多环芳烃中的女性优势(71年,72年]。零星PVOD病例主要是男性与一个老年诊断(41]。
诊断PVOD
临床特征
PVOD PAH共享一个共同的临床表现和发病的特点是阴险的疲劳和呼吸困难发展到终末期疾病。右心衰的症状类似于多环芳烃、诊断常常是延迟和大多数病人在纽约心脏协会的功能类III或IV的时候正式的诊断(25,73年,74年]。PH值的典型临床症状发现右心室使把劲,一声肺组件第二心音和收缩期杂音的三尖瓣返流与公开的右心衰代偿失调疾病的迹象。在肺部听诊的陶瓷器皿字段和胸膜积液可能存在,但这些特性是罕见的除了肺部水肿的情况复杂的肺血管舒张药治疗。肺血管舒张药治疗后水肿的发展强烈支持PVOD的诊断。尽管存在肺泡出血组织学检查和支气管肺泡灌洗(BAL)咯血临床明显不是比什么是观察到多环芳烃(更常见25]。夜总会和雷诺氏现象发生在PVOD和多环芳烃在相同的比例(25]。
多普勒超声心动图
经胸廓的超声心动图仍然是最广泛使用的技术,PH值的检测75年]。PVOD没有特定的特性是在超声心动图检查,发现和调查结果反映的存在前毛细管的PH值与三尖瓣返流速度升高或没有右侧室功能障碍取决于疾病的严重程度。超声心动图可能有用的左侧排除心脏疾病引起的肺部水肿。
右心catheterisation入侵血液动力学的评价
肺血液动力学在PVOD区别其他形式的前毛细管的PH值和的特点是一个肺动脉平均≥25 mmHg,正常肺动脉楔压(PAWP)≤15毫米汞柱和肺血管阻力升高。虽然疾病的主要解剖网站PVOD驻留在post-capillary小静脉,PAWP通常是正常的(7,25,70年]。在一个大的系列中,病理组织切片证实患者PVOD特发性多环芳烃进行了比较,在诊断肺血液动力学相似的两组(25]。
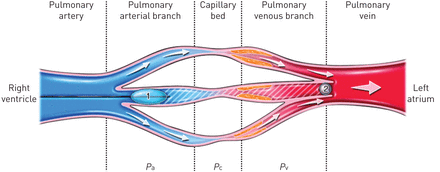
PAWP期间获得气球阻塞时,流终止远端堵塞肺动脉分支,产生一个静态列的血液,反映了类似的压力在肺静脉直径的闭塞动脉分支。换句话说,PAWP是一个测量的压力相对较大口径的肺静脉,不受该疾病影响图4)[76年]。在PVOD PAWP不是真实的反映肺毛细管压力,提升在PVOD由于下游阻塞肺小静脉。海拔肺毛细管压力性肺水肿的发生在PVOD解释说,这可能是导致肺血管舒张药导致的政府优惠肺小动脉和洪水的肺毛细血管的扩张。在临床实践中,直接测量肺毛细管压力是不可能尽管肺动脉压力衰减曲线的分析,提出了球囊闭塞后作为评估肺毛细管压力的理论方法,允许分区的血管阻力动脉和capillary-venous组件(77年,78年]。然而,有限的研究没有证明该技术的临床效用PVOD[的鉴别诊断79年,80年]。
正常肺动脉楔压在肺部静脉阻塞疾病(PVOD)。在PVOD,小肺静脉受到影响,导致该地区海拔压力(Pv),以及在真实肺毛细管压力(海拔Pc)和pre-capillary肺动脉压(P一个)。更大的肺静脉通常不受PVOD,实际上这里的压力,反映肺动脉楔压;血液的静态列(孵化)堵塞肺动脉导管楔入或气球通胀的肺动脉分支(气球1)反映了类似的压力在一个静脉直径(气球2),通常比那些规模更大的船只受到PVOD的影响。因此,该测量技术并不能反映压力的重要高程在小直径血管与PVOD有关。
在特发性PAH,执行急性血管扩张的挑战是强制性的,以确定患者(< 10%)的一个子集将测试呈阳性,证明长期应对钙通道阻滞剂(81年,82年]。此外,急性反应者在特发性多环芳烃有大幅改善预后与nonresponders [83年]。提出的ESC /人指南(1),一个积极的急性血管舒张反应(吸入一氧化氮,静脉注射epoprostenol和注射。腺苷)被定义为肺动脉平均下降≥10 mmHg的绝对水平≤40毫米汞柱,改变或改善心输出量。
在急性血管舒张药测试期间肺部水肿的发展一直在报道PVOD [70年,84年]。一系列24患者组织学证实PVOD没有报告任何肺部水肿的发生,当吸入没有(10 ppm)用于急性血管舒张药测试并给予简要5 - 10分钟(25]。因此,非常短期的政府的吸入PVOD没有似乎是安全的。然而,没有性肺水肿在急性测试期间不提供任何预测那些信息将随后发展肺部水肿后开始有针对性的多环芳烃疗法(25]。在先前的研究中,我们报告的积极回应41 PVOD患者的12.2%,但没有一个人看到一个长期应对钙通道阻滞剂(81年]。重要的是,PVOD患者反应敏锐地吸入不可能产生严重的肺部水肿迅速开始后的钙通道阻滞剂治疗(25,81年]。鉴于以上考虑,急性vasoreactivity测试不是经常需要在PVOD [1]。
射线的发现
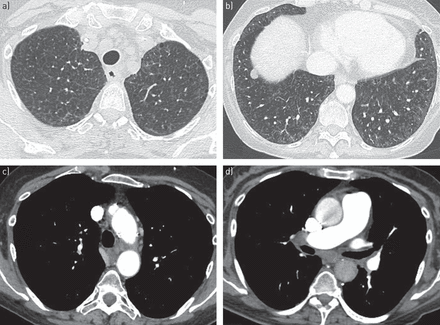
普通摄影通常的鉴别诊断提供有限的帮助PVOD除非明显肺部水肿存在(25,70年]。相反,HRCT的胸部已经成为支柱成像方式协助PVOD无创性诊断。一个三位一体的HRCT特征特性被描述PVOD [12,13,85年,86年,这包括:1)纵隔淋巴结肿大;2)小叶中心的毛玻璃的透明;和3)平滑增厚的小叶间隔(图5)。数据从病理组织切片证实患者PVOD HRCT的诊断效用,并演示了证实,75%的患者至少有两个上述HRCT异常(25]。然而,必然的结果是没有或只有一个HRCT的存在迹象并不完全排除PVOD的可能性。
高分辨率计算机断层扫描肺静脉阻塞疾病的功能。a, b)的间隔线和小叶中心的毛玻璃的透明。c, d) latero-aortic和隆突下淋巴结肿大。
Guntheret al。(51)记录,61.5%的患者系统性sclerosis-associated前毛细管的PH值至少有两个特征在HRCT上PVOD的迹象。值得注意的是,那些拥有至少两个PVOD迹象有关的高危性肺水肿PAH治疗后16个病人(8)和快速发展为死亡或肺移植。这些发现的重要预后和管理的影响需要进一步在更大的群组研究中进行确证系统性硬化患者。然而,组织学和影像学研究支持这一论断,静脉参与系统性sclerosis-associated前毛细管的PH值是一种常见的发生。
肺通气/灌注扫描
通气/灌注(V′/问′)肺扫描指南推荐的常规调查的诊断检查的PH值,以检测慢性血栓栓塞疾病,它的特点是无与伦比的灌注缺陷的存在(1]。虽然它已经表明,无与伦比的灌注缺陷也可能发现PVOD [3),最近的一项研究表明,绝大多数的V′/问′患者肺扫描PVOD实际上是正常(87年]。小未匹配的缺陷也很少看到PVOD患者(7.1%),发生在类似的利率特发性多环芳烃(10%)。因此,一个V′/问′肺扫描不应被视为一个有用的测试识别PVOD多环芳烃。
肺功能、气体交换和运动测试
尽管在HRCT上实质的存在异常,呼吸量测定法和肺容积通常保存在PVOD [25]。严重降低肺一氧化碳(的扩散能力DLCO)不到50%的预测值在PVOD[很常见25),在与特发性或遗传的多环芳烃DLCO相对保存很长一段时间(88年]。较低的DLCO观察到PVOD可以解释为更大的毛细血容量减少从受损的肺血管床和贫穷膜扩散的间质水肿。动脉血气分析通常揭示主要休息低氧血PVOD与特发性或遗传的多环芳烃。米ontaniet al。(25]表明,意味着PVOD动脉氧的分压病人平均61.3±17.3毫米汞柱与75.4±3.8毫米汞柱的多环芳烃。数据6分钟步行距离PVOD稀缺;然而,血氧饱和度下降最低点的6分钟步行试验的测试已被证明是在持续低PVOD与多环芳烃(19]。因此,DLCO和动脉氧合参数可作为辅助诊断工具来协助识别PVOD特发性多环芳烃。
心肺运动试验期间的生理反应PVOD最近报道了Lavenezianaet al。(89年在一群同构的遗传PVOD窝藏的病人EIF2AK4biallelic突变。PVOD集团与特发性肺动脉高压峰值耗氧量较低,更大的在运动中血氧饱和度下降,更大的通气效率低下,更高的静区通风在高峰运动和呼吸困难更大强度的Borg得分。多环芳烃和PVOD患者的基线匹配人体测量,肺功能和血液动力学。因此,在相似水平的血液动力学的错乱,PVOD患者高度呼吸困难的感觉,更糟糕的是有氧运动能力和更大的气体交换异常。
支气管肺泡灌洗
由于post-capillary块的存在,神秘PVOD肺泡出血是一种常见的组织学发现。Rabilleret al。(19)发现haemosiderin-laden巨噬细胞显著增加PVOD BAL流体的病人导致高Golde分数。虽然不是经常表现的诊断检查的PH值,支气管镜检查与BAL患者可以是一个有用的调查疑似PVOD,除非严重低氧血渲染过程存在不安全的。类似于PVOD胸部HRCT特征,缺乏PVOD肺泡出血不排除诊断。Transbronchial活检不应该表现在患者严重的PH值由于高得令人无法接受的风险,危及生命的出血。最后,最近的一项初步研究表明haemosiderin-laden巨噬细胞数量的增加也可以检测到在PVOD患者的痰标本90年]。痰液检查的临床效用作为非侵入性工具的检查PVOD需要进一步研究。
非侵入性诊断方法
虽然组织学仍然是明确诊断的金标准PVOD,肺活检是禁忌在临床上重要的PH值的设置1]。因为组织学确认只能上执行死后或移植肺标本,非侵入性的诊断方法是必需的。在法国转诊中心,我们一直在使用非侵入性诊断策略基于临床特征和从电池的调查结果(表2)。正如上面详细的,很多突出的特性可以帮助区分PVOD PAH:非常低的结合DLCO运动,低氧血,严重稀释,两个或两个以上的特征辐射对胸部HRCT和神秘的肺泡出血迹象BAL都可以用来支持PVOD的诊断。最后,基因分析可以确定遗传PVOD的存在EIF2AK4biallelic突变。由于常染色体隐性遗传PVOD的传播,血缘关系和家庭历史的PH值只有一代应该提高对遗传性PVOD的怀疑。
PVOD的自然历史和预后
PVOD的自然历史数据有限,但疾病通常是由不可阻挡的发展特征。预后是惨淡的,明显比其他形式的感叹词。生存数据已经在两个案例系列报道的文献。在一系列的11 PVOD病人,Holcombet al。(70年]报道1年内死亡率72%的诊断。最近的一个大系列,我们组发现,同时从诊断到死亡或肺移植是11.8个月,并首次报道症状到死亡的平均时间或肺移植是24.4个月25]。快速进步的PVOD要求临床医生高度怀疑的心理指标以达到及时诊断,尽早安排肺移植。
PVOD治疗选项
过去十年见证了一个巨大的扩张pharmacotherapeutic选项PAH患者。先进的治疗有针对性的PAH前列腺素类等药物,endothelin-1受体拮抗剂,5型磷酸二酯酶抑制剂和可溶性鸟苷酸环化酶刺激器大大改善了PAH患者的生活质量和前景(83年,91年]。相比之下,随机对照试验是缺乏PVOD仍然没有药物治疗和证明效力。
一般和支持措施
应该纠正低氧血氧政府防止进一步恶化缺氧性肺血管收缩的PH值。没有结果的数据在PVOD存在抗凝和它的使用已经从建议外推多环芳烃(92年]。类似于多环芳烃,原位血栓形成肺微循环的观察到PVOD [4),支持抗凝的生物学原理。然而,神秘的肺出血也是一个常见的发现PVOD和抗凝不应该给病人咯血史。最近ESC /人指导方针认为口服抗凝的证据仅限于特发性肺动脉高压的患者,由于anorexigens遗传多环芳烃和多环芳烃。没有提出了推荐的抗凝PVOD [1]。
针对多环芳烃疗法
全球监管机构已经批准了多环芳烃的众多药物治疗。目前通过PAH药物目标所涉及的三个主要途径之一PAH发病机理:环前列腺素,endothelin-1没有通路(表3)[83年]。所有PAH药物也常属性和变量抗增殖影响肺脉管系统(93年]。然而,数据的使用多环芳烃治疗PVOD软弱,是相互矛盾的。案例报告/系列和坊间的经验表明,一些病人血流动力学和功能上能获得PVOD改进与PAH疗法,或至少是稳定的疾病过程70年,94年- - - - - -104年]。然而,长期的临床反应很少了。
PAH患者治疗使用时必须非常小心PVOD和治疗只能在专家进行肺血管中心这个条件的管理经验。危及生命的肺部水肿是担心PVOD肺血管扩张性疗法的并发症和可能发生的任何类的多环芳烃药物(2]。启动后肺部水肿的发生率肺血管舒张药可能高达75%,钙通道阻滞剂(70年用有针对性的多环芳烃药物)和50% (25,51]。
最大的出版经验PVOD PAH疗法的使用注射。epoprostenol 12患者严重PVOD桥梁移植(97年]。Epoprostenol在低剂量范围(平均峰值剂量的ng·13公斤−1·敏−1),缓慢up-titration剂量。所有患者接受移植epoprostenol也同时上市。大剂量利尿剂循环需要减少肺部水肿的风险。温和的临床和血液动力学的改善可能观察到3 - 4个月后,但没有长期持续的影响。轻微的临床改善或稳定的疾病也被报道与其他多环芳烃等药物应用波生坦(101年- - - - - -103年),西地那非(99年,One hundred.,104年]和iloprost [98年]。
多个药物类现在可以治疗PAH,顺序使用面向目标的联合治疗方法已成为标准的照顾多环芳烃(83年,105年]。前期联合治疗也越来越采用PAH患者,特别是如果存在高风险的特性(106年- - - - - -108年]。我们报道一例系统性sclerosis-associated PVOD在序贯联合治疗导致严重的肺部水肿时添加西地那非是由于不适当的应对应用波生坦单方(109年]。我们认为所有病人诊断为PAH应该仔细筛查PVOD的可能性,和小心监测时,必须行使PAH疗法用于PVOD疑似病例进行。
免疫抑制治疗
发病机制中的一个潜在的炎症的可能性组件PVOD导致之前的传闻试图使用糖皮质激素等免疫抑制疗法,环磷酰胺和咪唑硫嘌呤3]。特发性PVOD,几乎没有报道描述了临床的症状缓解或改善免疫抑制治疗。同样PAH患者,免疫抑制目前的指南(不推荐1),虽然有一种全新的热情探索小说在PAH的免疫调节和更具体的目标。一个例外使用免疫抑制在上下文中的多环芳烃是系统性红斑狼疮和混合结缔组织病,在糖皮质激素联合环磷酰胺有可能连续作用和结果报告。相比之下,免疫抑制并不是有效的系统性sclerosis-associated多环芳烃。鉴于所涉及的潜在危害,免疫抑制不能推荐目前例特发性,遗传或系统性sclerosis-associated PVOD。
肺移植
肺或心肺移植仍是唯一明确的治疗提供PVOD患者长期生存的可能性。鉴于PVOD迅速进步,大多数患者存在严重的疾病,尽早安排用于移植的时候应该考虑诊断为符合条件的患者。双边肺移植是PVOD全球使用最广泛的技术,和移植后生存似乎与特发性肺动脉高压。最近的一项研究报告的进化49 PVOD挂牌肺移植患者(110年]。到6个月,22.6%的PVOD病人已经从名单中删除由于死亡,而不是11%的PAH患者。混杂因素调整后,诊断PVOD显著相关的风险更高等候名单上去除由于死亡与多环芳烃(风险比2.05;p < 0.05) (110年]。这些结果证实PVOD患者的不良预后和引用的重要性PVOD早期肺移植的患者。到目前为止,病理组织切片证实没有复发PVOD肺移植后报告。
结论和未来的发展方向
PVOD PH值的一种常见形式,但临床识别由于其惨淡的预后至关重要和PAH疗法停止响应。在临床诊断仍然是具有挑战性的,但高度的诊断信心可能是基于一系列的调查。发现biallelic突变的EIF2AK4基因遗传的疾病将铺平了道路,使一个更好的理解的分子发病机制PVOD,类似于发现的方式BMPR2多环芳烃的突变导致了知识的主要进步。PVOD将使小说的动物模型的治疗目标是人类研究测试和最终的翻译。肺移植是目前治疗的首选资格PVOD患者。
脚注
编辑评论:和J 2016欧元;47:1334 - 1335。
本系列之前的文章:没有。1:羽衣甘蓝人力资源,布拉德福德WZ Cottin V,et al。一个新时代在特发性肺纤维化:考虑未来的临床试验。欧元和J2015;46:243 - 249。2号:瑞尔森CJ, Cottin V,棕色的乐,et al。急性特发性肺纤维化恶化:将范例。欧元和J2015;46:512 - 520。3号:他,老爹啊,Cassandro R,et al。变化的一种罕见的疾病:lymphangioleiomyomatosis。欧元和J2015;46:1471 - 1485。
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
- 收到了2016年1月6日。
- 接受2016年2月4日。
- 版权©2016人队