文摘
结节病的特点是non-caseating肉芽肿,分泌促炎细胞因子,包括白介素(IL) -12年,IL-23,肿瘤坏死因子(TNF) -α。Ustekinumab和golimumab单克隆抗体,可以抑制il - 12 / IL-23和TNF-α,分别。
慢性肺结节病(肺组)患者和/或皮肤结节病(皮肤组)接受180毫克ustekinumab 0周后跟90毫克每8周,200毫克golimumab 0周后跟100毫克每4周,或安慰剂。病人接受皮质类固醇周16 - 28之间逐渐减少。主要终点是第16周百分比变化预测用力肺活量(ΔFVC % pred)肺组织。主要二级终端:星期28ΔFVC % pred, 6分钟步行距离,圣乔治呼吸问卷(肺组),和皮肤医生全球评估响应(皮肤组)。
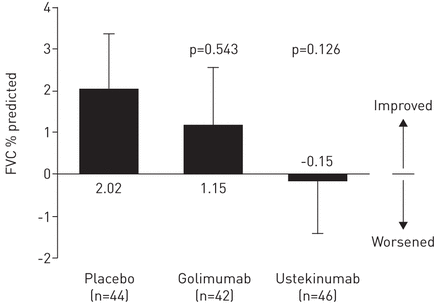
在第16周,没有观察到显著差异在ΔFVC % pred ustekinumab (-0.15, p = 0.13)或golimumab (1.15, p = 0.54)与安慰剂比较(2.02)。28周,没有明显的改善主要二级终端,尽管无意义的数字更大的皮肤医生观察全球评估反应后golimumab治疗与安慰剂相比(53%)(30%)。严重不良事件在所有治疗组相似。
虽然治疗耐受良好,无论是ustekinumab还是golimumab证明肺结节病的疗效。然而,观察趋势改善golimumab在某些皮肤端点。
文摘
无论是ustekinumab还是golimumab证明疗效治疗患者的肺结节病http://ow.ly/yaLt6
介绍
结节病是一个系统性、肉芽肿性疾病临床表现高度可变的自然历史和预后,主要影响肺和淋巴系统(1]。结节病的诊断是临床结果和确凿的组织学证据non-caseating上皮样细胞肉芽肿(2]。超过90%的患者肺参与(3),而皮肤损伤是∼25%的患者中观察到4]。虽然自发缓解发生在近三分之二的患者,慢性或进行性疾病是在10 - 30%5),与永久性肺部或肺外的后遗症在至少10 - 20%的患者。1 - 5%的疾病是致命的病人,通常由于进步的呼吸衰竭,中枢神经系统,或者心肌参与(5]。
目前,不批准治疗结节病的治疗。保健是口服糖皮质激素(OCS)的标准,这已被证明,以稳定或改善疾病,虽然常发生一次口服避孕药治疗复发是锥形或停止6]。替代品,如抗疟、细胞毒性和生物制剂,显示变量功效[7),尽管这些药物治疗也被停药后复发,毒性和/或潜在的严重副作用(1,8]。有大量需要更安全、更有效的治疗结节病。
虽然结节病的病因学是未知的,炎性细胞因子,肿瘤坏死因子(TNF) -α,是工具性的形成和维护non-caseating肉芽肿与结节病(9]。巨噬细胞炎性蛋白(MIP) 1β,免疫细胞化学引诱物(亚兰),是由TNF-α[10)和更高水平的炎症趋化因子在一些但不是全部结节病病人可能表明提高肿瘤坏死因子通路的激活患者的子集的最高水平。TNF-α抑制结节病已经被证明可以减少疾病患者症状和体征(11,12]。第二阶段,多中心、随机、双盲、安慰剂对照研究138例慢性结节病,英夫利昔单抗治疗(一种嵌合单克隆抗体,抑制TNF-α)导致比例显著提高预测用力肺活量(FVC)与安慰剂比较(1]。改进也观察到在其他疾病活动措施,比如胸片网状(R)的分数(13[],MIP-1β水平10),而血清血管紧张素转换酶(ACE)的水平(1]。在一系列案件的红斑狼疮患者54冻疮,接近或实现完整的决议在77%的病人接受英夫利昔单抗治疗接受系统性皮质类固醇(相比之下,只有19%的病人14]。
尽管TNF-α过剩的潜在致病作用肉芽肿性疾病(9,15- - - - - -18是有据可查,TNF-α并不仅仅占辅助细胞类型1 (th))细胞因子主导环境肉质的肺;特别是,高水平的干扰素(IFN) -γ也被牵连在结节病的发病机制19]。此外,从患者肺泡巨噬细胞结节病已被证明产生白介素(IL) -12除了TNF-α,IL-1β,IL - 6 (20.- - - - - -29日]。激活肺泡巨噬细胞表达il - 12,,导致增强的th1细胞增殖和活化,导致促炎症介质的表达增加IFN-γTNF-α,和细胞因子和趋化因子的分泌,反过来,招募和激活更多的t细胞。巨噬细胞也产生profibrotic介质,如纤连蛋白(30.],和转变增长factor-β[31日),为纤维肉芽肿的发展作出贡献。总的来说,这些数据表明,il - 12可能参与发起和永存的肉芽肿性炎症结节病。最近,转录组分析结节病皮肤病变的活检证实upregulation TNF-α和il - 12以及IL-21 IL-23,表明th)和可能th17 upregulation在结节病32]。Thus, inhibition of either TNF-α or IL-12/IL-23 could, potentially, be effective in the treatment of chronic sarcoidosis.
Golimumab是人类单克隆抗体结合TNF-α亲和力高、特异性和批准治疗严重的风湿性关节炎,溃疡性结肠炎,活跃的银屑病关节炎,强直性脊柱炎(33]。Ustekinumab是人类免疫球蛋白G1κ单克隆抗体结合,与高亲和力,共享人类il - 12和IL-23 p40单元和被批准用于治疗严重银屑病(34]。我们报告的结果多中心,随机,双盲,安慰剂对照研究使用ustekinumab或golimumab慢性肺患者和/或皮肤结节病。
材料和方法
病人
患者年龄在18岁到85岁都有资格报名病理组织切片证实如果他们的肺或皮肤结节病诊断筛查发生前2年以上,没有潜在的历史或活动性结核病。此外,负面Quantiferon-GOLD试验需要在筛选访问为了病人登记。进入肺组织肺实质疾病的证据需要一个胸部x光(阶段II, III或IV,但没有空洞的疾病),% pred FVC 45 - 80%,医学研究理事会的呼吸困难评分> 2和6分钟步行距离(6随钻测量)的100至550米。这些标准是基于前一个随机的结果,英夫利昔单抗对慢性肺结节病的安慰剂对照试验,一个重要反应是观察和亚组患者的上述标准有一个更健壮的响应(1]。进入皮肤组要求:活跃,悬而未决,慢性皮肤损伤≥3个月,尽管使用当前系统/局部治疗;一个病变≥2厘米或多个病变(≥3)和至少一个病变≥1厘米大小的最长尺寸;和皮肤医生的全球评估(SPGA)得分≥2。SPGA分数是基于医生无情的评估和红斑患者的皮肤损伤,每个评分0(没有)4(非常严重)。会议进入标准的病人肺和皮肤组织可以进入两组。所有的病人需要十到二十五毫克·天治疗−1强的松或其等价的口头和/或≥1免疫调制剂为≥≥3个月稳定剂量检查前4周。关键的排除标准:≥20包年吸烟史的人;治疗与其他anti-TNF-α剂、anakinra、白介素-或IL-23-targeted代理人;以前的环磷酰胺使用;局部注射治疗或在3个月或局部皮肤结节病治疗1个月之内;严重肺动脉高压临床接受血管舒张药治疗;和当前或历史的充血性心力衰竭。
本研究根据赫尔辛基宣言的原则。每个网站的机构审查委员会或伦理委员会批准了研究和所有病人提供书面知情同意。
研究设计
这是第二阶段,多中心,随机,双盲,安慰剂对照,三臂研究的安全性和有效性评估ustekinumab或golimumab慢性肺患者和/或皮肤结节病。1 - 4周的筛选后,病人被随机分配在分层比例比基线疾病(肺参与,参与皮肤,肺和皮肤的参与)和前anti-TNF-α生物使用(yes / no)使用交互式语音应答系统,接收ustekinumab皮下注射,golimumab或安慰剂。病人分配到ustekinumab收到180毫克在0和90毫克星期8,16日和24(与安慰剂在周4,12日和20维持致盲)。病人分配到golimumab 0周后收到了200毫克,紧随其后的是100毫克每4周通过24周(图1)。病人接受背景OCS通过第16周维持在一个稳定的剂量,如果临床上可能,使治疗效果的评估主要终点稳定背景方案。然后,如果临床稳定,患者口服剂量锥形通过周28日剂量减少50%在16周,20和24。信息商务和其他肉质的药物剂量的基线,基线中包含在线S1-S3补充表。
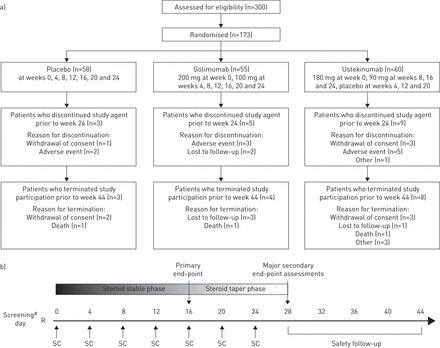
)研究设计和b)病人流的研究。R:随机;SC:皮下注射研究代理在周0,4、8、12、16、20和24。#:从-28天1筛选。
主要终点是基线的改变在第16周% pred FVC肺组(即。那些只肺和肺和皮肤的参与)。主要二级终端在28周在6随钻测量基线的改变(Δ6MWD),圣乔治呼吸问卷(SGRQ)总分,肺组比例预测FVC, SPGA反应者的比例(评分≤1,请参阅在线补充材料)在皮肤组(即。那些只有和肺和皮肤的参与。结节病的皮肤组也是评估活动和严重程度指数(SASI),修改从Baughmanet al。(35),(图S1)。收集的样品也在周0、4、8、16日28日和44探讨ACE的水平(研发系统,明尼阿波利斯,美国),c反应蛋白(CRP)(美国西门子浊度测定法、迪尔菲尔德,IL), MIP-1β(中尺度发现,罗克维尔市,医学博士,美国),和其他炎症生物标记。评估整体器官参与,肺外器官医生严重性工具(ePOST) [36执行),在每一个访问中,医生使用所有可用的信息。病人还完成了几个额外的病人报告结果(PRO)问卷,包括36-item简式健康调查(SF-36) [37),疲劳评估量表(FAS) (38),结节病评估工具(坐)39),和一个病人(PGA)的全球评估的总体幸福感视觉模拟尺度。一个独立的数据监测委员会回顾了所有可用的数据后15日随机患者完成了第16周访问,之后定期。患者随访到星期44。
统计分析
计划的总样本量180例包括病人肺≥135人口和人口≥45岁患者的皮肤。假设7%的标准差,45每治疗肺癌患者手臂提供了86.4%的电力检测从基线差异5% % pred FVC在第16周三个治疗整个0.05显著性水平,Bonferroni调整。ANCOVA用于主要终点分析。测试过程中组成一个整体测试安慰剂,ustekinumab, golimumab,其次是两个比较ustekinumab和安慰剂,golimumab和安慰剂。用于所有分析的显著性水平为0.05。这项研究被认为是积极的,如果整体测试达到统计学意义和至少一个golimumab或ustekinumab手臂明显优于安慰剂。
结果
患者基线特征
2009年9月至2012年8月,173例患者进入研究和治疗的47个网站在9个国家。173名患者随机,大约一半的人口(50.9%,n = 88)是男性,大多数白人(61.3%,n = 106) (表1)。总共15例终止他们的研究参与最后的研究之前访问(安慰剂n = 3, golimumab n = 4, ustekinumab n = 8) (图1)。
在治疗手臂基线特征是均衡的。大约有67%的患者肺参与,皮肤参与只有24%,10%的肺和皮肤都参与。
功效
在第16周,没有观察到的统计差异主要终点(基线的改变% pred FVC)在肺癌组和积极治疗与安慰剂相比(ustekinumab -0.15, p = 0.126;golimumab 1.15, p = 0.543;安慰剂(2.02)图2和表2)。主要终点的敏感性和亚组分析显示与主分析一致的结果(图S2)和包括吸烟状态(yes / no),身体质量指数(BMI) (≥30与< 30)、种族(白色/非白人),性别(男/女)、和(≥50岁与< 50年)。值得注意的是,患者体重指数较低的倾向于显示改善FVC golimumab治疗与患者BMI较高,倾向于恶化。分析槽golimumab血清水平的四分位数,建议从基线在第16周FVC倾向于增加两个更高的四分位数,但不是两个四分位数较低(图S3)。亚组分析,基于中值水平的基线生物标志物,没能证明任何显著改善反应FVC(表S4)。
主要终点在第16周肺组织,在均值±基线的改变SE%预测用力肺活量(FVC)。分析使用持续观察结转输入缺失值。
在28周,积极治疗与安慰剂相比没有显著改善在任何主要二级终端(表2)。没有观察到显著差异的变化从基线% pred FVC 28周的积极治疗武器(golimumab 0.29, p = 0.451;ustekinumab 0.56, p = 0.546)与1.59相比安慰剂肺组织。golimumab手臂Δ6MWD为12.53 m (p = 0.896)和-13.22米ustekinumab手臂(p = 0.063)相比,14.52年的安慰剂的手臂。周28日均值变化的基线SGRQ肺组总分:-9.50安慰剂,-6.86 golimumab (p = 0.374),和-4.25 ustekinumab (p = 0.073)。此外,没有观察到显著改善的积极治疗武器相对于安慰剂组的分数从职业问卷完成病人(SF-36, FAS、坐和PGA)。
肺组织商务在基线,接受一个名义上的大比例的golimumab-treated病人,但不是ustekinumab-treated病人,能够减少至少50%的口服剂量在taper-phase (golimumab 81.6%, p = 0.01;ustekinumab 57.9%, p = 0.63)与对照组(51.6%)。golimumab手臂,结果主要是由患者BMI < 30 (golimumab 85%,安慰剂组36%,p = 0.0134)的一般趋势改善患者的结果较轻的重量。在皮肤组织中,双臂倾向于减少至少50%的口服剂量(golimumab 70.0%, p = 0.23;ustekinumab 83.3%, p = 0.047)与安慰剂相比(40%)。比例的患者在肺和皮肤组完全撤军的口服避孕药使用前星期28日低,类似于安慰剂:golimumab 11 (28.9%) 38 (p = 0.41), ustekinumab 7 38 (18.4%) (p = 1.0),安慰剂6(19.4%)的31个肺组;golimumab 3 (30.0%) 10 (p = 0.36), 12 ustekinumab 1 (8.3%) (p = 1.0)和安慰剂皮肤2(13.3%)的15组。
改善皮肤组织,无SPGA反应后golimumab观察治疗(52.9%,p = 0.19)与安慰剂相比(30.0%),但不是ustekinumab治疗(14.3%,p = 0.28) (图3在28周的)。目标病变评分倾向于提高与golimumab但不是ustekinumab时间(ustekinumab golimumab -2.3, p = 0.07, -1.2, p =ns在28周的安慰剂-1.4)。类似的模式被认为与SASI分数(golimumab -2.57, p = 0.38;ustekinumab -0.50,与安慰剂比较,p = 0.89) (-0.52) (图3 b)。大数值的改进也观察到的皮肤领域ePOST golimumab-treated病人而不是ustekinumab-treated患者(图3 c)(p =ns,两个)。皮肤组,有显著改善肺外参与总体衡量ePOST golimumab,在20周、24日和28(分别为p = 0.004, 0.016, 0.005),但与ustekinumab (图3 d)。
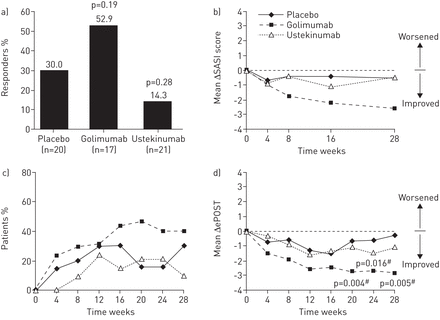
皮肤组人口评估。)皮肤医生反应者在28周的全球评估。b)在结节病活动从基线和严重程度指数(ΔSASI)得分。c)皮肤域的肺外器官医生工具(ePOST)严重程度定义为患者的百分比提高≥2分。d)从基线变化ePOST(ΔePOST)。#:名义假定值与安慰剂。
血清炎症标记物的测量(ACE、MIP-1β和CRP), MIP-1β,免疫细胞化学引诱物和药效学的标志anti-TNF-α治疗,证明从基线明显降低星期4,并维持这种差异是通过28周,治疗后golimumab(-84.57)与安慰剂相比(24.48,(p < 0.001)。观察与治疗ustekinumab没有差别(图4)。显著减少ACE观察治疗手臂在周4,8,16。ACE水平倾向于上升3武器后16在类固醇锥度阶段以每周28(图S4)。
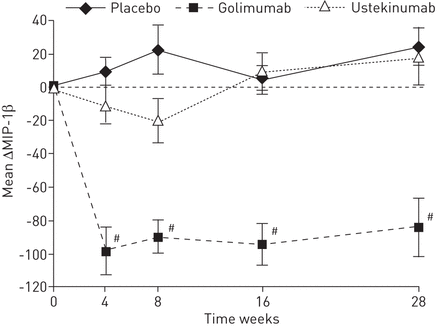
巨噬细胞炎性蛋白(MIP) 1β水平,对治疗的反应。#:golimumab p < 0.0001与安慰剂。Δ:改变基线。
安全
严重不良事件报告在整个研究过程中在15.5% (n = 9), 12.7% (n = 7),和16.7%的安慰剂组(n = 10), golimumab-treated分别和ustekinumab-treated患者(表3)。最高的报道事件是肺炎(golimumab n = 1, ustekinumab n = 3)。治疗紧急不良事件的发生在整个研究过程中患者93.1% (n = 54), 96.4% (n = 53),和93.3%的安慰剂组(n = 56), golimumab-treated ustekinumab-treated患者,分别为(表4)。注射部位反应发生在3.4% (n = 2), 20% (n = 11),和5.0%的安慰剂组(n = 3), golimumab-treated, ustekinumab-treated患者,分别和大多是轻微的。没有感染的发病率增加的积极治疗研究的武器(golimumab 61.8%, ustekinumab 65.0%)与对照组(65.5%)。报道1例肺结核golimumab-treated病人。
三个死亡是在研究报道:golimumab-treated病人死于败血症5个月后第一个也是唯一一个剂量的golimumab,随后被退出研究药品监督管理局由于呼吸困难;ustekinumab-treated病人死于急性呼吸衰竭后5个月的最后剂量ustekinumab在第12周;和一个接受安慰剂的病人去世后,突然间,3个月后的最后剂量研究代理。两个报告恶性肿瘤包括一个事件复发性鳞状细胞癌(SCC)病人的历史基底细胞癌和鳞状细胞癌(ustekinumab臂),和一个例乳腺癌病人有乳腺癌家族史(安慰剂)。一个额外的恶性肿瘤(慢性骨髓性白血病)在女性恶性肿瘤家族史的患者,2个月后完成药物剂量(ustekinumab臂)。回顾性研究实验室的价值观和储存血样的分析表明,恶性肿瘤在研究入口和预先存在的,因此,并不像一个治疗诱发的事件的记录。没有可能的过敏反应的报道或可能延迟超敏反应(血清sickness-like)通过44周的反应。
讨论
在这个随机、双盲、安慰剂对照试验,无论是golimumab还是ustekinumab表现出显著的影响主要终点,从基线在第16周% pred FVC在第16周肺组织,与安慰剂相比。此外,无论是药物遇到任何二级研究终端在28周(Δ6MWDΔSGRQ总分,ΔFVC % pred肺组,和皮肤组SPGA反应者的比例)。额外的敏感性和子群分析未能展示积极的研究药物和安慰剂之间的显著差异,尽管改善的趋势是持续观察皮肤组端点(SPGA, SASI和ePOST),系统进行条目设置golimumab患者。golimumab和ustekinumab演示了一个安全性与安慰剂这类患者中慢性结节病。
缺乏这两种活性药物的功效可以提供洞察结节病的免疫发病机理和治疗。让人感到奇怪的是,golimumab没有演示一个好处与安慰剂在这个实验中,因为其他TNF-α拮抗剂显示治疗结节病有利的结果,包括随机、双盲、安慰剂对照试验(1,14,36,40]。此外,肺组织的进入标准在这个实验中匹配的子群在之前积极试验涉及英夫利昔单抗对肺结节病,一种更健壮的响应(1]。有几种可能的解释缺乏应对golimumab这个审判。首先,有限的临床数据表明,并不是所有TNF-α拮抗剂是结节病同样有效。特别是,道,没有发现特别有效的各种形式的结节病(41,42和没有适合这个条件43]。虽然有限的数据是可用的关于adalimumab治疗结节病的好处,它似乎需要高剂量(皮下接种)和管理在更长一段时间最大化利益相比,英夫利昔单抗,这是管理静脉注射(43]。其次,可能golimumab用于这个试验的剂量是治疗结节病的不足。尽管额外的动力不足的敏感度分析和推测的,事实上,队列,而体重指数为30 <有统计学无意义的更大的进步与BMI≥30 FVC相比表明,golimumab剂量使用可能是太低了。进一步支持了这一假设是倾向FVC改进golimumab槽更高水平(图S2)。我们还发现,病人接受golimumab BMI较高利率较低的皮质类固醇比安慰剂手臂逐渐减少。第三,只有一个子集的结节病病人可能TNF-α驱动的疾病。一个子集的分析之前英夫利昔单抗肺结节病试验显示更好的改善患者FVC可测血清TNF-α水平基线(>下限检测4 pg·毫升−1)[10]。患者血清中位数TNF-α水平基线在当前研究∼5 pg·毫升−1,那些高水平基线在FVC略大的改进,但这不是一致的所有炎症生物标记物(表S1)。第四,因为糖皮质激素也抵销TNF-α的作用,有可能维护皮质类固醇剂量的病人“蒙面”golimumab的好处。支持这个假定,最近有关(44)积极英夫利昔单抗的审判的肺结节病(1)表明,患者接受≥15毫克·天−1强的松并没有证明额外受益于英夫利昔单抗。这种假定也可能解释为什么一个名义上的大比例的golimumab治疗病人,肺和皮肤组织,能够减少至少50%的皮质类固醇剂量与安慰剂相比在taper-phase手臂。第五,3个月的皮质类固醇锥度阶段试验可能是太短证明最大corticosteroid-sparing效果,虽然意味着皮质类固醇剂量28岁到44周(期同时病人并不在研究药物治疗)倾向于更低的golimumab(7.2毫克)和ustekinumab(7.9毫克)武器相比安慰剂手臂(12.2毫克)。最后,皮肤组可能是没有足够的动力去达成一个结论关于药物功效试验。
ustekinumab的缺乏有效性是一致的,没有明显的信号的功效主要终点,次要的端点,或敏感性和子群分析。这种缺乏疗效可能表明,il - 12 p40机制不是一个疾病过程的主要决定因素,尽管它是未知的,如果大剂量会对疾病的影响。的缺乏疗效ustekinumab必须调整对发现活跃结节病皮肤损伤显示upregulation il - 12和IL-23相对于控制组织(32),发现增加il - 12在结节病血清26),支气管肺泡灌洗(25和淋巴结45]。尤其是白介素,被认为是一个关键驱动因素的失调干扰素在结节病(25,32,46]。可能,这些介质不是积分在推动干扰素生产或调停肉质的肉芽肿形成。ustekinumab块il - 12和IL-23以来,它让打开的问题是否il - 12的封锁或独自IL-23可能是有效的。
这个试验的设计反映了问题固有的所有小说为结节病药物治疗试验。糖皮质激素是结节病非常有效。因为皮质类固醇的有效性,它可能有问题的证明的一个额外的好处在皮质类固醇药物效应研究[44]。因为这个试验的招生标准是相同的子群,有一个健壮的改善FVC在前面的英夫利昔单抗的审判,我们认为这是可能的好处至少golimumab在当前审判。我们添加了一个皮质类固醇锥在当前阶段试验,试图揭示研究药物的好处可能是被维护皮质类固醇治疗。其他研究设计可以包括逐渐减少糖皮质激素或剂量的病人恶化在进入他们的审判。然而,这些方法会延长试验的持续时间。可能,可能是有用的生物标记来确定药物反应随着c反应蛋白识别反应者,英夫利昔单抗在前面的随机,双盲corticosteroid-dependent肺结节病试验(47]。
数据从本研究可能会给洞察immunopathogenic通路的相对重要性在结节病。大量的样本收集过程中研究目前正在分析来评估治疗的影响疾病的分子签名和识别替代途径与潜在的治疗干预。antisarcoidosis活动此外,考虑到广泛的各种TNF-α对手当前可用,这些数据可能导致这些代理的进一步修改提高功效和评价的结合anti-TNF-α与其他关键致病机制
总之,尽管ustekinumab或golimumab治疗耐受良好,既展示了肺结节病的疗效。然而,观察趋势改善golimumab在某些皮肤端点。这个试验可能是动力不足要全面检查的作用研究药物在皮肤组织。
确认
作者和研究人员非常感谢并承认参与本研究的患者。作者还要感谢结节病调查人员和罗伯特·奥肯博(美国詹森科学事务,LLC PA)编辑和提交的手稿的支持。
研究人员包括:p . De Vuyst c .主持人w . Wuyts(比利时);动向Bendstrup(丹麦);a·伯丁p . Chanez b,伽马安基丁酸塔子,d . Valeyre b Wallaert(法国);美国Costabel, r·盖j . Muller-Quernheim n .联系美国要控制(德国);a·米勒·m·怀特s bir T.M.马赫(英国);c . Albera c . Saltini a . Pesci m . Luisetti g . Paone c . Agostini p Rottoli(意大利);右眼jonker, m . Wijsenbeek m . de Vries(荷兰);d . Ionita(罗马尼亚);r·鲍曼r·伯克·g·戴维斯,m .贾德森c .奇怪Huizar, m·帕迪拉h . Shigemitsu k·吉布森,n . Sweiss大肠白色,d .斑鸠m . Rosenbach l .麦尔j .巴尼Enelow r·e·克劳斯·r·古普塔(美国)。
脚注
社论评论看1123页。
可以从本文的补充材料www.qdcxjkg.com
临床试验:这项研究是在注册www.clinicaltrials.gov标识号NCT00955279
支持声明:本研究由詹森研发、LLC(春天的房子,PA,美国)。
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
- 收到了2014年1月2日。
- 接受2014年6月6日。
- ©2014人队