摘要
MELODY-1研究评估了macitentan在合并毛细血管前后PH值的左心疾病(PH- lhd)患者中的治疗效果。
63例PH-LHD患者,舒张压梯度≥7 mmHg和肺血管阻力(PVR) >3WU患者随机分为马西坦10 mg (n=31)或安慰剂(n=32),为期12周。主要终点评估了纽约心脏协会功能分级从基线到治疗结束的显著液体潴留(由于液体超载或肠外利尿剂给药导致体重增加≥5%或≥5 kg)或恶化的复合因素。探索终点包括第12周n端脑利钠肽前体(NT-proBNP)和血流动力学的变化。
7例马吉坦治疗组和4例安慰剂治疗组患者出现明显的液体潴留/功能等级恶化;治疗差异10.08% (95% CI−15.07-33.26;p = 0.34)。在第一个月,由液体保留成分驱动的差异是明显的。在第12周,与安慰剂组中,macitentan组PVR、平均右房压和肺动脉楔压无变化;心脏指数无显著增加(治疗效果0.4 (95% CI 0.1-0.7) L·min)−1·米−2), NT-proBNP降低(0.77(0.55-1.08))。马西坦的不良事件和严重不良事件在数值上更为频繁与安慰剂。
经马西坦治疗的患者在定量上更有可能出现明显的液体潴留与安慰剂。Macitentan在任何探查终点均无显著变化。
摘要
在合并毛细血管PH后和前的患者中,macitentan与显著液体潴留发生率的增加相关与安慰剂http://ow.ly/leop30hBkQm
介绍
肺动脉高压(PH)是心力衰竭(HF)的常见并发症[1].分类为第2组PH(毛细血管后PH),由左心疾病(PH- lhd)引起的PH与显著的发病率和不良预后相关[2].最初由左心房压力被动增加触发,PH可能在一系列可能导致血管重塑和右心衰的病理生物学事件的反应中进一步进展,包括内皮功能障碍、血管收缩和几种机制的放松[1,3.].
毛细管后PH值的血流动力学分类已被广泛讨论和争论。尽管最近受到挑战,目前的欧洲心脏病学会(ESC)和欧洲呼吸学会(ERS)指南定义了两种类型的毛细血管后PH: 1)分离毛细血管后PH (IpcPH;188bet官网地址舒张压梯度(DPG) <7 mmHg和/或肺血管阻力(PVR) <3木单位(WU))和2)毛细血管后PH与毛细血管前成分(称为复合毛细血管后和毛细血管前PH (CpcPH);DPG升高≥7 mmHg和/或PVR升高>3 WU) [2].与IpcPH相比,CpcPH可能与HF诱发的PH患者的预后更差有关[2,4].
心衰患者血浆内皮素-1水平升高,并与肺压升高相关[5]以及更高的死亡风险[6].基于这一观察,内皮素受体拮抗剂(ERAs)已被评估为心力衰竭的潜在治疗选择;潜在的益处尚未得到证实,这可能是因为早期过量液体潴留和HF恶化导致过早退出研究的发生率较高[7- - - - - -9].然而,迄今为止,没有研究根据PH-LHD的存在和严重程度对患者进行分层。考虑到它们的作用模式,ERAs可能对具有毛细血管前成分的PH-LHD患者有益。
Macitentan是一种获批用于肺动脉高压(PAH)长期治疗的ERA [10].总的来说,马西坦治疗PAH患者的浮肿并不是一个重要的安全性问题[11],使其成为PH-LHD评价的合适人选。由于液体潴留的潜在风险在铲运机的设置,与时代的主要目标MELODY-1 (Macitentan科目组合预处理和post-capiLlary肺动脉高压由于左心室功能障碍)是评价的安全性和耐受性Macitentan CpcPH患者10毫克。这是第一个专门在这一患者群体中评估ERA的研究。
方法
患者人群
年龄≥18岁的CpcPH患者经右心导管(RHC)证实(平均肺动脉压≥25 mmHg,肺动脉楔压(PAWP) >15 mmHg和<25 mmHg,静息PVR≥3 WU[≥240 dyn·s·cm]−5[和DPG≥7 mmHg))在筛查前或筛查期间的12周内符合条件。病人被要求有一个左心室射血分数(LVEF)≥30%,期间以超声心动图筛查和纽约心脏协会(NYHA FC)功能类II或III, 6分钟步行距离(6随钻测量)≥150米和一个优化稳定剂量的口服利尿(s)至少1周之前RHC和随机。接受ERAs、前列环素类似物、磷酸二酯酶-5型抑制剂或可溶性鸟苷酸环化酶刺激剂的患者被排除在外。
详情请参阅表S1.所有患者均获得书面知情同意。试验遵循了《赫尔辛基宣言》,研究方案得到了当地机构审查委员会或独立伦理委员会的批准。
研究设计
MELODY-1是一项多中心、双盲、随机、安慰剂对照、为期12周的II期研究(NCT02070991).筛查后,患者被随机分配(1:1)接受马西坦10mg或安慰剂,每日1次,按基线LVEF分层(<50%)与≥50%)。患者在第1、4、8和12周进行随机评估。过早停止研究治疗的患者需要在停止治疗后7天内进行治疗结束(EOT)访问。所有患者在永久停止研究治疗(研究访问结束)后进行至少30天的安全随访。在整个研究中监测不良事件(AEs)。
结果测量
与安全性相关的主要研究终点评估了从基线到EOT NYHA FC显著液体潴留或恶化的复合情况。显著的液体潴留被定义为任何时候由于液体超负荷或非肠道给药而使体重从基线增加≥5%或≥5 kg。其他安全终点包括在研究结束后30天内评估紧急治疗的AEs和实验室异常,以及利尿剂治疗的改变(即。增加剂量或额外给药)直到EOT。探索性疗效端点包括PVR和n端pro-brain利钠肽(中位数水平以上病人)的水平,在第12周表示为一个百分比的基线,基线的变化在其他血流动力学参数,第12周超声心动图参数和6随钻测量和恶化的住院发生的高频传输结束。为了确保所有RHC的质量,指导委员会提供了关于研究RHC指南的培训,并对每个地点随机分配的第一批患者的RHC追踪进行了审查,如果有必要,还会审查额外的追踪。
统计方法
由于研究的探索性,没有正式的功率计算。对于每个治疗组30例患者,马西坦和安慰剂在主要安全终点的比例上至少有30%的差异可以以95%的统计置信度排除。
主要安全终点在安全分析集上进行分析(所有接受至少一剂研究治疗的随机患者)。重要的液体潴留或恶化的患者的比例在FC给出了测试结束每个治疗组双侧95%置信区间(CIs)和治疗的不同报道双边95% CIs基于准确的二项分布和假定值基于确切概率法。其他安全性和耐受性终点(AEs,严重的AEs,由于AEs和实验室测量而停止)描述。
疗效分析基于完整的分析集(所有随机患者),在基线和第12周(时间窗+5天)评估观察病例。在第12周时间窗口中缺失的值不作为主要分析的估算值。在第12周对血流动力学变量的缺失数据进行了额外的分析,该分析是基于对仍然活着且未住院的患者的最后观察,而死亡或因心衰住院的患者的最差值被推断出来。以患者的最差值作为基线值,在同一治疗组中观察到的任何患者与基线相比恶化的百分比最高。第12周的PVR和NT-proBNP数据以基线的百分比表示,各治疗组均以几何均数和95% CIs表示,并以几何均数(95% CIs)比值表示macitentan的治疗效果与安慰剂。其他血流动力学和超声心动图参数及6MWD均以平均值(标准差(sd),并且从基线到第12周治疗差异的平均(95% CIs)绝对变化。使用统计分析系统版本9.3 (SAS Institute, Cary, NC, USA)进行统计分析。
结果
病人
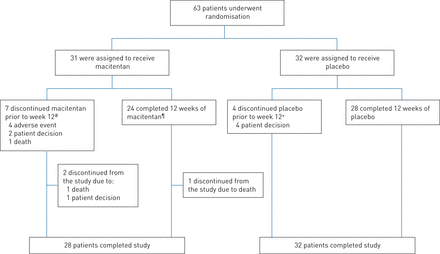
从2014年6月到2015年7月,在11个国家的28个地点对患者进行了筛查。共63例患者随机分为马西坦组(n=31)和安慰剂组(n=32) (图1).马西坦组的中位(范围)治疗时间为12.0(0.3-14.9)周,安慰剂组为12.1(8.0-14.1)周。11例(17.5%)患者过早停止治疗:马西坦组7例,安慰剂组4例。在63名随机分组的患者中,28名(90.3%)随机分组马西坦组和32名(100%)随机分组安慰剂组完成了30天的安全性随访。
耐心的性格。#:在7名在第12周之前停止使用马西坦治疗的患者中,有5人继续进行了他们的研究结束访问,并被认为完成了研究。其余两名患者没有进行研究结束访问(死亡n=1;病人决定n = 1)。¶:在24名完成12周马西坦治疗的患者中,1名患者没有结束研究访问(死亡n=1);+:所有4名在第12周之前停用安慰剂的患者都进行了研究结束访问,并被认为完成了研究。
总体上,中位年龄为71.0岁,87.3%的患者年龄≥65岁,中位体重指数为32.4 kg·m−2(表1).大部分患者(76.2%)LVEF保存(即。≥50%)和控制率心房颤动(73.0%)。基线时,该人群中位PVR为462.0 dyn·s·cm−5中位右心房压(mRAP)为13.0 mmHg (表2).基线中位NT-proBNP和6MWD为1515 pg·mL−1分别为300 m。与安慰剂组相比,马西坦组中女性和FC III患者比例更高。其他基线参数在两组之间保持平衡。
主要研究终点
macitentan组7例(22.6%)患者和安慰剂组4例(12.5%)患者经历了主要复合终点(表3).治疗差异为10.08% (95% CI) - 15.07-33.26),并由液体滞留成分驱动(治疗差异为13.21% (95% CI - 11.96-36.21)。在马西坦组中,所有7名达到主要安全终点的患者均出现显著的液体潴留,其中1名患者也报告FC恶化。在安慰剂组中,四分之三的患者由于显著的液体潴留达到了安全终点,一名患者由于FC从II期到III期恶化达到了安全终点。
在马西坦组,25例基线LVEF≥50%的患者中有6例(24.0%)报道了主要终点,6例基线LVEF <50%的患者中有1例(16.7%)报道了主要终点。在安慰剂组中,基线LVEF≥50%的23例患者中有3例(13.0%)报告主要终点,基线LVEF <50%的9例患者中有1例(11.1%)报告主要终点。
在马西坦组中,7例患者中有4例在随机分组的第一个月(第10、12、28、29天)出现明显的液体潴留;对于另外3例患者,液体滞留发生在第57、57和65天。在安慰剂组中,3名患者在第43、50和61天出现液体潴留。
其他安全/耐受性端点
马西坦组23例(74.2%)和安慰剂组19例(59.4%)发生至少一次AE。在马西坦组中,数字上更多的患者经历了至少一次严重的AE与安慰剂组11例(35.5%)与6例(18.8%)和因AEs而过早停止治疗(5 [16.1%])与0);这些差异是由满足主要研究终点(表S2和S3).马西坦组有8例(25.8%)患者和安慰剂组有6例(18.8%)患者出现至少一种与水肿和液体超载相关的AE (表S4).
总的来说,有2例患者死亡,均在马西坦组:1例患者在接受第一剂量马西坦后1天死亡,主要原因是细菌性呼吸道感染引起的呼吸衰竭,1例患者在完成12周治疗期后16天死亡,报告为猝死。这两起死亡被认为与治疗医生的研究治疗无关。
化验所并没有发现任何新的安全信号(表S5).血红蛋白值<100 g·L−1macitentan组有5例(17.9%),安慰剂组有2例(6.3%);在这些患者中,2名马西坦组患者和1名安慰剂组患者经历了主要终点。马西坦组有9例(29.0%)患者和安慰剂组有7例(21.9%)患者在EOT之前的利尿剂治疗有变化。在大多数情况下,利尿剂给药的变化与AE相关(在马西坦和安慰剂组中,分别有8 / 9和6 / 7的患者)。
血流动力学和超声心动图参数
使用马西坦后血流动力学变量无显著变化与安慰剂(表4,表S6).观察两组患者PVR、跨肺压梯度(transulmonary pressure gradient, TPG)、DPG和平均肺动脉压(mean pulmonary arterial pressure, mPAP)的改善情况。第12周休息时的PVR,以基线的百分比(几何平均值)表示,在两个治疗组中相似:马西坦为66.3% (95% CI 56.2-78.3),安慰剂为71.2% (95% CI 51.4-98.8)。第12周的治疗效果(macitentan/安慰剂的几何均数比)为0.93 (95% CI 0.64-1.36) -即。与安慰剂相比,macitentan的平均百分比降低- 7% (95% CI - 36-26%)。心脏指数,马西坦治疗第12周的平均疗效与安慰剂为0.4 L·min−1·米−2(95% CI 0.1 - -0.7)。两组患者的PAWP和mRAP均无变化。从基线到第12周,其他血流动力学参数和超声心动图参数的变化(表S7)在治疗组之间也相似。为了解释第12周的缺失数据,使用归因法对参数进行了评估,结果与主要分析的结果一致(表S8).
中位数水平以上病人
在第12周,NT-proBNP表达为基线百分比(几何平均值)为91.6% (95% CI 72.4-115.8;n=25)和118.9% (95% CI 92.5-152.8;N =26),安慰剂组(图2).马西坦组的NT-proBNP水平在第12周降低与安慰剂组,治疗效果(几何均数比)为0.77 (95% CI 0.55-1.08),表明macitentan的平均百分比降低了23%(−45-7%)与安慰剂。
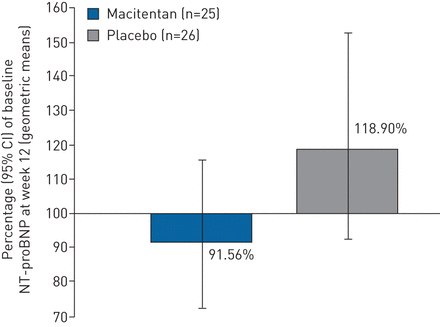
第12周基线n端脑利钠前肽(NT-proBNP)百分比。全分析集。误差柱代表95%置信区间(CI)。
6随钻测量
意思是(sd)从基线到第12周的变化,马西坦组(n=22)为- 5.9 m(71.8),安慰剂组(n=25)为8.4 m(76.4)。马西坦的平均处理效果与安慰剂为- 14.3 m (95% CI - 58.0-29.4)。
HF恶化至EOT的住院治疗
macitentan组5例(16.1%)患者和安慰剂组2例(6.3%)患者因HF恶化至EOT住院(治疗差异9.9% (95% CI−15.1-33.3))。所有因心衰恶化而住院的病例均与一个主要研究终点事件相关。
讨论
meldy -1是第一个评估ERA对CpcPH患者疗效的随机对照试验,也是为数不多的需要RHC诊断的PH-LHD试验之一。
一些用于治疗PAH的疗法,主要是针对一氧化氮和内皮素途径的,已经在HF和PH-LHD患者的研究中进行了评估[7- - - - - -9,12- - - - - -19].然而,结果并不一致;尽管一些研究报告了运动耐量、功能能力和临床状态的改善[18,19,其他的则没有显示出统计学上或临床上的显著改善[7,9].此外,ERAs研究中HF的早期恶化导致了人们对治疗期间水肿发展的安全性的担忧[6,7].
与其他HF中ERAs的研究相比,meldy -1主要针对PH-LHD伴CpcPH的患者,其中大多数患者的射血分数得到保留。患者群体表现出该疾病的典型特征(老年人、多重合并症、伴随药物治疗),多数患者存在一定程度的左室舒张功能下降、右室扩张和右室收缩功能障碍。与其他多环芳烃特异性药物治疗HF的研究相比,该人群的LHD更严重,NT-proBNP基线水平更高,基线血流动力学特征更差[14,15,17].有趣的是,我们观察到与以前的研究相比,房颤的发生率更高。
由于水肿已被确认为HF人群中ERAs的安全性问题,本研究的主要目的是调查马西坦在这一目标人群中的安全性和耐受性。在MELODY-1中,macitentan组中有更多的患者经历了明显的液体潴留或FC恶化,因此与安慰剂相比达到了主要复合研究终点。液体潴留是达到这一终点的主要驱动因素,马西坦组中多余的液体潴留事件发生在研究的早期。ENABLE研究也报道了晚期收缩期左心衰患者经波生坦治疗后早期出现液体潴留[7].此外,在MELODY-1中,与安慰剂相比,macitentan治疗的患者出现严重的AEs、中断研究治疗和因心衰恶化而住院的数量更高。达到主要研究终点的相同患者驱动了这些其他安全参数的治疗效果。据报道,马西坦组更多的患者血红蛋白值<100 g·L−1与安慰剂组(5与两个)。贫血是临床试验中经常报道的副作用。这种贫血的病因尚未阐明,但可能是,至少部分归因于血液稀释。
治疗12周后PVR无明显差异,两组患者PVR下降幅度相似(治疗效果:0.93;95%可信区间0.64 - -1.36)。有趣的是,mRAP没有变化(治疗效果为0.7 mmHg;95% CI−4.3-4.9)或PAWP(治疗效果−0.3 mmHg;95% CI−4.2-3.7),这可能提示马西坦与EOT时左右侧填充压力的恶化无关。由于缺乏可比较的有创血流动力学数据,我们的结果无法与以往研究ERA在心衰中的作用的试验进行比较[1,2,6- - - - - -8].同样有趣的是,我们观察到安慰剂组的PVR、TPG、DPG和mPAP有所改善,而PAWP没有变化。尽管这种观察结果的原因尚不清楚,但类似的观察结果以前曾在一项比较西地那非的研究中报道过与心衰患者的射血分数保留,安慰剂组的肺血流动力学改善,包括PVR, mPAP和PAWP [17].
NT-proBNP是一种成熟的心血管反应生物标志物,反映心脏负荷和左心室壁应力[20.].在HF中,NT-proBNP水平升高和升高与严重症状、液体潴留和更坏的预后相关[21,而减少则与结果的改善有关[22].与最近的两项心衰随机试验相比[14,17],我们观察到macitentan组NT-proBNP水平无显著性下降23%(治疗效果0.77;95%可信区间0.55 - -1.08)。虽然该观察的临床相关性尚不清楚,是否有利尿剂变化的影响尚未调查,但我们的研究结果表明,NT-proBNP的有利变化没有发生心脏充盈压力的恶化。
运动能力的限制是慢性心衰的主要表现[23].6MWD是一种测量运动能力的指标,已在许多PAH研究中用于评估治疗效果[24- - - - - -26].我们观察到macitentan的6MWD有下降的趋势(治疗效果- 14.3 m;95% CI−15.1-33.3)。此外,体重增加和水肿对6MWD的影响程度尚不清楚。
这项研究应该在其局限性的背景下加以解释。这是一项旨在探索安全性的试点研究,研究人群较小,且没有正式的功率计算。样本量使本研究对患者间的变异性敏感。此外,一些探索性变量的数据缺失比例较大,主要是由于过早停药。12周的持续时间很短,需要较长的随访时间才能通过超声心动图观察到心脏结构的变化。然而,这项研究是第一次探索治疗干预在毛细血管ph后和前患者中的作用。没有数据支持在PH-LHD中使用多环芳烃特异性药物,导致在ESC/ERS指南中使用该类药物的III级推荐[2].我们研究的目的是在一项适当设计的研究中,在毛细血管PH后和前的患者中获得更多PAH药物(ERAs)的潜在益处的证据,以解决这一领域未满足的需求。这些数据提醒我们,到目前为止,我们还没有针对这一患者群体的有效治疗方法。
结论
在这个II期探索性研究中,CpcPH患者人群表现为晚期和重度心力衰竭。与安慰剂相比,在头4周内,Macitentan与显著液体潴留的数值上更高的发生率相关,似乎没有证据表明EOT时心脏充盈压力增加。
补充材料
披露的信息
补充材料
m . Delcorixerj - 01886 - 2017 - _delcroix
m . Efficaceerj - 01886 - 2017 - _efficace
m . Hutyraerj - 01886 - 2017 - _hutyra
g .缺乏erj - 01886 - 2017 - _lack
k . Papadakiserj - 01886 - 2017 - _papadakis
l·鲁宾erj - 01886 - 2017 - _rubin
J.-L。Vachieryerj - 01886 - 2017 - _vachiery
确认
医疗写作协助由琳达·麦克沃伊提供,由Actelion制药有限公司资助。作者希望感谢研究人员对这项研究的参与。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
编辑评论欧元和J2018;51: 1702589。
支持声明:本研究得到Actelion Pharmaceuticals Ltd的支持。本文的资金信息已存入Crossref资助者注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2017年9月15日。
- 接受2017年11月20日。
- 版权©2018人队