摘要
背景淋巴管平滑肌瘤病(LAM)患者迫切需要疾病进展和治疗反应的生物标志物。基于活性的纳米传感器是一种新兴的生物传感器,可以检测失调的蛋白酶在活的有机体内并释放一名记者来提供疾病的泌尿读数由于蛋白酶在LAM中调控异常,可能直接导致肺功能下降,基于活性的纳米传感器可能能够定量、实时监测LAM进展和治疗反应。我们旨在评估基于活动的纳米传感器在肺LAM临床前模型中的诊断效用。
方法Tsc2雌性裸鼠静脉注射-null细胞,建立小鼠肺部LAM模型。一个包含14个活性纳米传感器的库,设计用于检测多种催化类别的蛋白酶,被注射到LAM小鼠和健康对照的肺部,收集尿液,并进行质谱分析以测量纳米传感器切割产物。然后用雷帕霉素治疗小鼠,并用基于活性的纳米传感器监测。通过机器学习来区分患病小鼠和健康小鼠,以及治疗小鼠和未治疗小鼠。
结果基于多种活性的纳米传感器(PP03(由金属,天冬氨酸和半胱氨酸蛋白酶裂解),p调整< 0.0001;PP10(被丝氨酸,天冬氨酸和半胱氨酸蛋白酶裂解),p调整=0.017))在患病和健康的肺中进行差异切割,从而可以使用机器学习模型进行强分类(曲线下面积(AUC)与健康的0.95)。在雷帕霉素启动后的2天内,我们观察到PP03和PP10的正常切割,机器学习能够准确地分类治疗反应(未治疗的AUC为0.94)。
结论基于活性的纳米传感器能够在LAM的临床前模型中实现无创、实时监测疾病负担和治疗反应。
摘要
无创测量肺部蛋白酶活性的纳米颗粒能够实时监测淋巴管平滑肌瘤病小鼠模型的疾病进展和治疗反应https://bit.ly/3z4cnAh
简介
淋巴管平滑肌瘤病(LAM)是一种罕见的肺部疾病,以囊性肺破坏、进行性肺功能下降及肺衰竭为特征[1].病理学上,LAM的特征是肺内平滑肌样LAM细胞异常增殖,这些细胞可能源于子宫[2].LAM细胞在结节性硬化症复合体(TSC) 1或2中具有双等位基因功能丧失突变,其作用是抑制雷帕霉素复合体1 (mTORC1)的机制靶点。LAM细胞异常表达蛋白酶(主要是基质金属蛋白酶(MMP) 2和9 [3.- - - - - -5]和组织蛋白酶K (CTSK)),它们具有胶原溶解活性[6]并可能直接导致肺退化及囊肿形成[7- - - - - -9].与mTORC1在这一疾病过程中的作用一致,雷帕霉素是LAM患者的标准护理方法[10,11].然而,雷帕霉素治疗不能治愈,当停止治疗时,疾病会恶化,需要持续治疗,并伴有相关的副作用[11,12].目前,肺功能测试,包括用力呼气量在1秒(FEV1),是监测疾病负担和治疗反应的标准方法[13].然而,FEV1容易出现技术上的变异性[14并且对治疗反应缓慢,阻碍了临床决策和临床试验的步伐。因此,迫切需要定量、准确、快速反应的生物标志物来监测LAM患者并评估新疗法的疗效。
鉴于现有LAM生物标志物的局限性,各种额外的血液生物标志物和成像工具已被探索[15].大多数LAM患者血清血管内皮生长因子(VEGF)-D升高[16,17]因此被提议作为一种候选生物标志物。然而,VEGF-D对LAM的敏感性不佳[17]且其水平不能可靠地预测对治疗的反应[16].最近的一项研究显示,在接受雷帕霉素和羟氯喹联合治疗的LAM患者血清中,32种循环生物标志物,包括VEGF-D发生了显著变化[18].然而,到治疗第3周,未发现分析物变化与FEV相关124周研究持续时间的变化。最后,高分辨率计算机断层扫描(HRCT)已被研究作为监测治疗反应的候选工具,但尚未显示成像结果因雷帕霉素治疗而改变[19].
由于失调的蛋白酶是LAM的一个标志,我们假设测量蛋白酶活性可以实现对疾病的准确和定量监测。我们的小组以前开发了“基于活动的纳米传感器”,用于测量疾病活动在活的有机体内通过查询病变部位蛋白酶活性[20.- - - - - -26].短的8 - 12氨基酸肽底物与纳米颗粒结合,静脉注射或气管内注射。在疾病部位,肽底物被失调的蛋白酶裂解,释放出被清除到尿液中的条形码“报告者”,在那里它们可以被质谱(MS)检测到。通过将每个基板附加一个唯一的报告器,可以同时测试多个基板。在这里,我们建立了基于活动的纳米传感器在肺部LAM的新型小鼠模型中的效用。使用机器学习,我们建立分类器,准确读取LAM疾病活动和进展,并快速检测对雷帕霉素治疗的反应。总的来说,这些结果支持了基于活动的纳米传感器的临床开发,用于监测LAM的进展和治疗反应。
方法
中提供了更多详细信息补充材料.
动物实验
所有动物研究均由麻省理工学院动物护理委员会(Cambridge, MA, USA)批准(规程0420-023-23)。对于所有需要麻醉的手术,小鼠均采用异氟醚(Zoetis, Parsippany, NJ, USA)吸入麻醉。
小鼠肺LAM模型
105K细胞用荧光素酶慢病毒编码和嘌呤霉素选择盒(LP-hLUC-Lv201-0200;Genecopoeia, Rockville, MD, USA),然后用嘌呤霉素(1 μg·mL)进行筛选−1).建立一个在活的有机体内LAM模型,注射3-4周龄雌性裸鼠注射。与5×105荧光化105K细胞(105K- luc)。疾病负担由IVIS监测在活的有机体内成像系统(PerkinElmer, Waltham, MA, USA)。为在活的有机体内在含0.25%聚乙二醇-200和0.25%吐温-80的载液中制备雷帕霉素。LAM小鼠腹腔注射雷帕霉素(LC实验室,Woburn, MA, USA)(1或3 mg·kg−1)或车辆,每周3-4次,并由IVIS系统监测。
在活的有机体内使用基于活动的纳米传感器进行疾病监测
纳米传感器(Glu-Fib-substrate-PEG-840 kDa)用于泌尿实验,由CPC Scientific (San Jose, CA, USA)合成,使用前用0.2 μm注射器过滤器进行无菌过滤。将总体积为50 μL,每个纳米传感器浓度为20 μM的甘露醇缓冲液(0.28 M甘露醇,5 mM磷酸单碱钠,15 mM磷酸二碱钠,pH 7.0 ~ 7.5)加入纳米传感器信息技术。灌注后立即皮下注射PBS (200 μL)以增加尿量。纳米传感器给药后60分钟膀胱排空,收集给药后60 - 120分钟产生的所有尿液。收集每只小鼠的尿液,并在−80°C冷冻。采用上文所述的液相色谱(LC -MS/MS) [21].
统计分析
对于所有尿液实验,LC-MS/MS生成的尿峰面积比(PAR)值归一化为注射剂量中每个纳米传感器的PAR,然后在进一步统计分析之前在给定尿液样本中的所有报告中进行平均缩放。为鉴别泌尿系统差异报告者,所有报告者均采用未配对双侧t检验进行分析,随后使用Prism 7.0版的Holm -Šídák方法对多个假设进行校正(GraphPad, San Diego, CA, USA)。p调整<0.05被认为是显著的。主成分分析(PCA)在平均缩放PAR值上执行,并使用prcomp包在R中实现,并使用ggplot2 (www.r-project.org).对于基于尿活动的纳米传感器特征的疾病分类,随机分配成对数据样本集,包括特征(平均缩放PAR值)和标签(如。“LAM(18天)”和“Rap(+2天)”)用于训练用MATLAB R2019b中的TreeBagger类实现的随机森林分类器(www.mathworks.com).对袋外误差的估计用于交叉验证,并在随机分配的测试队列上测试训练过的分类器。对每个分类问题进行10个独立的训练试验,并使用MATLAB计算的受试者工作特征统计量来评估分类性能。分类器的性能报告为10个独立试验的平均精度和曲线下面积(AUC)。
结果
Tsc2缺乏导致蛋白酶失调
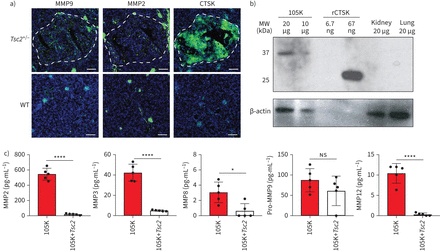
我们首先试图建立一个小鼠模型,以捕捉LAM的特征——失调的蛋白酶活性[1].我们用杠杆Tsc2-缺失的肾囊腺瘤细胞系,称为“105K”,以前来源于肾肿瘤,在a中自发形成Tsc2+ /−鼠标(27].分析与分离105K细胞相似的自发小鼠肾囊腺瘤,发现MMP2和MMP9点状表达,CTSK强烈、普遍表达(图1一个,最高)。这三种蛋白酶在野生型小鼠肾脏中均不存在(图1一个,底部)。与lam相关的CTSK活性依赖于酸性微环境的报道一致[28],中性pH培养的105K细胞的裂解物Western blot显示了一个37 kDa的条带,对应于pro-CTSK [29) (图1 b).当重组表达的小鼠CTSK蛋白在同一凝胶上运行时,检测到一条与活性蛋白酶形态大小一致的27 kDa条带。在野生型小鼠肾或肺匀浆中未观察到抗ctsk反应条带(图1 b).最后,我们发现105K细胞分泌多种金属蛋白酶在体外MMP2、MMP3、MMP8和MMP12的表达水平经重新引入后均显著降低Tsc2(图1 c).
Tsc2缺乏导致蛋白酶表达异常。a)小鼠肾脏自发形成的代表性原发病变(白色部分)中基质金属蛋白酶(MMP) 9、2和组织蛋白酶K (CTSK)的免疫荧光染色(绿色)Tsc2+ /−小鼠(上)与健康对照小鼠(下)的肾脏进行比较。蓝色:4 ',6-二氨基-2-苯基吲哚(核)。比例尺:200 μm。b) Western blot检测105K细胞裂解物、重组小鼠CTSK (rCTSK)和健康小鼠肾脏和肺中抗小鼠CTSK的抗体。每个样品均显示β-肌动蛋白免疫染色。每个通道的蛋白质量被记录下来。c)表达式(均值±sd),通过多重蛋白试验,在条件介质中检测来自105K细胞和105K细胞的MMPs,并重新引入逆转录病毒Tsc2(n = 5)。ns:不重要的;*:p < 0.05;****:通过双尾t检验,p<0.0001。WT:野生型;MW:分子量。
Tsc2-null细胞对雷帕霉素有反应在体外和在活的有机体内
的Tsc1和Tsc2基因分别编码错构瘤蛋白和结节蛋白,形成复合物抑制mTORC1级联[10,30.].错误蛋白或结节蛋白的缺失会导致mTOR信号的紊乱,从而导致细胞生长和增殖不受控制。我们试图评估雷帕霉素,一种mTOR抑制剂和LAM患者的一线治疗是否会抑制105K细胞生长。
我们首先用雷帕霉素处理105K细胞在体外并发现它们的生长以剂量依赖的方式减慢(补充图S1a).接下来,我们试图评估是否可以将105K细胞引入小鼠肺部,以诱导类似人类LAM的疾病。以前的LAM模型利用了Tsc2-null“TTJ”细胞作为侧翼肿瘤传代以增加侵袭性,但尚不清楚亲本“105K”细胞是否能有效地在肺中播种[9].要启用在活的有机体内为了追踪疾病负担,我们使用荧光素酶表达盒对105K细胞进行了慢病毒转导。然后进行尾静脉注射5×105荧光素酶+105K (105K- luc)细胞,并通过IVIS系统监测荧光素酶表达。我们发现105K-Luc细胞接种肺部,并在接种后3周内形成可检测的疾病负担,通过IVIS系统评估(补充图S1b(上)及组织学评估(补充图S2).这些病变呈增生性,所有病变均有明显的Ki-67染色(补充图S3).目的:评价雷帕霉素的疗效在活的有机体内,我们在105K-Luc细胞接种后立即用雷帕霉素治疗小鼠(“预防”)或接种后20天(“治疗”)。我们观察到,在第0天接受雷帕霉素治疗的小鼠疾病非常轻微,在第20天接受雷帕霉素治疗的小鼠疾病在8天内几乎完全消退(补充数字S1b和c和S2).
Tsc2-缺陷的病变存在异常蛋白酶活性
我们接下来试图调查蛋白酶的活性Tsc2不足的病变。我们首先注入1×106105 k细胞南卡罗来纳州。植入雌性裸鼠的侧翼,当肿瘤体积达到~ 500毫米时切除肿瘤3..我们孵育这些肿瘤的匀浆,以及健康裸鼠的肺,用16个淬灭荧光蛋白酶底物组成的小组,预计金属、丝氨酸和半胱氨酸蛋白酶广泛裂解,并随时间监测荧光(补充图S4a) [22,24].我们发现多种基质被优先裂解Tsc2-与健康肺相比,有缺陷的肿瘤均质(补充图S4b).通过对解理数据进行主成分分析,我们发现105K解理谱独立于健康肺部聚集,证明了蛋白水解景观的全球差异(补充图S4c).为了评估在肺中建立105K病变时是否保留了这些蛋白水解差异,我们启动了肺LAM模型通过注射。注入5×105105K-Luc细胞并于5、13和19天后采集支气管肺泡灌洗液(BALF)。我们在患病小鼠和健康对照组的13天和19天孵育BALF,另外还有16个淬灭荧光底物(补充图S4d),并通过主成分分析发现,随着疾病进展而增加的患病小鼠和健康小鼠肺蛋白酶活性的整体差异(补充图S4e).有趣的是,这项研究揭示了来自我们的LAM小鼠模型的BALF和匀浆中的蛋白酶优先裂解底物PP05和PQ16,这表明无论微环境如何,tsc2缺陷生物标本中的蛋白酶活性模式都是保守的(即。旁边的肿瘤与肺部病变)(补充图S4b和d).
然后,我们在BALF中进行ELISA,以定量105K病变小鼠肺部的MMP9和MMP2浓度。我们观察到,在接种105K细胞后13天(p=0.0028)和19天(p=0.0011),患病小鼠BALF中的MMP9浓度显著增加(补充图S5a).此外,我们发现MMP9浓度与疾病负担相关,通过IVIS系统评估(r2=0.63, p=0.0007) (补充图S5b).我们观察到患病小鼠BALF中MMP2浓度在第19天增加的趋势(p=0.16) (补充图S5c)并发现MMP2浓度与疾病负担相关(r2=0.49, p=0.0053)补充图S5d).免疫荧光染色显示第19天105K病灶中CTSK普遍表达(补充图S6).
基于活性的纳米传感器可以被蛋白酶有效地裂解
在建立了LAM小鼠模型,评估了其对雷帕霉素的反应性,并描述了其蛋白水解景观后,我们接下来寻求开发基于活性的纳米传感器,以检测这些蛋白酶。由于LAM的特征是广泛的蛋白酶失调,这在我们的小鼠模型中得到了重现,我们选择了一组由14个肽底物组成的面板,我们之前发现这些底物可被多个类别的蛋白酶切割,包括基质蛋白酶和组织蛋白酶[21].我们首先试图表征每种底物对不同催化类蛋白酶的敏感性。我们合成了每种底物的淬灭荧光版本,设计使荧光在蛋白水解裂解时被激活。我们将每个探针分别与重组人金属蛋白酶(MMP2)、丝氨酸蛋白酶(丝氨酸蛋白酶3 (PRSS3))、天冬氨酸蛋白酶(napsin a天冬氨酸肽酶(NAPSA))和半胱氨酸蛋白酶(CTSK)在蛋白酶浓度从10 pM到10 nM范围内孵卵,并监测荧光随时间的增加(补充图S7).我们发现面板上的每个探针都有一个独特的解理特征(补充数字S7和S8),每种蛋白酶都能裂解至少一个探针,在孵育1小时后,最低可检测到的蛋白酶浓度低至10 pM (补充图S8和补充表S1).因此,我们得出结论,14种提名的肽底物提供了广泛而敏感的催化类蛋白酶的覆盖范围。
PP03被天冬氨酸蛋白酶裂解Tsc2在酸性条件下-缺陷病变
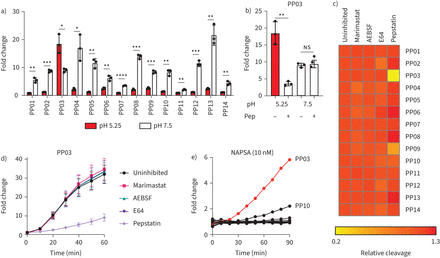
接下来,我们试图研究不同种类的蛋白酶的活性Tsc2并评估14肽底物检测每种蛋白酶类的能力。我们稀释了匀浆Tsc2在pH值7.5的缓冲液中,将其与14种含氟肽底物中的每一种孵育,含有或不含金属蛋白酶抑制剂(marimastat)、丝氨酸蛋白酶(4-(2-氨基乙基)苯磺酰氟盐酸盐(AEBSF))、半胱氨酸蛋白酶(E64)和天冬氨酸蛋白酶(pepstatin)。我们发现只有marimastat和AEBSF能明显抑制肽切割,这表明只有金属蛋白酶和丝氨酸蛋白酶在其中有活性Tsc2在中性pH条件下的-缺陷组织(补充图S9).鉴于最近报道的细胞外酸化驱动LAM病理性蛋白酶活性[28],在酸性(pH为5.25)缓冲液中重复此实验。在酸性pH下,14个肽中的13个肽的解理显著降低,而其中一个肽,PP03的解理显著增加(p调整= 0.011) (图2一个).因此,我们假设PP03可能被天冬氨酸蛋白酶或半胱氨酸蛋白酶裂解,这些蛋白酶在酸性条件下表现出最佳活性Tsc2缺乏组织。我们发现,在pH值5.25时,天冬氨酸蛋白酶抑制剂pepstatin几乎完全消除了PP03的裂解(p=0.0017) (图2 b),但不受丝氨酸、金属或半胱氨酸蛋白酶抑制剂的影响(图2 cd).根据这些观察,我们发现PP03是我们研究中天冬氨酸蛋白酶NAPSA裂解效率最高的肽段(图2 e).总的来说,这些数据表明,这14种底物广泛检测中性pH下的金属蛋白酶和丝氨酸蛋白酶,而PP03在105K肿瘤匀浆中特异性检测酸性pH下的天冬氨酸蛋白酶。
PP03被天冬氨酸蛋白酶裂解Tsc2a)用pH 5.25或pH 7.5缓冲液稀释的105K肿瘤匀浆孵卵30分钟后,PP01-PP14的荧光折叠变化。*: p调整< 0.05;* *: p调整< 0.01;* * *: p调整< 0.001;* * * *: p调整<0.0001采用双尾t检验,然后对多个假设进行调整,Holm -Šídák校正。b)用pH为5.25或pH为7.5的稀释液(含或不含蛋白酶抑制素(Pep))孵育30 min后PP03的荧光折叠变化。ns:不重要的;* *: p < 0.01。c)相对于未受抑制的匀浆,在pH值5.25的缓冲液中稀释,与或不与金属蛋白酶抑制剂(马里司他特)、丝氨酸蛋白酶(4-(2-氨基乙基)苯磺酰氟盐酸盐(AEBSF)、半胱氨酸蛋白酶(E64)或天冬氨酸蛋白酶(蛋白酶司他汀)孵育30分钟后的底物裂解。d) PP03与105K细胞肿瘤的匀浆在pH为5.25、加或不加蛋白酶抑制剂的条件下孵育,荧光随时间增加。e)与napsin A天冬氨酸肽酶(NAPSA)孵育的PP01-PP14荧光随时间增加。PP03用红色表示。
基于活性的纳米传感器能够对小鼠肺部105K病变进行无创检测
使复用蛋白酶活性测量在活的有机体内,这14种底物中的每一种都被唯一地标记为质量编码的泌尿报告。如前所述[20.],我们使用可变标记的14-mer谷氨酸纤维蛋白肽B (Glu-Fib)与稳定的同位素富集氨基酸,以唯一的条形码每个14肽底物。多重反应监测通过液相色谱三重四极杆质谱(LC-MS/MS)可在宽线性范围内定量评估尿报告浓度[21].最后,如前所述,将这14种条形码蛋白酶底物偶联到40 kDa八臂PEG纳米颗粒上[21].
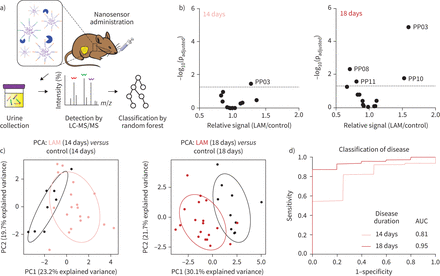
然后我们表演了注射。注入5×105105K-Luc细胞和IVIS系统监测疾病发展(补充图S10).我们使用14 plex纳米传感器面板信息技术。在疾病诱导后14天和18天,LAM小鼠灌注(图3一).收集给药后1 - 2小时内产生的所有尿液,并进行质谱检查。在第14天,我们观察到肺蛋白酶对PP03的活性显著增加,我们之前发现PP03在低pH值下被天冬氨酸蛋白酶裂解(图2),在LAM小鼠中相对于健康对照组(p调整= 0.034) (图3 b(左)。此外,在14天的LAM小鼠中,发现PP03信号正相关(r=0.5871, p=0.0082) (补充图S11a)与疾病负担,以及两个主要由丝氨酸蛋白酶裂解的传感器[21], PP08 (r=−0.6983,p=0.0009) (补充图S11b)和PP11 (r=−0.4617,p=0.0466) (补充图S11c),与疾病呈负相关。与这一发现一致的是,在18天,LAM小鼠中PP03的卵裂进一步增加(p调整= 1.4×10−5)和PP08的裂解(p调整=0.0047)和PP11 (p调整=0.026)显著降低(图3 b,对吧)。在这些差异切割纳米传感器的基础上,我们在两个测试时间点通过PCA无监督降维观察LAM和健康小鼠的分离(图3 c).然后,我们使用来自两个时间点的LAM小鼠子集和健康对照组训练了一个随机森林机器学习分类器,并测试了它在同一实验的独立队列中准确分类小鼠的能力。我们发现分类器早在第14天就将LAM小鼠与健康对照组区分开来(AUC 0.81),并且在第18天时分类得到增强(AUC 0.95) (图3 d).我们的结果表明,基于活性的纳米传感器可以测量肺LAM小鼠模型中疾病相关的蛋白酶失调,从而实现准确的疾病检测。
基于活性的纳米传感器区分淋巴管平滑肌瘤病(LAM)小鼠与健康对照。a)方法示意图。b)在14天比较LAM小鼠和健康对照组的平均标度尿报告浓度(LAM: n=19;对照组:n=9)和18天(LAM: n=19;对照:n=10)病诱导和−log后10(p调整)绘制了LAM与对照之间的折叠变化。通过双尾t检验计算显著性,然后对多个假设进行调整,并使用Holm -Šídák校正。虚线是p点调整= 0.05。c)疾病诱导后14天和18天,LAM小鼠和健康对照组尿报告量的主成分分析(PCA)。d)随机森林分类器在14天内对来自LAM小鼠子集和健康对照组的泌尿报告者进行训练(LAM: n=5;对照组:n=5)和18天(LAM: n=5;控制:n = 5)。受试者工作特征曲线显示了该分类器在独立试验队列中区分LAM小鼠和健康对照组的性能(LAM: n=14;对照组:n=4)和18天(LAM: n=14;对照组:n=5天。LC:液相色谱;MS:质谱; AUC: area under the curve.
基于活性的纳米传感器能够在LAM小鼠中快速评估治疗反应
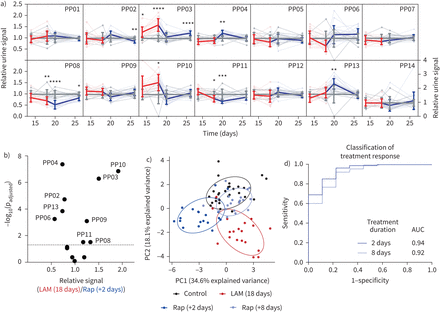
然后,我们试图评估基于活性的纳米传感器是否能够对LAM的治疗反应进行客观、定量和快速的评估。我们在疾病诱导后18天开始用雷帕霉素治疗LAM小鼠,并在雷帕霉素诱导后2天和8天用活性纳米传感器监测它们的肺蛋白酶活性。使用IVIS系统,我们观察到早在治疗开始后2天肺部疾病负担就显著降低(p<0.0001), 8天后进一步降低(补充图S10b).我们发现,在LAM小鼠中,PP03和PP10这两个信号在18天显著增加的传感器,在治疗诱导后2天内恢复到基线(p调整=从控制不显著)(图4一).值得注意的是,我们还观察到PP04的裂解在基线之上有短暂的增加(p调整=0.0012(对照组)和PP13 (p调整对照组=0.0042)。图4一).总的来说,14个纳米传感器中的9个被雷帕霉素治疗显著改变,这表明肺蛋白水解景观发生了深刻的变化(图4 b).与这一发现一致,我们通过主成分分析发现,接受雷帕霉素治疗2天的LAM小鼠与治疗前的LAM小鼠和健康对照组(图4 c和补充图S12).然而,继续雷帕霉素治疗8天导致肺蛋白酶活性与对照组密切聚集。最后,我们在第18天使用LAM小鼠亚群,在治疗2天或8天后使用雷帕霉素治疗小鼠训练了两个随机森林分类器,并在独立队列中测试了它们准确分类治疗小鼠和未治疗小鼠的能力。我们发现,在两个测试时间点,分类器都能准确地区分治疗小鼠和未治疗小鼠,在治疗诱导后2天,分类最强(AUC 0.94) (图4 d).因此,基于活性的纳米传感器可以快速可靠地检测肺部LAM小鼠模型对雷帕霉素的反应。
基于活性的纳米传感器能够快速评估淋巴管平滑肌瘤病(LAM)的药物反应。a) 14个基于活动的纳米传感器PP01-PP14的控制归一化泌尿报告信号。细线显示了每只小鼠随时间变化的基于活动的纳米传感器轨迹,而粗线是所有小鼠的平均轨迹。红线代表雷帕霉素治疗前的LAM小鼠(n=19),蓝线代表服用3mg·kg雷帕霉素的LAM小鼠−1雷帕霉素(每周3-4次)。灰线代表健康对照小鼠(n=10)。*:p < 0.05;* *: p < 0.01;* * *:p < 0.001;****: p<0.0001来自对照。错误条为sd.为了清晰起见,PP14以更大的规模呈现y设在。b)显示意义的火山图(−对数)10(p调整)),以及注射105K-Luc细胞18天后LAM小鼠(“LAM(18天)”)相对于雷帕霉素治疗2天后LAM小鼠(“Rap(+2天)”的各尿液报告者的折叠变化。虚线是p点调整= 0.05。c)在每个时间点将平均标度泌尿报告者浓度归一化至匹配对照,并进行主成分分析。d)在LAM(18天)小鼠(n=10)子集和Rap(+2天)(n=10)或Rap(+8天)(n=10)小鼠的尿报告器上训练两个随机森林分类器。受试者工作特征曲线显示了这些分类器在同一实验的独立测试队列中区分Rap(+2天)(n=9)和Rap(+8天)(n=9)小鼠与未处理LAM(18天)(n=9)小鼠时的表现。AUC:曲线下面积。
讨论
在这项工作中,我们展示了基于活动的纳米传感器在肺部LAM的一种新的临床前模型中监测进展和治疗反应的效用。我们发现,一个多路传感器面板能够对疾病进行分类,主要是由于针对两个传感器PP03和PP10的肺蛋白酶活性增加。此外,我们发现该蛋白酶活性在治疗开始2天后恢复到基线水平,能够近乎完美地分类治疗反应。
治疗反应监测体内Via蛋白酶活性的测量比其他替代终点(如血清生物标志物、成像和肺活量测定)有几个优点。在LAM中,肺蛋白酶失调可能直接导致肺退化,导致肺功能下降和肺衰竭[1,7,8].因此,测量疾病部位的蛋白酶活性可能提供评估疾病活动和预测长期结果的最直接手段。相反,在血液中发现的生物标志物具有内在相关性,这可以从LAM患者血清生物标志物浓度变化与长期临床结果之间缺乏一致性得到证明[16].尽管HRCT等成像方法能够直接显示囊肿体积,而囊肿体积与肺功能相关,但这些发现似乎并没有因治疗而逆转[31].最后,肺功能检测是测定肺功能的金标准方法,但由于技术的可变性和较长的滞后时间,其在治疗反应监测中的实用性受到限制[1].虽然需要临床研究来充分验证它们在预测长期结果方面的效用,但基于活动的纳米传感器可能提供最直接和最快速响应的方法来读取LAM中的疾病活动和治疗效果。
我们的工作还揭示了在我们的LAM小鼠模型中疾病进展和雷帕霉素反应的生物学的新见解。最近的共培养实验表明,拉姆相关成纤维细胞的细胞外酸化导致溶酶体蛋白酶CTSK的表达和活性增加TSC2−−/细胞(28].有趣的是,在LAM小鼠中被优先切割的两个纳米传感器PP03和PP10,是面板中唯一被典型溶酶体蛋白酶NAPSA (图2 e,补充数字S7和S8和补充表S1)及组织蛋白酶D [21]在酸性条件下。在这项工作中,我们还证明了CTSK在酸性缓冲液中对PP03和PP10的有效切割。最后,PP03是唯一在酸性条件下被105K肿瘤匀浆优先裂解的肽。这些发现表明,基于活性的纳米传感器可以实时监测LAM中蛋白酶活性的细胞外酸化和由此产生的畸变。值得注意的是,我们发现雷帕霉素治疗可使PP03和PP10迅速恢复到健康水平,这与雷帕霉素治疗抑制细胞外酸化和蛋白酶活性的发现一致在体外[28].疾病负担与尿PP08和PP11信号呈负相关,可见丝氨酸蛋白酶活性明显下降,这可能反映了丝氨酸蛋白酶抑制剂在疾病进展过程中的表达增加,这是其他肺部疾病的特征[32,33],但尚未在LAM中被描述。最后,我们观察到在雷帕霉素处理后,多个纳米传感器的切割瞬时增加。解理增加最显著的传感器PP04,解理效率最高在体外通过丝氨酸蛋白酶,包括参与免疫反应的丝氨酸蛋白酶[21].虽然还需要进一步的研究来充分阐明这种短暂增加的蛋白酶活性的机制,但我们的结果强调了基于活性的纳米传感器在直接查询疾病相关生物过程方面的强大功能在活的有机体内.
这项工作建立了基于活动的纳米传感器作为监测LAM进展和治疗反应的新范式,但未来的研究应该解决关键的局限性和未回答的问题。特别是,我们没有充分描述这里描述的小鼠模型的囊性肺破坏、淋巴受累或肺功能下降的证据,所有这些都是人类LAM的特征[1].此外,尽管许多研究都描述了金属蛋白酶的失调[3.,4]及CTSK [28]在LAM中,与疾病进展的明确因果关系尚未建立,MMP抑制剂多西环素的小型试验未能在LAM患者中产生临床获益[34].虽然我们证明了基于活性的纳米传感器的肺切割对小鼠雷帕霉素治疗快速反应,但我们没有评估这些变化是否与我们小鼠模型的长期功能结果相对应。临床试验将是必要的,以评估活动为基础的纳米传感器在预测治疗的长期反应方面的效用。最后,我们交付了基于活动的纳米传感器通过信息技术。滴注,但在人类使用时,需要临床兼容的给药方法,如干粉吸入或雾化。
总之,我们已经在LAM小鼠模型中证明了基于活动的纳米传感器在监测进展和治疗反应中的效用。在临床上,基于活性的纳米传感器可以快速评估接受雷帕霉素或新兴实验疗法治疗的患者的治疗反应。通过实现对疾病活动的实时监测,基于活动的纳米传感器可能大大加快临床试验的速度,并提供准确和及时的信息来指导患者护理。
补充材料
可共享的PDF
确认
我们感谢A.D. Warren和H.E. Fleming (Koch癌症综合研究所,MIT, Cambridge, MA, USA)分别协助研究的概念化和实验设计,以及对手稿的批判性编辑;A. Mancino (Syneos Health, Princeton, NJ, USA)进行质谱分析;以及科赫研究所斯旺森生物技术中心(MIT),特别是组织学核心和临床前建模、成像和测试核心,提供技术援助。
脚注
作者贡献:J.D. Kirkpatrick, J.S. Dudani, E.P. Henske和S.N. Bhatia发起了这项研究。J.D. Kirkpatrick和A.P. Soleimany进行了实验和统计分析。J.D.柯克帕特里克,A.P.索莱马尼,J.S.杜达尼,H-J。Liu, H.C. Lam, C. Priolo, E.P. Henske和S.N. Bhatia对实验设计和数据解释做出了贡献。S.N. Bhatia和E.P. Henske监督了这项研究。J.D. Kirkpatrick和S.N. Bhatia撰写了手稿的初稿。所有作者都参与了后续草稿的撰写和编辑,并批准了最终稿。
利益冲突:J.D. Kirkpatrick在研究期间报告了路德维希癌症研究基金的资助。此外,J.D. Kirkpatrick还有一项专利正在申请中(肺蛋白酶纳米传感器及其用途;PCT/US2019/052868, 2019年9月25日提交)。
利益冲突:A.P.索莱马尼没有什么可披露的。
利益冲突:J.S.杜达尼没有什么可透露的。
利益冲突:H-J。刘没有什么可透露的。
利益冲突:H.C. Lam没有什么可透露的。
利益冲突:C. Priolo没有什么可透露的。
利益冲突:E.P.亨斯克没有什么可透露的。
利益冲突:S.N. Bhatia报告了其他来自霍华德休斯医学研究所和国家环境健康科学研究所的支持,路德维希癌症研究基金的资助和科赫研究所大理石癌症纳米医学中心的资助,在进行研究期间;其他来自Vertex Pharmaceuticals, Glympse Bio, Maverick Therapeutics, Satellite Bio, CEND Rx和Moderna Therapeutics的支持,在提交的工作之外。此外,S.N. Bhatia还有一项专利正在申请中(肺蛋白酶纳米传感器及其用途;PCT/US2019/052868, 2019年9月25日提交)。
支持声明:本研究部分由国家癌症研究所(Swanson生物技术中心)的科赫研究所支持拨款P30-CA14051,国家环境健康科学研究所的核心中心拨款P30-ES002109,路德维希癌症研究基金和科赫研究所大理石癌症纳米医学中心支持。J.D. Kirkpatrick感谢路德维希中心奖学金的支持。A.P. Soleimany感谢美国国立卫生研究院分子生物物理学培训基金(NIH/NIGMS T32 GM008313)和美国国家科学基金会研究生研究奖学金的支持。J.S.杜达尼感谢国家科学基金会研究生研究奖学金、路德维希中心奖学金和西贝尔学者基金会的支持。S.N. Bhatia是霍华德休斯医学研究所的研究员。本文的资助信息已存入交叉参考基金注册.
- 收到了2021年3月4日。
- 接受2021年8月14日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org