摘要
饮食摄入与n-3 (ω-3)极长链多不饱和脂肪酸即。二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),在儿童中期和哮喘的风险很少。我们的目的是调查儿童时期从鱼类中摄取较多的EPA和DHA是否与发生哮喘的风险较低有关。
在雅芳父母和孩子的纵向研究中,通过7岁时的食物频率问卷来估计鱼的EPA和DHA的饮食摄入量。我们使用逻辑回归,控制混杂因素,分析EPA和DHA的摄入量(四分位数)与11岁或14岁时医生诊断的哮喘发病率之间的关系,并探索脂肪酸去饱和酶(时尚)多态性(rs1535)。在瑞典BAMSE出生队列中寻求复制。
没有证据表明从鱼类中摄入EPA和DHA与哮喘发病之间存在关联(n=4543)。然而,当按时尚基因型,优势比比较顶端与2025个小G等位基因携带者的最低四分位数为0.49 (95% CI 0.31-0.79;p趋势=0.006),但在纯合子大A等位基因组中未观察到负相关(OR 1.43, 95% CI 0.83-2.46;p趋势(p = 0.19)交互= 0.006)。在BAMSE中也复制了这种基因-营养相互作用对哮喘发作的影响。
在儿童中有常见的时尚不同的是,儿童时期从鱼类中摄取较多的EPA和DHA与直到青春期中期发生哮喘的风险较低密切相关。
摘要
患有常见脂肪酸去饱和酶的儿童(时尚)的变异,在儿童中期从鱼中摄取较多的二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)与直到青春期中期发生哮喘的风险较低密切相关https://bit.ly/2M4VxO6
简介
大量的流行病学证据表明,生命过程早期的饮食与哮喘和其他过敏性疾病的病因有关。然而,儿童的大多数证据来自横断面研究,因此限制了因果推断[1- - - - - -3.].鱼的摄入量引起了人们的特别关注,因为鱼是丰富的维生素d来源nω-3极长链多不饱和脂肪酸(VLC-PUFAs),即。具有抗炎作用的二十碳五烯酸(EPA)和二十二碳六烯酸(DHA) [4- - - - - -6].鱼中的其他营养成分,如维生素D和硒,也可以预防哮喘[7].
为数不多的纵向研究调查了鱼类和n3 VLC-PUFA摄入与哮喘和过敏性疾病的关系主要集中在孕期或婴儿期接触[8];一项出生队列报告称,儿童中期吃鱼与随后的哮喘之间没有关联,但没有调查两者之间的关联n-3 VLC-PUFA进气口[9].在雅芳父母与儿童纵向研究(ALSPAC)中,25%的儿童在7至14岁期间要么出现新的哮喘,要么哮喘缓解或持续存在[10];饮食中鱼类的摄入量n儿童期的-3 VLC-PUFAs可能在影响这一阶段的哮喘风险中发挥重要作用。此外,这些暴露对哮喘的有益影响可能在某些亚组中最为明显。内源性VLC-PUFAs的产生取决于脂肪酸去饱和酶(FADS)转化前体脂肪酸的效率[5].a的小G等位基因时尚在全基因组关联研究的元分析中,单核苷酸多态性(SNP) rs1535预测较低的血浆EPA和DHA浓度[11]以及参与怀孕期间补充鱼油的随机对照试验(RCT)的母亲[12].在后一项随机对照试验中,母亲携带G等位基因的孩子患哮喘的风险中,补充剂的有益作用最大[12],表明预先形成的EPA和DHA的外源性供应(如。对于具有这种G等位基因的个体来说,要想获得高的地位和EPA和DHA的健康益处是必要的时尚SNP。
在这项研究中,我们调查了鱼的摄入量和n-3从7岁的鱼身上提取的VLC-PUFAs,并在青春期中期发生哮喘。我们还探索了这些联想是否会被儿童的记忆所改变时尚基因型,以加强因果推理。
方法
研究人群
ALSPAC是一个以人口为基础的出生队列,主要招募了居住在英国前雅芳郡的白人孕妇,预产期为1991年4月1日至1992年12月31日(14541例)。自出生以来,研究人员对队列进行了年度问卷调查,自7岁起,在年度研究诊所进行了客观测量。研究方案已在前面描述过[13,14]及更多资料,请浏览www.alspac.bris.ac.uk,其中载有所有可用资料的详情(www.bristol.ac.uk alspac /人员/我们的数据).伦理批准获得了ALSPAC伦理和法律委员会(机构审查委员会批准00003312)和地方国家卫生服务研究伦理委员会的批准。使用所收集数据的知情同意通过根据当时ALSPAC伦理和法律委员会的建议,从参与者那里获得了问卷和诊所。
暴露评估
我们使用食物频率问卷(FFQ)在孩子54个月(~ 4岁)和81个月(~ 7岁)时收集的饮食信息,由孩子的母亲或主要照顾者完成。FFQ包括了多达56类食物和12种饮料的日常消费问题,有5个频率选项,从“从不或很少”到“每天超过一次”[15].鱼类摄入量包括五种:贝类、带面包屑或面糊的白鱼、不带包衣的白鱼、金枪鱼及油性鱼(详情载于补充材料).总能量和营养的摄入通过乘以估计的食物摄入量(g·day)来计算−1),按英国食物成分表的估计营养含量计算[16,17,然后把这些数据加起来。鱼类的脂肪酸组成是基于英国典型鱼类的概况[16].因此,每天从鱼类中摄取的EPA和DHA的总量n-6脂肪酸和花生四烯酸(ann-6 PUFA,这也取决于内源性生产的FADS)。产妇在孕32周时EPA和DHA的摄入量也由FFQ进行了类似的估计。
结果评估
我们感兴趣的主要结果是偶发哮喘。在91个月(~ 7.5岁)、128个月(~ 11岁)和166个月(~ 14岁)时,我们根据母亲们是否积极回答“医生是否真的说过您所研究的孩子患有哮喘?”,并至少回答以下同时出现的问题中的一个,即孩子在过去12个月内是否有喘息、喘息和胸部吹口哨、哮喘或哮喘药物。在那些在7.5岁时没有被诊断为目前医生诊断的哮喘的儿童中,我们将那些在11或14岁时被诊断为目前医生诊断的哮喘的儿童定义为偶发哮喘病例。关于次要结果的更多细节可在补充材料.
基因分型
在20个snp中n-3代谢,我们选择了一个SNPFADS2基因rs1535是我们的主要候选变体,因为先前有强有力的证据表明它可以预测血液中的EPA和DHA的水平[11],也改变了鱼油补充剂的效果[12].使用1000基因组参考面板(Phase 1, Version 3)对其进行了0.999的imputation质量(进一步细节)补充材料中是否有).有非欧洲血统遗传证据的参与者在归责前被排除。
统计分析
在8140名7岁儿童的膳食数据中,有4543名儿童的哮喘发作数据是完整的(补充图E1)。我们使用逻辑回归来检验鱼的摄入量,以及鱼的EPA和DHA(四分位数)与哮喘事件的关系,使用摄入量最低的四分位数作为参考类别。在模型中加入四分位数采食量作为拟连续变量,检验线性趋势。我们从现有文献中选取了已知的潜在混杂因素[18],然后利用有向无环图方法(图1) [19].多变量模型和协变量的细节在补充材料.
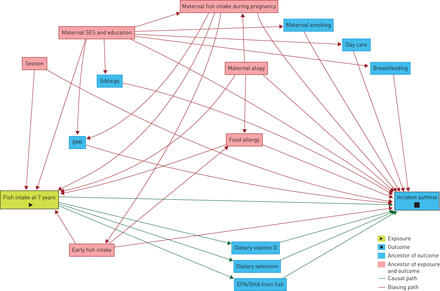
有向无环图研究儿童7岁时鱼类摄入量与哮喘发病风险之间的协变量和潜在的结构混杂偏倚。SES:社会经济地位;BMI:身体质量指数;二十碳五烯酸;DHA:二十二碳六烯酸。
我们进行了分层分析先天的探索潜在的改变饮食关联时尚基因型(rs1535:主要A等位基因纯合(AA)与小G等位基因杂合子+纯合子(GA/GG);合并后两种基因型进行分析,因为GG个体数量较少:n=393(占总数的10.8%),只有29例哮喘发作病例。使用似然比检验(p=0.26)检验rs1535等位基因频率分布是否偏离Hardy-Weinberg平衡。的交叉积项来评估潜在的相互作用时尚以四分位(中位数)作为回归模型连续变量的基因型。
作为时尚基因也与n-6途径,导致花生四烯酸的产生具有促炎作用,我们还探讨了摄入总n花生四烯酸和rs1535对哮喘的影响。我们还评估了累积暴露于EPA和DHA(定义为在4岁和7岁时始终处于摄入的顶部或底部四分之一)与哮喘发作的关系。4岁时的饮食信息不被认为是主要暴露,因为在这么小的年龄缺乏哮喘诊断意味着无法定义随后的哮喘事件。我们还探讨了母亲在怀孕期间摄入EPA + DHA与母亲的相互作用时尚11或14岁哮喘发作的基因型。最后,我们进行了几项敏感性分析,包括进一步调整、排除、限制性三次样条分析,以检验剂量-反应关系和逆概率加权,以纠正潜在的损失-随访偏差[20.](详情请参阅补充材料).所有统计分析均使用Stata 14.2版本(StataCorp, College Station, TX, USA)进行。
复制队列
我们使用瑞典基于人群的出生队列研究BAMSE(瑞典语儿童、过敏、环境、斯德哥尔摩、流行病学的缩写)来复制ALSPAC的主要发现。1994-1996年在斯德哥尔摩出生的4089名婴儿被纳入BAMSE队列,并被反复跟踪[21,22].在为期8年的临床测试中,父母们被要求填写一份FFQ,其中包含瑞典人经常消费的98种食品和饮料的问题,包括6个关于鱼类摄入量的问题[23].根据从瑞典国家食品管理局数据库获得的组成值,估计鱼类的EPA和DHA摄入量[24].在8岁、12岁和16岁时,我们定义了当前医生诊断的哮喘,与ALSPAC非常相似,因此在12岁或16岁时确定了偶然哮喘病例(n=2138)。我们使用了与ALSPAC中使用的相似的分析方法补充材料).
结果
ALSPAC鱼类摄入量的中位数(四分位数范围)估计为24.3 (11.1-38.6)g·天−1主要是白鱼(平均占总摄入量的74.6%),其次是金枪鱼(18.4%)。鱼的EPA和DHA摄入量分别为11.2(5.99 ~ 24.0)和17.6 (9.77 ~ 41.4)mg·d−1两者高度相关(r>0.95),因此我们的主要分析集中在EPA和DHA的综合摄入量上。表1显示了儿童及其母亲在四分之一儿童EPA和DHA摄入量中的特征。在7岁时,从鱼中摄取较多EPA和DHA的儿童更有可能是女性,总能量摄入量更高,通常更注重健康的饮食模式和更多的补充剂使用。这些孩子在出生后的第三个月更有可能是纯母乳喂养,在6个月前吃过鱼,在7岁前有食物过敏史。从鱼类中摄取较多EPA + DHA的孩子的母亲年龄较大,受教育程度较高,住在廉租房的可能性较低,并且在怀孕后期从鱼类中摄取较多EPA + DHA。在有食鱼资料的儿童中,3370人(56.3%)携带该小等位基因时尚基因型(rs1535)。没有证据表明AA和GA/GG基因型组在背景特征上有差异,除了AA组更倾向于健康意识饮食模式(补充表E1).
鱼的摄入量
在整个研究样本(n=4543)中,我们没有发现任何证据表明7岁时的鱼类摄入量与11或14岁时(n=393)的哮喘事件之间存在关联。然而,当按时尚基因型,在GA/GG组中,更多的鱼摄入量与较低的哮喘发作风险相关,但在AA组中没有(表2).当我们进一步调整EPA和DHA的摄入量时,小等位基因组的反关联显著减弱与下四分位0.86,95% CI 0.48-1.54;p趋势=0.57),但在调整维生素D摄入量时没有(OR 0.66, 95% CI 0.41-1.05;p趋势=0.08)或硒(or 0.61, 95% CI 0.37-0.99;p趋势= 0.05)。
鱼的EPA和DHA的摄入量
从鱼类中摄入EPA和DHA与哮喘发病风险没有显著相关性。然而,当我们按时尚基因型,在GA/GG组中观察到强烈的负相关,并有剂量反应关系的证据,但在AA组中没有(p交互= 0.006) (表3而且补充图E2).在GA/GG组中,EPA + DHA摄入量最低的四分之一组的儿童患哮喘的比例为11.4%,最高的四分之一组的儿童患哮喘的比例为6.6%。4年和7年的累积暴露(r=0.46)显示出更强的相关性:OR比较在两个时间点高摄入量与持续低摄入量的GA/GG组0.33 (95% CI 0.15-0.70)和AA组1.19 (95% CI 0.52-2.71) (p交互= 0.02)。
总摄入量n-6或花生四烯酸与哮喘发病无关,无论是总体上还是按时尚基因型(补充表E2).rs1535与哮喘发作无关(每小G等位基因OR 0.91, 95% CI 0.76-1.09)。我们没有观察到7岁时从鱼中摄入的鱼或EPA + DHA与11或14岁时发生湿疹的547例(12.7%)或花粉热的933例(19.6%)之间的关联,无论是总体上还是按时尚基因型(数据未显示)。
敏感性分析
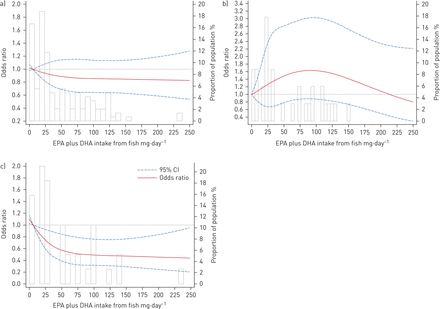
哮喘病发病的关系,尤其是那些时尚在排除59名(1.3%)非白人母亲的子女、749名(16.5%)有食物过敏史的儿童、390名(8.6%)有极端能量摄入的儿童后,对初次接触鱼类时的年龄、健康意识饮食模式评分、任何补充剂使用、7或14岁时的体重指数或主成分分析得出的群体亚结构遗传标记进行进一步调整后,也没有发生实质性变化。98名(2.2%)7岁有喘息的儿童和16名(0.3%)服用鱼肝油或n-3补充剂(补充表E3).EPA和DHA的摄入量也观察到了同样的关联模式(补充表E4和E5).限制性三次样条分析显示,小G等位基因(p非线性=0.04),但AA组无显著性差异(p非线性=0.11)或整体(p非线性= 0.50) (图2).此外,当我们使用逆概率加权法或能量调整的EPA和DHA摄入残差法(补充表E6).
在雅芳父母与子女纵向研究中,通过限制性三次样条分析,研究了来自鱼类的二十碳五烯酸(EPA) +二十二碳六烯酸(DHA)与哮喘发病风险之间的剂量-反应关系:a)总体上,b)主要等位基因a纯合者和c)次要等位基因G携带者。根据性别、7岁时的总能量摄入、母亲的教育程度、怀孕期间的住房期限、怀孕期间的经济困难、母亲的种族、母亲的特应性疾病史、母亲分娩时的年龄、纯母乳喂养、15个月时由日间托儿所托儿、母亲是否吸烟、哥哥姐姐、弟弟妹妹和完成食物频率问卷时的季节,对模型进行了调整。rs1535 GA/GG基因型组占56.3%。鱼的EPA + DHA摄入量范围为0 ~ 675 mg·d−1因为偏斜度,所以这个被截断了。
母亲在怀孕期间从鱼类中摄取EPA和DHA与11或14岁时发生哮喘的风险较低有微弱的关联(调整或比较前四分位数)与下四分位数0.69,95% CI 0.48-0.98);然而,没有证据表明效果的修改时尚基因型(补充表E7).重要的是,儿童7岁时EPA和DHA的摄入量与哮喘发病之间的关系与孕妇在怀孕期间的摄入量无关(补充表E5).
最后,我们测试了所有其他snp事后分析发现12个snp处于强连锁不平衡状态(10个snp带有rs1535, 2个snp带有rs3734398),因此得出了相同的结果(数据未显示)。我们没有发现其他7个SNPs的显著效应修饰的证据,尽管根据rs1535,有微弱的证据表明,从鱼类中摄取EPA和DHA与某些SNPs的小等位基因携带者发生哮喘之间存在负相关(补充表E8).
讨论
在携带小G等位基因a的ALSPAC儿童中,超过一半的儿童时尚多态性(rs1535),我们发现在儿童中期和哮喘发作之间,鱼的摄入量和从鱼中获得的EPA和DHA之间存在很强的负相关。在BAMSE出生队列中,这些基因-营养相互作用对哮喘事件的复制证实了主要发现不太可能是偶然出现的。据我们所知,这些新发现对各种敏感性分析都是可靠的。
儿童中期鱼类摄入量与哮喘发病之间的整体关系仅在之前的一项研究中进行过调查,即BAMSE队列研究;与我们的研究结果一致的是,在该研究中也没有观察到任何关联[9].然而,我们发现微弱的证据表明,在未成年人携带者中时尚等位基因,更多的鱼摄入量与较低的哮喘风险相关,这在以前没有报道过。虽然儿童中期的鱼类摄入量可能反映了生命过程中早期类似的家庭饮食习惯,但我们的研究结果不太可能被母亲的鱼类摄入量所混淆n-3 VLC-PUFA来自于怀孕期间的鱼类或婴儿期早期接触鱼类。
在小G等位基因携带者中,鱼类摄入量与哮喘发病之间的负相关主要是由EPA和DHA解释的。缺乏关于儿童时期饮食中EPA和DHA摄入量与哮喘发病之间联系的纵向数据。虽然之前没有研究报道过改变饮食摄入和n-3 ldl - pufas与哮喘的关系时尚在最近的一项随机对照试验中,Bisgaardet al。[12]在怀孕期间补充鱼油对儿童早期哮喘风险的保护作用同样被修正时尚母亲的基因变异。我们的发现扩展了这些观察结果,并提示在某些个体中可能有预防儿童晚期发作哮喘的潜力。与ALSPAC队列相比,BAMSE队列整体上的反相关可能反映了相对较高的发病率n-3 VLC-PUFA进气及更高时尚小等位基因频率(62%)与56%)。
当我们比较持续的高水平时,我们显示了更强的关联性与4岁和7岁时的摄入量一直很低。这可能反映了长时间接触的有益影响或减少接触的错误分类,使用两个时间点的膳食数据。尽管如此,它加强了因果关系的论据。一个重要的问题是,与疾病相关的饮食调整可能产生反向因果偏差,特别是在食物过敏儿童中。然而,当我们排除有任何食物过敏史的儿童时,我们的主要发现并没有实质性的改变。
机制
EPA和DHA可以通过多种途径调节炎症过程,如增加促炎、消炎或消炎作用较弱的介质[4,25].而血药浓度n- 8岁时的VLC-PUFAs与BAMSE既往哮喘发病呈负相关[26],生物标记的使用不能区分外在(膳食)和内在来源。孕妇鱼油补充剂的随机对照试验isgaardet al。[12的研究也发现,抗炎作用只对后代哮喘有影响,而对其他过敏相关疾病没有影响,这表明抗炎机制可能仅限于呼吸道。主要内生来源n-3 VLC-PUFAs通过的途径主要是由编码的去饱和酶调控时尚基因,它将植物转化为n-3 PUFA前体α-亚麻酸(ALA)合成EPA再合成DHA。rs1535小等位基因的携带者FADS2)的ala - epa转化率较低。因此,他们的血液中EPA和DHA的浓度往往较低[11],因此更依赖于饮食来源。这可能解释了为什么在这一基因亚群中,高EPA和DHA的饮食摄入量与较低的哮喘发病风险相关。值得注意的是,FADS2影响两个n3和n-6 PUFA通路,我们观察到的效果修饰是特定于EPA和DHA的摄入,而不是n-6脂肪酸或花生四烯酸,进一步加强了因果推理。
优势与局限
ALSPAC出生队列的优势包括其基于人群的前瞻性设计,大的规模,丰富的饮食信息(在多个时间点)和潜在的混杂因素,以及可用性时尚基因型数据。详细的,重复的,表型结果测量提供了一个机会来研究事件而不是流行的病例。与任何观察性研究一样,不能排除未测混杂或残留混杂的可能性,尽管我们在分析中控制了许多潜在混杂因素。我们不能检查与特应性和特应性哮喘的纵向联系,因为皮肤刺刺试验只在7岁时进行。由于缺乏以后任何时间点哮喘状况的信息,有一部分7岁的合格儿童(25.6%)没有纳入我们的分析。然而,在纵向研究中,失去随访偏差仅被证明略微改变了相关性[27我们的逆概率加权分析证实,它不太可能对我们的结果产生偏差。虽然我们使用的FFQ没有与其他工具(如饮食日记)进行正式校准,但它是基于Y使用的FFQ阿奈尔等.[28]已根据称重膳食记录进行验证,并根据本地称重膳食调查进行更新[29].虽然饮食接触可能存在一些错误的分类,特别是由于FFQ缺乏份量大小的定量信息,相互作用n-3 VLC-PUFA进气口和时尚基因型反对大量的暴露错误分类。此外,就哮喘而言,任何此类错误分类都可能是随机的,这将倾向于使效应估计偏向于零。在这一背景下,我们在一项独立队列研究(BAMSE)中发现的重复性得到了加强,因为两国偏好的鱼类种类和制备方法不同。然而,就绝对摄入量给出明确的建议还为时过早n考虑到FFQs的半定量性质和估计的差异,3 VLC-PUFA需要在哮喘风险方面获得最大收益nALSPAC和BAMSE人群之间的-3摄入量,更重要的是观察性研究在建立因果关系方面的内在局限性。
目前英国的建议是每周吃两份鱼(相当于280克·周)−1对于成年人来说),其中一种应该是富含油脂的鱼类[30.].在过去十年中,英国儿童的鱼类消费量略有增加[31];然而,只有4.2%的儿童达到了推荐摄入量[30.].如果我们的发现是因果关系,这可能最终导致根据基因型在人口的大亚群中进行个性化一级预防的策略。与此同时,应注意增加鱼类摄入量的公共卫生信息。
结论
尽管在ALSPAC中缺乏整体关联的证据,但我们已经在患有共同时尚基因变异与较差的内源性合成n-3 VLC-PUFAs,儿童时期从鱼类中摄取较多的EPA和DHA与发生哮喘的风险较低相关。
补充材料
可共享的PDF
确认
我们非常感谢所有参与这项研究的家庭、帮助招募他们的助产士,以及整个雅芳父母和孩子纵向研究团队,其中包括面试官、计算机和实验室技术员、文书工作者、研究科学家、志愿者、经理、接待员和护士。我们也感谢参与BAMSE队列的儿童和家长,以及多年来参与这项研究的所有工作人员。我们还要感谢Annabelle Bédard (Université Paris- saclay, Paris, France)在这个项目开始时提供的帮助。这篇论文是为了纪念我们已故的同事约翰·亨德森。
脚注
本文的补充资料可从www.qdcxjkg.com
作者贡献:M. Talaei和S.O. Shaheen构思了这项研究。M. Talaei进行了统计分析。M. Talaei和S.O. Shaheen一起起草了手稿。P.C.考尔德,L.R.琼斯和P.M.埃米特在饮食和营养方面提供建议。R. Granell建议哮喘变量。E. Sdona、A. Bergström和E. Melén进行了复制研究。所有作者都协助解读数据,并对手稿进行批判性编辑。所有作者都看过并认可了手稿的最终版本。R. Granell和S.O. Shaheen将为其内容提供担保。 S.O. Shaheen had full access to all the data in the study and had final responsibility for the decision to submit for publication.
利益冲突:M. Talaei没有什么可透露的。
利益冲突:E. Sdona没有什么可透露的。
利益冲突,p。c。考尔德没有什么要透露的。
利益冲突:L.R. Jones报告了雀巢营养公司在提交作品之外的资助。
利益冲突:下午埃米特报告了雀巢营养公司在提交工作之外的资助。
利益冲突:r·格拉纳尔没有什么可透露的。
利益冲突:A. Bergström没有什么可透露的。
利益冲突:E. Melén没有什么可透露的。
利益冲突:s.o Shaheen没有什么可透露的。
支持声明:该项目和M. Talaei由Rosetrees Trust和the Bloom Foundation (M771赠款)资助。英国医学研究理事会、维康信托基金(拨款217065/Z/19/Z)和布里斯托大学为ALSPAC提供核心支持。全基因组关联研究数据由威康桑格研究所和LabCorp(美国实验室公司)的样本物流和基因分型设施在23andMe的支持下生成。有关奖助金及资助的详细名单可浏览ALSPAC网站(www.bristol.ac.uk / grant-acknowledgements.pdf alspac /外部文件).BAMSE研究得到了瑞典心肺基金会、瑞典研究委员会、斯德哥尔摩地区(ALF项目和数据库管理)、瑞典健康、工作生活和福利研究委员会、Formas和瑞典哮喘和过敏研究基金会的资助。E. Melén由欧洲研究理事会资助(TRIBAL;757919)。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2020年9月25日。
- 接受2021年1月14日。
- 版权所有©作者2021
此版本在知识共享授权许可4.0的条款下发布。