抽象的
α-1抗胰蛋白酶缺乏(AATD),主要是由于PI * ZZ基因型serpina1.,是最常见的遗传性疾病之一。由于PI*ZZ与高疾病负担相关,并可通过戒烟部分预防,因此通过基因分型识别PI*ZZ个体可以改善健康结果。
我们检查了来自英国Biobank的患者的个体的PI * ZZ基因型的频率,并评估了基因型与临床结果和死亡率的关联。进行了苯胺 - 伟大的协会研究(PPEPAS)以揭示与基因型的疾病关联。1 s中强制呼气量的多基因风险评分(PRS)(FEV1)/用力肺活量(FVC)比值用于评价PI*ZZ的变异外显率。
在英国Biobank的458名欧洲祖先参与者中,140名患有PI * ZZ基因型,只有九次(6.4%,95%CI 3.4-11.7%)被诊断出赤行。具有PI * ZZ的COPD(或8.8,95%CI 5.8-13.3),哮喘(或2.0,95%CI 1.4-3.0),支气管扩张(或7.3,95%CI 3.2-16.8),具有显着较高的COPD(或8.8,95%CI 1.4-3.0),肺炎(或7.8,95%CI 1.5-4.9)和肝硬化(或7.8,95%CI 2.5-24.6),与PI * mm(野生型)相比,死亡率较高(2.4,95%CI 1.2-4.6)危害)(n = 398 424)。这些协会在吸烟者中更强大。PPEMAS展示了脓胸,气胸,恶病虫害,多环血症,动脉瘤和胰腺炎的少数。多基因风险评分和PI * ZZ与FEV独立相关1/ fvc <0.7(或1.4 / 1-SD.改变,95%CI 1.4-1.5和或4.5,95%CI 3.0-6.9)。
通过吸烟的诊断,可以通过基因型引导诊断来改善AATD的重要下诊所,其结果是部分预防的。
抽象的
只有6.4%的基因型定义的α-1抗胰蛋白酶缺乏症患有这种严重的疾病在英国Biobank患有这种严重的疾病。基因型引导诊断可以帮助识别英国的数千人与这种部分可预防的疾病.https://bit.ly/3dMu5Ng
介绍
α -1抗胰蛋白酶缺乏症(AATD)是欧洲血统人群中最常见的遗传性呼吸道疾病之一[1].α -1抗胰蛋白酶(AAT)是一种蛋白水解酶弹性蛋白酶的抑制剂,严重缺乏AAT会增加中性粒细胞弹性蛋白酶的负担,导致肺气肿[2].此外,非分泌AAT肝肝肝疾病对肝脏疾病的暂存[2].
AATD是由突变引起的serpina1.导致蛋白质的电泳迁移率变化的基因易于与不完全穿透的AATD [3.,4].最常见的疾病相关突变是PI*Z (p.Glu342Lys), PI*ZZ纯合子是AATD最常见的表型[2].化合物杂合学基因型PI * SZ,其中PI * S是另一个畸形突变(P.VAL264GLU),与吸烟者中肺气肿的风险更温和地相关[5].pi * mm是指野生型等位基因的纯合子。
AATD经常在鉴定具有家族史的个人鉴定COPD或肝病之后临床诊断,并且诊断的平均年龄为~45岁[6].一份先前的报告,利用文献中估计的等位基因频率[7,但在没有直接基因分型的情况下,估计在30509个PI*ZZ和PI*SZ个体中,只有1068个被纳入了国际AATD登记[8].
考虑到aatd特异性治疗的部分疗效[9]和提供戒烟咨询,对AATD的早期诊断可以促进更早的戒烟治疗干预,并允许识别高危家庭成员。鉴于英国最近宣布要对500万人进行基因测序[10.],可能存在有机会识别具有高风险基因型的个体,并加入适当的诊断程序以减少这种疾病的负担。
在这里,我们试图了解的普遍存在serpina1.评估AATD的诊断率。我们接下来探讨了两者之间关联的大小serpina1.基因型和呼吸条件,肺量测定结果的变化,其他肺外条件和全因死亡率。利用英国生物样本库的大样本量,我们开展了一项全现象相关性研究(PheWAS)来调查潜在的相关性serpina1.有其他结果的基因型。最后,我们计算了1秒用力呼气量(FEV)的多基因风险评分(PRS)1(强制生命能力(FVC)的比例评估相互作用serpina1.基因型和影响肺功能的常用变体。
材料和方法
英国Biobank研究科目
英国Biobank是一名基于人口的队列,招募了来自英国40-69岁的人。我们选择了欧洲血统的458个参与者(定义在补充资料,图S1和S2,表S1常数)serpina1.Z和S基因型信息(RS28929474和RS17580)。这两种变异都在英国Biobank进行了基因分型,因此我们的研究不依赖于估算。RS28929474和RS17580的次要等位基因频率分别为0.020和0.048。列出了基因型的基因型定义和质量控制度量补充表S2.非欧洲血统的Z和S等位基因状态列于补充表S3.
道德合规性
英国BIOBANK被西北部多中心研究伦理委员会批准,并在参加之前从所有参与者获得知情同意。
临床数据确定
流行疾病是通过医生自我报告的诊断、自我报告的疾病最近用药信息、与医院事件统计相关的国际疾病分类(ICD)-9和-10代码确定的(见补充表S4),如英国生物样本库之前的研究[11.,12.].我们承认,常见的疾病通常在初级保健环境中进行管理,因此除了医院阶段统计外,我们还包括自我报告的医生所诊断的疾病确定标准。英国Biobank研究协议可在线获购[13.].愈合诊断是AATD的所有已知并发症(补充表S4)[14.- - - - - -17.].UK Biobank的ICD-10编码没有ICD-10编码的AATD亚分类(E88.01),但提供了E88.0的诊断,这代表了血浆蛋白代谢紊乱的联合诊断,可能包括除AATD外的诊断,如纤溶酶原缺乏和双白蛋白血症。为了评估AATD诊断的患病率,我们确定了报告医生诊断为AATD和/或使用药物治疗AATD的个体;或者拥有AATD的ICD-9诊断代码。的补充材料提供症状的详细定义和肺活量测量质量控制(补充表S5).
统计分析
回归模型拟合评估serpina1.PI*MM基因型与临床结果比较。所有模型都根据年龄、性别、基因分型序列、评估中心和前5个主成分进行了调整,以解释人口结构。随后,我们根据吸烟状况对参与者进行了分层。在每个基因型组内,FEV下降1按年龄估计为FEV的线性回归1按年龄,根据上述调整相同的协变量,因此这些不通过纵向数据来源。使用单变量Cox比例危险模型进行存活分析,以估算死亡的危害。在补充材料中提出了吸烟状态定义和生存分析的详细方法(补充表S6).
我们估计了英国PI * ZZ基因型状态的国家普遍存在,假设等位基因频率在英国BIOBANK和欧洲祖先市民的祖先人物之间没有差别。这可能是低估PI * ZZ基因型频率,因为英国Biobank不是人口代表性的队列,因为它只招募了40岁以上的人并拥有一些健康的志愿者偏见。接下来,我们使用来自国家统计局办公室的数据[18.]来估计欧洲血统的英国公民的比例,并估计携带PI*ZZ基因型的英国人的数量。
敏感性分析
我们在ICD-10编码中包含了e88.0的那些,以诊断AATD并重新计算诊断的AATD的患病率。随着英国Biobank包括对亲属,我们从与第三学位(Kinship系数≥0442)相关的每对一对随机选择的参与者,留下449 991个无关的参与者,以评估受家庭效应影响的关联的通货膨胀。调整年龄调节的多变量Cox比例危险模型也申请存活分析。
Phenome-wide协会研究
接下来,我们探讨了serpina1.与其他疾病的基因型使用PheWAS设计。具体方法见补充资料(补充表S7及S8).
结果
我们确定了欧洲血统的458名164名参与者,欧洲血统的BIOBANK是58岁的中位数(局势范围(IQR)50-63岁),有61名(0.013%)的人被诊断为拥有AATD(表格1,补充图S2).140例PI*ZZ基因型患者中,只有9例(6.4%,95% CI 3.4-11.7%)被诊断为AATD (表2.).鉴于英国有65.6万公民[20.],其中87%估计为欧洲血统[18.),我们估计在英国有17 439个欧洲人携带PI*ZZ基因型。
与PI*MM组相比,PI*ZZ组有更多的呼吸道症状(45%)与25%),较低的FEV1/ FVC(中值0.74与0.77)和较低的FEV1预测的百分比(中位数为86%与94%) (表2.).共有37名(37%)与PI * ZZ的参与者有FEV1/ fvc <0.7(表2.).在17 790例COPD患者中,PI*ZZ基因型患者有31例(0.17%),且其气道阻塞较PI*MM严重。最后,只有7名PI*ZZ患者(23%,95% CI 11-40%)被诊断为慢性阻塞性肺病(AATD)。表3),并且在1407名参与者中,肝硬化的诊断中,三个(0.21%)有PI * ZZ基因型,并且它们都被诊断为AATD。
PI * ZZ基因型与临床结果的关联
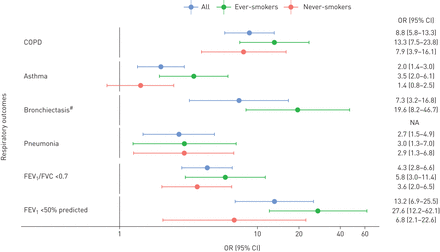
PI * ZZ的那些具有较高的COPD风险(或8.8,95%CI 5.8-13.3; P = 1.1×10-24)、哮喘(OR 2.0, 95% CI 1.4-3.0;p = 5.3×10−4),支气管扩张(或7.3,95%CI 3.2-16.8; P = 2.4×10−6)和肺炎(OR 2.7, 95% CI 1.5-4.9;p = 1.2×10−3)与PI*MM相比。无论是否吸烟,PI*ZZ基因型患者COPD风险更高,但对吸烟者的影响更大(OR 13.3, 95% CI 7.5-23.8)与或7.9,95%CI 3.9-16.1)。在从不吸烟者中,PI * ZZ基因型没有明显与哮喘或支气管切除有关(图1和补充表S9).当调节COPD诊断(或1.5,95%CI 0.8-2.8; P = 0.21)时,PI * ZZ与肺炎的肺炎没有独立相关。
PI * ZZ基因型与普遍存在含有吸烟状态分层的初步条件的森林图。与年龄,性别,基因分型阵列,评估中心和前五个遗传主成分调整的PI * mm(野生型)基因型进行逻辑回归模型计算逻辑回归模型。FEV1:用力呼气量,1 s;FVC:用力肺活量;拿拿淋:不适用。#:未吸烟者被诊断为支气管扩张。
在我们治疗的肺外疾病中,PI*ZZ基因型与肝硬化诊断相关(OR 7.8, 95% CI 2.5-24.6;p=0.004)、肝癌(OR 13.7, 95% CI 3.4-56.0;p = 2.7×10−4)和Panniculitis(或71.8,95%CI 9.6-534.9; P = 3.1×10−5)(补充表S9).
PI*ZZ患者有更多的呼吸道症状(OR 2.5, 95% CI 1.8-3.5;p = 6.5×10−8),如喘息(OR 2.1, 95% CI 1.5-3.0;p = 4.0×10−5)、呼吸短促(OR 3.3, 95% CI 1.9-5.8;p = 3.0×10−5),持续咳嗽(或4.2,95%CI 2.2-7.8; P = 9.7×10−6)和持续咳痰(OR 4.1, 95% CI 2.0-8.2;p = 9.1×10−5).对于从不吸烟的人来说,持续咳嗽是唯一与PI*ZZ相关的症状(OR 3.3, 95% CI 1.3-8.9;p = 0.016) (补充表S10).PI*ZZ基因型患者更易发生FEV1/ FVC <0.7(或4.3,95%CI 2.8-6.6; P = 1.1×10-11)并有fev1<50%pred(或13.2,95%ci 6.9-25.5; p = 1.2×10-14)(图1,补充表S10).FEV的线性回归1按年龄估计FEV降低1年龄为68.3 mL·年−1(95%CI 47.1-89.7)在PI * ZZ参与者中,与35.6毫升·年相比−1(95% CI 35.4-35.8)表2.,补充表S10).FEV降低的差异1由于缺乏统计权力(ZZ)在PI * ZZ个人之间的每年吸烟者和从未吸烟者之间的年龄不确定(补充表S11).与PI * MM基因型(危险比2.4,95%CI 1.2-4.6相比,PI * ZZ基因型与全导致死亡有关.. P = 9.9×10−3)在中位后续时间为7.0年(IQR 6.4-7.7年)(图2,补充表S12).敏感性分析的所有结果都在补充中提出(补充表S12和S13).
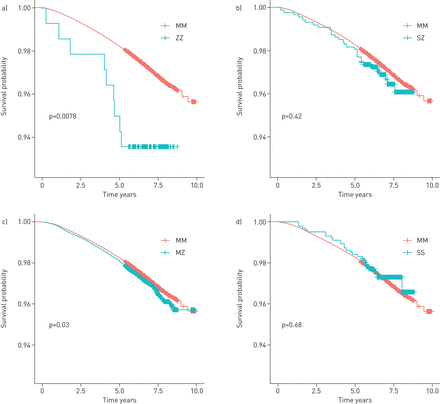
全因死亡率的存活曲线分层serpina1.基因型。a)pi * zz与π*毫米基因型;b)pi * sz与π*毫米基因型;c)π* MZ与π*毫米基因型;d)pi * ss与pi * mm基因型。所有p值都是通过日志秩测试计算的。
Phenome-wide协会研究
PI*ZZ基因型与其他代谢紊乱(包括AATD)、肺气肿、阻塞性慢性支气管炎和慢性气道阻塞(补充图S3).此外,PI*ZZ与依赖呼吸器或补充氧气、脓胸和气胸、恶病质、红细胞增多、动脉瘤和胰腺炎的风险增加相关,所有这些都有统计学意义(p<6.1×10−4)在本杰里尼 - Hochberg校正在主要分析中,保守地假设测试的所有斑纹都是独立的(补充图S3和表S14).敏感性分析的更详细结果是在补充材料.
除PI*ZZ外的aatd相关基因型
此外,与PI * MM相比,我们分析了PI * SZ,PI * MZ和PI * SS的参与者。
PI*SZ和PI*MZ基因型与FEV略有升高有关1/ FVC <0.7(或1.3,95%CI 1.0-1.6; P = 0.022和1.1,95%CI 1.0-1.1; p = 0.032),但与临床诊断的COPD风险增加无关(图3,补充表S9和S10).在重度吸烟者(>20包-年)中,PI*SZ与FEV风险增加2倍相关1/ FVC <0.7(或2.0,95%CI 1.3-3.1; P = 2.6×10−3),而PI * MZ与略微增加的FEV风险有关1/ FVC <0.7(或1.2,95%CI 1.1-1.4; P = 4.5×10−4)(补充表S10).PI*MZ还与肝硬化风险增加相关(OR 1.5, 95% CI 1.2-1.8;p = 0.002) (图3),肝炎(或1.4,95%CI 1.1-1.8; P = 4.6×10−3)和肉芽肿合并多血管炎(OR 2.2, 95% CI 1.2-3.9;p = 9.9×10−3)(补充表S9).所有其他研究结果均载于补充资料(补充图S4、S5及表S9-S12、S15-S17).
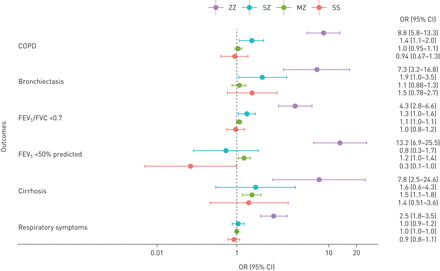
之间的森林情节serpina1.基因型和常见情况。通过logistic回归模型计算PI*MM(野生型)基因型在年龄、性别、基因分型阵列、评估中心和前5个遗传主成分调整后的优势比。FEV1:用力呼气量,1 s;FVC:强迫致命能力。
FEV的多基因风险评分1/ FVC.
相关系数的平方(r2)1/ FVC和FEV1/ PRS预测的FVC在总群体(n = 328 638)中预测的3.5%(95%CI 3.4%-3.6%),其高于FEV之间的相关性1/FVC和吸烟情况(2.4%,95%可信区间2.3%-2.5%)。PRS与其他非遗传危险因素无关(S18补充表美国).我们根据参与者的PRS (图4).在PI * ZZ个人中,PRS最低四分位数的人IE。多基因风险最低的患者(n=29), FEV较高1/ FVC结果与其他PI * ZZ个体相比(n = 72)(中位数(IQR)0.79(0.67-0.85)与0.72 (0.66 - -0.77), p = 0.019)。多元logistic回归显示1-SD.PRS和PI*ZZ的变化与FEV独立相关1/ FVC <0.7(或1.4,95%CI 1.4-1.5; P <2×10-16和4.5,95%CI 3.0-6.9;p = 2.3×10-12分别)(补充表S19).
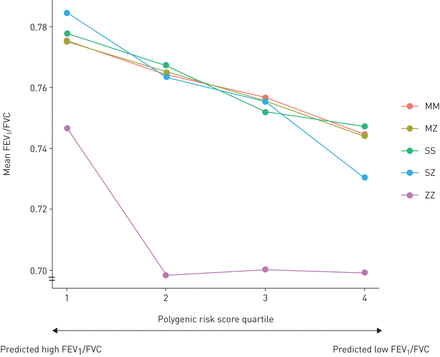
观察到的强制呼气量在1 s(FEV)的平均值1)/强迫肺活量(FVC)分层多基因风险评分四分位。采用全基因组关联研究FEV汇总统计,采用LDpred计算多基因风险评分1/ fvc来自绣线菊属财团,由欧洲血统的个人组成。详细方法描述于补充材料.
讨论
进行大规模评估对普遍存在的serpina1.基因型,它们相关的发病率和死亡率的几率和邦德的疾病诊断率,我们发现绝大多数具有PI * ZZ的个体未被诊断为具有AATD。然而,这些人的呼吸道症状,疾病和全导致死亡率大大增加了几率。我们估计英国~17 000人携带PI * ZZ基因型,其类似于先前人群的新生儿筛查研究的估计[21.,22.].尽管如此,这可能是一个低估的,因为英国Biobank只招募了那些年龄> 40岁,而且患病的人不太可能参加。因此,虽然通过基因分型努力检测的所有英国人的比例都很小,但绝对数量不是。
PI * ZZ基因型对健康状况的影响是惊人的。PI * ZZ与不管吸烟状况如何增加COPD和肺炎的风险,但吸烟者之间的效果大小在吸烟者中显着大。此外,PI * ZZ基因型与吸烟者中哮喘和支气管扩张的风险增加有关。这表明吸烟停止有可能预防PI * ZZ基因型的潜力从开发多种呼吸系统疾病。
几乎一半的PI*ZZ基因型患者有严重气流阻塞的症状,全因死亡风险增加。FEV的线性回归1根据年龄,PI*ZZ个体的FEV下降幅度较大1与PI*MM个体相比。在PheWAS中,PI*ZZ与依赖呼吸器或补充氧气、脓胸和气胸、恶病质和继发性红细胞增多症显著相关,这些都可能是AATD的后遗症。我们的研究也重复了先前被描述为与PI*ZZ相关的肺外疾病,如肝硬化、肝癌、脂膜炎、胰腺炎和动脉瘤,其发病机制被认为是由蛋白酶-抗蛋白酶失衡引起的[23.].
即使在诊断为COPD的受试者中,在本研究中也有77%的PI*ZZ患者未被诊断为AATD。以前的调查表明,在那些实际确诊的患者中,症状出现到确诊之间的平均延迟时间为5到8年[6,24.],延迟与呼吸道症状更严重的呼吸症状和加速肺气肿进展相关[25.].诊断不足的潜在原因包括对这一疾病认识不足,特定地区缺乏适当的检测和/或治疗,IE。英国没有AAT替代疗法的可用性[26.,27.].目前AATD的实验室检测方法是首先定量血浆AAT水平并测量c反应蛋白,然后进行蛋白表型和/或Z和S基因分型[28.,29.].由于与测量AAT相比,基因型数据受到批量效应的影响,因此已知在炎症条件的背景下增加的蛋白质[30.,我们的结果表明,基因分型可能是有效识别PI*ZZ携带者的一步。在目前的研究中,80%的AATD发生在PI*MZ个体中。这可能反映误诊或其他疾病易感突变的影响serpina1.未与基因分型阵列检测到的基因。
PI * ZZ个体具有最低的PRS的PRS具有相对较高的FEV1/FVC,可能提示影响肺功能的多基因因素部分解释了PI*ZZ基因型的变量外显率[3.].基因组基因分型,可以计算PRS和serpina1.基因分型,可能是另一种方法serpina1.- 鉴于AATD的筛选策略,鉴于其相对较低的成本(在研究上下文中的40美元)中进行了基因分型。
此外,我们的研究还提供了几次PI * SZ和PI * MZ基因型的影响的见解。总的来说,虽然PI * SZ与FEV的两倍增加了两倍的风险1在重度吸烟者中,PI*SZ和PI*MZ基因型对肺活量测定定义的阻塞性肺损伤(FEV)的风险有中度影响1/ FVC <0.7)和严重的气道阻塞(FEV1<50%pred)与先前发现相比,PI * SZ具有三倍的COPD风险(95%CI 1.24-8.57)[5[PI * MZ的COPD风险增加了五倍(95%CI 1.27-21.15)[31.].然而,这些病例对照研究描述了非常大的置信区间,并且从指数PI * MZ COPD患者中招募了PI * MZ参与者[31.],可能偏向与COPD相关的其他共同的遗传因素。pi * mz基因型,但不是pi * sz,与肝硬化的风险增加显着相关,并且在本研究中的所有导致死亡率的风险略有增加。PI * SZ和PI * MZ基因型之间的不等调可以通过PI * SZ个体缺乏统计功率驱动,而不是PI * MZ的20倍。PHEMAS发现PI * MZ与多种疾病相关,即胆石病的风险增加,并且心血管疾病的风险降低。有几项研究[32.- - - - - -35.虽然验证性研究和功能调查是必要的,但可能支持这些假设。
以前对PI*ZZ个体的流行病学研究大多是病例-对照研究[36.,37.[目前的研究是评估效果的最大研究之一serpina1.在单个大型人口队列中的多个健康状况的基因型状态。先前的基于家庭的研究包括非诊断PI * ZZ个体的非index家族成员,其血液测量结果更严重(平均fev1/ fvc 0.61和平均fev172.3%pred)[38.]比那些在英国Biobank(表2.),这可能反映了其他共同遗传因素的影响。这项研究的主要局限性是,英国生物样本库不能代表一般人群,因为有充分的证据表明“健康志愿者”存在偏见[39.].因此,我们并没有试图推导出普遍的疾病流行率,而是旨在报告PI*ZZ基因型和多种健康状况的相关性。另一个缺点是AATD的诊断是基于问卷调查和/或医院事件统计,这依赖于每个临床医生的诊断,可能存在“临床顺序”偏倚[40.].然而,PI*MM个体中哮喘(14%)、COPD(3.9%)和支气管扩张(0.69%)的估计患病率与之前的报道相似[41.- - - - - -43.],这可能支持我们如何确定疾病状况的方法的有效性。PPEMAS证明PI * ZZ与囊性纤维化的风险增加有关,这可能代表支气管扩张的误诊。基于ICD编码的PPEMAS可以受到动力,因此观察到PI * ZZ和肝病或哮喘之间没有显着的关联,这并不排除较小的效果。最后,英国Biobank没有AAT测量,因此我们无法测试高风险基因型的人是否具有低水平的血浆AAT。虽然我们没有测试AATD人口级别筛查的成本效益,但基因组基因分型可能有助于筛查风险的个体,例如重重吸烟者或肺病的家族史,以鉴定有未确诊的AATD的人。由于这是一个遗传研究,具有潜在的临床意义,需要未来的努力来解决偶然调查结果的问题,例如应用美国医学遗传学和基因组学[44.关于如何报告次要结果的建议。
总之,我们提供的证据表明,根据英国生物样本库的定义,绝大多数PI*ZZ患者没有被诊断为AATD。然而,这些人的多重症状和疾病的负担大大增加,全因死亡的风险也大大增加。找出这些人士,可有助推行有针对性的戒烟计划[45.]和家庭成员的确定,以及特定疾病的治疗[9].我们的数据提供了潜在的途径,以实现英国正在出现的全国性基因组研究的临床效益。
补充材料
可共享的PDF
确认
我们欣赏参加英国Biobank的个人。
脚注
这篇文章的补充材料可从www.qdcxjkg.com
作者贡献:构思与设计:T. Nakanishi和J.B. Richards。数据分析:T. Nakanishi。数据采集:T. Nakanishi, V. Forgetta和J.B. Richards。数据解读:T. Nakanishi, V. Forgetta, T. Handa, T. Hirai, V. Mooser, G.M. Lathrop, W.O.C.M. Cookson和J.B. Richards。对手稿的智力贡献:T. Nakanishi, V. Forgetta, T. Handa, T. Hirai, V. Mooser, G.M. Lathrop, W.O.C.M. Cookson和J.B. Richards。所有作者都参与了手稿的进一步草稿的准备工作,并对内容进行严格的修改。所有作者最终批准了即将出版的版本。T. Nakanishi和J.B. Richards是担保人。通讯作者证明所有列出的作者都符合作者资格标准,没有遗漏其他符合标准的人。
利益冲突:中西汉太郎没有什么可透露的。
利益冲突:五。forget没有什么可披露的。
利益冲突:T. Handa受雇于Teijin药业有限公司资助的合作研究实验室。
利益冲突:T. Hirai报告了来自日本厚生劳动省(Ministry of Health, Labor and Welfare)难治性呼吸道疾病和肺动脉高压研究小组(The疑难呼吸道疾病和肺动脉高压Research Group)的拨款。
利益冲突:穆泽没有什么可披露的。
利益冲突:通用莱思罗普没有什么可披露的。
利益冲突:W.O.c..M.COOKSON没有什么可披露的。
利益冲突:j·b·理查兹没有什么可透露的。
支持声明:T. Nakanishi得到了日本促进科学(JSP)的研究奖学金,为年轻科学家和JSPS海外挑战计划为年轻研究人员提供了支持。J.B. Richards由加拿大卫生研究院(CIHR)提供支持,Fonds deRechercheQuébec桑特(FRQS)临床研究奖学金。T. Handa由JSP(17K09612)提供支持。T. Hirai通过授予难治性呼吸系统疾病和肺动脉高压研究组,卫生,劳工和福利部,日本的危害。资金来源在:研究的设计或行为中没有作用;数据的收集,管理,分析和解释;或准备,审查或批准稿件。理查兹研究小组得到了犹太普通医院和FRQ的戴维斯夫人研究所的CIHR。使用英国BioBank资源进行了这项研究(项目编号:27449)。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年4月27日。
- 接受2020年6月25日。
- 版权所有©ers 2020
此版本在Creative Commons归因非商业许可证4.0的条款下分发。