摘要
elexacaftor、tezacaftor和ivacaftor三种组合的临床前研究的阳性结果,在从II类囊性纤维化跨膜电导调节(CFTR)突变F508del-CFTR患者获得的气道上皮细胞培养中进行。转化为令人印象深刻的临床结果的受试者携带这种突变的临床试验和批准Trikafta。
受到这种相关性的鼓励,我们开始评估elexacaftor、tezacaftor和ivacaftor三种组合对来自罕见II类cf致突变(G85E、M1101K和N1303K)个体的原发鼻上皮培养物的影响,Trikafta未获批准用于此类突变。
M1101K纯合子的培养物在调节通道功能和蛋白加工方面的改善优于G85E和N1303K的培养物。当不同的突变在HEK293细胞中表达时,观察到三重组合具有类似的基因型特异性效应,支持这些调节剂可能直接作用于突变蛋白的假设。在鼻腔培养和HEK293细胞中进行的详细研究表明,该校正器(e - exacaftor)具有校正器和增强器的双重活性,并提示增强器活性有助于其药理活性。
这些临床前研究使用鼻腔上皮培养确定了突变基因型,其中elexacaftor、tezacaftor和ivacaftor可能产生临床反应,与F508del-CFTR观察到的反应相当或更低。
摘要
在鼻培养中使用F508del的临床预临床研究作为基准,本研究确定了Tripafta可能临床有效的其他CF突变https://bit.ly/3mbMOqL
介绍
囊性纤维化(CF)是由CF跨膜电导调节基因(CFTR)的突变引起的,CFTR基因编码一个离子通道,介导氯和碳酸氢盐在上皮细胞中的运输。CF患者多器官疾病;然而,早期死亡率主要是由进行性破坏性肺部疾病引起的[1-3.].随着第一批CFTR调制器的临床成功,ivacaftor (VX-770)和lumacaftor (VX-809) [4.-6.]美国食品和药物管理局(FDA)最近批准了下一代CFTR调制器三维县。这种高效的CFTR调制器由两个校正分子,Elexacafeor(VX-445)和Tezacafetor(VX-661)组成,其协同基础上有助于处理被错误折叠的CFTR蛋白到细胞膜,以及增加通道开口的电阻仪Ivacaftor [7.那8.].第3阶段与Tripipta的临床试验表明肺功能显着提高,减少肺部加剧和患者患者的寿命的改善,携带至少一个C.1521_1523Delctt(F508del)-cftr等位基因[7.那9.].
F508del-CFTR是典型的II类CFTR突变,由于蛋白质错误折叠、蛋白在细胞表面稳定性降低和通道门控功能失调,导致CFTR蛋白运输缺陷[10].罕见的II类突变,如C.3302T> A(M1101K),C.254g> A(G85E),C.1705t> G(Y569D)和C.3909C> G(N1303K),其在0.2%中被发现分别为0.7%,0.03%和2.4%的CFTR2注册的CF患者(https://cftr2.org).此前已有报道,其中一些罕见突变(即。M1101K, G85E和N1303K)在CFTR加工中显示缺陷,类似于F508del-CFTR [11那12].M1101K和N1303K突变在异源表达系统中表达后,lumacaftor校正和ivacaftor增强后仅表现出适度的挽救[13-15].
在目前的工作中,我们旨在评估Trikafta对罕见II类CFTR突变的影响,使用来自CF患者的纯合子M1101K、G85E和N1303K的鼻上皮细胞培养。
材料和方法
病人
从参加加拿大个性化CF治疗计划(CFIT)的CF患者中获得鼻腔上皮细胞培养(https://lab.research.sickkids.ca/cfit) [16].该研究得到了疾病儿童医院和圣迈克尔医院(REB1000044783)(加拿大多伦多,ON,加拿大)的研究伦理委员会的批准。所有研究参与者或其监护人签署知情同意书。
细胞培养
人胚胎肾293 GripTite细胞(HEK239)在添加非必需氨基酸(Life Technologies, Waltham, MA, USA)的DMEM (Wisent, St-Bruno, QC,加拿大)和10%胎牛血清(Wisent)(37°C和5% CO条件下)中维持2如前所述[17].本研究中使用的所有CFTR变体均根据之前描述的制造商协议,使用PolyFect转染试剂(Qiagen, Hilden, Germany)在HEK293细胞中瞬时表达[18].
16HBE14o- cells, CRISPR/Cas9编辑以表达N1303K-CFTR,来源于囊性纤维化基金会(CFF 16HBEge N1303K-CFTR) [19].如前所述,在个别患者进行鼻刷后产生鼻上皮细胞培养[20.那21].
鼻上皮细胞膨胀并在第1段中冷冻。通过Pneumacacult-Ex加(Stemcell Technologies,Canada,加拿大)在第2段中解冻并扩增这些通道1细胞,然后在胶原涂层的Transwell刀片上播种为通道3(直径为6.5毫米,孔径为0.4μm;康宁,Tewksbury,Ma,美国)。汇合一旦,将细胞在具有基础分化培养基(Pneumacacult-Ali; Stemcell Technologies)的空气液体界面(ALI)中培养14天。16那22那23然后进行功能和蛋白质研究。
CFTR通道在HEK293和CFF-16HBE14o- N1303K-CFTR细胞中的功能
HEK293细胞在96孔板(Costar; Corning)中播种。24小时后,用M1101K-,G85E或N1303K-CFTR构建体转染细胞,并用以下CFTR调节剂处理18小时后转染后:0.1%二甲基亚砜(DMSO),3μmVx-809,3μmVx-809或3μmS.-VX445+3µM VX-661在37°C下放置24 h。如前所述,16HBE14o-细胞在96孔板(Costar)上融合后在37℃下生长5天[24].在荧光成像平板阅读器功能测定(FLIPR;Molecular Devices, San Jose, CA, USA)。然后用蓝色FLIPR膜电位染料溶解于无氯缓冲液(136 mM葡萄糖酸钠,3 mM葡萄糖酸钾,10 mM葡萄糖,20 mM HEPES, pH 7.35, 300 mOsm,浓度0.5 mg·mL)中-1)在37°C下放置30分钟。使用FLIPR Tetra在37℃下测定CFTR功能。建立基线荧光读数(激发530 nm/发射560 nm) 5 min后,使用forskolin (FSK)(10µM;Sigma)和电位器VX-770(1µM)或S.vx - 445(1µM)。CFTR介导的质膜去极化检测到荧光增加,随后CFTR抑制剂CFTRinh-172(10µM;加入EMD Millipore, Burlington, MA, USA)灭活CFTR。相对于基线荧光,CFTR激动剂的荧光峰值变化归一化(Δ)F/F0.) [24那25].
采用腔室法对原代鼻上皮细胞进行研究
第14天在6.5毫米Transwell中的第14天鼻腔上皮细胞安装在循环的循环室(生理仪器,San Diego,CA,USA)和测量以评估CFTR功能如前所述[26].灌注浴(126mm NaCl,24 mm Nahco3., 2.13 mM K2HPO.4., 0.38 mM KH2宝4., 1 mM MgSO4.1毫米CaCl2和10mm葡萄糖)保持在pH的7.4,温度为37℃,并用5%的CO连续加入2/ 95%啊2混合物。测量是在对称的氯离子浓度下进行的,在开路模式下,并以经上皮细胞电流(一世情商;μ·厘米-2).经上皮阻力为250±122 Ω·cm-2对于健康控制鼻细胞和330±130Ω·cm-2CF鼻细胞。实验前用0.1% DMSO处理细胞,3µM VX-809+1µM VX-770, 3µM VX-661+3µM VX-809+1µM VX-770R.-VX-445 +1μmVx-770或3μmVx-661 +3μmS.-VX-445 +1μmVx-770 48小时。在实验期间,还急于加入1μmVX-770。CFTR功能是在amiloride(30μm;谱化学,Gardena,CA,USA)的存在下确定的,并通过FSK营地激活(一世情商野生型(WT)为0.1µM或10µM, F508del-、M1101K-、G85E-和N1303K-CFTR为10µM;Sigma-Aldrich, St Louis, MO, USA)。CFTR活性被确认为一世情商CFTRINH-172的CFTR抑制后差异(一世情商CFTRinh-172, 10µM) [20.那27].最大反应一世情商FSK被计算为测量的稳定基线之间的差异一世情商在阿米洛利抑制和最低测量峰之后一世情商随后加入ivacaftor/elexacaftor + FSK。
免疫印迹
将第14天含有含有蛋白酶抑制剂鸡尾酒(Roche)的改性放射免疫训练测定法(50mM Tris-HCl,150mM NaCl,1mM EDTA,pH 7.4,0.2%SDS和0.1%Triton X-100)裂解含有蛋白酶抑制剂鸡尾酒(Roche,曼海姆,德国)10分钟[28].可溶性组分在6%的Tris-glycine凝胶(Life Technologies, Carlsbad, CA, USA)上用SDS-PAGE分析。电泳后,将蛋白转移到硝化纤维素膜(Bio-Rad, Hercules, CA, USA)中,并在5%的牛奶中孵育。用人CFTR特异性小鼠mAb 596(核苷酸结合域(NBD) 2,1024 - 1211;北卡罗莱纳大学,教堂山,NC,美国)使用1:500稀释。用增强化学发光剂(ECL;在线性曝光范围内(2-45分钟)使用奥德赛Fc成像系统(LI-COR Biosciences, Lincoln, NE, USA) [29-31].使用ImageStudioLite (LI-COR Biosciences)的免疫印迹密度测定法测定CFTR蛋白的相对水平。
化合物的描述
VX-809、VX-661和VX-770来自Selleck Chemicals (Houston, TX, USA);R.-vx-445(N(1, 3-dimethylpyrazol-4-yl) sulfonyl-6 - (3 - (3 3 3-trifluoro-2 2-dimethyl-propoxy) pyrazol-1-yl) 2 - ((4R.) 2, 2, 4-trimethylpyrrolidin-1-yl) pyridine-3-carboxamide)和S.-vx-445(N(1, 3-dimethylpyrazol-4-yl) sulfonyl-6 - (3 - (3 3 3-trifluoro-2 2-dimethyl-propoxy) pyrazol-1-yl) 2 - ((4S.)-2,2,4-三甲基吡咯烷-1-基)吡啶-3-甲酰胺)来自Medchemexpress(Monmouth Junction,NJ,USA)[24].
统计分析
数据以带有标准差的平均值表示。组间比较采用配对双尾t检验或单因素方差分析,p<0.05为显著水平。多组比较采用Tukey’s多重比较检验,α=0.05。所有统计检验均使用Prism 7.0版本(GraphPad, San Diego, CA, USA)。
结果
三调节剂组合VX-445+VX-661+VX-770部分修复了F508del在鼻上皮细胞培养中的加工和功能缺陷
鉴于FDA已批准VX-445+VX-661+VX-770三种药物组合用于CFTR突变体F508del,我们首先在3名F508del/F508del患者的患者来源的鼻腔上皮细胞中评估了CFTR对该药物组合的反应,作为基准实验。由于缺乏临床批准的三联药物组合中VX-445对映体的详细信息,我们对两者进行了测试R.- - -S.- VX-445的血清治疗S.-VX-445+VX-661+VX-770的增幅有统计学意义一世情商FSK和VX-770在F508del/F508del鼻上皮细胞中急性应用后,FSK和VX-770在F508del/F508del鼻上皮细胞中甚至有更大的增加一世情商CFTRinh-172,该结果与增强剂VX-770慢性治疗后CFTR通道活性增强一致。的R.-对映体调节这种反应的效果较差(图1一个- c)。用VX-770进行的慢性和急性应用实验表明,如果长期添加VX-770,增强的FSK响应比急性添加VX-770和FSK (图1 bc).这与慢性VX-770抑制F508del-CFTR功能表达的报道一致(图1一个- c) [32那33].由于慢性VX-770治疗被认为能更好地反映这些联合药物的临床药代动力学,我们继续在慢性使用VX-770的情况下测试CFTR调节剂的效果。为了证明VX-445和VX-661的结合,而不仅仅是VX-661,与VX-809处理相比,引起了更大的反应,我们对VX-809和VX-661的F508del/F508del鼻上皮细胞进行了对比实验,结果表明VX-445和VX-661的反应(补充图S1).由于VX-809是临床批准的药物Orkambi的一个组成部分,我们继续在其余的实验中使用VX-809。
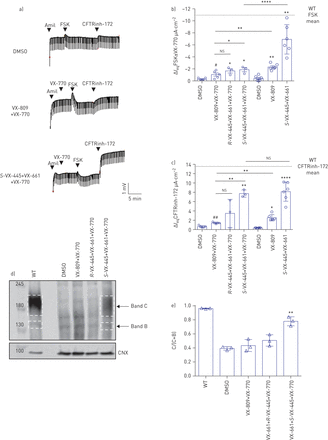
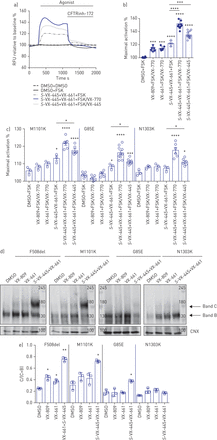
F508del囊性纤维化跨膜电导调节因子(CFTR)突变是由三组VX-445+VX-661+VX-770在三名F508del纯合子患者的鼻腔上皮细胞中挽救的。DMSO:二甲亚砜;阿米尔:阿米洛利;移频键控:forskolin;一世情商: transepithelial电流;WT:野生型;CNX: calnexin。使用含F508del/F508del的CF患者在没有或存在小分子校正器的情况下,对鼻腔上皮细胞培养中的CFTR功能进行腔室测量。上面的线反映了经上皮电位差的测量值,而下面的偏转则反映了经上皮电阻。b)最大响应一世情商经FSK(10µM)±VX-770(1µM)刺激后,对3例患者的鼻腔培养进行1 ~ 2次技术重复实验。不同的前处理(37℃48 h): DMSO(0.1%)、VX-809(3µM)+VX-770(1µM)、R.-vx-445(3µm)+ vx-661(3µm)+ vx-770(1µm)S.vx - 445(3µM) + vx - 661(3µM) + vx - 770(1µM), vx - 809(3µM)或R.-vx-445(3µm)+ vx-661(3µm)。数据点为单用室实验。比较分析显示,VX-809+VX-770、VX-445+VX-661与急性和慢性VX-770治疗组鼻上皮细胞差异有统计学意义。c)一世情商通过CFTR抑制剂CFTRinh-172 (10 μ M)进行b)。d) CFTR调节剂处理后WT或F508del稳态表达的免疫印迹。C波段:成熟的络合糖基化CFTR;B带:未成熟,核心糖基化CFTR。划线框提供了一个示例,说明如何选择用于蛋白质丰度定量的区域。kDa的标记。e) 3例患者鼻上皮细胞C带/(C带+ B带)比值。比较分析显示,DMSO处理的鼻上皮细胞与VX-445+VX-661±VX-770处理的鼻上皮细胞差异有统计学意义。数据以平均值±表示sd.单因素方差分析之后是土耳其事后采用检验进行统计学分析(*:p<0.05;* *: p < 0.01;* * * *: p < 0.0001)。配对t检验显示DMSO处理的鼻上皮细胞与VX-809+VX-770处理的鼻上皮细胞有统计学差异(#: p < 0.05;##: p < 0.01)。ns:不重要的。
Western blot分析处理过的F508del/F508del鼻上皮细胞培养物显示,经处理后,F508del- cftr蛋白的成熟形式(C带)显著增加S.-VX-445+VX-661+VX-770与DMSO处理相比,占WT-CFTR蛋白处理的约70% (C波段/(C波段+ B波段))。的R.VX-445 -亚型对CFTR蛋白表达无影响。这些发现支持通过以下方法纠正患者来源的鼻上皮细胞中F508del-CFTR的加工缺陷S.-VX-445 + VX-661 + VX-770导致CFTR功能改进(图1 de)。为了从临床相关的角度比较不同CFTR突变之间的药物反应,我们以F508del/F508del结果为基准,研究三联用药对其他II类突变的影响。自这些实验开始以来,已证实S.-对映体是临床化合物。
对于其他II类突变,VX-445+VX-661+VX-770挽救水平不同
我们接下来研究了VX-445+VX-661+VX-770对M1101K、G85E或N1303K纯合子患者鼻上皮细胞培养中CFTR功能的影响。对3个M1101K纯合子个体的鼻上皮培养物进行治疗S.-VX-445+VX-661+VX-770导致CFTR功能显著增加,测量为FSK +电位器的急性电流响应或增加一世情商cftrinh - 172 (图2一个,g和h)。来自三个F508DEL / F508DEL患者的鼻上皮细胞中观察到的三重组合的CFTR反应。通过成熟CFTR蛋白的增加来支持这种功能救援。Western印迹分析显示在处理后的M1101K-CFTR蛋白处理(带C /(带C +带B)的显着增加S.-VX-445+VX-661+VX-770相对DMSO (图2 b和j).与R.-对映体也增加了M1101K-CFTR的功能,但程度较小(图2 g,h和j)。
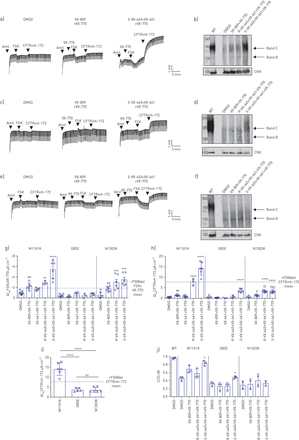
来自其他II类囊性纤维化跨膜传导调节剂(CFTR)突变纯合子患者的鼻上皮培养物表现出低CFTR功能和VX-445+VX-661+VX-770不同程度的挽救作用。DMSO:二甲亚砜;阿米尔:阿米洛利;移频键控:forskolin;CNX: calnexin;一世情商: transepithelial电流;WT:野生型。使用腔室测量CFTR功能的CF患者的鼻上皮细胞培养中,具有a) M1101K/M1101K, c) G85E/G85E和e) N1303K/N1303K小分子校正器的缺失或存在。免疫印迹法检测了CFTR调节剂处理后WT和b) M1101K, d) G85E和f) N1303K的稳态表达。kDa的标记。C波段:成熟的络合糖基化CFTR;B带:未成熟,核心糖基化CFTR。g)最大响应一世情商经0.1% DMSO、VX-809(3µM)+VX-770(1µM)预处理(37°C 48 h)后,3例患者携带M1101K或G85E, 2例供体携带N1303K,共1 - 3个技术重复。R.-VX-445(3µM)+VX-661(3µM)+VX-770(1µMS.-vx-445(3µm)+ vx-661(3µm)+ vx-770(1µm)。h)一世情商通过CFTR抑制剂CFTRINH-172(10μm)用于鼻上皮细胞培养物,从一中的三种技术复制3例轴承M1101K或G85E和两个轴承N1303K的供体复制。i)比较一世情商CFTRinh-172跨越II类突变M1101K, G85E和N1303K的鼻腔上皮细胞培养从1到3个技术重复,3名携带M1101K或G85E的患者和2名携带N1303K的供体。g-i虚线)表示获救的(r) VX-445+VX-661+VX-770鼻细胞F508del/F508del的平均结果。j) 3例携带M1101K或G85E的患者和2例携带N1303K的患者的一个技术复制的C波段/(C波段+ B波段)比值。数据以平均值±表示sd.使用单向ANOVA进行分析,然后使用土耳其事后测试(*:p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.000)。配对t检验显示DMSO处理的鼻上皮细胞与VX-809+VX-770处理的鼻上皮细胞有统计学差异(#: p < 0.05;##: p < 0.01)。ns:不重要的。
用G85E纯合子处理三个受试者的鼻上皮细胞S.-VX-445 + VX-661 + VX-770显示CFTR功能的小但显着增加,当测量时一世情商与dmso处理的鼻细胞相比,cftrinh -172对电流敏感。的S.vx - 445 + vx - 661 + vx - 770增加介导的一世情商CFTRinh-172达到了大约一半一世情商在F508del/F508del鼻上皮细胞中检测到CFTRinh-172增加(图2 c与CFTR功能的增加同时,相对于DMSO预处理,G85E-CFTR蛋白成熟度也有少量但显著的增加(图2 d和j)。在这种突变中,三倍组合与R.-对映体无显著影响(图2 g,h和j)。
来自两名N1303K纯合子患者的鼻细胞显示CFTR功能显著增加一世情商移频键控和一世情商48小时治疗后CFtrinH-172S.-VX-445+VX-661+VX-770和VX-770的急性添加(图2 e然而,有趣的是,在N1303K-CFTR蛋白加工过程中,由S.-VX-445+VX-661+VX-770对N1303K-CFTR蛋白(图2 f和j)。这表明没有发生N1303K-CFTR功能的增加通过改进的蛋白质加工,而不是通过增强膜残留的N1303K蛋白的功能。同时,有趣的是,我们注意到三联疗法S.——R.- 托体米有类似的效果。
VX-445是一种校正剂和增强剂
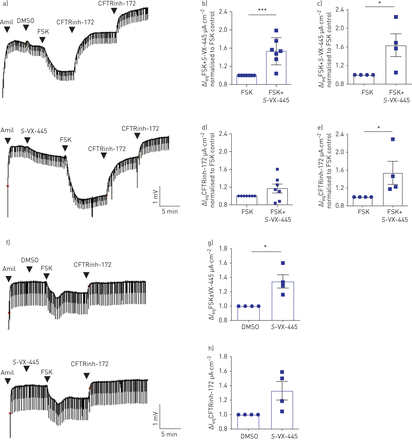
解释VX-445 + VX-661 + VX-770诱导的N1303K-CFTR功能和蛋白质表达之间诱导的差异的一种方法是组合药物,也许VX-445,表现出增强剂活性。为了测试假设,除了其校正活体活动,VX-445作为CFTR强调剂,我们首先检查了急性增加的效果S.-VX-445对WT-CFTR通道功能的影响,分别使用来自非cf对照和非cf肺移植的鼻腔和支气管上皮细胞。有趣的是,急剧增加的S.vx - 445增加一世情商WT-CFTR鼻和支气管上皮细胞培养中的FSK (图3一- c)。虽然一世情商急性后cftrinh - 172S.-VX-445和添加FSK在原代鼻上皮细胞中与单独急性添加FSK相比无显著差异(图3 d),主要是由于组成型CFTR电导的可变水平,急性S.-VX-445应用显著增加一世情商CFTRinh-172在原发性支气管上皮细胞中的作用(图3 e).同样,急性加法S.-VX-445增加了VX-661抢救后F508del-CFTR在鼻上皮细胞培养中的FSK反应(图3 f- h)。初步研究表明,VX-445的增强子活性被CFTR的磷酸化状态所修饰。我们未观察到VX-661抢救后F508del-CFTR增强S.-VX-445,如果激活后添加10 μM FSK(数据未显示)。然而,如补充图S2,在WT-CFTR鼻腔培养中添加0.1 μM FSK后,我们确实观察到适度但显著的增强作用。有趣的是,McCarty小组报告了一个类似的观察结果,显示CFTR变异的VX-770增强活性受到磷酸化水平的影响[34].
VX-445增加了鼻和支气管上皮细胞中野生型(WT)囊性纤维化跨膜电导调节因子(CFTR)的通道激活。阿米尔:阿米洛利;DMSO:二甲亚砜;移频键控:forskolin;一世情商:Transepithelial电流。a)代表性描记表显示来自非CF供体(WT-CFTR)的鼻上皮细胞培养物中CFTR功能的UFTR功能。B,c)FSK(10μm)+增加S.-VX-445(3µM)-activated Δ一世情商与FSK(10µM)对照相比,b) 1至2个技术复制的鼻上皮细胞来自4个健康对照和c)来自4个供体的支气管上皮细胞(n=4)。d, e) Fold increase in一世情商通过CFTR抑制剂CFTRINH-172(10μm)在d)鼻上皮培养物和e)支气管上皮细胞培养物。f)代表性描记表显示使用48小时的F508del突变的CF患者在鼻上皮细胞培养物中的CFTR功能在用VX-661(3μM)(F508DEL-CFTR)处理后的CF患者的鼻上皮细胞培养物中的CFTR功能。反复给出CFTrinH-172(10μm)以确保完全抑制CFTR。g)FSK(10μm)+增加S.-VX-445(3µM)-activated Δ一世情商与FSK(10µM)对照相比,来自两个CF供体的纯合子F508del的两个技术复制的鼻上皮细胞。h)相应的fold increase in一世情商CFTRinh-172(10µM);数据以平均值±表示sd.使用配对的双尾T检验进行比较分析(*:P <0.05; ***:P <0.001)。在未处理的细胞和急性治疗的细胞之间显示统计学显着的差异S.vx - 445。
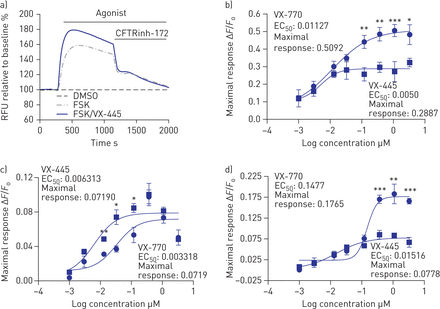
我们研究了VX-445增强对F508del-CFTR和HEK293细胞中罕见II类突变体在低温(27°C)孵育后的剂量依赖性(图4一b).在所研究的罕见突变体中,只有G85E在低温下未能校正[12].在该系统中,使用FLIPR膜电位染料测定测量FSK(10μm)-CFTR的FSK(10μm)活化通道功能的Vx-445介导的助性,因为它促进了对多剂量的研究。对于F508DEL-CFTR,VX-445作为电位含点的功效明显小于VX-770,但对于所有研究的突变体并非如此。在图4 cd,我们展示了VX-770和VX-445增强M1101K和N1303K的剂量-响应曲线。有趣的是,F508del、M1101K和N1303K基因型的增强子反应存在差异。VX-445作为增强剂对N1303K的疗效小于VX-770,对M1101K的疗效不明显,两种化合物的疗效相似。未来的研究需要了解不同基因型间差异增强因子反应的结构基础。
VX-445增强HEK293细胞中温度挽救的F508del、M1101K和N1303K囊性纤维化跨膜电导调节(CFTR)突变。RFU:相对荧光单位;DMSO:二甲亚砜;移频键控:forskolin;电子商务50:半最大有效浓度(μ M)。a) f508del - cftr依赖的氯离子流出的代表性痕迹(膜去极化分析,3µMS.-VX-445 +10μmfsk)在27℃温育后用F508del-cftr稳定地转染的HEK293细胞中。B-D)VX-770的剂量 - 响应曲线或S.- vx -445(0.001-3µM)+FSK(10µM)在b) F508del-, c) M1101K-或d) N1303K-CFTR HEK293细胞(n=5个生物学重复和4个技术重复)。相对于基线荧光,CFTR激动剂的荧光峰值变化归一化(Δ)F/F0.).数据以平均值±表示sd.使用单向ANOVA进行分析,然后使用土耳其事后测试(*:p < 0.05;* *: p < 0.01;* * *: p < 0.001)。
接下来,在用VX-661 +预处理后,我们研究了在HEK293细胞中表达的F508DEL,M1101K,G85E和N1303K突变体上的VX-445的增强活性S.-VX-445 at 37°C (图5).所示图5一个b,用VX-661和VX-661校正F508del-CFTR后S.-VX-445,后续添加的VX-770或S.-VX-445增强其fsk依赖通道活性。对于罕见突变,我们证实了之前在鼻上皮细胞培养中发现的结果,VX-809和VX-661单独不能挽救VX-770增强的通道功能,但VX-445和VX-661联合可以挽救VX-770增强的M1101K、G85E和N1303K的活性(图5 c).使用CRISPR/Cas9编辑的16HBE14o细胞表达N1303K-CFTR突变体(CFF 16HBEge N1303K-CFTR) (补充图S3a和b).有趣的是,S.-VX-445还显著增强了VX-661+ vx -445纠正的罕见变异的fsk激活功能。
VX-445+VX-661+VX-770挽救的HEK293细胞中表达F508del囊性纤维化跨膜电导调节因子(CFTR)突变和其他罕见CFTR突变。RFU:相对荧光单位;DMSO:二甲亚砜;移频键控:forskolin;CNX: calnexin。a)经DMSO或预处理的F508del-CFTR稳定转染的HEK293细胞中F508del-CFTR依赖的氯离子流出(膜去极化试验)的代表性痕迹S.-VX-445(3µM)+VX-661(3µM)在37℃下放置24 h。b) FSK(1 0µM)±VX-770(1µM)和/或刺激后f508dl - cftr的最大激活S.vx - 445(1µM)。c)瞬时转染M1101K-、G85E-或N1303K-CFTR的HEK293细胞,用DMSO、VX-809(3µM)、VX-661(3µM)或DMSO在37℃处理24 hS.-vx-445(3µm)+ vx-661(3µm)。FSK(10µM)±VX-770(1µM)和/或刺激后M1101K-、G85E-和N1303K-CFTR的最大激活量S.-VX-445(1µM) (n= 3-10)。d) 37℃下DMSO、VX-809(3µM)、VX-661(3µM)、M1101K-、G85E-、N1303K-CFTR处理24 h后F508del-、M1101K-、G85E-、N1303K-CFTR的稳定表达免疫印迹S.-vx-445(3µm)+ vx-661(3µm)。kDa的标记。C波段:成熟的络合糖基化CFTR;B带:未成熟,核心糖基化CFTR。e)比率带C /(频带C +带B)(n = 3)。数据以平均值±表示sd.采用单因素方差分析进行比较分析,然后采用土耳其的方差分析事后测试(*:p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001)。
表达CFTR突变体HEK293细胞的Western blot分析重现了我们在患者来源的鼻细胞上的发现(图5 d).用修正剂VX-809或VX-661处理F508del-CFTR的处理过程有一定改善,但对M1101K或g85e - cftr表达细胞没有改善(图5 de)有趣的是,和我们在鼻腔细胞中看到的相似,用S.-VX-445+VX-661并未导致N1303K成熟CFTR蛋白的增加。与我们在过表达N1303K-CFTR的HEK293细胞中发现的结果一致,表达N1303K-CFTR的16HBEge细胞在治疗后也出现了功能挽救S.-VX-445+VX-661+VX-770未显示CFTR蛋白成熟增加(补充图S3C和D.).我们建议存在足够量的成熟糖基化的N1303K-CFTR蛋白,以介导电量介质诱导的CFTR通道活性。然而,N1303K-CFTR C波段的蛋白质信号在CFF 16hbege N1303K-CFTR和主要鼻上皮细胞中弥漫,如前所述[35].
最后,我们测试了S.-VX-445 + VX-661 + VX-770在鼻细胞中,来自Y596D / Y596D的一名患者纯合(补充图S4)来自两个患者G542x / N1303K的杂合(补充图S5).所示补充图S4和S5,药物组合S.-VX-445 + VX-661 + VX-770未引起这些突变中的任何一个中CFTR功能的任何增加。
总而言之,我们观察到了S.-VX-445 + VX-661 + VX-770三重组合在不同类II突变的功能救援上(图2我).
讨论
在这项研究中,我们证明了CFTR调制器的新型三重组合,即。Trikafta中包含的两种校正化合物(VX-445和VX-661)和增强剂化合物(VX-770)改善了F508del-CFTR在患者纯合子鼻上皮细胞培养中主要突变的加工和通道活性。这一结果复制了先前通过原代支气管上皮细胞培养获得的临床前数据[7.并支持使用原代鼻上皮细胞培养来研究调节剂的功效。有趣的是,在目前的研究中,我们发现在体外对这三种组合的反应在II类突变基因型中是可变的。这些发现促使了对elexacaftor (VX-445)在鼻上皮细胞培养中的深入研究,其中我们确定它表现出两种活性,既作为校正器和作为增强器。此外,这些研究支持这样一种观点,即根据基因型的不同,elexacaftor的任何一个或两个活动都可能有助于其挽救效果。鉴于来自罕见加工突变纯合子个体的初级支气管上皮细胞培养相对难以获得,我们的研究结果支持使用患者来源的鼻上皮细胞培养进行治疗干预的临床前研究及其作用机制的研究。
在临床试验中,F508del纯合子的CF患者采用三联Trikafta治疗效果显著,肺功能改善,1 s内预测用力呼气量百分比增加10%,汗液氯浓度降低45 mmol·L-1以及生活质量的提高[36].在使用原代支气管上皮细胞培养的临床前研究中,这种组合导致F508del突变体的显著功能挽救,超过了Orkambi的挽救[7.].因此,支气管上皮细胞培养模型的临床前反应大小可以预测临床效果大小。类似地,在体外在F508del-CFTR纯合子患者的原代鼻上皮细胞培养中对这种组合的反应也可能提供临床反应的生物标志物。其他的课题需要研究,但我们建议在体外F508del/F508del鼻上皮细胞培养的三联挽救可能为预测罕见突变个体的临床疗效设定阈值。
我们比较了vx -770增强的fsk依赖电流和相应的cftrinh -172敏感电流(图2我)显示不同基因型的反应存在差异。有趣的是,与F508del相比,表达M1101K的患者来源的鼻上皮细胞培养显示出更好的功能挽救。表达G85E和N1303K的鼻上皮细胞培养反应较小。对突变蛋白加工的相应研究为这些基因型特异性差异的可能机制提供了线索。与Orkambi (即。VX-809 + VX-770)适用于F508del, M1101K和G85E,但不适用于N1303K。Lukacs小组最近的一项研究调查了VX-445校正的分子机制[37].VX-445在生物物理研究中稳定NBD1;作者认为,在全长蛋白中,它直接作用于这个结构域。它对位于不同结构域的罕见II类突变的纠正效果支持了它具有变构效应以促进多结构域组装的观点。当前文章的发现支持这些观察和假定的变构作用机制VX-445。在鼻上皮细胞培养中,M1101K和F508del对VX-445+VX-661+VX-770慢性治疗的功能反应大小之间的差异,需要进一步的研究来确定细胞表面的差异蛋白稳定性与HEK293细胞。
有趣的是,与VX-809+VX-770相比,N1303K-CFTR虽然在功能挽救方面有相对改善,但其蛋白质加工并没有改善。我们认为VX-445+VX-661+VX-770的功能修复反映了极低残留表面表达的增强。这种增强是由VX-770和VX-445(双作用校正/增强复合物)介导的。有趣的是,P桓et al。[38]在HBE细胞系中表明N1303K在表达N1303K CFTR的HBE细胞系中的功能拯救,仅加入两个增强剂,没有矫正器[38].他们还表明,使用Fischer甲状腺大鼠细胞以及来自N1303K / N1303K患者的鼻腔和支气管上皮细胞的特异性增强调节剂以及来自N1303K / N1303K患者的鼻腔和支气管上皮细胞有效调节N1303K-CFTR [38那39].最近,我们还发现,AbbVie制药公司提供的另一种分子组合,一种增强剂(AP2)和一种双作用校正剂/增强剂化合物(AC2.2),诱发了N1303K-CFTR的功能挽救,但在其加工过程中没有显著改善[35].总之,我们发现N1303K-CFTR对调节因子有一致的响应,这些发现支持了VX-445的增强因子活性对该突变体的功能挽救至关重要的说法。
总之,我们证明了II类基因型对elexacaftor、tezacaftor和ivacaftor的不同反应,同时鉴定了elexacaftor的双重活性。我们的研究还强调了患者来源的鼻上皮细胞培养的实用性,以测试药物疗效和收集关于药物活性的机制的见解。
补充材料
可分享的PDF.
脚注
作者捐款:O. Laselva,T.J.Moraes,C.E. Bear和Gonska设计了实验。O. Laselva和C. Bartlett进行了实验并分析了数据。H. Ouyang和T.N.A.Gunawardena培养了患者样品。O. Laselva,C.E. Bear和Gonska写了这篇论文。T.J.莫拉斯和p.d.w。Eckford编辑了这篇论文。
本文提供了补充材料www.qdcxjkg.com
利益冲突:O. Laselva没什么可透露的。
利益冲突:C. Bartlett没有什么可透露的。
利益冲突:T.N.A.古纳瓦德纳没有什么可透露的。
利益冲突:欧阳没有什么可透露的。
利益冲突:P.D.W. Eckford没什么可透露的。
利益冲突:T.J.莫拉莱斯没什么可透露的。
利益冲突:C.E. Bear报告了加拿大CF和加拿大卫生研究所在研究进行期间的拨款;这是贾格尔·巴什(Jagle Bash)在提交作品之外对作者所在机构的慈善捐赠。
利益冲突:T. Gonska报告了CF加拿大/SickKids基金会在进行研究期间的拨款;演讲和参加Vertex制药公司顾问委员会的旅费报销,在提交的工作之外。
支持陈述:通过CF CANA-Sickids计划获得原发性鼻细胞培养物用于个体化CF治疗(CFIT)。CFIT计划提供了由CF加拿大和SickiDS基金会提供的资金的CFIT计划的支持。这项工作由加拿大政府通过加拿大基因组和安大略省基因组学院(OGI-148)资助。本研究由安大略省政府资助。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年4月11日。
- 公认2020年11月20日。
- 版权©2021人队
这个版本是在知识共享署名非商业许可4.0的条款下发布的。