摘要
背景在流感相关心肌炎合并难耐性心源性休克(rCS)患者中,缺乏机械循环支持(MCS)的证据。我们试图研究MCS使用联合静脉-动脉体外膜氧合(VA-ECMO)和微轴流泵(ECMELLA概念)在流感相关心肌炎合并rCS中的影响。
方法这是一项前瞻性的观察性分析,来自最近两个流行流感季节的单中心汉诺威心脏卸载登记处(HACURE)。我们分析了确诊为流感相关心肌炎并发rCS的患者,这些患者因MCS而入住我们的重症监护病房(ICU)。随后,我们对急性心肌梗死(AMI)合并rCS和非缺血性心肌病(DCM)相关rCS患者进行倾向评分(PS)匹配分析。
结果我们描述了7例rcs并发流感相关心肌炎患者(平均年龄56±10岁,58%男性,甲型流感(n=2)/乙型流感(n=5))。没有病人在流感季节之前接种过疫苗。采用VA-ECMO联合Impella微轴流泵提供MCS。2例院外心脏骤停患者植入VA-ECMO进行体外心肺复苏。所有患者均在入院后18天内死亡。通过与AMI或dcm相关rCS和合并MCS患者的ps比较,流感相关rCS的30天死亡率显著高于AMI或dcm相关rCS。
结论尽管rcs合并流感相关心肌炎患者联合MCS初步稳定,但休克的有害过程无法停止,所有患者均死亡。流感病毒感染可能严重影响除心脏外的其他器官,导致不可逆的终末器官损伤,MCS无法弥补,因此导致毁灭性的结果。
摘要
联合机械循环支持治疗顽固性心源性休克(ECMELLA)可能无法挽救流感相关心肌炎和严重终末器官损伤患者,相反,对原发性心脏原因的治疗效果良好https://bit.ly/3dmonC4
介绍
流感病毒通常引起季节性呼吸道感染,并周期性地导致流行和大流行。呼吸衰竭和肺炎是常见的呼吸道并发症,与生存受损有关[1]。约10%的病例心肌受到影响,通常始于症状出现后第4天至第7天之间[1,2]。心肌表现因变异性、非特异性和症状起发而诊断不足[3.]。1957年亚洲流感大流行期间,33例未事先怀疑心肌受累的意外死亡病例中,有三分之一确诊为急性心肌炎[4]。流感相关心肌炎的表现形式不一,从亚临床型到暴发性心肌炎,可伴有或不伴有明显的心源性休克,最终可导致心力衰竭导致死亡[1]。cs合并流感相关心肌炎是罕见的,在他们对184例心肌炎合并流感感染的系统回顾中,Hekimianet al。[5]报道48例CS患者采用机械循环支持(MCS)治疗。
指南建议儿茶酚胺稳定CS患者的血压,但由于全身血管收缩,儿茶酚胺会导致继发性多器官衰竭[6,7]。在难耐性心源性休克(rCS)中,经皮MCS被认为是对液体负荷和血管升压药无反应的患者的可选治疗方法[7]。在本分析中,我们试图研究MCS联合静脉-动脉体外膜氧合(VA-ECMO)和Impella微轴流泵(ECMELLA概念)在rcs并发流感相关心肌炎中的疗效。
方法
研究设计和参与者
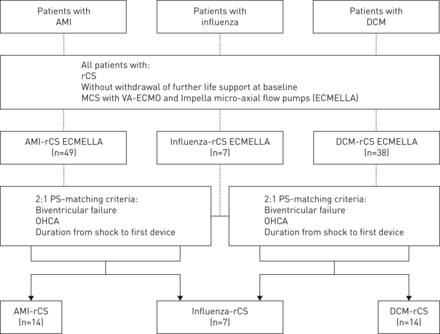
我们的分析是根据赫尔辛基宣言进行的,并已获得当地伦理委员会的批准(#3566-2017)。在分析中,分析了所有在最近两个流感流行季节(2013年和2018年)入住汉诺威医学院心内科的rcs并发流感患者,并使用VA-ECMO和Impella微轴流泵接受MCS治疗。在当地数据库(汉诺威心脏卸载注册中心(HACURE) [8]),对2013年1月至2018年6月期间接受MCS联合VA-ECMO和Impella微轴流泵治疗急性心肌梗死(AMI)或非缺血性心肌病(DCM)导致的rCS的患者,分别标记为AMI-rCS组和DCM-rCS组,按照中所述进行倾向评分(PS)匹配图1。入院时休克严重程度评分、静脉-动脉ECMO (SAVE)后生存评分[9]、人口学资料、实验室资料及住院期间并发症的记录。
学习报名流程图。AMI:急性心肌梗死;DCM:非缺血性心肌病;rCS:难愈性心源性休克;AMI-rCS:与ami相关的rCS;流感-rCS:与流感相关的rCS;DCM-rCS: dcm相关rCS;MCS:机械循环支架;VA-ECMO:静脉-动脉体外膜氧合;ECMELLA:采用VA-ECMO和Impella微轴流泵组合的MCS; PS: propensity score; OHCA: out-of-hospital cardiac arrest.
患者治疗及定义
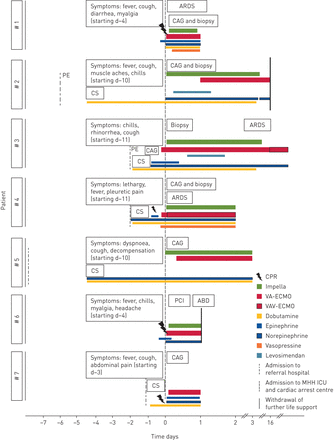
咽拭子PCR检测证实流感感染。rCS定义为低血压和/或终端器官低灌注的持续或恶化,即。乳酸水平升高(≥2.5 mmol·L−1)加上一个或多个灌注不足的临床征象(如。皮肤湿冷,心动过速,精神状态改变,少尿(< 30ml·h)−1),或肺水肿),尽管根据心血管血管造影和干预学会(SCAI)临床专家共识声明,给予儿茶酚胺(两种或两种以上儿茶酚胺的体重调整最大剂量)和适当的标准休克治疗[10,11]。病人均按现行指引治疗[7]以及CS和心脏骤停的局部治疗算法(HaCRA) [12]。详细的病人治疗信息在图2在补充材料。
流感病毒感染引起的难治性心源性休克(rCS)合并心肌炎患者的治疗时间进程ARDS:急性呼吸窘迫综合征;CAG:冠状动脉造影;CS:心源性休克;PE:心包积液;PCI:经皮冠状动脉介入治疗;ABD:缺氧性脑损伤;CPR:心肺复苏;VA-ECMO:静脉-动脉体外膜氧合;VAV-ECMO:静脉-动脉静脉体外膜氧合; MHH: Hannover Medical School; ICU: intensive care unit.
统计分析
分类参数以n(%)表示,正态分布度量变量以均值±标准差(sd)和非正态分布度量变量作为中位数(四分位范围(IQR))。时间点间比较采用方差分析,Mann-Whitney u检验作为非参数检验,多重比较校正采用Bonferroni检验或Dunn's检验。采用非配对t检验作为参数检验,Mann-Whitney检验作为非参数检验,对ps匹配的度量参数组进行统计分析。采用卡方检验比较名义上缩放的参数。使用Kaplan-Meier曲线计算30天生存期,并在组间进行对数秩比较。采用Cox回归分析计算95%置信区间(ci)的风险比。报道的p值是两面的,p<0.05被认为有统计学意义。数据分析使用GraphPad Prism 7.04版(GraphPad Software, San Diego, CA, USA), R 3.3.3版(R Foundation for Statistical Computing,www.r-project.org)和SPSS统计版本25 (IBM公司,Armonk, NY, USA)。详细的PS匹配在补充材料和补充图S1。
结果
病人的特点
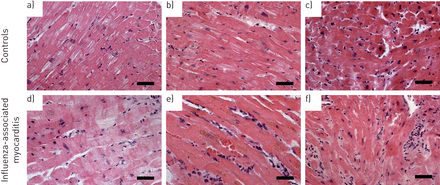
分析了7例既往未接种流感疫苗并伴有rcs并发流感感染、接受MCS治疗的白种人患者(平均年龄:56±10岁)。PCR分析证实5名患者为B型流感患者,2名患者为A型流感患者(4号和7号患者)。在4例患者(编号1至4),左心室心肌内膜活检已经进行。组织学检查显示间质淋巴细胞浸润及局灶性肌细胞坏死(图3)。心肌炎临床诊断依据症状、心肌酶升高及超声心动图表现[13)。中位SAVE评分为−11 (IQR - 12至−8)表明即使在VA-ECMO支持下,估计死亡率为82%。2013年1月1日至2018年6月30日,共有87例ami相关rCS (n=49)或dcm相关rCS (n=38)患者在我院接受ECMELLA治疗。经1:2 PS匹配后,选择ami相关rCS组14例(“AMI-rCS组”)和dcm相关rCS组14例(“DCM-rCS组”)进行进一步比较图1。两组间的基线特征没有统计学意义上的差异。患者特征见表1而在补充表S1。
经皮机械循环支持(MCS)支持的难耐心源性休克(rCS)并发非缺血性心肌病(DCM)和流感相关心肌炎患者的心肌内膜活检(a-c)对照组:经皮MCS合并rcs并发DCM患者的心脏左室活检。在这些心肌内膜活检中,心肌细胞显示不规则肥厚的迹象,相应的细胞核有不同程度的深染。还可见分布不均匀的轻度嗜酸性收缩带,以及轻度细胞内和细胞外水肿。虽然有一些稀疏的间质炎症浸润,但不符合活动性心肌炎的标准(根据Dallas分类)。根据定义,扩张型心肌病的组织学改变是非特异性的,使得组织病理学诊断被排除。特殊疾病的征象,如肉芽肿性炎症、心肌包涵体或铁沉着症均不存在。(d-f)流感相关心肌炎:rcs并发流感相关活动性心肌炎患者的心肌内膜活检。间质炎性浸润明显,但分布不均匀,大部分由活化的t淋巴细胞组成。所有活检都显示心肌细胞损伤的证据,从显著的收缩带到高嗜酸性粒细胞坏死(早期)阶段。 Adjacent capillaries are dilated, packed with erythrocytes and their endothelial nuclei are activated. Cardiomyocytes as well as the cardiac interstitium show accompanying oedematous changes. As in (a–c), signs of specific disorders such as granulomatous inflammation, myocardial inclusions or siderosis are absent. Scale bars=50 µm.
重症监护和MCS特征
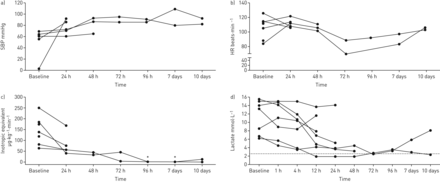
在重症监护病房(ICU)中位3天(IQR 1-16天)期间,所有患者均采用机械通气。2例患者(编号3和4)从转诊医院进行了VA-ECMO转诊。4例患者在入院前发生心脏骤停。所有复苏的患者都目睹了骤停和旁观者复苏。在2例患者(1号和6号)植入VA-ECMO用于体外CPR (eCPR)。2例患者(第3和第4例)发生急性呼吸窘迫综合征(ARDS)引起的呼吸衰竭,导致静脉-动脉-静脉体外膜氧合(VAV-ECMO)升级[14]。2例患者(1例和6例)基于左心室扩张和肺充血,在VA-ECMO后继发插入Impella微轴流泵。入院乳酸水平、心脏骤停频率和从休克发作到使用第一种设备、VA-ECMO或Impella微轴流泵的持续时间在匹配组之间无显著差异。基于ICU和MCS特点的临床病程总结于表2和补充表S2。MCS提供血流动力学稳定(数字4和b),导致收缩性药物和血管升压药物的输注减少(图4 c)用于流感相关心肌炎相关rCS患者。在MCS期间乳酸水平迅速下降,两例患者在左室恢复后乳酸水平升高,可能是基于肺炎和ARDS后的败血症(图4 d)。
机械循环支持(MCS)对流感病毒感染所致顽固性心源性休克(rCS)合并心肌炎患者血流动力学的影响(其中a)收缩压(SBP);b)心率(HR);C)肌力等效水平;D)乳酸水平)。基于经皮MCS,尽管血流动力学参数趋于稳定(随之而来的肌力等效水平下降),rCS状态抵消(随之而来的乳酸水平下降),但患者在入住汉诺威医学院(MHH)重症监护病房(ICU)和心脏骤停中心18天内死亡。儿茶酚胺剂量采用收缩力等效法(其中[ug·kg−1·敏−1] =多巴胺+多巴酚丁胺+ 100 *肾上腺素+ 100 *去甲肾上腺素+ 100·异丙肾上腺素+ 15·药物)(15]。*: p < 0.05与基线。
安全的结果
在一名患者(第7位)中,Impella微轴流泵在升主动脉脱位后无法重新放置在左心室。在两名患者(编号2和3)中,Impella微轴流泵是在初次左心室恢复后(在主动左心室卸载369小时(编号2)和312小时(编号3)后移植的。3例肺流感感染并发急性呼吸窘迫综合征(1、3、4),2例继发性细菌性肺炎(2、5),并发连续感染性休克。5例患者入院时出现肝衰竭(71%;1号和4号到7号)。入院后无患者存活30天(图5)。由于多器官衰竭和长期rCS(患者2号)和复苏后明显的缺氧脑损伤(患者6号),一致意见决定停止进一步的生命支持(图2)。其余5名患者(1号、3至5号和7号)在最高程度的重症监护中死亡。在MCS期间,没有明显的血栓栓塞事件发生。
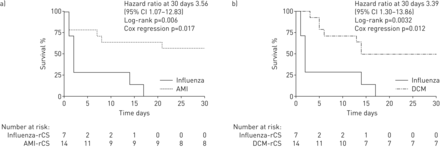
倾向评分(PS)匹配的30天生存期。a) flu - rcs和AMI-rCS的匹配。b)流感- rcs和DCM-rCS的匹配。CI:置信区间;AMI:急性心肌梗死;DCM:非缺血性心肌病;rCS:难愈性心源性休克;AMI-rCS:与ami相关的rCS;DCM-rCS: dcm相关rCS;flu -rCS:与流感相关的rCS。
与DCM-rCS组相比,流感相关心肌炎相关rCS患者更容易发生继发性肺炎和随后的呼吸衰竭,需要升级到VAV-ECMO。安全结果总结于表2,补充图S2和补充表S3。
倾向评分匹配组的30天死亡率
在ps匹配组中,57%的AMI-rCS组(n=8)和50%的DCM-rCS组(n=7)患者存活到ICU入院后第30天,而两组患者在VA-ECMO(基于SAVE评分)上的预测死亡率均为82%。所有流感相关心肌炎相关rCS患者均在18天内死亡。因此,流感- rcs组(n=7)与匹配的AMI-rCS组之间的30天生存率有显著差异(风险比3.56,95% CI 1.07-12.83;p = 0.006;n=14)和DCM-rCS组(危险比3.39,95% CI 1.30-13.86;p = 0.003;n = 14)。中提供了Kaplan-Meier曲线图5。
讨论
我们目前的分析包括7例rcs并发流感相关心肌炎患者,使用Impella联合微轴流泵和VA-ECMO循环支持(ECMELLA概念)治疗。根据SAVE评分(中位数- 11,IQR - 12至- 8)确定的休克程度,这些患者的死亡风险极高。ECMELLA战略[16,17]明显改善了这些患者的血流动力学障碍,减少了对收缩性药物的需求,并导致两名患者在左室恢复后停用Impella微轴流泵。然而,尽管ECMELLA最初改善了血液代谢,但我们的流感相关、心肌炎相关rCS严重受损患者无一存活。当将PS匹配应用于ami相关rCS或dcm相关rCS患者队列时,考虑到血流动力学损害,流感相关、心肌炎相关rCS患者显示出明显更高的30天死亡率。rCS合并流感相关心肌炎患者伴有不可逆的终末器官功能衰竭并发心脏骤停(n= 4,57%)和/或肝衰竭(n= 5,71.4%),这并不一定是rCS的后果,而是由流感感染本身引起的直接心外器官损伤。因此,与AMI或DCM导致rCS的患者相比,MCS联合ECMELLA可能对这些患者的预后有轻微影响。在这些实体中,末端器官衰竭的症状最有可能是血流动力学恶化的结果。相比之下,流感感染会导致多重心外损伤,这些损伤与血流动力学恶化无关,MCS的血流动力学稳定无法改善终末器官损伤。MCS策略产生了一种有前途的治疗概念,可以中断rCS的致命后果[18,19]。由于许多MCS设备总体上缺乏证据,特别是在心肌炎的rCS等罕见疾病中的应用,有关MCS的决策是一个基于当地经验的个体过程。
在rCS患者中,与单一VA-ECMO治疗相比,联合治疗MCS (ECMELLA)可改善预后[20.]。值得注意的是,回顾性分析也包括了心肌炎相关的rCS患者,但可能只涉及局限于心脏本身的感染。据我们所知,cs并发流感相关心肌炎的MCS入路(VA-ECMO或Impella微轴流泵)仅限于零星病例报告[5,21,22]。
在我们的分析中,5名患者(71%)在经过一段时间延迟后从转诊医院转到我科(从休克到第一台设备的中位时间为26小时,IQR 18-40小时)。基于入院前病程的长短、临床表现的变异性、合并症和流感病毒检测的挑战,对合并流感感染的心肌炎进行早期诊断具有挑战性[23,24]。这可能会推迟将严重受损的患者转移到三级医院。此外,并不是所有的边缘性或代偿性CS患者都普遍采用侵入性血流动力学监测。对抗CS心脏代谢恶化的一个明显因素是支持时间的大门[8,25]。因此,除了入院时双心室衰竭和院外心脏骤停(OHCA)外,我们还考虑了ps匹配中从休克到第一装置的持续时间。在ICU入院30天内,与流感组相比,两个匹配组的生存率均显著高于流感组,并与SAVE评分预测一致。
ECMELLA的概念,以及我们ICU的标准化护理,显然能够使严重受损的rCS患者受益。然而,患有流感相关、心肌炎相关rCS的患者并不能从血流动力学稳定中获益。左室心肌内膜活检显示流感相关、rcs并发心肌炎引起的心脏终端器官损伤(图3)。此外,流感相关心肌炎心肌损伤的严重程度因细胞因子和压倒性的炎症反应而增强[24,26- - - - - -28]。我们的结论是,与ps匹配的DCM队列相比,这些患者的心肌恢复概率低于预期。
乍一看,我们的结果似乎与先前的病例报告相反,这些病例报告表明,VA-ECMO或Impella微轴流泵支持的流感相关、cs并发心肌炎患者的死亡率较低(补充表S4)。总的来说,我们的队列和历史病例之间流感相关心肌炎患者的住院生存率差异可能是由他们的年龄较小(55.6±9.5岁)所解释的与39.5±13.2年),无其他流感相关并发症,CS的严重程度和随后的终端器官损伤差异。
同样,在当前另一种具有挑战性的rna病毒(严重急性呼吸综合征冠状病毒2 (SARS-CoV-2))大流行中,老年和共病以及病毒相关并发症和终末器官损伤与预后受损有关[29]。感染后出现流感样症状(如。发热、咳嗽、头痛、疲劳、肌痛和呼吸短促),最终可导致多器官功能障碍,包括ARDS、急性肝衰竭、急性肾损伤(AKI)和急性心力衰竭[29- - - - - -31]。最近发表的两篇文章描述了通过高敏肌钙蛋白I和肌钙蛋白T水平升高检测到的2019冠状病毒病(COVID-19)相关心肌损伤[32,33]。值得注意的是,在这两项分析中,心肌损伤与较高程度的住院死亡率相关。以类似于流感病毒感染的方式,I报告的病例nciardi等。[34]描述可能表现为急性心肌炎的心肌损伤。然而,由于rCS中与确诊的COVID-19诊断相关的MCS病例报告很少,ECMELLA对这些患者死亡率的影响无法从我们的分析中推断出来,因此仍不确定[29,35]。然而,在流感相关、心肌炎相关的rCS患者中获得的无效原因的经验,由于病毒引起的心外终末器官损伤,很可能适用于COVID-19病例。
总之,所有与流感感染相关的rCS病例都是在两个流行季节未接种疫苗的患者中观察到的。因此,医生应强调流感疫苗接种对健康人士及已患有心脏病的病人的重要性[36]。此外,AMI和dcm相关的rCS主要选择性地影响心肌细胞,而流感感染通过全身炎症反应继发影响心脏,同时也影响其他重要器官。因此,与在rCS的主要心脏原因中观察到的有益影响相比,流感会导致严重的终末器官损伤,MCS可能无法挽救。因此,在流感相关心肌炎相关rCS患者中应仔细考虑MCS,特别是与致命结局相关的MCS。然而,在这些患者中,没有终末器官衰竭不可逆阶段的指标或流感感染的诊断,MCS策略似乎是治疗急性血流动力学恶化和预防早期死亡的唯一选择。进一步分析流感相关、心肌炎相关rCS患者的ECMELLA支持情况,有必要验证我们的假设。
限制
基于回顾性和观察性设计,没有随机对照组。观察性登记仅报告了一小部分rcs并发流感病毒感染的患者。登记为罕见疾病的治疗方法提供了相关信息,虽然结果可能产生假设,但流感相关、心肌炎相关的rCS患者很少,并且代表了严重受损患者的一个子集。因此,在本分析中,我们无法推断早期植入MCS是否会产生有益的效果,以及呼吸衰竭、ARDS和继发性肺炎在多大程度上导致了死亡。此外,小患者数量的ps匹配结果只能根据潜在未知协变量的可能偏差仔细推断[37]。
结论
我们发现,在流感相关心肌炎的rCS似乎有一个致命的过程,尽管植入联合MCS。因此,我们的数据不支持在这些患者中标准化积极使用MCS的概念。然而,没有MCS的替代方案往往会引发植入;然而,这可能不会以相关的方式影响预后。
补充材料
可共享的PDF
确认
我们感谢ICU和心脏骤停中心(汉诺威医学院心脏病和血管学系)的护理人员对这项研究的支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:J-T。siweke和M. Akin对手稿有同样的贡献。启动制冷。siweke, A. Schäfer和J. Bauersachs设计了注册表。启动制冷。siweke, M. Akin, S. Stetskamp, C. Riehle, U. Flierl, T.J. Pfeffer, V. Hirsch, J. Dutzmann, M.M. Hoeper和C. Kühn招募患者并收集数据。启动制冷。siweke, M. Akin和S. Stetskamp分析和解释了数据。启动制冷。siweke, M. Akin, C. Riehle, J. Bauersachs和A. Schäfer撰写了手稿。 J-T. Sieweke, M. Akin, U. Flierl, J. Dutzmann and A. Schäfer performed the literature review. D. Jonigk rated and analysed the endomyocardial biopsies of patients supported by MCS with influenza-rCS and DCM-rCS. All authors revised the manuscript critically. J. Bauersachs and A. Schäfer accurately approved the manuscript.
利益冲突:J-T。siweke报告了Abiomed在提交工作之外的旅行支持。
利益冲突:M. Akin没有什么可透露的。
利益冲突:S. Stetskamp没有什么可透露的。
利益冲突:C. Riehle报告了Abiomed在提交工作之外的差旅支持。
利益冲突:D. Jonigk没什么可透露的。
利益冲突:u。Flierl没有什么可透露的。
利益冲突:tj·普费弗没什么可透露的。
利益冲突:V.赫希没有什么可透露的。
利益冲突:J.达兹曼没有什么可透露的。
利益冲突:M.M. Hoeper报告了Actelion,拜耳,MSD和辉瑞公司的讲座和咨询工作的个人费用,在提交的工作之外。
利益冲突:C. Kühn没有什么可披露的。
利益冲突:J. Bauersachs报告了来自诺华、BMS、辉瑞、拜耳、施维雅、MSD、勃林格殷格翰、阿斯利康、雅培、美敦力和Daiichi Sankyo的个人费用,以及来自Abiomed、Zoll、Vifor和CvRX的个人费用。
利益冲突:A. Schäfer报告了Abiomed在研究进行期间的资助和个人费用。
支持声明:本研究得到Klinische Forschergruppe (KFO,奖励311-TP1)和Deutsche Forschungsgemeinschaft (DFG,奖励BA 1742/9-1)的支持。本文的资助信息已存入交叉参考基金注册。
- 收到了2020年4月3日。
- 接受2020年5月1日。
- 版权所有©ERS 2020
本版本根据知识共享署名非商业许可4.0的条款发布。