文摘
急性纤维素性肺炎和组织(AFOP)肺移植后肺功能迅速下降。然而,与慢性肺部同种异体移植物功能障碍(复合)仍不清楚。我们调查之间的关系检测AFOP异体肺活检的临床重要的端点。
我们回顾了从468年异体肺活检病人肺移植医院鲁汶大学(2011 - 2017)。AFOP被归类为最近诊断为早期(≤90天移植后)或最近诊断为晚期(> 90天移植后);与CLAD-free生存,移植物存活率,供体特异性抗体,气道嗜酸性粒细胞和血液。
早期和晚期AFOP中检测出24(5%)和30例(6%)患者,分别。CLAD-free生存显著低于AFOP晚期患者(平均生存2.42年;p < 0.0001),而与患者早期或没有AFOP特别是与发展相关限制性的同种异体移植物综合征(或28.57,95%可信区间11.34 - -67.88;p < 0.0001)。同样,移植物存活率显著低于AFOP晚期患者平均生存4.39年;p < 0.0001),而与患者早期AFOP或没有AFOP。晚AFOP而且与循环供体特异性抗体的检测(或4.75,95%可信区间2.17 - -10.60;p = 0.0004)与患者早期或没有AFOP相比,和高气道嗜酸性粒细胞和血液(分别为p = 0.043, p = 0.045)与早期相比AFOP病人。
最近诊断为晚期AFOP与预后差和高复合发展的风险,特别是限制性的同种异体移植物综合症。我们的发现表明最近诊断为晚期AFOP可能发挥作用的限制性的同种异体移植物综合症的早期发病机制。
文摘
本研究链接急性纤维蛋白的组织肺炎和肺移植后的不良预后显著相关。这些发现表明,急性纤维素性肺炎和组织在严格的同种异体移植物综合症的发病机制中发挥作用。https://bit.ly/3aof9n9
介绍
肺移植是一个接受治疗的患者各种慢性终末期肺部疾病。然而,肺移植后长期的结果仍然是阻碍发展的慢性肺部同种异体移植物功能障碍(复合)在大约50%的患者肺移植术后5年(1]。穿着病人代表一个异构人口:临床、放射检查和基于组织病理学结果。一般来说,两个主要的临床表型的定义:闭塞性细支气管炎综合征(BOS)和限制性的同种异体移植物综合症(RAS) (2,3]。首先是定义为一个进步的和不可逆转的阻塞性肺功能缺陷,后者由限制性肺功能缺陷,特点是持续pleuroparenchymal混浊在计算机断层扫描和预示一个贫穷的结果3,4]。
急性纤维素性肺炎和组织(AFOP)最初在2002年描述B斯-et al。(5)作为一种独特的组织学模式与急性肺损伤有关。它的特点是突出的存在intra-alveolar纤维蛋白沉积和组织肺炎,不同于其他组织模式,如弥漫性肺泡损伤(爸爸)或嗜酸性肺炎。两个不同形式的疾病进展和临床结果描述:快速的爆发形式疾病进展导致死亡和亚急性形式有更好的预后(5]。
2013年,警araskeva等。(6)确定AFOP作为小说实体在22个194(11%)肺移植受者,总是伴随着快速下降后呼吸功能和死亡中位数时间为101天。亚急性形式描述了B斯-等。(5在这些病人中)是没有见过。此外,Paraskeva等。(6)没有检测的组织学证据AFOP病人诊断为“RAS-like”综合症,而最近外植体肺组织病理学分析显示存在AFOP大约50%的临床定义终末期RAS患者(7]。因此,AFOP的临床行为及其与RAS在肺移植受者的关系仍有待阐明。
此外,time-of-onset AFOP在结果的重要性没有被评估。为其他损伤模式,比如爸爸和组织肺炎,一个重要的时间效应的time-of-onset CLAD-free损伤,观察移植物存活(8,9]。具体地说,爸爸最近诊断为晚期(>移植后3个月)与风险增加有关的后续RAS发展,而早期的爸爸与早期死亡率和BOS相关(8]。
因此,本研究的目的是调查之间的关系AFOP异体肺活检一方面和另一方面功能和临床相关的结果。我们提出,最近诊断为晚期AFOP可能RAS和糟移植物生存与发展。
材料和方法
病人选择、组织病理学和影像学评估
这项研究包括所有病人肺移植医院鲁汶大学(比利时鲁汶)2011年1月至2017年12月。再移植被认为是作为一个单独的事件在我们的分析。后续审查在9月1日,2018年。所有诊断性活检(transbronchial活检(TBB)、计算机断层扫描引导活检和手术活检)最初是由一个有经验的评估肺部病理学家组成了一个系统的和详细的描述性的病理报告。在目前的研究中,所有诊断性活检的病理报告,监测和显示活检(如。怀疑感染或拒绝),综述了。Haematoxylin-eosin-stained幻灯片和染色是微生物的初步报告符合AFOP被两名有经验的重新评估肺部病理学家失明患者数据,直到达成共识。如果多个积极活检对一名患者是可行的,第一个活检显示AFOP被认为是最近诊断为AFOP的时间。基于最近诊断为AFOP日期,早期(≤90天后肺移植(post-Ltx))与最近诊断为晚期(> 90天post-LTx) AFOP定义,通过应用相同的90天截止之前用于调查的重要性的时候出现组织学损伤结果(图1)[8]。如果可用,外植体肺活检(获得尸检或再移植)从患者移植物丢失也重新评估。AFOP被诊断为根据提出的标准斯-等。(5)的存在至少两个主要特性(即。突出intra-alveolar纤维蛋白、组织肺炎和片状分布),没有证据表明透明膜,嗜酸性渗透或肉芽肿性炎症5]。胸部计算机断层扫描成像技术在诊断胸AFOP经过有经验的放射科医师,失明的研究设计。移植监测计划,组织病理学和影像学评估中详细描述补充材料。
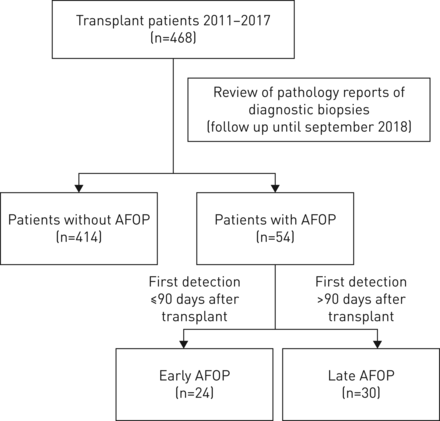
病人选择的流程图。AFOP:急性纤维素性肺炎和组织。
实验室结果
Broncho-alveolar灌洗(BAL)期间执行例行支气管镜检查2×50毫升的盐水滴剂,如前所述[10]。同样,外周血样本收集在支气管镜检查的时间。道达尔和微分白细胞(WBC)计数、c反应蛋白(CRP)和持续的存在新创反人类白细胞抗原(HLA)供体特异性抗体(员)进行评估,如前所报道(11]。
移植包损失和诊断
贪污损失被定义为死亡(即。全因死亡率)或再移植。包被定义为一个持久(> 3个月)在1 s (FEV用力呼气量1)下降至少20%的均值两个最好的术后FEV1测量了> 3周(随访直到2018年9月),在没有另一个原因4]。RAS定义额外的> 10%肺活量下降(TLC)和/或下降> 20%用力肺活量(FVC)和持续辐射混浊的证据3]。CLAD-free生存之间的时间被定义为移植,FEV最初出现> 20%1下降。
生存sub-analysis
执行sub-analysis定义是否检测AFOP末是一个独立的预后因子。因此,我们年底CLAD-free和移植物存活率相比AFOP病人,病人没有指示活检(即。因这一原因活检> 90天post-LTx),表明患者活检(n≥1),但与正常发现和说明患者活检(n≥1)发现异常(即。出现急性排斥反应或感染,但缺乏AFOP)(病人特点提供了表S3)。移植患者的生存≤90天这个生存sub-analysis post-LTx被排除在外,因为的存在表明活检事实上的不应评税。
数据表达和伦理方面的考虑
用于生存分析kaplan - meier和log-rank测试分析;AFOP之间的关系,分析了RAS和地区体育会使用确切概率法。使用Mann-Whitney BAL和外周血数量比较测试。调整CLAD-free和移植物存活率分析使用Cox比例风险模型调整本机肺病(肺气肿,肺间质疾病、囊性纤维化、支气管扩张或其他),移植,年龄性别、移植类型、发作的急性排斥反应,淋巴细胞性细支气管炎发作,感染和巨细胞病毒感染的组织学证据,时代(第年和发生新创持久的地区体育会。GraphPad统计软件(棱镜,version 7.01中,圣地亚哥,美国)和SAS (SAS研究所,9.3版本,卡里,NC)是用于分析。一个假定值< 0.05被认为是显著的。本回顾性研究经当地伦理委员会批准(S52174)。
结果
大多数的所有468个包括病人从未显示AFOP诊断性活检(n = 414, 89%),而24例(5%)患者出现早期最近诊断为AFOP;患者和30例(6%)晚些时候最近诊断为AFOP (图2)。病人特征总结表1和概述诊断提供了活检的病理结果表2。对AFOP hiv病人的治疗方案中描述补充材料。
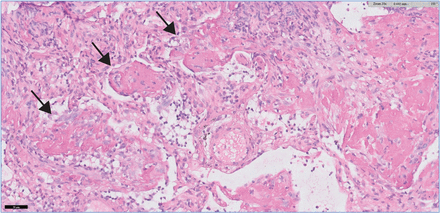
急性纤维蛋白的组织学和组织肺炎(Haematoxylin-Eosin污点,×20)。著名的松intra-alveolar出现肺泡内纤维蛋白球空间(箭头)和成纤维细胞。酒吧= 50μm规模。
CLAD-free生存
CLAD-free生存显著低于AFOP晚期患者(平均生存2.42年;p < 0.0001),而与患者没有AFOP或患者早期AFOP (图3一)。85名(21%)患者没有AFOP发达复合(RAS, n = 14 (16%);BOS, n = 71(84%), 4例(17%)患者早期AFOP发达复合(RAS, n = 1 (25%);BOS, n = 3(75%), 19例(63%)患者晚期AFOP发达复合(RAS, n = 15 (79%);BOS, n = 4 (21%)) (表3)。RAS是临床诊断使用> 10% TLC下降25的30 (83%)RAS病人和> 20% FVC下降剩下的病人。
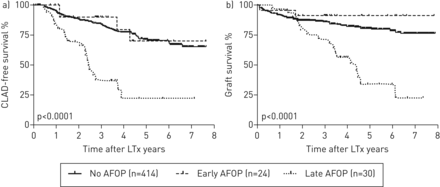
kaplan meier)曲线说明慢性肺部同种异体移植物功能障碍(复合)无生存post-lung移植(第)。CLAD-free生存显著恶化晚期急性患者纤维蛋白的组织肺炎(AFOP)与患者早期AFOP相比,或病人没有AFOP (p < 0.0001)。b) kaplan meier曲线说明贪污post-LTx生存。移植物存活率显著恶化AFOP晚期患者与早期AFOP患者或患者相比没有AFOP (p < 0.0001)。
AFOP晚期患者更有可能发展RAS,相比之下,患者没有AFOP(或28.57,95%可信区间11.34 - -67.88;p < 0.0001)。有趣的是,三个患者晚期AFOP进展从BOS RAS表型的复合AFOP末和检测后不久被视为RAS病人进行进一步分析。中间间隔临床RAS的诊断和检测晚AFOP−16天(差−72 - 14)。相反,早期AFOP证明无显著相关性与后来的RAS开发(或1.24,95%可信区间0.11 - -7.19;p = 0.58)。
移植物存活率
移植物存活率显著降低AFOP后期患者(平均生存4.39年;p < 0.0001),而与患者没有AFOP或患者早期AFOP (图3 b)。贪污损失发生在74名(18%)患者没有AFOP(死亡、n = 67;再移植,n = 7)和两个(8%)患者早期AFOP(死亡,n = 1;再移植,n = 1)。贪污损失是指出AFOP末17例(57%)患者(死亡,n = 13;再移植,n = 4),主要是由于复合(n = 15,特别是RAS, n = 13),体液排斥反应(n = 1)或败血症(n = 1)。
肺组织病理学结果外植体
外植体肺活检17晚11(65%)的纤维蛋白/组织移植物失功肺炎患者。间质纤维化改变,与RAS一致,出现在10 11名患者(91%)。非特异性间质纤维化的模式存在于三个11名患者(27%),AFOP三11名患者(27%),和pleuroparenchymal fibro-elastosis四11名患者(36%)。此外,闭塞性细支气管炎病变中发现10 11名患者(91%)。组织病理发现在早期AFOP外植体肺(n = 2)所描述的补充材料。
放射性的发现
胸部计算机断层扫描成像技术可用在所有54 AFOP AFOP诊断患者(表2)。晚AFOP患者伴有放射性混浊在27个30例(90%),主要是广泛存在于23例(77%)患者。AFOP晚期患者更困气和更少的胸膜积液相比早期AFOP患者(分别为p = 0.006, p = 0.01)。
存在地区体育会
持续的发生新创地区体育会在晚期患者更普遍AFOP (n = 11, 37%)相比,患者没有AFOP (n = 45岁,11%)或患者早期AFOP (n = 2, 8%) (p = 0.024) (表3)。晚AFOP显著地区体育会的存在(或4.75,95%可信区间2.17 - -10.60;p = 0.0004),而与患者没有AFOP。发生地区体育会AFOP晚期患者移植物存活率没有显著影响(p = 0.058),相比之下,没有地区体育会AFOP晚期患者。同样,检测地区体育会没有影响CLAD-free AFOP年末生存患者(p = 0.15)。早期AFOP与地区体育会的存在无相关性(或0.75,95%可信区间0.17 - -2.98;p > 0.99)。
BAL和外周血
BAL流体微分细胞计数得到19(79%)的24 AFOP早期患者和23例(77%)患者在30个AFOP末。BAL患者嗜酸性粒细胞明显高于后期AFOP(中值0.5%,差0 - 5.20),与患者早期AFOP差0 - 0.40(平均0%)(p = 0.043)。七个(23%)患者晚期AFOP相伴BAL嗜酸性粒细胞> 2% (即。正常在我们实验室的上限),而只有一个(2%)患者早期AFOP了BAL嗜酸性粒细胞> 2% (p = 0.054)。分析BAL液体并没有发现感染率差异(p = 0.74;细节补充材料)。
血液白细胞分化可供18(75%)的24早期AFOP和29例(97%)患者30 AFOP晚期患者。血嗜酸性粒细胞明显高于晚期患者AFOP·µL(中位数100细胞−1;差0 - 200)相比,患者早期AFOP·µL(中位数0细胞−1;差0 - 100)(p = 0.045)。其他BAL和外周血测量两组之间没有显著差异(表S1)。
调整和生存sub-analysis
多变量分析表明,检测AFOP末是一个独立的危险因素CLAD-free生存(HR 3.11, 95%可信区间1.76 - -5.27;p < 0.0001)和移植物存活率(HR 3.03, 95%可信区间1.71 - -5.36;p= 0.0001)(表S2)。此外,生存sub-analysis显示检测的后期AFOP预示着CLAD-free和移植物存活率明显降低与异常指示患者活检相比,但没有AFOP (p = 0.035;p = 0.0003;分别)(图4)。(病人特点和指示活检中提供的信息表S3和S4)。之间的关系的可视化表示最近诊断为AFOP,检测地区体育会,CLAD-free和移植物的生存提供了S1和S2的数据。CLAD-free和移植物存活率分析应用不同的否决早期和晚AFOP (即。3米、6米、9米、12米,18米,24米)提供S3和S4数据,所有确认晚AFOP差的结果。
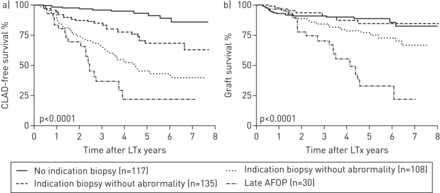
kaplan meier)曲线说明慢性肺部同种异体移植物功能障碍(复合)无生存post-lung移植(第)。b) kaplan meier曲线说明贪污post-LTx生存。CLAD-free生存和移植物存活率明显恶化患者晚期AFOP相比表明活检患者异常,表明患者活检没有异常或病人没有指示活检(分别p < 0.0001和p < 0.0001)。患者移植物的生存≤90天post-LTx (n = 18)被排除在外,因为存在一个指示活检(即。因这一原因活检>移植后90天)事实上的不应评税。
讨论
我们在诊断性活检调查AFOP之间的关系,不同的功能和临床参数诊断性活检群体的肺移植患者。本研究的主要发现是我)低CLAD-free贪污AFOP晚期患者的生存期,而早期AFOP证明没有相关结果;(二)强烈的RAS AFOP末和发展之间的联系;和iii) AFOP末和地区体育会之间的联系。
Paraskeva等。(6]之前证明检测AFOP在肺移植患者总是与贫困有关结果,并报告平均只有101天的生存。我们的研究结果并不完全支持这个观察,发现最近诊断为早期AFOP没有影响的结果在我们的病人队列。发现最近诊断为晚期AFOP强烈与贫穷的结果,和复合发展的高危患者,尤其是RAS。AFOP之间可能的联系和RAS曾被我们研究小组报道基于外植体肺组织病理学分析,揭示了存在的AFOP大约50%的临床发现RAS患者(7]。相比之下,Paraskeva等。(6)不符合AFOP观察组织学变化患者“RAS-like”临床表型(但没有TLC确认)6]。
我们发现,首次发现了AFOP大致陪同RAS的临床和放射学诊断,这可能支持假设AFOP代表早期发病机制的组织病理学特点RAS发展,导致呼吸功能的快速下降和死亡的暴发性课程,或穿着病人幸存的急性发作。
我们的研究结果与以前的观测表明一个特定的组织病理学模式之间的联系(即。最近诊断为晚期爸爸和组织肺炎)和RAS发展8,9]。我们没有发现早期AFOP和CLAD-free之间的联系或移植物生存;这表明AFOP发病的时间效应CLAD-free生存。事实上,似乎早AFOP主要代表一个瞬态过程,解决没有过度的发展。然而,随着早期和晚期AFOP组织学上无法区分的,预后可能依赖AFOP的根本原因。
AFOP典型的斑片状分布,明确排除基于小型TBB AFOP可能困难。上下文中的高临床怀疑,一个负TBB可能因此引发进一步的调查(如。额外的TBB抽样)。此外,一个明确的诊断AFOP基于TBB可以挑战其他组织学模式(如。爸爸,嗜酸性肺炎)可能像在AFOP[组织病理变化5]。
我们发现一个重要AFOP末和持久的存在之间的联系新创地区体育会。有趣的是,后期AFOP病人专门发达地区体育会对HLA II型DQ抗原。持续的新创地区体育会,特别是DSA-DQ抗体,包已经关联到一个更高的风险尤其是RAS (11,12]。潜在的病理生理学和他们的潜在作用在RAS致病途径仍不清楚,但这些结果与以前的报告,证明抗体介入排斥和RAS(之间的联系13]。我们目前的研究结果支持这一假设,可能指向intra-alveolar纤维蛋白沉积的关键作用。我们以前认为微血管损伤,至少部分由抗体介导的排斥反应,可能是最初的事件导致毛细管泄漏和intra-alveolar纤维蛋白沉积(7)(图S5)。下一阶段,似乎有一个低效的清算intra-alveolar纤维蛋白,从而形成松散的纤维蛋白球(14]。接下来,成纤维细胞增殖和浸润纤维蛋白球,导致典型AFOP模式。最终,这纤维化反应可能导致的模式(子)胸膜和隔纤维化RAS的特征。此外,闭塞性细支气管炎损伤被发现在绝大多数AFOP下旬外植体肺患者,一个未知的致病性AFOP和闭塞性细支气管炎病变之间的联系可能存在。
我们观察到血液中嗜酸性粒细胞水平较高和BAL AFOP晚期患者的样本,而早期AFOP病人。然而,我们没有观察到增加组织嗜酸性粒细胞AFOP活检,在这种情况下,相应传染病或嗜酸性肺炎应该被排除。我们先前表明,嗜酸性粒细胞BAL≥2%倾向于后来RAS发展(15),以及降低生存在RAS诊断(16]。嗜酸性粒细胞可能发挥作用在复合的病理生理学,虽然底层机制仍然未知。
我们的研究也有一些局限性。首先,病人选择进行回顾性基础上修订的病理报告。其次,本研究从只有病人和基于数据,尽管我们报告一个大病人群体,推断这些结果得出一般结论的肺移植手术的病人可能会受到限制。第三,血液和BAL微分细胞计数没有对所有AFOP患者可用,由于技术困难获得足够的在临床上不稳定患者的样本。此外,血液和BAL患者相比,细胞计数不能没有AFOP,因为没有合适的参考时间点可以定义没有AFOP的病人。
总之,我们证明最近诊断为晚期AFOP CLAD-free和移植物存活率较低有关,特别是发展RAS。我们相信这些发现提供证据,可能表明AFOP RAS的早期发病机制中的关键组织病理学特征。致病机制的进一步描述AFOP和RAS发展应该有助于更好地理解AFOP和拉之间的复杂关系。
补充材料
可共享的PDF
确认
我们要感谢“鲁汶肺移植组”:这包括以下重要的合作者,我们的肺移植项目人直接参与关爱我们的肺移植受者在过去年:列文j .杜邦乔纳斯Yserbyt, Laurent Godinas Anke Van Herck Annelore Sacreas,珍妮ka,托拜厄斯海格尔苏菲Ordies,阿恩·Neyrinck薇罗尼卡Schaevers,保罗•德•Leyn德克·e·范Raemdonck威利Coosemans, Philippe Nafteux赫伯特Decaluwe, Hans Van转向列文Depypere,安娜·e·弗里克劳伦斯j . Ceulemans和marie - paule Emonds。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:概念和设计:a . Vanstapel S.E. Verleden, B.M. Vanaudenaerde,通用Verleden和r . Vos;数据分析和解释:a . Vanstapel S.E. Verleden, b . Weynand e . Verbeken l . De Sadeleer和r . Vos;起草重要知识的手稿内容:a . Vanstapel S.E. Verleden, b . Weynand e . Verbeken l . De Sadeleer B.M. Vanaudenaerde,通用Verleden和r·沃斯。
利益冲突:a . Vanstapel没有披露。
利益冲突:S.E. Verleden没有披露。
利益冲突:b Weynand没有披露。
利益冲突:大肠Verbeken没有披露。
利益冲突:l . De Sadeleer没有披露。
利益冲突:B.M. Vanaudenaerde没有披露。
利益冲突:通用Verleden没有披露。
利益冲突:r . Vos没有披露。
支持声明:a . Vanstapel是由基础研究拨款FWO (1102020 n)。S.E. Verleden是由FWO的资助(FWO12G8715N)和KU鲁汶(C24/18/073)。B.M. Vanaudenaerde是由KU鲁汶(C24/050)。r .支持Vos FWO(临床高级研究员)和由罗氏公司从比利时移植研究资助的社会。支持通用Verleden Broere慈善基金会。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2019年11月27日。
- 接受2020年4月16日。
- 版权©2020人队