抽象
遗传易感性可以改变肺部疾病的发生,但环境因素是至关重要的决定因素。迫切需要研究暴露物——环境暴露总量——以了解肺部疾病的病因。http://bit.ly/2YG5XpP
定义exposome
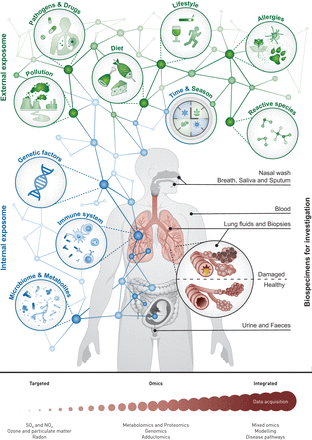
由于人类基因组进行测序,广泛的努力已经被放置到在疾病的发病基因定位的作用。据预计,我们将能够解释疾病的病因,了解健康的遗传基础。然而,我们发现,虽然个别疾病的遗传贡献发生变化,非遗传因素有更大的归因危险,常在80-90%的范围内。非遗传成分的亮点为主导,环境慢性病的重要性风险,并导致exposome科学的新兴领域的出现。在其最广泛的意义上,exposome可以被定义为所有暴露的从概念起的全部[1]。这个包罗万象的描述包括多重暴露,从污染、过敏原、饮食、生活方式因素和感染,到人类和微生物的新陈代谢(图1)。所述exposome的更具体的建议的定义是环境暴露的累积效应和相关的生物反应[2]。
该exposome概念。所述exposome从概念涵盖了累积接触起,整合内外部暴露。多个生物标本可以被采样,以获取基于exposome数据,用分析方法,从单个目标收购基于组学概要分析和综合建模。在其最真实的意义上说,exposome包括流程的全套显示在此图中,代表着我们的努力,了解环境的呼吸系统疾病的病因学中的作用的显著分析和后勤挑战。
暴露体的概念最初被引入是为了承认基因和环境在癌症病因学中的重要性[1]。遗传学已证实对呼吸系统疾病的发病机制相对温和的影响。从单卵双生子数据指向的48.6%基因组驱动的人群归因分数(PAF)用于治疗哮喘,其表示理论上可以防止如果整个基因型(加上共享曝光)可以被移除的情况下的比例[3.]。在单卵双生子哮喘的PAF是最大为任何的28种慢性疾病和症状,包括慢性阻塞性肺病(PAF 18.5%)和肺癌(PAF 9.89%)[3.]。这些可归因的风险指示,而遗传易感性可以改变肺部疾病的起始和轨迹,环境触发是必要的因素。
暴露组通常被解释为代表个体表型的非遗传贡献的组学尺度特征,包括表观基因组的产物以及蛋白质组、代谢组和外来DNA/RNA。当与人口特征相关的元数据结合时,exposome激发了确定疾病病因的调查。我们强调,在肺部疾病的背景下,暴露物不仅仅是公认的引发肺损伤的空气污染物的集合,包括反应性气体、颗粒物和环境烟草烟雾。实际上,空气中的颗粒物含有多种细菌、病毒和真菌,它们通过感染和调节免疫系统影响呼吸健康。相反,暴露体的概念是明确承认暴露于这些空气中的污染物以及其他环境污染物可以与基因组结合微生物群、饮食和生活方式因素相互作用,从而影响肺部疾病的发病率和严重程度。因此,有必要了解这些因素对呼吸健康的综合影响,并确定需要缓解敏感人群压力的组合。
分析exposome
在呼吸道疾病的病原学研究中,暴露体的特征是一个重要的分析挑战。有人建议,更实际的做法是关注体内的化学特征,以识别过去接触的痕迹。例如,血液、尿液、牙齿和头发中的化学信号可能包含以前接触过的证据。最近的疾病病因学研究使用基于质谱的代谢组学来发现循环小分子,这些小分子在疾病病例和对照组之间的丰度不同。这一策略的优点是既包括来自外源性来源(包括饮食)的小分子,也包括来自内源性来源(包括微生物代谢)的小分子。这种方法可以估计个性化的内部暴露的全部补充,包括1)外源性化合物的测量(例如的环境化学品的定量),2)曝光或曝光代谢物协会代谢印记(例如孕妇尿中总砷与肠道细菌代谢产物TMAO的关系[4]),3)暴露的生物学影响(例如乙酰胆碱酯酶活性有机磷酸酯是暴露的生物标志物)和4),其反映磨损在单个过程(例如端粒长度和表观衰老时钟)。然而,除了一些职业调查,没有针对性代谢组学与10 - 50μL强劲的血液不能检测污染物通常出现在正常人群血药浓度1000倍低于因饮食和内源性来源(5]。因此,方法的组合应考虑到组学级非靶向分析用的公知的环境化学品面板集成。这可以通过努力,如国家健康和营养调查(NHANES)或通过构建统计模型时,简单地串联数据集来实现。鉴于一般低浓度的血液中的污染物,这将与具有可分析量有限队列研究生物标本存档具有挑战性。为了解决这一点,有一种迫切需要具有增加的灵敏度和特异性以及增加的样品体积的生物库两者的分析方法。
除了小分子轮廓(例如代谢),有必要获取外部和内部exposome的附加生化签名(例如蛋白质中,miRNA,病毒DNA / RNA)。这些化学和生物化学特征的基于组学的测量将需要与生活方式,社会学和心理学的暴露估计(补充例如绿地,噪音水平,压力)。移动技术和智能穿戴设备可以成为基于exposome的数据收集的组成部分,并代表了收集个性化曝光数据的可行方法。虽然分析的复杂性令人望而生畏,但可以用数据驱动的不可知论方法来评估这一丰富的信息,以确定作为“下一代暴露评估”范式一部分的重点因果关系研究的潜在目标。这些方法需要新的数据分析策略,包括基于机器和深度学习人工智能的大规模数据查询方法。例如,最近的一项exposome研究报告称,在研究的2.4年中,有700亿个不同的变量,其中只有15个个体[6]。应用这些方法在队列或人口水平将需要大量的计算能力,最有可能涉及到访问超级计算机设施。
暴露体的内合物
基于代谢组学的方法已经被用来测量暴露体的化学成分以及评估暴露的生物学和代谢/毒理学表现(即。内部环境)。传统的代谢组学虽然有效,但不能捕获不稳定或反应性强的化学物质(例如4-hydroxynonenal、丙烯醛、丙二醛)。代谢过程会产生一系列具有生物活性的反应性亲电试剂,因为它们与体内的亲核位点(包括DNA和功能蛋白)发生反应,形成大分子加合物。与DNA加合物不同的是,蛋白质加合物不能修复,而且往往在较高的水平上形成。因为这些活性代谢物代表了曝光体的重要组成部分,由于它们的瞬态性质,不能直接测量体内在美国,他们的测量引发了一个被称为“内收肌”的领域,该领域测量循环蛋白或DNA特定位点的加合物。目前这种非靶向的方法主要集中在人血清白蛋白(HSA) Cys34的加合物上。HSA的内收学与肺部疾病的研究特别相关,因为空气中的化学物质与暴露于烟草烟雾后Cys34加合物的形成有关[7],室内燃烧产物[8],和大气污染物[9],和具体的加合物已与试点研究慢性阻塞性肺病和心脏疾病有关[9]。该方法还发现了与膳食脂肪相关的蛋白质加合物(例如亚油酸)[10),以展示获取饮食和接触的综合暴露概况的能力。与反应性羰基相关的加合物可能与肺监测特别相关,因为它们可以提供环境暴露、炎症过程、自身免疫和肺部疾病之间的联系。分析肺部吸入物中的HSA加合物,筛选肺液中不常见的脂质(例如独特的表面活性剂)和新颖的氧化产物,可作为直接肺部暴露的分子标记。蛋白质加合物,不像许多其他生物标记物,可以定量地反映前几周或几个月的暴露(取决于蛋白质的半衰期),而且一些加合物的长半衰期可以使它们成为有用的化学暴露剂量计。进一步的工作应该扩大使用高分辨率质谱分析方法来开发蛋白质加合物的全球筛选,这可以作为环境和饮食暴露的敏感指标。
微生物群、饮食与暴露
该微生物(包括细菌,病毒,真菌和寄生虫)是一个新兴的贡献者exposome可与主机直接互动通过释放的微生物代谢产物的(例如微生物挥发性有机化合物,短链脂肪酸,胞外囊泡和DNA / RNA)。该微生物,环境因素,生活方式和饮食之间的相互作用产生不同的套人与微生物的代谢产物的,可以在有趣和意想不到的方式有助于健康和疾病。例如,ω-6和ω-3脂肪酸的消耗假设的施加在肺部疾病的病理生理学中的作用。而ω-6脂肪酸(例如亚油酸)已与哮喘和过敏的发病,ω-3脂肪酸(例如二十二碳六烯酸(DHA)、二十碳五烯酸(EPA)被建议用于促进呼吸健康,特别是应对污染和吸烟。例如,亚油酸途径已被报道与空气污染和成人哮喘有关[11],而更高的ω-3摄入具有降低室内PM的效果相关联2.5条(粒子50%切断空气动力学直径2.5µm)在儿科哮喘发病率(12]。此外,作用于肠道菌群的饮食已被证明影响气道反应,并建议作为一种方法来预防哮喘[13]。
脂肪酸代谢为在肺部疾病具有有效的生物功能下游脂质介质(例如花生酸类)。这是最有可能的是,这些脂质调节代谢产物负责的脂肪酸观察到健康的影响。例如,亚油酸的产品(例如据报道,白细胞毒素、白细胞毒素二醇与急性呼吸窘迫综合征和慢性阻塞性肺病(COPD)以及EPA和DHA衍生的专业促分解介质有关(例如缓解因子,保护素)降低肺部炎症和提高微生物清除率。然而,最近的工作已经证明,这些过程可以通过肠道微生物,它转换亚油酸到生物活性脂质(被驱动例如12,13- DiHOME,isoleukotoxin二醇)链接到哮喘[14]和代谢性疾病[15]。反过来微生物组可以通过环境暴露的影响,用有机磷杀虫剂,重金属和交通相关的空气污染(TRAP)报道与微生物生态失调相关联16]。因此,饮食上,微生物和环境暴露,可以调节呼吸健康之间显著的串扰。这表明,肺,肠轴内的环境相互作用代表进行调查卓有成效的领域。这些复杂的相互作用为exposome方法的必要性,以调查肺部疾病的病因和病理生理学据理力争。这是不可行的,了解在隔离的底层机制;而不是一个全面的,基于系统的方法才能达到肺部疾病的起源有充分的了解。
解释的时间性质
所述exposome是高度动态的,具有时空可变性,和曝光的定时可影响相关的健康影响。要考虑个人和在成长,发展的各个阶段所处的环境,以及老化轨迹需求的相互作用。该exposome的动态特性,导致其暴露的时间能够发挥在疾病发作强烈影响易感性的窗口的概念,提高公众对肺部疾病的产前和产后环境诱因的相对重要性的问题。例如,增加PM2.5条在妊娠晚期特定的产前时间窗内的水平被发现与脐血中mtDNA含量的降低有关,脐血中mtDNA含量是氧化应激的一个标志[17]。Infants at risk of asthma were reported to exhibit transient gut microbial dysbiosis during the first 100 days of life, suggesting a window in which microbial-based therapeutics may be efficacious in preventing the development of asthma [18]。最近的研究发现,黑碳颗粒积聚在胎侧胎盘的,这表明潜在的机制解释的负面健康影响在子宫内暴露[19]。有因此,需要研究生命阶段和环境暴露的时间相关性,这需要具体的研究设计。例如,虽然出生前暴露于全氟辛酸和全氟壬在1秒在儿童具有较低用力呼气量相关联,也不清楚是否有三个月特异性作用[20]。还应该强调的是,曝光的动态性质延伸到成年期,并应考虑到队列设计时,与成人人口。将暴露的终生动态波动纳入基于暴露的研究是一个重大挑战;然而,有一个明确的需求。一种方法是在更多的时间点收集额外的样本。然而,这自然会导致研究成本的增加,以及收集和分析时间的增加。另一种方法是侧重于分析基质,如牙齿,它提供了足够的时间分辨率,在特定的时间间隔内分配暴露,或蛋白质加合物,延长半衰期。
生物采样测量曝光
由于呼吸系统直接连接到空气环境,它的独特位置反映了空气中的暴露以及基因与环境的相互作用。然而,由于有40种不同的细胞类型,肺的复杂性使得确定与呼吸系统疾病相关的暴露体的最合适的检查策略具有挑战性,特别是在机制研究中。关注气道上皮细胞大大减少了细胞类型的数量,考虑到它是绝大多数吸入污染的受体,这是一种合理的方法。因此,上皮刷可能是特别有洞察力的机制调查;然而,这在队列规模上显然是不可行的。目前大规模的暴露方法主要集中在血液上,并且在哮喘和慢性阻塞性肺病中都观察到了肺生物学循环特征。然而,从肺液(例如支气管肺泡灌洗液,支气管洗),或更远端的流体(例如呼出气冷凝物,痰,唾液,鼻腔洗涤物)可以是更相关的呼吸系统疾病(图1)。特别是唾液已被建议是非常适合的exposome的纵向取样。有必要制定标准化战略(例如细胞类型/计数或被homeostatically控制蛋白质/代谢物标记),以用于评估exposome的影响,并为肺部疾病的调查存档生物标本比较和选择最合适的生物流体(多个)。理想情况下,队列将包括整个种群的纵向取样。虽然这可能是不可行的,您可以为整个队列的分组进行重复抽样调查内和学科及其对暴露 - 反应关系的衰减的贡献之间的曝光差异的来源。这将是执行在其中多个生物标本分别从不同的位置,以便确定哪个隔室提供肺部疾病的最相关的分子标记,以及相关联的曝光收集聚焦研究非常有用的。这些信息将是非常翔实的学习/队列设计,保证长期的样品适用性。
Actionising的exposome
全球趋势,包括气候变化,城市化进程加剧,营养不良人数增加和微生物生态失调会合并,以增加肺部疾病的发病率。了解这些因素之间的激烈串扰和相互需要exposome方法。这些努力的一个重要组成部分将是捕捉到这些复杂的风险的生物影响。记录的曝光不足;有必要证明,以actionise的exposome和超越协会了解曝光的休闲途径的努力的一部分相关的生物和健康影响。然而,为了测量exposome,我们需要加强传统的分析化学和环境健康的方法,包括曝光的无针对性的措施。虽然分析进展,包括高分辨率质谱法将发挥重要作用,我们还需要整合大数据的方法来获得全面曝光的配置文件。目前仍然能够融合来自外部和内部exposome测量新兴多维和纵向数据流的统计方法的基本需要。广泛的协作将在为了实现数据采集的必要的规模是必需的。至于exposome的审讯分析方法继续前进,将有可能对调查具有高分辨率既多个遗传因素(GWAS)和曝光(EWAS)。 This could be performed with a genome-wide inferred study (GWIS) approach, which provides an approximation of GWAS summary statistics for a phenotype that is a function of other phenotypes. Without such parity, we are unlikely to understand the impacts of genes, environment and their interactions on the incidence and mitigation of respiratory diseases.
问题仍然是:我们如何行动的曝光?虽然在理解疾病过程中,终生接触的综合标记的效用是明确的,但仍有必要将这些信息翻译到临床,并最终翻译到患者。理想情况下,曝光模式将使个人做出特定的生活方式选择,以改变他们对特定暴露,特别是混合暴露的敏感性。虽然我们离这个场景还很远,但这个概念并不属于科幻小说的范畴。将个人可穿戴设备与临床信息和遗传历史相结合,最终将使个人能够监测他们的实时暴露情况,并将这些数据与他们当前的疾病状态(例如肺量测定法包)。基于机器的环境数据反映社会行为的可扩展现实挖掘的出现,将为基于曝光的映射提供丰富的信息。尽管其规模令人生畏,但现在已经可以采取初步步骤。队列研究的设计可以尽可能多地纳入暴露数据(例如NHANES),这将使传统的分析。这些数据可以来自智能传感器,GIS建模和便携式监控器,以及关注的已知的化学物质的有针对性的分析(例如全氟化的烷基化的物质)。组学数据,特别是高分辨率质谱数据,可被收集并用于搜索曝光数据库(例如Exposome资源管理器,血液Exposome DB,有毒Exposome DB)提供全面的化学签名。这些数据可以被放置在储存库(例如MetaboLights,代谢组学工作台),使这两个再分析新的数据处理工作流程的开发以及荟萃分析。这种方法的潜力已经取得的资源,明确如ExpoApp [21],这使得基于智能手机的实时监控的个性化exposome轮廓。智能技术的曝光数据和直接接触病人的耦合会在询问环境暴露,饮食,微生物组与肺部疾病之间的复杂关系的强大推进。肺医学需要的未来,包括这种基于exposome的方法来了解疾病,这将使个人actionise他们的实时exposome。
可共享的PDF
脚注
利益冲突:C.E. Wheelock没有什么要披露的。
利益冲突:S.M.Rappaport无需披露。
支持声明:该作品由瑞典心肺基金会(HLF 20170734,20170736)和瑞典研究理事会(2016-02798)资助。CE值会德丰是由瑞典心肺基金会(HLF 20180290)的支持;S.M.拉帕波特由美国国家癌症研究所(R33CA191159)和国立环境健康科学(P42ES004705)的支持。本文资金的信息已交存交叉引用出资者注册。
- 收到2019年10月22日。
- 接受2019年12月9日。
- 版权所有©ERS 2020