文摘
仍然是一个未满足的需要有效,同时在儿科患者治疗选择不能完全控制哮喘,因为安全是至关重要的。
数据汇集从五个随机、双盲、安慰剂对照研究评估tiotropiumµg 5到2.5与安慰剂的附加治疗患者的1到17岁的哮喘症状。分析包括不良事件(AEs)和严重的AEs(节约)在治疗后30天。
治疗的1691例患者,1119收到tiotropium。报告的AEs很低,可比在所有组:tiotropium 5µg (51%), 2.5 tiotropiumµg(51%)和安慰剂(54%)。报道的与毒品有关的AEs,那些导致停药和节约也低,治疗组之间的平衡,无论年龄、疾病严重度或性行为。AEs与哮喘症状和发作的数量降低了tiotropium(5µg)与安慰剂相比,尤其是在这些AEs的季节性高峰。
这一大安全综合分析数据库允许子群分析,往往不切实际的个人每日一次的试验,为安全提供进一步支持tiotropium Respimat附加疗法在儿科患者哮喘症状。
文摘
每天换一次tiotropium Respimat附加儿科患者的治疗是安全的,减少不良事件相关的哮喘发作症状,尤其是在季节性高峰http://ow.ly/ujHw30of3xk
介绍
哮喘是最常见的慢性疾病之一,在儿童和青少年,影响∼10%的儿童和青少年在英国和美国1- - - - - -3]。研究表明,> 50%的4-18-year-old仍然尽管症状治疗哮喘的患者至少一个吸入激素(ICS) [1,2]。对于这些患者来说,第一个干预是改善病人的教育和自我管理。这包括确保遵守规定的治疗和设备的最佳使用,在可能的情况下,确认避免过敏原暴露于环境污染物和烟草烟雾。该症状持续,升压治疗可能被考虑。治疗方法包括添加长效β2受体激动剂(腊八粥)和/或白三烯受体拮抗剂(LTRA)维持治疗方案和/或进一步增加剂量ICS (4]。ICS治疗是影响孩子的成长,尤其是当管理中级到高级剂量超过一段时间;因此,替代增加ICS剂量将有吸引力的(5,6]。常见的副作用与腊八包括增加心率、心悸和震颤,尽管地震一般解析后最初几个剂量(7]。的LTRA montelukast通常被认为是安全的用于儿童,虽然不如ICS的功效[8]。相反,研究利用瑞典药品不良反应数据库,瑞典,调查儿童常用药物组,表明montelukast是药物2005年最常见的药品不良反应。大多数的这些主要是在5岁以下儿童和精神在本质上(9]。另一项研究也强调了一些特定的神经精神病学的不良事件(AEs)的用户应该认知的(10]。因此,有一个未满足的需要更多的喷雾耐受良好且有效的治疗选择的治疗儿科患者哮喘症状。
Tiotropium Respimat(勃林格殷格翰集团、殷格翰集团莱茵、德国)(以下称为“Tiotropium”)是一个长效毒蕈碱的对手。它已经在一个全面的评估作为一个附加治疗2和3期临床试验项目包括6000多名成人和儿科患者哮喘症状(11- - - - - -24]。基于这些试验的证据,tiotropium是有效的附加治疗,安全性和耐受性与安慰剂比较的个别研究。Tiotropium表示为每日一次使用在欧盟(两个吸入2.5µg)和美国(两个地吸入1.25µg)当严重哮喘患者维持治疗≥6岁(25,26]。除了tiotropium附加治疗的安全报告的个人临床试验,深入、系统的安全评估和成人患者的耐受性(27,28],本文提供的分析,涉及大样本的儿科患者,可以提供更大的权力,以发现任何尚未不明身份的安全信号,并允许子组的安全分析与个别试验是不切实际的。
当前分析的目的,因此,进一步评估的安全性和耐受性tiotropium人口集中的儿科哮喘症状患者(17岁)在不同的全球倡议治疗哮喘(吉娜)的步骤,并调查相关AEs的季节性哮喘发作症状和人口集中。
方法
汇集分析包括所有第三阶段与这些相应平行的组织研究(11岁)儿童和青少年(12 - 17年),以及1 - 5岁儿童的2/3期研究,包括在临床开发计划署tiotropium的哮喘。所有试验的随机、双盲、安慰剂对照的设计,在12周和1年时间(表1)[18,19,21- - - - - -23]。治疗历史(治疗步骤招生)中指定的每个试验不同,反映了病人的严重程度(表1)。
试验药物
在治疗期间在所有的实验中,患者接受tiotropium(5或2.5µg)或安慰剂(由Respimat吸入器为两个泡芙)每天一次。Tiotropium还附加疗法ICS维持治疗有或没有其他控制器疗法。NinoTinA-asthma研究[231 - 4岁),患者在筛选被要求使用一个Aerochamber + Flow-Vu装有阀的控股室(通常被称为一个垫片;Trudell医疗国际,伦敦,加拿大),戴上面罩吸入试验的药物。5岁儿童在筛选被允许使用Respimat有或没有间隔和喉舌,这取决于偏好。
端点
一起安全的评估(功效)是一个主要目标在所有5个试验。6岁到17岁,在试验的四个小孩主要疗效终点是改善用力呼气量在1 s,这就是权力的计算是基于。试验中涉及儿童年龄< 6年,没有正式权力计算相关的一个端点,但招聘被认为是充分的描述性评价疗效和安全性。这个分析是基于AEs之间发生第一药物吸入和后30天,直到最后一个剂量的试验药物,使用医学字典编码的监管活动(MedDRA) 18.1版(www.meddra.org)。进一步的细节和定义的AEs和严重的AEs(节约)中可以找到补充材料。
复合终点,分组AEs MedDRA-preferred相关术语群“哮喘急性加重和哮喘相关的症状”,从池中所有的研究分析也进行了分析。首选项包含在分析中列出补充表E1。
池安全数据提出了以下分析组:所有病人,和子组年龄、哮喘严重程度和性。
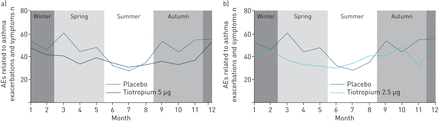
此外,AEs的数量与哮喘急性加重和症状汇集数据被月策划,与南半球转移通过6个月的数据对齐季节(北半球:6月= 6月;南半球:12月=月6)。
分析治疗组,定义为所有患者随机接受至少一个剂量的试验药物。分析评估叙述地和没有进行推论统计。分析AEs相关症状和哮喘急性加重汇集数据被月作为绘制事后因此只考虑探索性分析。
据报道,每个研究按照修改赫尔辛基宣言。伦理研究各自的机构的董事会批准了这项协议,签署,知情同意是获得所有的病人和/或他们的父母。看到原始出版物详情(18,19,21- - - - - -23]。
结果
共有1691名患者由治疗组(表2):560患者接受tiotropium 5µg, 559名患者接受tiotropium 2.5µg和572名患者接受安慰剂治疗。总的来说,意味着暴露于药物研究是314年,304年和314年tiotropium 5µg白细胞数量,分别tiotropium 2.5µg和安慰剂。
安全
AEs患者总数的一般治疗组之间的比较,包括安慰剂(表3)。大约一半的病人(n = 879(52%)至少经历了一次AE (n = 283(51%)接受tiotropium 5µg;2.5 n = 286(51%)接受tiotropiumµg;n = 310(54%)接受安慰剂)。很少AEs导致治疗中断:两个病人接受tiotropium 5µg和五个病人接受安慰剂。唯一的AE导致中止报告超过一个病人是哮喘恶化/恶化(两个病人接受tiotropium 5µg和两个病人接受安慰剂)。investigator-defined毒品AEs患者的发病率很低,治疗组之间的比较,包括安慰剂。所有的毒品AEs tiotropium治疗组严重或导致治疗中断。唯一的AE评估药物相关,在两个以上的病人咳嗽(一个病人接受tiotropium 5µg;一个病人接受tiotropium 2.5µg; four patients receiving placebo). The overall frequency of patients that experienced SAEs was low and comparable between treatment groups. No SAEs were considered drug related or led to treatment discontinuation. The only SAEs reported for more than two patients were asthma exacerbation/worsening/crisis (five patients receiving tiotropium 5 µg; three patients receiving tiotropium 2.5 µg; five patients receiving placebo) and appendicitis (two patients receiving tiotropium 5 µg; two patients receiving tiotropium 2.5 µg; one patient receiving placebo). No deaths occurred during any of the trials.
最频繁的报道与疾病概要文件一致,AEs,≥5%的患者报告的,哮喘恶化/恶化,减少峰呼气流量(PEF)率、鼻咽炎、鼻咽炎和病毒性呼吸道感染(表3;AEs≥2%的患者报告所示补充表E2)。这些报告了类似的比例tiotropium和安慰剂组的患者,除了哮喘恶化/恶化,由少报道患者tiotropium治疗组。
患者报告的频率复合终点,分组与哮喘发作相关的所有AEs和哮喘症状,较低的tiotropium治疗组与安慰剂(安慰剂:217事件的患者(37.9%);tiotropium 5µg: 177事件的患者(31.6%),率比例在安慰剂0.76 (95% CI 0.63 - -0.93);tiotropium 2.5µg: 195事件(34.9%),患者比例在安慰剂0.87 (95% CI 0.72 - -1.05))。安全的描述可以在感兴趣的主题补充材料。
子组的年龄
安全在不同年龄类别一般人口集中的比较(表4)。较低比例的患者哮喘恶化/恶化作为AE tiotropium组与安慰剂组相比,最显著的患者中观察到1 - 5岁(6.5% tiotropium 5µg;13.9% tiotropium 2.5µg;29.4%安慰剂),类似的趋势在6尺11寸岁患者(26.4% tiotropium 5µg;25.5% tiotropium 2.5µg;32.8%安慰剂),12 - 17年(14.4%为tiotropium 5µg;16.3% tiotropium 2.5µg;安慰剂)为16.8%。
没有节约患者报道tiotropium 1-5-year-old组和AEs在这个年龄段导致任何治疗组(停药表4;节约的年龄所示补充表E3)。哮喘是唯一AE首选项报道≥5%,或在10或更多的病人,在治疗组。
汇集的数据的分析研究与病人年龄≥6年详细补充表E4。
子组的哮喘严重程度
安全在不同的哮喘严重程度分类一般人口集中的比较(表5)。然而,相比之下,人口集中,更温和的哮喘患者报告至少一个AE和更少的严重哮喘患者报告至少一个AE。这是最有可能由于长期的研究为中度哮喘中哮喘(48周与12周严重哮喘)。值得注意的是,严重哮喘患者,PEF下降率报告更少的病人tiotropium组比安慰剂组。
子群分析腊八,LTRA使用随机也执行;正如预期的那样,结果被严重程度与子群分析一致,因为腊八/ LTRAs主要是采取更严重的哮喘患者。
子组的性
在分析AEs的性,有更少的女性比男性在每个治疗组;比例,略少报道AEs与男性相比,女性尤其是tiotropium 5µg和安慰剂组无显著差异的比例与毒品有关的AEs或AEs导致患者停药(表6)。整体分析,患者经历节约的频率很低,治疗组之间的可比性。
讨论
在这个综合汇总分析,tiotropium耐受性良好,安全性比得上安慰剂。具体来说,病人的发病率报告与毒品有关的AEs, AEs导致停药,节约和AEs通常与抗胆碱能治疗通常很低,治疗组之间的平衡,包括安慰剂。基线人口统计学和疾病的特点是比较治疗组之间在每个试验(表2)。药代动力学数据1-5-year-old集团(包括那些使用装有阀的控股室)曾被证明是可比较的结果6-17-year-old组织调整的体型时,指示充足率系统性接触tiotropium [29日]。
疗效数据表明tiotropium ICS是一种有效的插件,有或没有额外的控制器疗法,在儿童和青少年哮喘(16- - - - - -19,22,23]。结果汇总分析提供更多有利的安全性的证据tiotropium在儿童和青少年哮喘症状(17岁)28,29日]。
一个重要的发现是,AEs与哮喘症状和发作在tiotropium 5µg报道较少的患者治疗组与安慰剂相比,与特定的影响在减少春天和秋天季节高峰。虽然报道作为安全参数,这个信号也可能被视为在疗效方面,尤其是在非常小的孩子患有哮喘,验证工具有效性的评估临床试验目前有限的(23]。有趣的是,这种效应tiotropium添加到ICS /腊八已经观察到与其他干预措施,包括集成电路/腊八组合(30.和生物制剂31日]。作为长期在儿科患者的哮喘恶化试验保持道德挑战,这种分析突出了另一个端点调查儿童这样的功效。这些数据也强调审判时机的重要性占季节性恶化高峰时12个月研究长度是不实际的。然而,由于这一发现是探索性的,它应该在一个预定义的研究证实,也可以调查,年龄群最大的利益。
报道类抗胆碱能类的影响包括上呼吸道感染、心动过速、口干和其他胃肠道并发症,以及尿潴留,尿路感染32- - - - - -35]。病人报告这些AEs的发生率很低在目前的分析,总体来说,tiotropium的安全性与安慰剂比较在所有试验报告(29日]。值得注意的是,心脏事件报道只有两个病人,他们都是在安慰剂组。
分析人口的子组内定义的年龄,哮喘严重程度、性和腊八/ LTRA使用基线,病人报告AEs和节约的比例一般治疗组之间的比较,包括安慰剂。这是进一步支持的近期疗效和安全性的系统评价tiotropium与严重哮喘症状(6 - 11岁儿童36]。作者得出的结论是,所有的三个研究纳入分析(两个都包含在本文提供的分析)显示增加的速度AEs或节约tiotropium组与安慰剂比较(36]。
这一分析的主要力量是所有与可比安慰剂对照试验设计,因此提供最有效的比较来评估AEs。此外,所有患者继续接受他们平常的维护治疗(腊八中度哮喘患者除外),允许调查tiotropium在不同环境下的并发药物治疗,从而使其代表在现实生活环境中的临床试验设置是可以实现的。病人的样本是非常大的和年龄范围很广;患者从不同的人口和地理位置,包括一个高比例的拉丁美洲病人(人口中有高发病率和高儿童哮喘的严重程度)。汇集分析的局限性包括五项包括试验持续时间的差异在48周(两个,三个在12周),没有> 48周。
结论
每天换一次tiotropium作为附加至少ICS在1到17岁的患者维持治疗哮喘症状在不同吉娜治疗步骤是一个当前的治疗方案,在安全性和耐受性方面更好与安慰剂相比较。没有新的安全信号确定在这个综合分析,支持每日一次的有利的风险概要tiotropium附加维护ICS有或没有额外的控制器在儿科患者哮喘症状。此外,减少病人报告AEs相关哮喘急性加重和tiotropium 5µg观察哮喘症状,尤其是在发作相关的季节性高峰。
补充材料
确认
作者充分的责任范围、方向、内容和编辑的决定有关的手稿,都在开发的所有阶段,并批准提交的手稿。所有作者都完全访问所有的数据在这项研究中,并负责数据的完整性和数据分析的准确性,包括,特别是任何不利影响。这项工作是由勃林格殷格翰集团财务支持。医疗援助,写作形式的准备和修改的手稿,勃林格殷格翰集团财务支持,并提供了乔纳森·布伦南(我公司媒体,曼彻斯特,英国)作者的概念方向,基于作者的反馈。作者要感谢所有参与这些试验的病人和他们的家属,他们也延长由于调查员。
脚注
可以从本文的补充材料www.qdcxjkg.com
ClinicalTrials.gov登记细节:NinoTinA-asthma,NCT01634113;CanoTinA-asthma,NCT01634139;VivaTinA-asthma,NCT01634152;RubaTinA-asthma,NCT01257230;PensieTinA-asthma,NCT01277523。以确保独立的临床研究结果的解释,勃林格殷格翰集团授予所有外部作者访问所有相关材料,包括participant-level临床研究数据,并根据需要相关材料由他们履行他们的角色和义务,作者根据国际标准。此外,临床研究文档(如。研究报告,研究协议,统计分析计划)和参与者临床研究数据可共享主手稿出版后在同行评议的杂志上发表,如果监管活动是完整的和其他标准/勃林格殷格翰集团政策透明度和出版的临床研究数据:https://trials.boehringer-ingelheim.com/transparency_policy.html。提供之前,文档将被检查,如果有必要,编辑和数据将会消除识别信息,保护研究参与者的个人数据和人员,并尊重研究对象的知情同意的边界。临床研究报告和相关临床文件可以请求通过:https://trials.boehringer-ingelheim.com/trial_results/clinical_submission_documents.html。所有这类请求将由文档分享协议。善意的,合格的科学和医学研究人员可能会请求访问消除识别信息,可以分析的参与者临床研究数据与相应的文档描述数据集的结构和内容。批准,由一个数据共享协议,数据共享在一个安全的数据访问系统有限段1年,这可能是扩展的要求。研究人员应该使用https://clinicalstudydatarequest.com要求对研究数据的访问。
作者的贡献:m .恩格尔和点Moroni-Zentgraf参与研究设计,数据分析和解释。g . El Azzi s.d Vulcu参与数据分析和解释。所有作者都参与写作手稿和决定提交出版的手稿。
利益冲突:c . Vogelberg报告进一步研究机构支付从勃林格殷格翰的发言,在进行研究;个人费用咨询委员会工作,从勃林格殷格翰集团和诺华讲课,在提交工作。
利益冲突:中华民国Szefler报告机构基金咨询公司从勃林格殷格翰的发言,Aerocrine,诺华,第一三共制药和罗氏公司,机构基金从Genentech手稿准备和咨询委员会工作,研究经费和机构资金会议考勤从葛兰素史克公司和顾问委员会工作,机构资金用于教育活动从阿斯利康,机构基金咨询委员会工作从Teva,外提交的工作。
利益冲突:E.J.L.E. Vrijlandt没有披露。
利益冲突:A.L.大错没有披露。
利益冲突:m .恩格尔是勃林格殷格翰集团的一名员工。
利益冲突:g . El Azzi受雇于勃林格殷格翰的发言,在进行这项研究的。
美国南达科他州的利益冲突:Vulcu是勃林格殷格翰集团的一名员工。
利益冲突:下午Moroni-Zentgraf是勃林格殷格翰集团的一名员工。
利益冲突:o . Eickmeier报道国际勃林格殷格翰集团公司的薪酬进行研究。
利益冲突:大肠Hamelmann Allergopharma咨询,碱性,Bencard,勃林格殷格翰的发言,葛兰素史克,哈尔过敏,诺华,纽迪希亚,Stallergenes;他已经收到了德国社会的研究支持研究,国家教育部和北威州的研究,和德国教育和研究。
支持声明:这项工作是由勃林格殷格翰集团国际GmbH(殷格翰集团莱茵,德国)。医学写作援助被勃林格殷格翰集团国际GmbH简约补偿。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年9月26日。
- 接受2019年3月19日。
- 版权©2019人队
这个版本分布在创作共用署名非商业性许可证的条款4.0。