摘要
背景
相当多的哮喘儿童尽管接受了吸入糖皮质激素治疗,但仍有症状,导致显著发病率、生活质量下降、医疗费用增加和上学时间减少。本研究的目的是评估每日一次tiotropium Respimat®5 μg、2.5 μg和1.25 μg附加到中剂量吸入皮质类固醇(含或不含白三烯修饰剂)对6-11岁有症状哮喘的儿童的疗效、安全性和耐受性。
方法
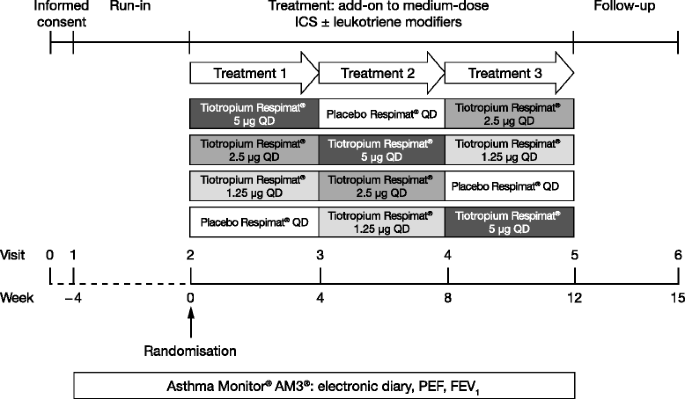
在这项II期、双盲、安慰剂对照、不完全交叉、剂量范围研究中,患者被随机分为四种治疗方案中的三种:在12周(三周)的晚上,每天服用一次噻托溴铵Respimat®5μg、2.5μg或1.25μg或安慰剂Respimat® × 4周)治疗期。
结果
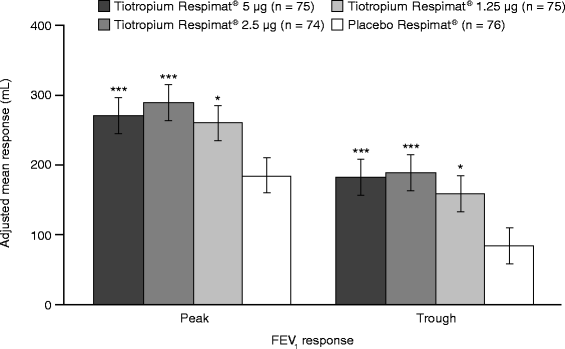
总共有76、74、75和76例6-11岁的患者分别服用了tiotropium Respimat®5 μg、2.5 μg、1.25 μg和安慰剂Respimat®。对于主要终点(给药后3小时内测量的1秒内强迫呼气量峰值),tiotropium Respimat®5 μg (272 mL)、2.5 μg (290 mL)和1.25 μg (261 mL)的调整平均反应显著大于安慰剂Respimat®(185 mL;P = 0.0002, P < 0.0001, P = 0.0011)。tiotropium Respimat®所有剂量的安全性和耐受性与安慰剂Respimat®相当,没有严重的不良事件,也没有导致停药的事件。
结论
Tiotropium Respimat®在中剂量吸入皮质类固醇(含或不含白三烯修饰剂)的基础上,对有症状的儿童哮喘患者均有效,且与安慰剂Respimat®具有相当的安全性和耐受性。
试验注册
ClinicalTrials.gov标识符NCT01383499
背景
哮喘是儿童发病的主要原因[1]。仅在美国,就有约700万儿童和青少年患有哮喘[2]在英国,2-15岁的每七名儿童中,哮喘症状需要定期治疗[3.]。与成人一样,吸入皮质类固醇(ICS)指导治疗未能充分控制相当大比例的儿童哮喘,这是一个值得关注的健康问题[4]。除了对患者的生活质量产生负面影响外,这还大大增加了他们未来病情恶化的风险,并相应增加了医疗利用需求和成本[5-7]。美国的数据显示,2011年,56%的哮喘儿童曾发作[2,近20%的人会去急症科[8]。
而哮喘儿童的治疗目标[9,10]与成人基本相同(为了改善控制、减少恶化、减少抢救用药、减少住院和尽可能多地参与正常日常活动),治疗可能会因这个年龄段特有的或更明显的问题而变得复杂。儿童和青少年对哮喘药物的依从性明显较差[11,而每天2次ICS治疗方案的依从性可能不佳,特别是在无症状期。此外,由于受影响的儿童和他们的父母往往低估了他们的哮喘严重程度,从而阻碍了对哮喘控制不良儿童的发现和适当的管理[5,6,11-14]。
鉴于儿童哮喘失控的普遍性及其对健康、教育和经济的影响,显然有必要进一步改善哮喘的控制并防止该人群的哮喘恶化;长效抗胆碱能支气管扩张剂噻托溴铵是此类患者的一种潜在附加疗法[15,16]噻托溴铵已证明对成人哮喘有疗效[17-21]和青少年[22]。在这里,我们报告了噻托溴铵治疗6-11岁有症状的哮喘儿童的首次评估数据。本研究评估了三种剂量噻托溴铵在ICS维持治疗的症状性哮喘儿童中的有效性、安全性和耐受性。
方法
研究设计
这项II期随机、双盲、安慰剂对照、不完全交叉、剂量范围研究于2011年8月23日至2012年9月25日在6个国家的24个中心进行。该研究符合所有当地法律和监管要求,符合《赫尔辛基宣言》、良好临床实践和良好出版实践指南。该方案由每个研究中心的独立伦理委员会批准,所有患者及其父母或法定监护人均提供书面知情同意。
四周后磨合过程,在此期间,患者接受ICS维持治疗有或没有白三烯修饰符,在1:1:1:1比患者随机接受每日一次tiotropium 5μg, 2.5μg、1.25μg或安慰剂,所有通过Respimat®SoftMist™吸入器(勃林格殷格翰集团制药GmbH & Co .公斤,德国莱茵殷格翰),在三个4周的治疗期间。患者接受了四种可用治疗中的三种,在治疗期间没有洗脱(图)1)众所周知,慢性阻塞性肺疾病患者服用噻托溴铵3周后可达到药效稳定状态[23,24]。所有研究治疗(tiotropium Respimat®5 μg、2.5 μg、1.25 μg和安慰剂Respimat®)均在父母监督下每晚自我给药,双盲附加中剂量ICS (200-400 μg布地奈德或等效剂量)的维持治疗,含或不含白三烯修饰剂。患者和家长在第1次来访(筛查)和第2次来访(随机)以及随后的来访(如有需要)接受了关于Respimat®SoftMist™吸入器使用的培训。一直保持到数据库锁定。在筛查和整个治疗期间,允许紧急用药(开放标签沙丁胺醇吸入器,每次100 μg)。在试验期间,抗生素的使用没有受到限制;允许暂时增加ICS的剂量或添加全身类固醇,以及添加短效茶碱制剂以治疗急性加重。
采用固定分组随机法,以确保为每个治疗分配平衡的患者数量。患者分配到治疗序列的顺序是随机的。随机列表由勃林格·英格尔海姆使用带有伪随机数生成器的经验证系统生成,并提供种子数。
研究人群
年龄在6-11岁、哮喘病史≥6个月并经筛查确诊的男性和女性患者均符合纳入本研究的条件。所有患者都需要有支气管扩张剂可逆性,导致1秒内用力呼气量(FEV)1)增加≥12%在服用200μg沙丁胺醇后15-30分钟内出现症状,并且在筛选和随机分组前出现症状,如七个问题的哮喘控制问卷(ACQ-7)所定义,平均得分为≥1.5.所有患者均接受了中等剂量(200–400μg布地奈德或等效剂量)的ICS维持治疗,作为单一治疗或与长效β-干扰素联合治疗2-激动剂(LABA)或白三烯修饰剂在筛查前使用≥4周(LABA必须在筛查前至少24小时停止;然而,白三烯修饰剂在整个试验中都被允许使用)。此外,所有患者必须进行支气管扩张剂前FEV160-90%的患者在筛查时预测正常,并显示支气管扩张剂前FEV1与筛选值相比,随机化可变性在±30%以内。排除标准包括筛查前4周内除哮喘、先天性心脏病、任何急性哮喘加重或急性呼吸道感染外的其他严重疾病,筛查前4周内使用长效吸入或全身抗胆碱能药物或全身(口服或静脉)皮质激素治疗。
研究终点
所有研究终点均被评估为一个反应,定义为三个4周治疗期结束时与基线(随机,第2次就诊)的差异。主要疗效终点是FEV峰值1给药后3小时内(FEV峰值1(0-3h)).次要终点包括低谷FEV1,FEV.1给药后3小时内曲线下面积(AUC(0-3h))给药后3小时内的最大用力肺活量(FVC(0-3h))、谷FVC、FVC AUC(0-3h)以及给药前早、晚呼气峰流量(PEF)。其他终点包括个体FEV1给药后3小时测量,4周时平均用力呼气流量为FVC的25-75%。采用ACQ-7和标准化儿科哮喘生活质量问卷(PAQLQ[S])分别评估哮喘控制和生活质量。
评估
在第1-5次访视时进行肺功能评估和生命体征评估。肺功能评估分别在筛选时吸入研究药物后30分钟、1小时、2小时和3小时,在4周磨合期结束时和每个4周治疗期结束时进行。患者使用asthma Monitor®AM3®设备(Care Fusion, Höchberg, Germany),结合电子峰值流量计和电子日记,记录每天两次PEF值和哮喘症状、生活质量和抢救用药的详细信息,研究人员在每次门诊开始时对这些数据进行审查。平均PEF测量是在每个治疗期的最后一周确定的,以避免先前治疗效果的结转。ACQ-7和PAQLQ(S)数据分别于来访1-5和2-5收集。记录每次来访的不良事件(AEs)。
统计分析
假设FEV峰值患者内差异的标准偏差为280 mL1(0-3h),使用完全交叉设计,需要64名完整患者的样本量,以检测FEV峰值100 mL的治疗差异1(0-3h)基于两个样本t-以80%的功率和2.5%的I型误差概率进行试验。使用方程n = 3*m/2,经计算,本研究中使用的不完全区组设计需要96名患者。因此,据估计,完成研究的大约104名患者的样本足以进行计划的统计分析,考虑到青少年患者的类似研究中观察到的8%的辍学率[22]。
主要疗效分析使用完整的分析集进行,定义为所有接受至少一剂研究药物治疗的随机患者,具有基线数据,并在4周治疗期后进行至少一次治疗疗效测量。tiotropium Respimat®治疗优于安慰剂Respimat®,采用混合模型重复测量分析,以α = 0.025(单侧)的水平进行序列分级,以“治疗”和“周期”为固定效应,“患者”为随机效应。研究终点的基线值作为协变量包含在统计模型中。计算调整后的平均值、治疗对比、95%置信区间和p值。使用完整的分析集和混合模型重复测量分析分析次要终点。治疗组用于安全性评估,定义为所有接受至少一剂研究药物的随机患者。
结果
总共,101例患者随机接受研究治疗。76例患者接受tiotropium Respimat®5 μg, 74例接受tiotropium Respimat®2.5 μg, 75例接受tiotropium Respimat®1.25 μg, 76例接受安慰剂Respimat®(补充文件)1:图S1)。100名患者完成了所有三个治疗期,其中1名患者提前终止了研究(在接受tiotropium Respimat®5 μg治疗的前4周期间,由于非ae相关原因,撤回了同意);该患者被排除在整个分析集之外。
基线人口统计资料和疾病特征
大多数患者为男性(68.3%),平均年龄8.8岁,平均哮喘持续时间4.5年1)。只有5.9%的患者曾接触过家庭/二手烟。大约三分之二的患者在筛查时患有伴随疾病(63.4%),最常见的是过敏性鼻炎(53.5%)。
在筛查前的3个月内,所有患者均接受了ICS治疗,36.6%的患者也接受了LABA治疗,45.5%的患者服用了额外的白三烯调节剂。在随机分组时(第2次就诊),所有患者均服用ICS,45.5%的患者也服用白三烯调节剂。磨合或治疗期间不允许使用LABA。
表中总结了患者的基线哮喘特征2.筛查时,支气管扩张剂使用前后的平均FEV1值(±标准差:1.539±0.385 L, 1.909±0.469 L)分别为预测正常值的79.7%和98.9%。使用支气管扩张剂的平均可逆性(%前支气管扩张剂)为370±171 mL(24.6%)。在基线,平均FEV1为1.640±0.386 L(85.4%), 29.7%的患者有FEV1值>为预测正常的90%。
功效
对于主要疗效终点,峰值FEV差异有统计学意义1(0-3h)观察到tiotropium Respimat®剂量组与安慰剂Respimat®治疗4周后的反应(图)2).tiotropium Respimat®5 μg、2.5 μg和1.25 μg与安慰剂Respimat®的校正平均差异分别为87 mL (p = 0.0002)、104 mL (p < 0.0001)和75 mL (p = 0.0011)。在接受tiotropium Respimat®治疗的患者中,没有观察到剂量依赖性反应,在FEV峰值时,不同剂量之间只有轻微的、无统计学意义的差异1(0-3h)治疗4周后有反应。
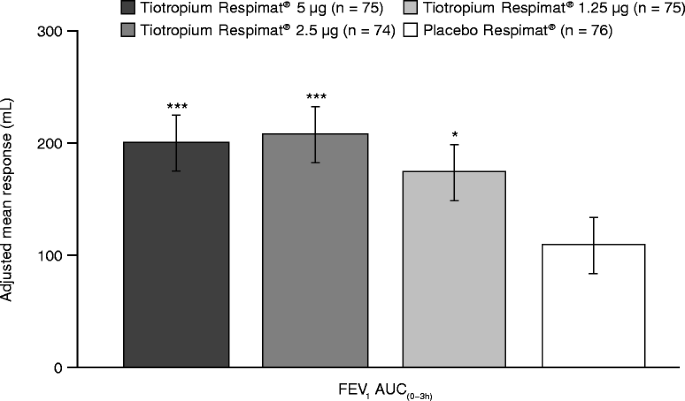
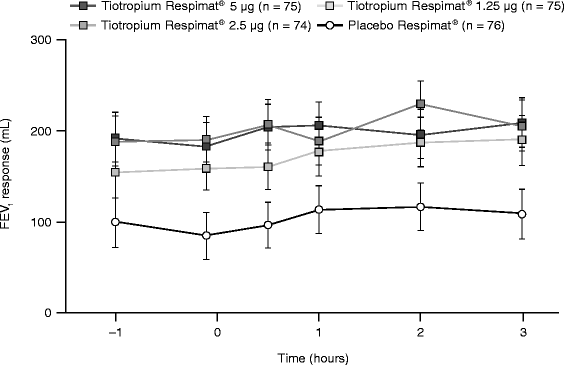
Tiotropium Respimat®还改善了次要和额外的疗效终点,包括低谷FEV1反应,FEV1AUC(0-3h)响应和FEV1给药后3小时内的反应。调整后的平均谷FEV在统计学上有显著差异1观察每个噻托溴铵Respimat®剂量组与安慰剂Respimat®的反应(图2):5μg = 98毫升(p < 0.0001),2.5μg = 105毫升(p < 0.0001)和1.25μg = 75毫升(p = 0.0023)。校正平均FEV的统计显著差异1AUC(0-3h)与安慰剂Respimat®相比,每个tiotropium Respimat®剂量组也观察到反应(图)3.):5μg = 91毫升(p < 0.0001),2.5μg = 99毫升(p < 0.0001)和1.25μg = 68毫升(p = 0.0013)。FEV1所有剂量tiotropium Respimat®的反应均显著优于安慰剂Respimat®,持续至给药后3小时(图)4).
虽然峰值FVC(0-3h),通过FVC和FVC AUC(0-3h)tiotropium Respimat®治疗改善了反应,仅在FVC AUC方面改善有统计学意义(0-3h)2.5 μg剂量有反应(p = 0.0383)。
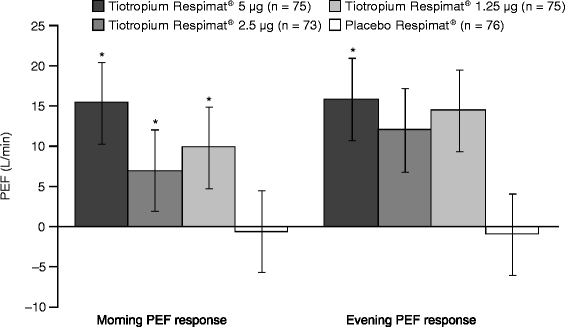
4周后,所有tiotropium Respimat剂量组的早晨和晚上PEF反应均较基线有所增加。三种tiotropium Respimat®(5 μg = 16 L/min [p = 0.0036]、2.5 μg = 13 L/min [p = 0.0215]和1.25 μg = 15 L/min [p = 0.0061])均观察到调整后的平均早晨PEF反应有显著改善,与安慰剂Respimat®相比,5 μg剂量组的调整后平均夜间PEF反应改善17 L/min (p = 0.0024),具有统计学意义(图)5).
显著改善调整意味着用力呼气流量25 - 75%反应在所有时间点观察3小时post-dosing所有tiotropium Respimat®剂量组与安慰剂Respimat®:5μg = 318毫升/秒,2.5μg = 319毫升/秒和1.25μg = 296毫升/秒3小时post-dosing(所有p<0.0001)。没有观察到剂量依赖性反应,三组tiotropium Respimat®剂量组之间没有显著差异。
虽然没有统计学显着,但在用安慰剂respimat®处理后观察到哮喘控制和生命质量的数值改善,而安慰剂respimat®(ACQ-7调整的平均反应:5μg=-0.088,2.5μg= -0.120和1.25μg) = −0.057; total PAQLQ[S] adjusted mean response: 5 μg = 0.091, 2.5 μg = 0.029 and 1.25 μg = 0.024).
安全性和耐受性
在三组tiotropium Respimat®剂量组和安慰剂Respimat®治疗组中,接受研究治疗时发生的AEs发生率相当,每组中约10%的患者报告了事件(表)3.).研究期间未报告死亡、严重不良事件、导致停药的不良事件、药物相关不良事件或预先指定的严重不良事件。只有一名患者因非不良事件相关原因退出同意书而提前停药。报告的所有其他类型不良事件的患者不到3%,且无ind在任何治疗组中,有两名以上的患者报告了IVIA双AE。
讨论
在本研究中,每日一次的噻托溴铵Respimat®添加到中等剂量ICS,无论是否添加白三烯调节剂,都可以改善有症状哮喘儿童的肺功能。对于主要终点,FEV峰值在统计学上显著改善1(0-3h)观察所有tiotropium Respimat®剂量组与安慰剂Respimat®治疗4周后的反应。
次要和额外疗效终点的分析也普遍证明了所有噻托溴铵Respimat®剂量试验的优越性,其谷FEV在统计学上有显著改善1,FEV.1AUC(0-3h)和峰值FEV1与安慰剂Respimat®相比,tiotropium Respimat®在所有时间点观察到3小时后。观察到的FVC改善通常与安慰剂Respimat®的观察无显著差异,考虑到该患者群体的年龄,这是一个预期的观察结果。
PEF监测是测量气道变化的重要工具,特别是对于那些可能无法准确感知其症状恶化的患者[25].与FEV相比,PEF结果(代表每日值的周平均值)可能提供更可靠的数据1测量值,表示在病人的真实生活环境之外的诊所中一天内采集的单个值。本研究的数据表明,所有剂量的tiotropium Respimat®都优于安慰剂Respimat®用于早晨PEF。tiotropium Respimat®5 μg剂量也优于安慰剂Respimat®,高于2.5 μg和1.25 μg剂量。
关于患者报告的结果,在所有三种剂量的噻托溴铵Respimat®治疗后,在本研究中观察到ACQ-7和PAQLQ(S)评分改善的积极趋势。需要对持续时间较长且患者人数较多的平行组试验进行额外分析,以进一步研究噻托溴铵Respimat®对症状性哮喘儿童哮喘控制和生活质量的影响。
该研究表明,每日一次的tiotropium Respimat®添加到中剂量ICS(含或不含白三烯修饰剂),在6-11岁有症状哮喘的儿童中具有与安慰剂Respimat®相当的安全性和耐受性。这与成人患者的数据相似,并进一步加强了这一数据,其中每日一次tiotropium Respimat®在有或没有LABA ICS的症状性哮喘患者中显示与安慰剂Respimat®相比具有类似的安全性和耐受性[20,26,27]。
虽然噻托溴铵Respimat®剂量之间的比较只是描述性的,但我们注意到,对于主要或任何次要或附加疗效终点,均未观察到明显的剂量依赖性反应。对成年和青少年哮喘患者进行的II期研究结果清楚地表明,其对哮喘的反应更大在这些II期研究中,每日一次的10μg、5μg、2.5μg或1.25μg剂量均能改善肺功能,且耐受性良好,5μg剂量可实现最大的支气管扩张[17,18,22,28]。噻托溴铵Respimat®5 μg的长期临床疗效和安全性已在两项大型III期研究中得到证实,研究对象为接受ICS + LABA治疗的有症状哮喘成人患者[20]。
与加压计量吸入器和干粉吸入器相比,Respimat®SoftMist™吸入器可能具有优势,特别是在治疗儿童哮喘方面。虽然正确的技术仍然很重要,但使用SoftMist™吸入器增加的气溶胶生产时间可能有利于吸气容量低或吸气至驱动时机不佳的年轻患者[29]。单每日给药的单个装置还可以改善患者的粘附,在儿童和青少年中尤其是差的[11]。
应该注意的是,这项研究在方法上有一些局限性。不完全交叉设计意味着所有患者没有接受所有研究治疗;然而,该研究设计减少了患者间的变异性,减少了达到统计功效所需的患者数量,治疗之间缺乏洗出促进了患者的依从性。研究持续时间短意味着重点是评估肺功能,不允许全面评估哮喘症状控制或恶化率。
这份手稿中提供的数据鼓励并证明了未来在儿科患者中进行的大型III期试验,以证实这些结果,并检查tiotropium Respimat®附加治疗对长期疗效、安全性和耐受性的影响。其他研究将有助于确定tiotropium Respimat®在未来治疗指南中的适用范围,特别是在有或没有LABA的高剂量ICS维持治疗方面。
结论
这项首次对症状性哮喘儿童进行的噻托溴铵Respimat®研究表明,噻托溴铵Respimat®添加到中等剂量ICS中,无论是否添加白三烯调节剂,都是有效的,并且具有与安慰剂Respimat®相当的安全性和耐受性。需要进行更大规模的III期研究来证实这些有希望的初步发现。
缩写
- ACQ-7:
-
哮喘控制七题问卷
- AE:
-
不良事件
- AUC(0-3h):
-
给药后3小时内曲线下面积
- 体重指数:
-
体质指数
- FEV1:
-
1秒内用力呼气量
- FVC:
-
用力肺活量
- ICS:
-
吸入糖皮质激素
- 拉巴:
-
长效β2受体激动剂
- PAQLQ (S):
-
标准化儿科哮喘生活质量问卷
- FEV峰值1(0-3h):
-
给药后3小时内1秒内的最大用力呼气量
- PEF:
-
最大呼气流量
- QD:
-
每天换一次
- SD:
-
标准偏差
参考
- 1
Papadopoulos NG,Arakawa H,Carlsen KH,Custovic A,Gern J,Lemanske R等。关于(图标)儿童哮喘的国际共识。过敏。2012;67:976–97。
- 2
2011年全国健康访谈调查(NHIS)数据。2011年终身哮喘、当前哮喘、当前哮喘患者中的哮喘发作[http://www.cdc.gov/asthma/nhis/2011/data.htm.]。
- 3.
欧洲的肺健康:事实和数字[http://www.europeanlung.org/assets/files/en/publications/lung_health_in_europe_facts_and_figures_web_vfour.pdf]。
- 4.
儿童哮喘控制现状:来自儿童哮喘控制特征和患病率调查研究(ACCESS)的结果。J Pediatr。2010;157:276 - 81。
- 5.
Guilbert Tw,Garris C,Jhingran P,Bonafede M,Tomaszewski KJ,Bonus T等人。不受控制的哮喘与增加的医疗保健利用率和生活质量降低有关。j哮喘。2011; 48:126-32。
- 6.
Haselkorn T、Fish JE、Zeiger RS、Szefler SJ、Miller DP、Chips BE等。根据专家组报告3指南中的损害领域定义,持续控制非常差的哮喘增加了哮喘流行病学和自然史中未来严重哮喘恶化的风险:结果和治疗方案(TENOR)研究.过敏临床免疫杂志.2009;124:895–902.e4。
- 7.
Custovic A, Johnston SL, Pavord I, Gaga M, Fabbri L, Bel EH,等。EAACI对哮喘加重和严重哮喘的立场声明。过敏。2013;68:1520-31。
- 8.
哮喘对国家的影响:来自CDC国家哮喘控制项目的数据[http://www.cdc.gov/asthma/impacts_nation/asthmafactsheet.pdf]。
- 9.
哮喘管理和预防全球战略。2014年修订版[http://www.ginasthma.org/local/uploads/files/GINA_Report_2014_Jun11.pdf]。
- 10
儿童和青少年哮喘:诊断和管理的综合方法。过敏免疫杂志。2012;43:98-137。
- 11
Desai M,Oppenheimer JJ.哮喘儿童和青少年的药物依从性.Curr过敏性哮喘报告2011;11:454–64。
- 12
哮喘对儿童和青少年日常生活的全球影响:呼吸室调查。Pediatr Pulmonol。2012;47:346-57。
- 13
哮喘与青少年:改善控制策略的回顾。J Sch Nurs. 2013; 29:39-51。
- 14.
Rhee H,Belyea MJ,Halterman JS。青少年对哮喘症状和医疗保健利用的看法。J Pedias'theach保健。2011; 25:105-13。
- 15.
噻托溴铵(Tiotropium, Spiriva)在阻塞性肺疾病中的机制考虑和临床表现生命科学。1999;64:457 - 64。
- 16.
抗胆碱能药物对methacholine诱导的哮喘支气管收缩的保护作用比较。J哮喘。2008;45:397 - 401。
- 17.
贝特曼ED, Kornmann O, Schmidt P, Pivovarova A, Engel M, Fabbri LM。噻托溴铵在维持B16-Arg/Arg哮喘患者肺功能改善方面不比沙美特罗差。中国临床免疫杂志。2011;128:315-22。
- 18.
Kerstjens HAM, Disse B, Schröder-Babo W, Bantje TA, Gahlemann M, Sigmund R, et al.;噻托溴铵改善严重不可控哮喘患者的肺功能:一项随机对照试验中国免疫学杂志。2011;128:308-14。
- 19.
Peters SP, Kunselman SJ, Icitovic N, Moore WC, Pascual R, Ameredes BT,等。噻托溴铵加强治疗成人哮喘失控。中华医学杂志2010;363:1715-26。
- 20
Kerstjens HAM, Engel M, Dahl R, Paggiaro P, Beck E, Vandewalker M,等。噻托溴铵在标准联合治疗哮喘控制不良中的作用。N Engl J Med. 2012; 367:1198-207。
- 21
Beeh KM、Moroni Zentgraf P、Ablinger O、Hollaenderova Z、Unseld A、Engel M等。噻托溴铵对哮喘的作用:一项针对中度哮喘成年患者的双盲、随机、剂量范围研究。Respir Res.2014;15:61.
- 22
张志刚,张志强,张志强,等。噻托溴铵在吸入糖皮质激素后仍有哮喘症状的青少年中的应用:一项随机剂量范围研究和医学。2014;108:1268 - 76。
- 23
Littner先生,Ilowite JS,Tashkin DP,Friedman M,Serby CW,Menjoge SS等。稳定期慢性阻塞性肺疾病患者的长效支气管扩张,每日一次噻托溴铵(Spiriva)。我是Respir Crit Care医学院的院长。2000;161:1136–42.
- 24
van Noord JA、Smeets JJ、Custers FLJ、Korducki L、Cornelissen PJG。噻托溴铵在慢性阻塞性肺疾病患者中的药效稳定状态。《欧洲反应杂志》,2002年;19:639–44.
- 25
Peak flow monitoring in pediatric asthma management: a clinical practice column submission.高峰流量监测在儿童哮喘管理中的应用儿科杂志。2010;25:12-7。
- 26.
Kerstjens HAM, Bleecker E, Meltzer E, Casale T, Pizzichini E, Schmidt O等。噻托溴铵作为吸入性糖皮质激素治疗对症哮喘患者的附加治疗:肺功能和安全性[摘要4629]。Eur Respir J. 2013;42(增刊57):980 - 1。
- 27.
张志强,张志强,张志强,等。噻托溴铵(tiotropium)作为低剂量吸入性糖皮质激素补充治疗症状性轻度持续性哮喘患者的III期试验:设计和计划分析[摘要P4133]Eur Respir J. 2013;42(增刊57)。
- 28.
杨志强,杨志强,杨志强,等。噻托溴铵在哮喘中的作用:在中度持续性哮喘成人患者中的剂量发现研究[摘要A1283]。《呼吸危重症护理杂志》2013;187。
- 29.
Dalby R, Spallek M, Voshaar T. Respimat®Soft Mist™吸入器的开发综述。国际医药杂志。2004;283:1-9。
确认
这项工作得到了勃林格殷格翰公司的支持。前勃林格殷格翰统计学家李志林起草了统计分析计划,进行了统计分析,并对手稿进行了审查。Marshall Naden代表Complete healthviszion提供了医疗写作协助,该公司由勃林格殷格翰签订合同并予以补偿。
作者信息
隶属关系
通讯作者
额外的信息
相互竞争的利益
CV,ML-K和EH没有申报利益冲突。SS是一位顾问,并为Merck Serono提供了咨询委员会,并为Genentech的稿件开发提供了贡献,已经参加了Boehringer Ingelheim的咨询委员会和会议,是GlaxoSmithkline儿科指导委员会的主席,并获得了授权科罗拉多大学丹佛丹佛医学院为题为“通过改善内城的哮喘关怀推进教育”,为NHLBI护理网络提供了贡献。PM-Z,Rs和Me是Boehringer Ingelheim的员工。
作者的贡献
CV和SS提供了关于研究设计、方案审查、结果讨论、数据审查和手稿开发的输入。RS对统计分析和手稿开发做出了贡献。EH是本次试验研究地点的首席研究员,参与了研究结果的讨论和手稿的编写与讨论。PM-Z和ME致力于研究概念、设计、实施、管理和数据分析。ML-K参与了研究结果、不良事件和不良事件的临床术语的讨论。所有作者阅读并批准了最终的手稿。
这篇文章的勘误表可在http://dx.doi.org/10.1186/s12931-015-0290-7..
额外的文件
附加文件1:图S1
注册、随机化和研究完成。AE,不良事件。
权利和权限
这是一篇基于知识共享署188滚球软件名许可协议(http://creativecommons.org/licenses/by/4.0),允许在任何媒介上不受限制地使用、分发和复制,但须注明原作的出处。创作共用及公共领域专用豁免书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条中提供的数据,除非另有说明。
关于这篇文章
引用这篇文章
沃格尔,C., Moroni-Zentgraf, P., Leonaviciute-Klimantaviciene, M.。等。噻托溴铵(tiotropium Respimat)对吸入性糖皮质激素有症状的哮喘儿童的随机剂量范围研究回应16,20 (2015). https://doi.org/10.1186/s12931-015-0175-9
收到:
接受:
发表:
关键词
- 哮喘
- 哮喘控制
- 孩子们
- 每天换一次
- 泰乌托品
- 肺功能
- 儿科
- Respimat®