文摘
透明质酸(HA)及其降解产物肺部病理生理学和气道重塑中发挥重要作用在慢性阻塞性肺病(COPD)。
我们调查如果HA及其降解酶透明质酸酶(HYAL) 1与慢性阻塞性肺病严重程度和结果。
血清HA是评估中发现的80名慢性阻塞性肺病患者在稳定状态和加剧。哈,HYAL-1和HYAL-1酶活性在稳定状态进行评估,638年急性加重慢性阻塞性肺病患者急性加重和4周后的承诺验证队列。
在发现人群中,血清HA较高较稳定的状态在急性加重(p = 0.015)。在验证队列,HA在中度和重度发作高于基线(p < 0.001), 4周后保持较高(p < 0.001)。HA强烈预测与时间相关的总生存期以来死亡(p < 0.001)的独立调整Charlson得分,一年一度的恶化率和波德(体重、气流阻塞,呼吸困难,运动能力)指数。血清HYAL-1在适度增加(p = 0.004)和严重急性加重(p = 0.003),但4周后下降(p < 0.001)。HYAL-1酶活性与FEV稳定状态呈负相关1% pred (p = 0.034)和生存时间(p = 0.017)。
血清HA与慢性阻塞性肺病严重程度和预测总体存活率有关。公顷退化与气流限制和肺功能的损害。
文摘
血清透明质酸(HA)与慢性阻塞性肺病严重程度有关,结果和预测总体存活率。酶促降解的HA与气流限制和肺功能的损害。http://ow.ly/COl830n2IcQ
介绍
慢性阻塞性肺疾病(COPD)是一个复杂的异构疾病的特点是气流限制的逐步发展,在很大程度上是不可逆转的。慢性阻塞性肺病急性加重可能发生在任何阶段的慢性阻塞性肺病,和与病人的死亡率和发病率1,2]。
慢性阻塞性肺病是气道重构的一个关键特性,描述了细胞外基质(ECM)的严重改变影响气道壁厚,弹性阻力和(3]。ECM由一个动态的组合结构分子胶原蛋白和粘多糖等。透明质酸(HA)是无处不在的,自然产生的粘多糖在哺乳动物中发现高浓度的结缔组织,包括肺(4,5]。HA合成ΗΑ合成酶的作用和它的退化是透明质酸酶(HYALs) [6,7]。有新兴的证据表明,HA及其降解产物在肺部病理生理学发挥重要作用。
HA的生物功能取决于其分子大小。高分子量公顷(> 1000 kDa),这是生理上可用的形式,促进细胞生存,抗炎,抗血管生成和免疫抑制效果。相比之下,低分子量公顷(150 - 350 kDa)过程中产生炎症;它促进细胞迁移,促炎和pro-angiogenic属性(8- - - - - -12]。
研究在动物模型的炎性肺条件和哮喘患者建议的潜在作用高分子量公顷用于治疗呼吸道疾病(13- - - - - -15]。在慢性阻塞性肺病的小鼠模型,aerosolised哈保护内源性哈在肺组织对香烟smoke-generated活性氧,降解,减少空气空间扩大和缓解弹性纤维损伤(13]。
之前我们已经表明,在COPD患者气道平滑肌细胞,HA代谢受损,以降低合成哈,以上的差别与对这些ΗΑsynthase-1和upregulation HYAL-1 [16]。此外,慢性阻塞性肺病急性加重与HYAL活动增加支气管肺泡灌洗和随后的退化的哈,这可能导致气道炎症发作期间和随后的肺功能下降(17]。除了哈,其他ECM的降解产物分子胶原蛋白和弹性蛋白等也与临床相关的有关结果在慢性阻塞性肺病18]。
在目前的研究中,我们分析了血清HA水平和HYAL-1在两个相配的COPD患者群。我们假设,HA与COPD恶化和严重程度,并预测总体存活率在慢性阻塞性肺病。
方法
研究设计和参与者
两阶段研究设计用于减少不必要的浪费患者样本。初步分析了在80年发现的慢性阻塞性肺病患者疾病稳定(n = 65)或在恶化(n = 15)包含在正在研究(COPD)巴塞尔协议研究,横断面观察,monocentric研究(图1)。发现分析仅限于评估血清HA水平和之前进行全面详细的分析验证群组成的638名患者,包括在PROMISE-COPD队列(预测结果使用系统性标记在严重的慢性阻塞性肺疾病急性加重;ISRCTN注册表标识符ISRCTN99586989)(图1)。investigator-driven PROMISE-COPD研究,多中心,纵向试验在11个三级呼吸中心在八个欧洲国家。正在和PROMISE-COPD遵守赫尔辛基宣言和良好的临床实践指南,并被大学的机构审查委员会批准的巴塞尔(EKBB05/06和EKBB295/07)。所有的病患为研究评估提供了事先书面同意。
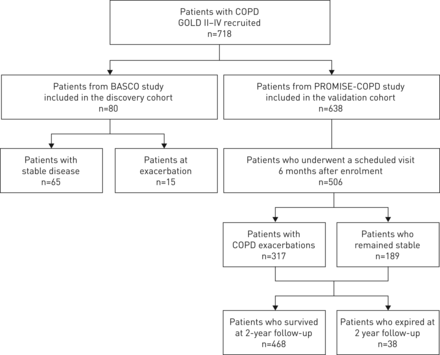
研究设计。慢性阻塞性肺病:慢性阻塞性肺疾病;黄金:慢性阻塞性肺疾病的全球倡议。发现的80名患者从正在的队列研究。验证组的638名患者是由包含在PROMISE-COPD研究。黄金分类II-IV对应于中度到严重的慢性阻塞性肺病。
验证组,我们连续招募了638名病人,在基线,出现临床稳定的,中度到严重的慢性阻塞性肺病(用力呼气量在1 s (FEV1)% pred < 80%, FEV1/用力肺活量(FVC)≤0.7),根据体格检查和肺量测定法,至少4周后最新的恶化是解决19- - - - - -21]。所有患者与吸烟史≥≥40岁10久。排除标准迅速致命的疾病与死亡预期在6个月,除了COPD肺条件为主要呼吸道疾病(如。支气管扩张、哮喘或肺纤维化),免疫抑制包括器官移植或长期使用类固醇(> 20毫克·天−1强的松当量),或肌肉骨骼或神经肌肉过程防止移动。
在基线,痰病人进行临床评估,分析和标准管理一个吸入短效支气管扩张剂后肺量测定法。阻塞的严重程度和条件的病人分级是根据疾病的阶段定义的全球倡议对慢性阻塞性肺疾病(黄金),分为黄金组II-IV。6分钟步行试验的测试,每个病人经历了生活质量并提供信息使用圣乔治呼吸问卷(SGRQ)和短Form-36问卷。此外,修改后的医学研究理事会呼吸困难评分,波德(体重、气流阻塞,呼吸困难,运动能力)指数和年龄调整Charlson得分为每个病人测定。并发症包括相关药物治疗评估基线,恶化和一年两次的访问。Νon-contrast-enhanced多层螺旋计算机断层扫描(CT)图像数据集在150年收购了患者在吸气屏息。从这些数据集,使用开源软件自动提取肺容积是内部开发和基于ImageJ22]。从这些数据,肺容量和之前描述的基于直方图分布密度值包括低衰减面积< -950胡锦涛(%),调整后的肺密度(g·L−1)提取和自动评估量化肺气肿23]。基线的访问后,患者每6个月安排访问,并在恶化和4周后不定期。中位随访24个月。
对病人中发现队列,血清样本,在稳定状态或恶化,收集在支气管镜检查的日子。验证组,血清样本收集在稳定状态,在恶化(中度和重度)和后续(4周后恶化)。
稳定的慢性阻塞性肺病的诊断和加重了根据黄金准则。根据标准的定义,恶化了慢性阻塞性肺病的诊断为急性事件的特点是患者的呼吸道症状恶化超出正常的日常变化和导致药物的变化。一般来说,病人有恶化的一个或多个以下典型症状:咳嗽的频率和严重程度增加,增加吐痰,痰液颜色的变化,和/或增加呼吸困难。慢性阻塞性肺病急性加重被定义为中度(需要抗生素和/或肠外皮质激素)或严重(需要住院治疗或导致死亡)2]。
测量在慢性阻塞性肺病患者的血清HA和HYAL-1
HA整除的测量发现队列的COPD患者血清获得稳定状态恶化,和慢性阻塞性肺病患者的验证队列在稳定状态,在恶化,4周后一个恶化使用HA绑定蛋白质夹心ELISA (Corgenix、威斯敏斯特有限公司、美国)。Intra-assay变异系数:≤7.7%;inter-assay变异系数:≤8.3%。
HYAL-1测量整除的COPD患者的血清获得验证队列在稳定状态,在恶化,4周后一个恶化使用夹心ELISA(武汉EIAab科学,武汉,中国)。Intra-assay变异系数:≤4.3%;inter-assay变异系数:≤7.5%。
血清HYAL活动
HYAL活动以整除的血清(5μL稀释血清1/100)从慢性阻塞性肺病患者获得验证队列在稳定状态的HA衬底zymography 10%聚丙烯酰胺凝胶含有0.17毫克·毫升−1公顷(σ,圣路易斯,密苏里州,美国)。凝胶是用0.1 HCOONa缓冲区,特里同x - 100年0.03 M氯化钠和2.5%,pH值4.0,1 h在室温下,然后孵化0.1甲酸缓冲和0.03 M氯化钠,pH值4.0,20 h在37°C。洗后用20%的乙醇/ 10%醋酸为20分钟,凝胶阿尔新蓝沾0.5% 20% 10%乙醇/乙酸,没有染料脱色和相同的解决方案。HA裂解乐队是量化使用计算机辅助图像分析程序(美国伊士曼柯达公司,罗彻斯特,纽约)。
测定ECM营业额的标志
血清标志物的ECM营业额胶原蛋白降解片段等类型,IV(α1链和α3链)和VI, pro-forms胶原蛋白类型III, V和VI,测量和中性粒细胞弹性蛋白酶与北欧生物科学(Herlev、丹麦)化验,如前所述[18,24]。
统计分析
SPSS为Windows版本23.0(美国SPSS,芝加哥,IL)是用于数据分析。细节描述的补充材料。
结果
病人
基线人口统计学和临床特点的80名慢性阻塞性肺病患者正在研究,发现队列中所示补充表S1。这个群体包括有关吸烟史的患者,严重的阻碍,温和的通货膨胀,损伤肺一氧化碳(扩散能力的DLCO)和严重的肺气肿。所有患者充分的治疗。
招募的638名患者的验证中,共有506名患者参加了在6个月的访问,因此有资格列入后续分析(图1)。基线人口统计学和临床特点的病人中验证队列所示表1。两个组别配合的非常好。大多数患者是男性,有一个相当大的吸烟史、临床相关疾病(至少一个恶化需要医生注意前一年)和多个并存病(补充表S2)。在稳态的访问中,155名患者(30.6%)能够产生痰质量好微生物分析。从这些,48个样品(30.9%)证明潜在的致病细菌的增长。患者随访期间中位数(四分位范围(差))722(395 - 762)天。在随访期间,317名患者(62.6%)患有至少一个恶化和38例(7.5%)死亡。
病人有恶化进行计划外的访问,采样后2天(范围0 - 5天)内的事件:21.8%的患者采样当天,16.1%的患者样本1天事件后,14.0%的患者样本2天事件后,10.1%的患者样本3天事件后,8.3%的患者样本4天后事件和5.7%的患者样本事件后5天。
2年随访期间内的临床结果所示补充表S3。从基线到恶化的平均时间为338天,严重的恶化是701天。
在慢性阻塞性肺病急性加重公顷增加
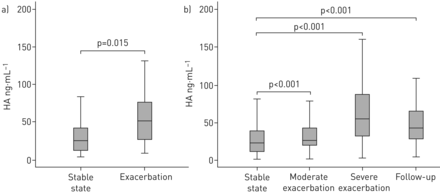
血清HA水平测定慢性阻塞性肺病患者在80年发现的。在这些患者中,65例有稳定的疾病和15例有恶化。血清中HA的浓度明显高于慢性阻塞性肺病患者在稳定状态的恶化与患者相比(p = 0.015) (图2一个)。
血清透明质酸(HA)的慢性阻塞性肺疾病(COPD)患者。血清HA浓度测量通过ELISA)的80名参与者发现队列(65处于稳定状态的患者和15例有慢性阻塞性肺病恶化),和b)的506名参与者验证队列在稳定状态(n = 506),在温和的恶化(n = 219),严重恶化(n = 88), 4周后随访恶化(n = 92)。测量都是在重复执行。
随后,我们评估血清HA含量验证群506名慢性阻塞性肺病患者。HA测量在稳定的状态,在急性加重(中度和重度),在随访(4周后恶化)。HA显著增加在中度和重度发作与比较的稳定状态(p < 0.001) (图2 b)。在随访,血清HA水平仍明显高于与血清水平稳定状态(p < 0.001)。
血清HA水平基线参数的相关分析,炎症和疾病的标记结果
在慢性阻塞性肺病患者的血清HA水平稳定状态与病人的年龄呈正相关(p < 0.001), post-bronchodilation FEV1% pred (p = 0.002), FEV1/ FVC (p = 0.025),年龄调整Charlson得分(p = 0.001)。关于炎症标记物,血清HA水平adrenomedullin有显著相关性(p = 0.001)和心房利钠肽(p < 0.001) (表2)。没有显著相关的血清HA水平与体重指数、吸烟史、Borg呼吸困难量表或步行距离。此外,没有显著相关性的哈DLCO或与任何定量CT扫描参数,表明HA与肺气肿。
此外,HA明显相关(p < 0.001)与时间死亡(HR 1.019, 95% CI 1.009 - -1.029)。Cox回归多元分析显示,这个协会是独立的调整Charlson得分,年度恶化率和波德指数组件(表3)。
随后,在一个探索性的分析中,我们使用线性混合模型来测试各种临床特征之间的关系在基线和血清HA水平稳定状态之间的变化和中度或重度发作。在102年基线预测测试,post-bronchodilation FEV1% pred显著预测为公顷增加(p = 0.0186)中急性加重(补充表S4)。调整后,调整Charlson分数重要预测因子(分别为p = 0.0275, p = 0.0328)为公顷增加严重急性加重(补充表S4)。
在恶化,血清HA水平没有显著相关标记等系统性炎症的白细胞计数、c反应蛋白(补充表S5)。
血清HA水平和痰细菌学
在稳定状态,155名患者可能产生痰液质量好微生物分析,发现潜在的致病细菌增长48例。中值(差)患者血清HA水平类似的积极文化的潜在致病菌在痰(21.3 ng·毫升(13.8 - -39.9)−1)与病人没有增长的潜在致病菌痰(19.0 ng·毫升(6.5 - -35.3)−1)(p = 0.076)。同样,没有明显的差异值(差)血清HA水平恶化之间积极的患者痰培养和消极的患者痰文化在中度急性加重(26.1 (20.8 - -46.3)与34.3 (21.6 - -59.1)ng·毫升−1;p = 0.575)和严重的急性加重(44.5 (28.8 - -83.6)与83.2 (44.3 - -104.2)ng·毫升−1;p = 0.362)。
HYAL-1在COPD患者的血清
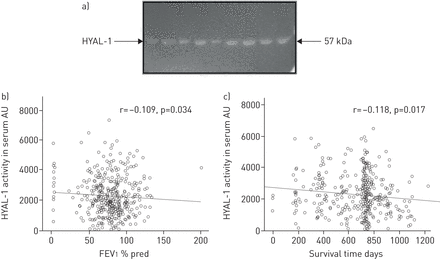
HA的生物效应是由其分子量,我们进一步研究了酶活性和蛋白质含量HYAL-1,这是主要的酶降解哈,血清中。酶活性的COPD患者的血清HYAL稳定状态明显是一个裂解乐队迁移的分子质量57 kDa对应HYAL-1 (图3一)。量化的酶裂解乐队的COPD患者血清验证组(n = 506)透露,HYAL-1酶活性与post-bronchodilation FEV呈负相关1% pred (r =−0.109, p = 0.034)和生存时间(r =−0.118, p = 0.017) (图3 b和c)。没有明显的相关性HYAL-1活动随着年龄的增长,体重指数、吸烟史,FEV1/ FVC, Borg呼吸困难量表或步行距离(补充表S6)。
透明质酸酶(HYAL) 1活动血清样本的慢性阻塞性肺病(COPD)患者。FEV1:在1 s用力呼气量;HA:透明质酸。酶活性的HYAL-1评估血清样本(5μL稀释血清1/100)慢性阻塞性肺病患者的稳定状态(n = 506)由HA衬底zymography验证队列。)代表哈衬底zymography九COPD患者血清样本所得的稳定状态。裂解乐队迁移在57 kDa对应HYAL-1活动。b, c)值之间的相关性(枪兵的ρ)HYAL-1活动稳定状态量化的柯达FEV计算机辅助图像分析程序和b)1% pred和c)的生存时间。
HYAL-1水平在慢性阻塞性肺病患者的血清稳定状态与年龄显著相关,和调整,调整Charlson得分(p < 0.001),与步行距离负相关(p = 0.001)。关于标记的炎症,HYAL-1与原降钙素血清水平显著相关(p = 0.011), adrenomedullin (p < 0.001), copeptin (p = 0.004)和心房利钠肽(p < 0.001) (表4)。没有明显的相关性HYAL-1DLCO或任何定量CT扫描参数,表明HA与肺气肿的酶促降解。
HYAL-1血清水平显著增加,中度急性加重(p = 0.004)和严重急性加重(p = 0.003) (图4)。在随访4周后加重,HYAL-1水平明显降低控制水平对中度和重度急性加重(p < 0.001)。
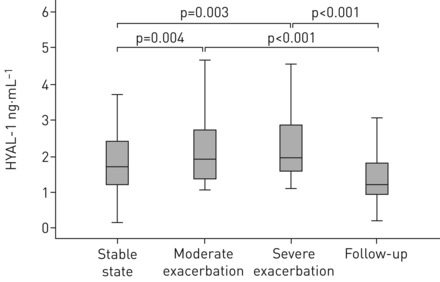
透明质酸酶(HYAL) 1在慢性阻塞性肺疾病患者的血清群的验证。血清浓度HYAL-1 506年由ELISA测定验证组的参与者在稳定状态(n = 506),在温和的恶化(n = 219),严重恶化(n = 88), 4周后随访恶化(n = 92)。测量都是在重复执行。
治疗对血清HA水平和HYAL-1的影响
我们进一步探讨各种治疗是否会改变血清HA水平和HYAL-1慢性阻塞性肺病患者在稳定的状态。所示表5中值(差)ΗΑ血清水平没有差异患者接受治疗吸入糖皮质激素(女性)(21.7 ng·毫升(10.1 - -38.8)−1)和病人不接受女性(22.6 ng·毫升(13.1 - -44.5)−1)(p = 0.437)。此外,中值没有明显差异(差)血清HA水平之间的病人服用,患者没有接受治疗系统性皮质类固醇(20.0 (9.0 - -46.9)与22.3 (10.3 - -38.8)ng·毫升−1;p = 0.846)或与长效β的结合2受体激动剂(腊八粥)和皮质类固醇(21.2 (9.4 - -38.1)与23.3 (13.6 - -44.2)ng·毫升−1;p = 0.093)。同样,长效毒蕈碱的对手并不影响值(差)血清HA水平(21.2 (9.7 - -38.0)与25.2 (12.1 - -41.2)ng·毫升−1;p = 0.324)。
即使我们FEV的调整1% pred,我们不能发现任何血清HA水平显著差异之间的病人接受或不接受任何上述治疗方法。此外,系统性皮质类固醇的使用在中度发作4周后没有明显与HA水平相关的后续分析显示的配对样本(p = 0.458)。
同样,中值(差)HYAL-1血清水平没有差异患者接受治疗女性(1.7 ng·毫升(1.2 - -2.4)−1)和病人没有接受ICS (1.6 ng·毫升(1.1 - -2.4)−1)(p = 0.632) (表5)。此外,没有明显差异(差)HYAL-1血清中值水平之间的病人服用,患者没有接受治疗系统性皮质类固醇(1.7 (1.4 - -2.6)与1.7 (1.2 - -2.4)ng·毫升−1;p = 0.637)或腊八和皮质类固醇(1.7 (1.2 - -2.5)与1.7 (1.1 - -2.4)ng·毫升−1;p = 0.640)。同样,长效毒蕈碱的对手并不影响值(差)HYAL-1血清水平(1.7 (1.2 - -2.4)与1.7 (1.1 - -2.5)ng·毫升−1;p = 0.936)。
即使我们FEV的调整1% pred,我们不能发现任何HYAL-1血清水平的显著差异之间的病人接受或不接受任何上述治疗方法。
HA协会和HYAL-1 ECM营业额的生物标志物
我们进一步研究了HA和HYAL-1分子协会反映ECM营业额,包括胶原蛋白类型的碎片,III, IV和VI, pro-forms胶原蛋白类型III, V和VI,中性粒细胞elastase-generated弹性蛋白片段(表6)。血清HA水平与血清水平显著相关的pro-forms III型胶原和VI型(p < 0.001)。
pro-form HYAL-1水平显著相关的胶原蛋白类型六世,和胶原蛋白的降解片段类型VI (p = 0.012)和α3链的胶原IV型(p = 0.020)。
讨论
在目前的研究中,我们调查了血清HA水平在两个独立的、和谐的群慢性阻塞性肺病患者,我们报告,HA与慢性阻塞性肺病严重程度和结果。我们所知,这是第一个研究表明HA及其降解产物产生的行动HYAL-1可能在慢性阻塞性肺病扮演一个角色,这疾病活动和随后的结果可以通过检测循环设想公顷。当前的分析提供了新的见解慢性阻塞性肺病的病理生理学。
HA ECM的天然组成部分,参与许多生理过程,如细胞迁移和增殖,水体内平衡、组织修复、炎症、cell-matrix信号、和血管生成25]。HA具有特殊的亲水特征,可以绑定∼自身重量1000倍的水。因此,在ECM, HA产生高度粘性凝胶在组织内稳态和生物力学完整性起着关键作用[12]。哈可以绑定到特定的细胞表面受体和诱发细胞内信号转导,还创建了一个矩阵外套细胞和保护他们免受周围环境。
在目前的研究中,我们提供的证据表明,血清HA水平在稳定状态随时间显著相关死亡的独立调整Charlson得分,年恶化率和波德索引组件。它已经表明,血清HA水平升高患者dyslipidaemia和高心血管风险(26]。在我们的研究中,病人中验证群有很多并发症,包括动脉高血压和冠状动脉疾病。然而,HA与时间死亡的协会是独立于年龄调整Charlson得分权证所观察到协会的HA与慢性阻塞性肺病的结果不是一个附带现象,循环HA在COPD患者生存可以作为一个独立的预测因素。
准确预测死亡率是非常重要的识别慢性阻塞性肺病患者的实施将有利于强化治疗措施,如肺移植(27]。几项研究试图找到对慢性阻塞性肺病患者的存活率和探索协会的临床特征与特定的生物标志物的疾病活动和/或进展(28,29日]。描述了几种血清生物标志物是独立与死亡风险增加有关(30.,31日]。一些生物标记已经被证明,进一步导致预测死亡率,当添加到已知的临床评分如预示指数(28,32,33]。由于慢性阻塞性肺病是一个复杂和异构疾病与各种表型,一组预后生物标志物反映相关的并发症和不同pathobiological通路可能改变这种疾病提出了(29日,31日,34]。同时水平升高adrenomedullin、精氨酸加压素和心房利钠肽已被证明与稳定的慢性阻塞性肺病患者死亡的风险增加(34]。在目前的研究中,我们提供的证据表明,HA adrenomedullin和心房利钠肽显著相关,HYAL-1与adrenomedullin, copeptin,原降钙素和心房利钠肽。我们所知,这是第一个研究表明HA的相关性及其降解酶与这些慢性阻塞性肺病预后生物标志物。还有待阐明是否伴随HA和HYAL-1加上完善的死亡率估计预测将有助于增加死亡率的预测的准确性。
我们曾表明,增加公顷退化支气管肺泡灌洗的COPD患者与气道阻塞有关,而不是与肺气肿(17]。缺少一个重要血清HA水平和HYAL-1之间的联系DLCO或定量CT扫描参数代表肺实质的状态,我们观察在目前的研究进一步表明,HA和HYAL-1肺气肿并不相关。它还有待阐明公顷退化与破坏的终端和过渡细支气管,最近已被证明代表初始损伤的慢性阻塞性肺病甚至在疾病的早期阶段(35,36]。然而,这种分析需要一种新型的多分辨率CT成像协议,在目前的研究。
在肺,哈是一个动态的分子与生理功能,其分子量密切相关。有证据表明组织损伤产生的低分子量公顷增加炎症反应,而生理上发生高分子量HA是保护和抗炎作用[10- - - - - -12]。在这里,我们提供证据,第一次HYAL活动在506名慢性阻塞性肺病患者的血清与FEV负相关1% pred和存活时间。这些结果表明,生理上发生的酶促降解高分子量HA在COPD患者与气流限制有关,损伤肺功能和时间。与这些数据协议,之前的研究表明,短片段的HA检测支气管肺泡灌洗液(7,17,37- - - - - -39)和薄壁组织(7]在许多肺部疾病,表明HA营业额是一个主要组件的开发、发展和解决炎症性肺部疾病7,17]。
除了哈,其他ECM的降解产物分子也在慢性阻塞性肺病与临床相关的结果。Pro-forms和片断的胶原蛋白已被证明在慢性阻塞性肺病和疾病严重程度发挥重要作用的结果(18,24]。在目前的研究中,我们表明,血清HA水平显著相关pro-collagen类型III和VI,肺间质中的胶原蛋白主要在大支气管。HYAL-1血清水平与pro-collagen VI型以及IV型胶原的降解产物和VI型胶原主要发现在基底膜。这些结果表明,哈,符合胶原蛋白,是一个ECM营业额增加慢性阻塞性肺病的一部分,这一过程决定了疾病的严重程度和临床相关的结果。
慢性阻塞性肺病急性加重的是自然历史的重要事件影响疾病进展的疾病,健康状况和生存。因此,有一个未满足的需要了解的病理生理机制在慢性阻塞性肺病加重病人的识别分子与气流限制在加重。在目前的研究中,我们提供的证据表明,血清HA水平显著增加,中度和重度慢性阻塞性肺病加重病人的疾病的稳定状态。HA水平恶化并没有相关的细菌感染或急性炎症的标志白细胞计数、c反应蛋白等。与此同时,HYAL-1血清水平也在恶化,增加表明慢性阻塞性肺病急性加重与增加公顷退化形成的短片段。在过去的二十年广泛的研究已经表明,信号通过短哈碎片导致免疫细胞在炎症的积累网站(40- - - - - -42),以及随后释放促炎细胞因子和metalloelastases [43,44]。
我们研究的另一个有趣的发现是急性加重,4周后,血清HA水平仍明显高于与稳定状态相比,尽管HYAL-1水平下降到稳态水平。因此,它很容易设定的终止的作用HYAL-1之前的短片段的HA循环。
我们的研究有一些局限性。测量血清HA浓度大小的ELISA不能提供信息哈。不幸的是,到目前为止,没有适当的方法估计的规模这么大的粘多糖在血清样本。HYAL-1因此,平行测量,这是主要的HYAL在人类血清检测,提供最好的指示HA的大小。我们研究的另一个限制是,血清HA水平可以通过治疗被修改,因为它已被证明,ΗΑ营业额由糖皮质激素改变,腊八[45- - - - - -47),而大多数的慢性阻塞性肺病患者参与了本研究在治疗女性(81%的患者)或ICS +腊八组合(61.3%的患者)。然而,当我们分层分析HA和HYAL-1治疗,即使接受治疗的组织和团体没有接受治疗的不平衡对数量的病人,我们不能观察之间的任何显著差异公顷或HYAL-1水平组接受女性,全身皮质类固醇或ICS +腊八组,没有接受任何治疗。
我们的研究的主要力量是大样本大小和全面的临床患者的描述,使我们与死亡时间建立,HA的协会是独立于调整Charlson得分,年恶化率和波德索引组件。进一步的强度与两阶段设计有两个相配的人群。发现群旨在最大化机会建立HA作为一个潜在的分子与疾病严重程度和结果,并减少不必要的浪费患者样本。额外的优势是纵向采样进行三个时间点(在稳定状态,恶化和后续)和纵向临床数据使我们能够确定疾病的结果。
总之,我们的研究结果表明,HA与慢性阻塞性肺病严重程度和结果,并预测整体的生存。在慢性阻塞性肺病急性加重,HA与气流限制有关的酶促降解和肺功能的损害。因此,HA及其降解酶HYAL-1可能被证明作为潜在的目标控制在COPD气道炎症和重塑。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充方法:统计分析。erj - 01183 - 2018 - _methodology
补充表S1。基线人口统计学和临床特点的80名慢性阻塞性肺病患者中发现队列(正在研究)。erj - 01183 - 2018 - _table_s1
补充表S2。并存病的506例患者中验证队列。erj - 01183 - 2018 - _table_s2
补充表S3。临床结果在2年随访期内的COPD患者验证队列。erj - 01183 - 2018 - _table_s3
补充表S4。协会的各种预测与HA基线稳定状态之间的变化和中度或重度发作。erj - 01183 - 2018 - _table_s4
补充表S5。相关分析(枪兵的ρ)血清中透明质酸的中度和重度COPD患者急性加重炎症生物标记。erj - 01183 - 2018 - _table_s5
补充表S6。相关分析(枪兵的ρ)慢性阻塞性肺病患者的血清中透明质酸酶的活性(n = 506)。erj - 01183 - 2018 - _table_s6
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:大肠Papakonstantinou没有披露。
利益冲突:即Bonovolias没有披露。
利益冲突:m·罗斯没有披露。
利益冲突:m.t amm没有披露。
利益冲突:d·舒曼没有披露。
利益冲突:f . Baty没有披露。
利益冲突:r·路易没有披露。
利益冲突:b Milenkovic没有披露。
利益冲突:w . Boersma没有披露。
利益冲突:斯蒂尔吉斯没有披露。
利益冲突:k Kostikas没有披露。
利益冲突:f·布拉西没有披露。
利益冲突:J.G. Aerts没有披露。
利益冲突:G.G.U.罗德没有披露。
利益冲突:a . Lacoma没有披露。
利益冲突:a .托雷斯没有披露。
利益冲突:t Welte没有披露。
利益冲突:d Stolz没有披露。
支持声明:本研究由瑞士Nationalfonds苏珥Forderung der Wissenschaftlichen大幅减退(PP00-P3_128412/1),瑞士Lungenliga(2015 - 18)和巴塞尔大学2182 (DMS)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年6月24日。
- 接受2018年12月10日。
- 版权©2019人队