摘要
虽然型1,2和3型先天淋巴细胞(分别是ILC1,ILC2S和ILC3S)作为调节组织稳态,重塑和炎症的重要细胞群体,但我们的绝大多数知识源于体外和小鼠实验,并需要彻底确认人类疾病。
通过流式细胞仪在慢性鼻窦炎患者的流式细胞术中通过流式细胞术评估ILCs的相对水平,没有鼻息肉(CRSSNP)和鼻息肉(CRSWNP),考虑到患者的临床参数和疾病的合并症。
我们报道了人类ILC2s的CD117和IL-1RI的表达状态取决于局部组织环境。只有CD117+IL-1RI+ILC2s,只存在于CRSwNP,具有与人类上呼吸道粘膜的2型T辅助细胞细胞因子和嗜酸性粒细胞水平的相互关系。在CRSSNP,主要是CD117-IL-1RI-尽管高水平的ILC 2 S增加,ILC2S增加,屈服于这种疾病的嗜酸性粒细胞粒细胞菌。
这些数据揭示了CD117-和CD117+与我们可以从中得出的结论相反,在本地人类ILC2种群中的分数并不是一个随机现象体外IL-1RI的表达在ilc2中并不普遍在活的有机体内在人类中,这无法评估通过体外和小鼠实验。
摘要
人ILC2S中的CD117表达取决于局部组织Milieu,IL-1RI表达在ILC2S中不受欢迎http://wly/iea230mckz5
介绍
慢性鼻窦炎(CRS)是一组影响鼻腔和副鼻窦黏膜的异质性慢性气道炎症性疾病,或伴有鼻息肉形成(CRSwNP),或表现为无息肉(CRSsNP) [1].CRS在成人中显示出高达15%的高达15%,往往导致随后的呼吸道条件的开发,特别是哮喘[2].CRSsNP和CRSwNP是不同的疾病实体,CRSwNP与息肉中高白介素(IL)-5和嗜酸性粒细胞阳离子蛋白(ECP)浓度的T-helper type 2 (Th2)倾斜的嗜酸性粒细胞炎症相关,而CRSsNP的特征是在发炎的筛部粘膜中具有明显的干扰素(IFN)-γ水平的更主要的Th1环境[1].此外,新的证据表明CRSwNP亚组中存在相当大的异质性,这决定了共病哮喘的风险。尽管研究不断取得进展,有助于进一步揭示这些慢性气道疾病的病理生理学,但其病因仍然知之甚少,而且似乎是多因素的。
近年来,一类依赖于IL-2受体共同γ链和IL-7Rα (CD127)信号通路的先天性效应细胞引起了广泛关注。这些细胞被称为辅助先天淋巴样细胞(ILCs) [3.- - - - - -5].与T-和B细胞相反,该ILC谱系不能表达重组,抗原特异性受体,并且基本上在阻挡表面处表示。基于谱系定义转录因子的表达和对TH细胞的功能相似性,可以区分三个辅助ILC的子集,以三个全局ILC组排列。
第1组ILC除了IFN-γ分泌辅助ILC亚群(称为ilc1)外,还包括细胞毒性传统自然杀伤细胞和上皮内1型先天淋巴样细胞。IL-12、IL-15和IL-18激活ilc1产生IFN-γ。它们已被证明与抵御病毒、细菌和原生动物有关。据报道ilc1主要存在于慢性炎症的粘膜组织中,在正常生理条件下不存在[6].第2组ILCS目前仅由ILC2组成,该ILC2分泌典型的TH2细胞相关细胞因子IL-4,IL-5,IL-9和IL-13。它们生产amphiregulin,表皮生长因子家族的成员参与限制和修复组织损伤。在早期免疫反应期间涉及ILC2S对Helminth感染的影响,但对过敏原诱导的气道炎症和组织修复也很重要。ILC2S可以通过各种细胞因子激活,例如IL-33,IL-25,胸腺基质淋巴泛菌素(TSLP)和IL-1β,以及脂质介质,如果索糖蛋白,包括前列腺素D2和白酮二烯D4 [7].第3组ILCs由淋巴组织诱导剂(LTi)细胞、自然细胞毒性受体(NCR)细胞组成。+ILC3S和NCR.-ILC3S。ncr.+和NCR.-ILC 3分别分别产生IL-22和IL-17,并被视为粘膜阻隔函数的防护障碍,其涉及免疫细胞外细菌和自身免疫疾病。在IL-1β和IL-23激活后,两种细胞群体都会产生细胞因子[4,5].LTI细胞在胎儿发育过程中形成淋巴结[8].
在其初次表征后,据报道,ILC2S在CRSWNP患者的上气道粘膜中大量存在[9[Sinonasal组织变得流行,将机械发现转化为ILC的研究。然而,这些研究的大多数翻译部分是对报告没有或有限的临床数据的患者的少数患者进行,因此没有考虑合并症的潜在效果[9- - - - - -11].此外,CRSsNP患者上气道粘膜中其他ILC亚群的存在较少受到关注。
在本报告中,我们发现在非炎症条件下,ILCs是鼻窦组织中最突出的ILCs。在CRSwNP中,ILC1s减少,ILC2s减少本身有没有增加。专注于CD117.+和il-1ri+ILC2S中的馏分,并考虑到合并症,我们揭示了ILC2S在CRSWNP中的确切贡献;我们描述了CD117的明确增加+IL-1RI+CRSwNP中ILC2s水平与Th2细胞因子和嗜酸性粒细胞水平相关。在CRSSNP,主要是CD117-IL-1RI-尽管总ILC2S含量高,但含有ilc2s的增加,屈服于这种疾病的嗜酸性粒细胞症。
方法
流式细胞仪染色
组织本地劳工公约门控为生活,lymphogate CD45+血统负(CD3──CD11C.──CD14.──CD19──CD34──BDCA2──FcεR1──CD94──CD1A.──CD123──TCRαβ.──)细胞。ILC1进一步表型为CD127+Crth2.──CD117──NKp44──,ilc2作为cd127+Crth2.+和ilc3作为cd127+Crth2.──CD117+IL-1RI+NKp44──对于NCR.──分数和CD127+Crth2.──CD117+IL-1RI+NKp44+对于NCR.+基于先前报告的门控策略[12]根据所示的门控策略补充图E1.不同ILC亚群的水平表示为总活细胞的百分比。进一步的方法细节描述于补充材料.
体外新鲜孤立的ILC2s评估功能响应
将单个细胞重悬于含IL-2 (5 ng·mL)的组织培养基中−1).用50ng·mL激活细胞−1PMA(Sigma,St Louis,Mo,USA)和1μg·ml−1在5%二氧化碳存在下在37℃下在37℃下进行离子霉素(Sigma)。PMA /离子霉素处理开始后1小时,Brefeldina(5μg·ml−1) (eBioscience, Waltham, MA, USA)。用流式细胞术对样本进行染色,如前面和中所述补充材料.
组织匀浆
用于ILC流式细胞术的同一受试者的冷冻组织样本通过机械破坏的方法均质补充材料.
炎症介质的测量
通过使用氟因素地图多重人细胞因子试剂盒(R&D Systems,Minneapolis,Mn,USA)在Bio中通过Luminex XMAP技术测量炎症介质IL-4,IL-5,IL-12和IL-25测量组织匀浆。-pllextm 200阵列读者(Bio-rad,Hercules,CA,USA)。使用Unicap(Phadia,乌普萨拉,瑞典)测量组织ECP水平
统计分析
通过非参数曼诺惠特尼U-Test进行统计分析。P值<0.05被认为是统计上显着的(GraphPad,San Diego,CA,USA)。
结果
对照组,CRSSNP和CRSWNP人的上气道粘膜中ILCs的相对水平
因为CD45的水平+CRSSNP和CRSWNP中细胞比对照细胞更高(补充图E2A.),虽然不同主题群之间的总脱敏细胞数量相似(补充图E2B.),流式细胞术数据表示为总活细胞的百分比。为了允许读者将不同ILC组的水平与ILCS表示为CD45的百分比的百分比+单元格,在本节中,结果以两种方式呈现[9- - - - - -11].
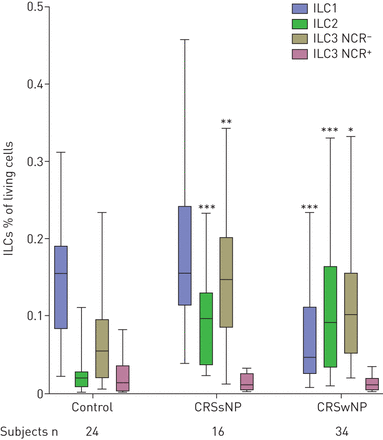
所有三个ILC组的成员都存在于所有患者群体的人上气道粘膜中。在非对控制条件下,ILC1S表示最突出的子集,其次是NCR-ILC3s, ILC2s和NCR+ILC3s丰度最弱(图1和补充图E3)。在CRSsNP患者组,在ILC2和NCR一个显著上升-观察ILC3群体与对照组粘膜的比较,而ILC1和NCR的水平+ILC3细胞相似(图1和补充图E3)。CRSwNP患者的炎症黏膜中ilc1的水平显著低于非炎症对照组,而ILC2和NCR水平显著低于非炎症对照组-ILC3种群数量显著增加。NCR+ILC3细胞的丰度维持在较低水平,与对照粘膜相似(图1和补充图E3)。
对照组、无鼻息肉(CRSsNP)的慢性鼻窦炎患者和有鼻息肉(CRSwNP)的患者中三种固有淋巴样细胞(ILC)组分的相对数量。值以总活细胞中ILCs的百分比表示,并用盒须图表示最小值和最大值、上、下四分位数和中位数。NCR:天然细胞毒性受体。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制。
ILCS在对照的上呼吸道粘膜,CRSSNP和CRSPNP:合并症的效果
由于常见的CRS共病过敏和哮喘可能会影响黏膜中ILC亚群的水平,我们也考虑了这些共病。
在对照组和CRSsNP患者组中,过敏、哮喘和过敏性哮喘的存在对任何ILC子集的数量没有影响(图2- - - - - -4).
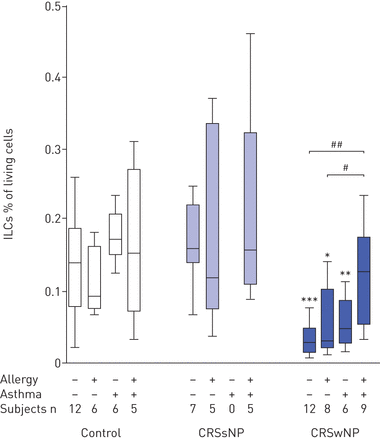
对照、无鼻息肉的慢性鼻窦炎(CRSsNP)和有鼻息肉(CRSwNP)的患者中1型先天淋巴样细胞(ilc1)的相对数量。数据以ilc1在总活细胞中的百分比表示,并用盒须图表示最小值和最大值、上、下四分位数和中位数。−:缺席;+:礼物。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制;#: p < 0.05;##: p < 0.01相对指定的主题组。
未分化CRSwNP患者组中ILC1细胞水平显著降低(图1)可以归因于在CRSwNP患者ILC1s的数量减少而不合并症和从共患过敏或哮喘的共病的那些苦难(图2.).然而,重要的是,CRSwNP伴发变态反应性哮喘患者的ILC1水平与同等对照的变态反应性哮喘但没有慢性上呼吸道粘膜炎症的患者相比没有降低(图2.).
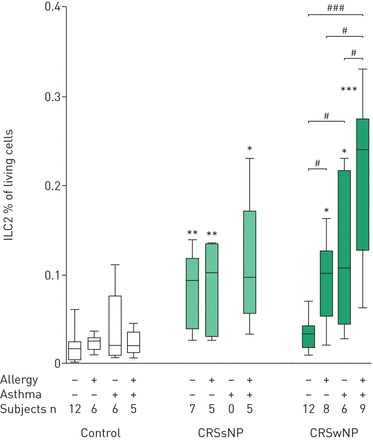
出乎意料的是,ILC2s的水平也在Th1型细胞因子偏斜疾病CRSsNP显著更高相比于相应的对照患者群体。此外,不同的合并症对ILC2细胞的水平没有影响(图3.).ILC2s不参与CRSwNP的病理生理学,因为没有共病的CRSwNP患者的炎症粘膜中含有的ILC2s与对照组的非炎症粘膜相似(图3.).患有可混合过敏和哮喘的患者的ILC2水平显然有变化,过敏性哮喘是最明显的(图3.).
对照组2型先天淋巴细胞(ILC2S)的相对数量,慢性鼻窦炎的患者没有鼻息肉(CRSSNP)和鼻息肉(CRSWNP)分离在合并症状态。数据呈现为总活细胞的ILC2百分比,并且呈现为显示最小值和最大值,下距离和中值的箱子和晶须图。−:缺席;+:礼物。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制;#: p < 0.05;# # #: p < 0.001相对指定的主题组。
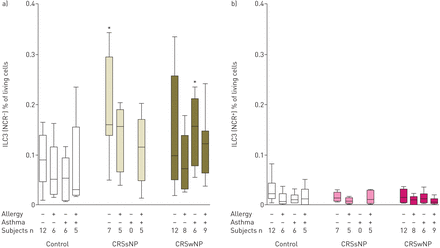
而NCR.-与对照组相比,未分化CRSsNP和CRSwNP患者组中ILC3水平轻微但显著升高(图1),当将共病考虑在内时,可以观察到的变量结果仅在无共病的CRSsNP患者和CRSwNP伴发哮喘患者中产生统计学显著升高(图4A).NCR的水平+ILC3在所有患者群体中总体仍然很低,没有机理没有影响力(图4B.).
a)自然细胞毒性受体 - 阴性的相对数量(NCR-(b) - 呈阳性(NCR+)3种先天淋巴细胞(ILC3S)的对照,慢性鼻窦炎的患者没有鼻息肉(CRSSNP)和鼻息肉(CRSWNP)分离在合并症状态。数据作为总活细胞的百分比ILC3呈,并作为框和晶须图显示,显示最小值和最大值,下部和上四分位数和中位数。−:缺席;+:礼物。*:P <0.05相对控制。
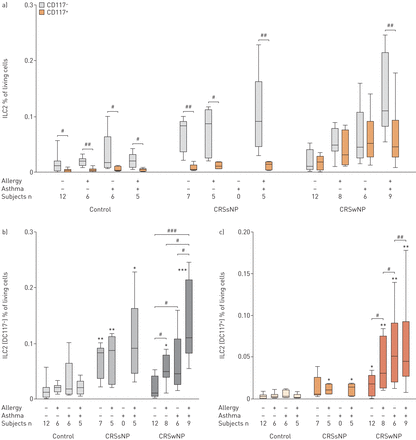
在ILC2人口CD117和IL-1RI的表达
接下来,我们评估了ILC2人群中cd117阳性和阴性部分的相对水平[3.,5,9],并结合文献对比研究IL-1RI在ILC2细胞上的表达[5,10,13- - - - - -15].
无论是否存在过敏、哮喘或过敏性哮喘,在对照组和CRSsNP患者组中,大多数ILC2细胞为CD117-,在统计学上显著高于CD117+细胞;后者实际上缺席(图5A).与此相反,在CRSwNP的红肿粘膜无合并症的CD117+ILC2部分升高,CD117部分升高-分数保持在对照中发现的水平,产生两个缺乏统计差异的分数(图5A).CD117的水平+和CD117-在CRSwNP ILC2馏分合并症变态反应和哮喘(的影响下进一步增加图5B.c),除了CRSPNP患者的粘膜外,在两种分数中保持相似数量的细胞,其具有明显较高的CD117数量-ILC2与CD117相比+细胞(图5A).
相对数量的a)和b)cd117-2型先天淋巴样细胞(ILC2s)和a)和c) CD117+ILC2S在对照中,慢性鼻窦炎的患者没有鼻息肉(CRSSNP)和鼻息肉(CRSWNP)分离在合并症状态。值表示为总活细胞的ILC2百分比,并且呈现为显示最小值和最大值,下或上四分位数和中值的箱子和晶须图。−:缺席;+:礼物。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制;#: p < 0.05;##: p < 0.01;# # #: p < 0.001相对指定的主题组。
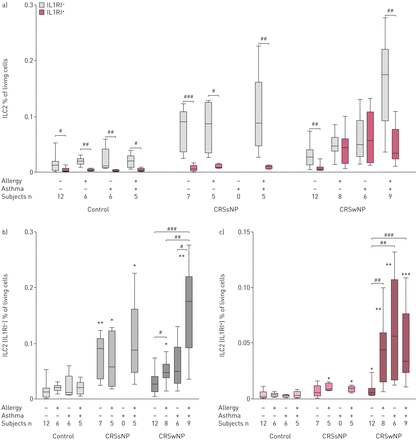
类似于CD117观察到的,在对照受试者和CRSSNP患者组中,大多数ILC2细胞属于IL-1RI-分数。这部分始终显著高于IL-1RI+馏分,几乎没有(图6A).的IL-1RI-ILC2级分不受同伴的过敏和/或哮喘的影响(图6B.).对于CRSwNP,IL-1RI的数目+患有合并过敏和/或哮喘(哮喘)的细胞显然更高图6C.),结束了与IL-1RI的相似水平+和il1r.-ILC2S在CRSWNP患者过敏或哮喘(图6A).值得注意的是,过敏和哮喘对IL-1RI水平的影响+ILC2s在过敏性哮喘患者中没有添加,其水平与过敏性CRSwNP和哮喘CRSwNP患者相似(图6C.),而IL-1RI的水平-ILC2在患有可嗜血症的患者中增加,在过敏性哮喘中最明显(图6B.).无论是IL-1RI-也不是IL-1RI+由于CRSWNP的病理过程而没有组合的病理方法,显然地增加了ILC2细胞(图6B.和c)。
a)和b)白细胞介素受体类型I(IL-1RI)-2型先天淋巴细胞(ILC2S)和A)和C)IL-1RI+ILC2S在对照中,慢性鼻窦炎的患者没有鼻息肉(CRSSNP)和鼻息肉(CRSWNP)分离在合并症状态。数据呈现为总活细胞的ILC2百分比,并且呈现为显示最小值和最大值,下距离和中值的箱子和晶须图。−:缺席;+:礼物。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制;#: p < 0.05;##: p < 0.01;# # #: p < 0.001相对指定的主题组。
该选通步骤评估CD117和IL1RI对ILC2细胞群在控制表达的代表性图中,CRSsNP和CRSwNP从共患过敏性哮喘所有的痛苦示于补充图E4.CD117+和CD117-ILC2部分含有IL-1RI+和il-1ri-亚群(补充图E5)。
体外新鲜孤立的ILC2s评估功能响应
细节提供补充材料.
组织细胞因子水平
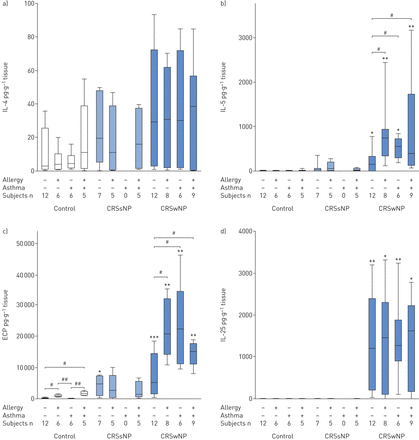
与对照组相比,CRSsNP和CRSwNP中IL-4水平略高,未达到统计学意义(图7A).在CRSwNP患者组中,每种共病状态的IL-4水平相似(图7A),因此与CRSwNP中ilc2的数量没有并行性(图3,5和6).
量化的组织)白介素(IL) 4, b) IL-5, c)嗜酸性粒细胞阳离子蛋白(ECP)和d) IL-25蛋白质含量通过Luminex多路复用(a, b, d)或UniCAP (c)在控制,慢性鼻窦炎鼻息肉患者(CRSsNP)和鼻息肉(CRSwNP)分离的疾病状态。数据以盒须图的形式表示,图中显示了最小值和最大值、上、下四分位数和中位数。−:缺席;+:礼物。*: p < 0.05;* *: p < 0.01;***:P <0.001相对控制;#: p < 0.05;##: p < 0.01;相对指定的主题组。
在所有CRSWNP合并症亚组中,IL-5水平显着增加相对相应的控制主题组。在CRSWNP患者中,具有合并过敏,哮喘和过敏性哮喘的受试者显着高于没有这些合并症的患者的IL-5水平显着较高。CRSSNP患者没有显着差异(图7B.).
所有CRSwNP共病亚组的组织ECP水平均显著高于相应的对照组。在CRSwNP患者中,共病的过敏、哮喘和过敏性哮喘受试者的ECP水平显著高于无这些共病的患者。在CRSsNP中观察到的水平也增加相对对照组,但仅对无共病的患者组有显著意义(图7C.).
IL-25仅在CRSwNP中可测量,在每种共病状态中均产生相似水平(图7D.).所有样品IL-12均低于检测限(数据未显示)。
讨论
从目前的三个ILC组观察到,ILC1在非炎症组织中最丰富,这与文献中ILC1细胞只在炎症条件下存在的教条相矛盾[6].胃肠组织可能是真的[16,17[这似乎不可转让给气道粘膜。此外,相反似乎是真的,因为发炎的CRSWNP粘膜显示出比对照粘膜的较低水平的ILC1。由于CRSWNP特别称为Th2细胞因子偏置的嗜酸性嗜氨基脲炎症条件,息肉中具有高IL-5和ECP浓度[1],减少ILC1水平似乎是与此一致。然而,虽然未分化CRSwNP组在此Th2细胞因子签名可以进一步通过伴随增加ILC2水平,不同的合并症的基础上区分CRSwNP患者组证实表明ILC2人口不CRSwNP的病理生理学牵连本身.实际上,如果没有合并过敏和/或哮喘的CRSWNP患者粘膜中ILC2S的水平不太高于对照。然而,在患有合并过敏和/或哮喘的CRSPNP患者的发炎粘膜中,ILC2水平增加。从这些结果来看,我们推测以前的研究,其中作者对发炎的鼻息肉中的ILC2S相反的作者[9- - - - - -11],主要包括CRSWNP患者患有合并过敏和/或哮喘,但这些临床数据没有传达。我们的结果强调了详细报告和分析患者临床数据的重要性,以便做出正确的解释。
与CRSWNP相比,CRSSNP的特征在于,在发炎的符号粘膜中具有主要的TH1 Milieu,具有发炎的符号粘膜中的IFN-γ水平,组织学显示发炎组织的纤维化状态[1随着转化生长因子(TGF)-β水平的增加,TGF -β是参与这一重构过程的关键因子[18].尽管有这种Th1特征,我们在这里表明,CRSsNP患者的粘膜中ilc1的水平与对照组相似。值得注意的是,CRSsNP患者的黏膜中ILC2s水平明显升高,但与CRSwNP相比,不同的共病在其中没有作用。最近,Forkel等.[19]报告了ILC2S在人肝纤维化中的作用,其证实了涉及ILC2在小鼠肝中纤维化发育中的ILC2的方法[20.].ILC2S的这些功能特征可以与发炎的CRSSNP组织的纤维化状态一致,为CRSSNP中的ILC2S水平增加提供了可能的功能解释。实际上,据报道,TGF-β是纤维化产生的重要调解蛋白,增强了ILC2S的迁移[21,支持Th1疾病(如CRSsNP)中ILC2s的增加。此外,有报道称TGF-β可直接抑制il -33诱导的ILC2s中IL-5和IL-13的产生[22,23].
问题出现了为什么ILC2S在CRSWNP中没有导致展示OEDEMATOUS状态的纤维化。我们提出CRSSNP中的ILC2S不具有与CRSWNP组织中存在的组织居住表型特性相同。的确,虽然CD117-ILC2可在对照组、CRSsNP和CRSwNP患者组中发现,我们的数据显示CD117+ILC2人群实际上没有在对照和CRSNP中缺席,而它明确存在于CRSPNP患者的发炎粘膜中。因此,CD117的增加程度+ILC2S可以归因于CRSWNP病理学,并与过敏或哮喘结合产生最明显的扩张。关于CRSWNP中的ILC2S的功能影响,CD117(也称为C-KIT)是干细胞因子的受体,最适用于其在血液生成干细胞增殖,存活和粘附中的基本作用[24].此外,在小鼠c-kit信号减弱的情况下,ILC2s未能发育[25].与小鼠相比,据报道,据报道成熟的ILC2是专门的CD117+[4,在人类中都是CD117+和CD117-观察到ILC2种群[4,5,使得功能解释变得不那么简单。l我是等.[26]在PMA /离子霉素刺激培养的血液衍生CD117后观察到IL-13生产中没有不同的水平-和CD117+ILC2S的级分,但作者还报道了CD117的表达受培养条件的影响,其中CD117-细胞获得CD117和反之亦然.我们的研究结果表明,原生的表型离体在没有积极刺激的情况下3小时培养后,ILC2已经改变;ILC2s从CRSsNP(天然缺乏CD117表达)制定CD117衍生+分数类似于CRSwNP本身观察到的,而CD117+CRSwNP组织中的ILC2s在PMA/离子霉素刺激下下调表面CD117和CRTH2的表达。这些结果表明,ILC2s的表面表达状态依赖于不同病理固有的特定局部组织条件,并不能准确评估不同病理中ILCs的特征体外方法采用培养细胞和人工刺激方法。此外,L我等.[27在鼠ILC2上表明ILC2S比以前认为的那么多样化,由此经常用于鉴定ILC2S的各种标记的表面表达水平取决于它们的活化模式,随着时间的推移和不同的变化和不同的组织隔室不同。此外,在仔细检查来自b的数据时AL.等.[10],经血源性ILC2培养获得的ILC2群体完全为CD117+.此外,这些CD117+ILC2s以前由同一个研究小组认为是不太敏感相比,CD117-ILC2s [9].然而,当通过IL-25补充其实验中的培养基时,通过两种细胞群产生相等的IL-13 [9].因为我们的数据表明,IL-25的水平完全在大量患者CRSwNP的黏膜增加,可以认为CRSwNP的组织特异性环境也产生功能性活性CD117+ILC2s。
CRSwNP中ILC2s和CRSsNP粘膜中ILC2s的第二个重要表型区别是IL-1RI (il -1 β的活性受体)的表达状态。而CRSsNP和对照组织缺乏表达活性IL-1β受体IL-1RI的ILC2s+在CRSwNP中ILC2s明显存在,在共病的过敏或哮喘患者中ILC2s尤其高。ILC2s最初被认为明确表达IL-1RI [3.,5,但在一篇评估人类CD127异质性的文章中+通过单细胞RNA测序的方法,BJörklund.等.[13]在非炎症扁桃体组织的ILC2s中未见IL-1RI表达。我们报道,在人类上呼吸道粘膜中,ILC2s中IL-1RI的表达水平依赖于不同病理或正常气道粘膜生理所固有的特定局部组织条件。事实上,在对照组和CRSsNP中,几乎所有的ILC2s都缺乏IL-1RI的表达,无论是否存在任何共病。在CRSwNP患者组中,IL-1RI表达明显高于共病的过敏和/或哮喘患者。因为来自外周血的ILC2细胞已经有大量IL-1R1的表面表达[15[我们的数据(通过缺乏IL-1RI表达在B的扁桃体扁桃体组织中缺乏缺乏IL-1RI表达式。Jörklund.等.[13])使我们可以假设,在正常生理和CRSsNP条件下,局部组织水平的ILC2s中IL-1RI表达下调,可能是由于缺乏维持IL-1RI表达的特定触发器,或者是由于存在下调IL-1RI表达的触发器。另外,对照组和CRsNP的局部粘膜组织环境可能只吸引IL-1RI-来自血液的ILC2S,而CRSWNP中的组织炎症环境使得IL-1RI的趋化性+子集。无论哪种理由可能有效,祛斑病症实验都表明,驻留在非含量组织中的ILCS主要通过自我更新,从血液发生前体的最小贡献,并没有系统地重新分配[28,进一步证实了局部组织环境能够将不同的ILC亚群调整为最终表型。究竟是什么触发了IL-1RI在CRSwNP中明确的表达,而不是在CRSsNP中,仍有待进一步研究。在功能上,IL-1β与IL-1RI的结合可以通过诱导低表达的转录因子T-BET和细胞因子受体链IL-12Rβ2直接影响人的ILC2s,这随后允许IL-12诱导这些活化的ILC2s转化为ILC1表型[10,15].由于我们在任何疾病状态下无法检测到这种组织中可测量的IL-12水平,因此这种功能可塑性在人的上呼吸道粘膜中的重要性变得不确定。据报道,IL-1β显着增强IL-25,IL-33和TSLP对ILC 2细胞的受体的表达,并使它们对这些细胞因子的反应提高。IL-1β-处理的ILC2细胞响应于IL-33和IL-25而不是未接受IL-1β的IL-25产生显着更高的TH2细胞因子[10,15].CRSsNP中ILC2s上缺乏IL-1RI表达,CRSwNP中ILC2s上存在IL-1RI表达,这与相应疾病状态中IL-5产生的缺失和存在是一致的。
在我们研究中将ILC2S的水平与TH2调解员的水平进行比较时,显然CD117的数量没有关系-IL-1RI-ILC2s及IL-5和ECP在不同疾病状态和共病中的浓度变化相反,CD117+IL-1RI+ILC2S是最有可能导致CRSWNP中TH2环境的成形的最有可能的,从观察结果结束,即该ILC2子集明显遵循IL-5水平的模式和通过ECP评估的嗜酸性粒细胞的数量浓度。后一种数据证实了先前的研究,在CRSPNP患者中显示出嗜酸性粒细胞和ILC2水平之间的相互关系[29].我们的数据显示,这可能主要是由于CD117+IL-1RI+与CRSwNP相比,尽管ILC2总体水平增加,但CRSsNP中的嗜酸性粒细胞水平较低,ILC2s主要是CD117-IL-1RI-在crssnp。
结论
我们已经证明在人上气道粘膜中存在三种ILC亚群。在非炎症条件下,ilc1是最显著的亚群。在CRSwNP中,ilc1减少而ilc2不增加。但是,聚焦于CD117+和il-1ri+考虑到共病,我们揭示了ILC2s在CRSwNP中的精确作用。我们只描述CD117+IL-1RI+ILC2s(仅存在于CRSwNP中)与人上气道粘膜Th2细胞因子和嗜酸性粒细胞水平存在相互关系。事实上,在CRSsNP中,主要是CD117-IL-1RI-尽管高水平的ILC 2 S增加,ILC2S增加,屈服于这种疾病的嗜酸性粒细胞粒细胞菌。此外,这些数据首次推出了CD117-和CD117.+在人类ILC2人群中,IL-1RI的表达并非普遍存在。两者都受特定炎症条件下的局部组织条件的影响。特定的ILC2表达状态可以进一步塑造组织特异性环境,这可能与CD117和IL-1RI表达对ILC2释放炎症介质的功能影响有关。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充方法和结果。ERJ-00742-2018_SUPPOREMENT.
图E1。门控策略;组织本地ILC被门控,淋巴结CD45+血统负(CD3-CD11C.-CD14.-CD19-CD34-BDCA2-FcεR1-CD94-CD1A.-CD123-TCRαδ-)细胞。ILC1进一步表型为CD127+Crth2.-CD117-NKp44-,ilc2作为cd127+Crth2.+, ILC3为CD127+Crth2.-CD117+IL-1RI+NKp44-对于NCR.-分数和CD127+Crth2.-CD117+IL-1RI+NKp44+对于NCR.+分数。Crth2(灰色覆盖层)的荧光减去一种(FMO)在鉴定ILC2群体的直方图中表明。CD117和IL1RI的FMO数据作为灰点图,旁边的点图旁边,评估ILC2群体中CD117和IL1RI表达的水平和识别ILC1,NCR的点绘图-ILC3和NCR.+ILC3人群都伴随着对CD117和的NKp44 FMO数据。erj - 00742 - 2018 - _fig_e1
图E2。CD45的相对数+在对照中,CRSSNP和CRSWNP主体组表示为总活细胞(a)的百分比,并且活细胞的相对数量为所有事件(b)的百分比。数据显示为框和晶须图,显示最小值和最大值,下部和上四分位数,中位数。***:P <0.001;ns:不重要。erj - 00742 - 2018 - _fig_e2
图E3。相对数在对照中,CRSsNP和CRSwNP 3个ILC馏分。值表示为CD45%的国际劳工公约+细胞,并呈现为盒须图,显示的最小和最大值,下和上四分位数和中位数。Δ:与对照;ΔΔ:P <0.01;ΔΔΔ:P <0.001。erj - 00742 - 2018 - _fig_e3
图E4。浇注步骤的代表性点曲线图评估CD117和IL1RI对ILC2细胞群的表达(上面板),CRSSNP(中间板)和CRSWNP(下图)中的ILC2细胞群。在这些实施例中,所有患有过敏性哮喘的个体。如图所示,CD117和IL1RI用于CD117和IL1ri的荧光减去一种(FMO)作为右侧的小点图中的灰色覆盖。erj - 00742 - 2018 - _fig_e4
图E5。ILC2s亚群CD117的相对数量-IL-1RI-,CD117-IL-1RI+,CD117+IL-1RI-,CD117+IL-1RI+对照组中,CRSsNP和CRSwNP受试者按共病状态进行分离,如下图所示。值以总活细胞的ILC2亚群%表示,并以盒状和须状图表示最小值和最大值、上、下四分位数和中位数。erj - 00742 - 2018 - _fig_e5
图E6。图中显示了国际法委员会水平的个别数据点图1主要文件中的7个主要文件和晶须图。erj - 00742 - 2018 - _fig_e6
脚注
本文提供了补充材料www.qdcxjkg.com.
利益冲突:无声明。
支持声明:本研究得到了根特大学专项研究基金(01G01317)和科学研究基金(FWO) (G.0444.17N)的资助。S. Taveirne由FWO (12N4515N)支持。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2018年4月19日。
- 接受2018年10月3日。
- 版权所有©ers 2018