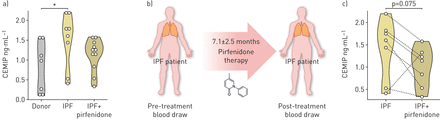文摘
尽管pirfenidone有益治疗特发性肺纤维化(IPF),目前还不清楚如果肺成纤维细胞(神奇动物)是主要的治疗目标。
为了解决这个问题,我们采用一个比较转录组的方法和分析肺匀浆(LH)和FB来自有或没有pirfenidone IPF患者。
在facebook, pirfenidone疗法主要影响生长和细胞分裂途径,表明主要细胞代谢转变。LH样本,pirfenidone治疗主要是与炎症相关的流程。在facebook和LH,调节基因在基因本体节点中被“细胞外基质”。我们确定了低表达的细胞migration-inducing hyaluronan-binding蛋白质(CEMIP) LH和FB pirfenidone-treated IPF患者。等离子体CEMIP水平升高在IPF患者与健康对照组和减少pirfenidone 7个月后治疗。CEMIP表达式在FB glioma-associated致癌基因homologue-dependent的方式表达下调和CEMIP沉默IPF FB减少胶原蛋白生产和减毒细胞增殖和迁移。
总体来讲,我们的方法表明,pirfenidone施加有益的影响通过其作用在多个通路在facebook和其他肺细胞,通过其控制细胞外基质的能力架构和炎症反应。
文摘
Pirfenidone在人体肺部的作用方式是一个复杂的interactome包括炎症相关的基因和细胞外基质的结构http://ow.ly/26NN30lpGON
介绍
特发性肺纤维化(IPF)是一种破坏性疾病的平均生存< 5年以下诊断和死亡率超过许多类型的癌症。IPF诊断导致高发病率的生活质量较差的负担。尽管最近批准的医疗治疗,肺移植仍然是唯一明确的治疗选择1]。
IPF的基本病理机制的特点是肺泡上皮细胞的损伤和激活,肌成纤维细胞增殖和特异表达的转录和翻译后控制细胞外基质(ECM)成分,如胶原蛋白和透明质酸(HA)、肺。结果,让人想起过度疤痕形成,发生变化与不可逆损伤肺架构,导致通风,干扰灌注和气体交换,最终死于心肺衰竭(2]。
尽管抑制性影响肺成纤维细胞(神奇动物)增殖和胶原蛋白生产、几个治疗策略IPF患者未能显示出积极的效果;这些包括interferon-γ[3),酪氨酸激酶抑制剂伊马替尼(4)和选择性内皮素受体拮抗剂应用波生坦(5]和ambrisentan [6]。因此,一个强大的或有条件的负面的建议已被归因于这些治疗的概念在当前国际IPF(临床实践指南7]。目前,只有两种药物治疗IPF的批准,pirfenidone和nintedanib7]。Pirfenidone (5-methyl-1-phenyl-2 (1 h) -pyridinone)是一种口服可用合成药物,在2011年批准在欧洲和在2014年在美国治疗轻度至中度的IPF。迄今为止,四个随机安慰剂对照第三阶段研究已经证明,pirfenidone显著减缓疾病进展通过减少下降用力肺活量(FVC) (8- - - - - -11]。结合能力1和2的数据以及提升试验显示显着的效益对无进展生存,6分钟步行试验和呼吸困难评分(8,9]。此外,从四个三期试验的数据汇总分析表明降低全因死亡率在pirfenidone治疗(12]。pirfenidone治疗IPF的真实世界的观察性研究,pirfenidone FVC下降是一致的影响临床试验的结果(13]。
尽管最近的研究结果表明,pirfenidone施加对许多细胞类型(多效性的影响14,15],pirfenidone放缓IPF进展的机制并不清楚。这里,通过一个复杂的无偏转录组方法采用1)肺组织从pirfenidone-treated pirfenidone-naive IPF患者,2)孤立FB来自同一患者和3)培养FB IPF患者在体外pirfenidone,我们发现pirfenidone施加的大部分对肺的影响通过调节基因的表达参与炎症和ECM架构。
方法
的描述中提供了方法补充材料;在这里,只有IPF患者信息。
人类的肺
人类肺样本来自IPF患者接受部门的肺移植手术,胸外科,医科大学的维也纳,奥地利的维也纳。协议和组织使用被批准的机构伦理委员会(976/2010),肺移植前病人同意了。微观部分准备和苏木精和伊红染色评估纤维化肺的形态。
结果
研究人群
肺移植来自14个IPF患者临床特征明显被用于这项研究。IPF患者的人口学特征和临床数据实验和验证组,包括pirfenidone (Esbriet®/ Pirfenex)药物治疗,报告表1。这些参数没有显示治疗和摘要团体之间的显著差异。所有肺具有古典特色的实质与通常的间质性肺炎的典型模式改造(补充图S1)。
pirfenidone对表达谱在肺匀浆和孤立的成纤维细胞
确定pirfenidone治疗分子特征的影响原位1)上,我们进行了基因表达分析肺匀浆(LH)样品和2)孤立的人类肺FB pirfenidone-treated (P)或pirfenidone-naive IPF患者。LH样本是异构的组织样本,可以用来识别单个基因,有强烈的平均治疗引起基因表达的变化,指出过程由pirfenidone直接或间接改变了。相比之下,分析孤立FB pirfenidone治疗的细胞类型特异的反应可以确定。实验设计提出了图1一个。
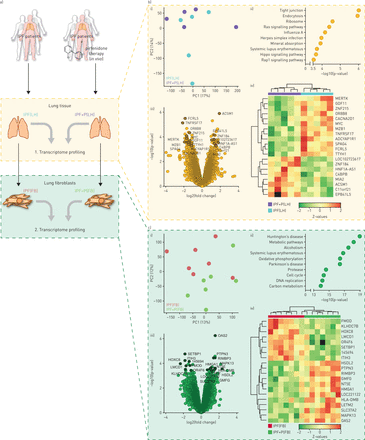
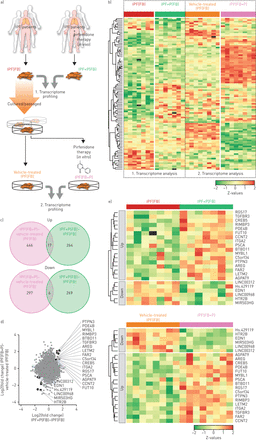
转录组分析的人类肺匀浆(LH)和人类肺成纤维细胞(神奇动物)源自特发性肺纤维化(IPF) pirfenidone患者(P)。实验设计的原理概述。IPF LH的b)转录组分析。b我)主成分(PC)分析显示pirfenidone-treated之间的分离和pirfenidone-naive IPF LH样本。b, ii)京都基因和基因组的百科全书(KEGG)的基因功能分析显示影响最大的十大通路在IPF LH pirfenidone治疗后。b, iii)火山情节的全球分销log2(褶皱变化表达式)和假定值。标签显示最高的20个基因的意义。b, iv)热量地图之间的集群处理和摘要样本排名前20位的调节基因在b,三世。c)转录组分析IPF的神奇动物。c i)电脑分析情节显示清晰分离pirfenidone-treated和pirfenidone-naive IPF FB。c, ii) KEGG分析显示十最重要的摄动通路在IPF FB pirfenidone治疗。 c, iii) Volcano plot indicating the global distribution of log2 (fold change in expression) and p-value. The labelling shows the 20 genes with the highest significance. c, iv) Heat map representing expression at single-patient level for the top 20 genes as in c, iii.
整个基因表达谱的比较,主成分分析(PCA)只显示小LH pirfenidone-treated样本之间的全球变化(IPF + P (LH))和pirfenidone-naive (IPF (LH))患者(图1 b,我),全球基因测试使用基因和基因组的京都百科全书(KEGG)显示几个显著摄动通路(图1 bii)。这些包括炎症过程和信息联系的变化(如。紧密连接,内吞作用)。所有基因的全球分布根据各自的日志褶皱变化(利物浦),假定值描述在火山的阴谋图1 b第三,图1 b第四,显示了排名前20位的调节基因的表达水平在同一病人的水平。
表达谱的FB隔绝pirfenidone-treated (IPF + P(神奇动物))和pirfenidone-naive (IPF(神奇动物))患者不同,给好的分离PCA (图1 c,我)。最显著改变通路在FB表明细胞拥有一般代谢改变有关生长和细胞分裂(如。DNA复制、细胞周期)和改性蛋白质周转(如。蛋白酶体)(图1 cii)。根据假定值排名前20名监管基因在火山情节突出显示图1 c第三,single-patient-level表达式所示图1 c第四。
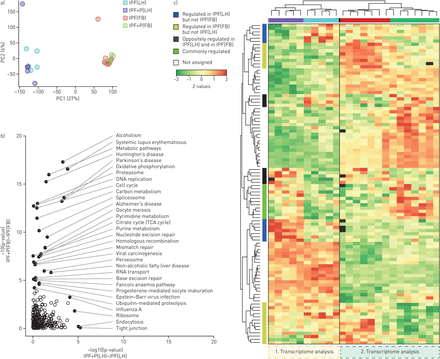
比较LH (IPF (LH), IPF + P (LH))和facebook (IPF(神奇动物),IPF + P (FB))利用主成分分析法(PCA)样品给一个清晰的分离,主要LH和FB(之间的歧视图2一个)。全球基因测试显示更多的显著摄动pirfenidone-induced通路在FB LH (图2 b)。这是预期的,因为资料获得LH代表许多细胞类型的反应,细胞类型特异的微扰,这样定义的路径更加难以确定。分析最大的100个基因差异显示清晰的分离的LH和FB表达谱在层次聚类分析(欧氏距离和完整的链接;图2 c)。基因聚类显示几组数据源特定的基因调控与pirfenidone治疗(监管在FB LH但不是集群(蓝色),监管在FB而不是LH集群(黄色),相对监管LH和FB(灰色集群),同时监管LH和FB集群(绿色))(图2 c和补充表S1)。
比较转录组概要文件在人类肺匀浆(LH)和人类肺成纤维细胞(神奇动物)源自特发性肺纤维化(IPF) pirfenidone患者(P)。a)主成分分析(PC) LH和肺FB pirfenidone-treated和pirfenidone-naive IPF患者。b)京都百科全书的基因和基因组途径分析比较之间的通路富集FB和LH样本。c)热图基因表达显著变化的颜色分组(左边)的前100 FB和韩之间的差异调节基因。
Pirfenidone诱发不同的基因调控在LH和孤立的神奇动物
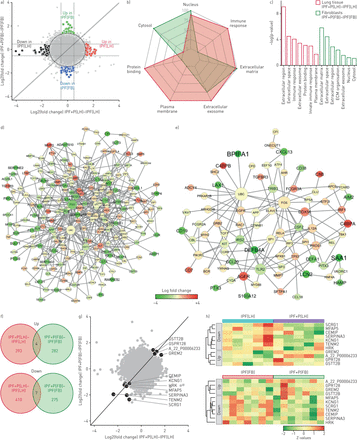
了解转录曲目被专门监管回应pirfenidone在隔间里,我们选择基因只在一组规范,LH或facebook。为此,阈值设置为利物浦>定义调节基因和< | | 1.41 | 0.5 |定义不规范基因(彩色点图3一并列为“只有在LH /只在facebook”补充表S1)。这种方式我们专注于基因诱导由至少两个变化或压抑的至少50%。代表分析这些选择性地调节基因与基因本体论(去)节点显示在FB,所选择的基因包含在“细胞外基质”,“胞质”和“核”节点。LH,所选择的基因中来自“细胞外基质”和“免疫反应”节点(图3 bc)。由于他们强劲丰富我们的分析,我们首先探讨了ECM内分子相互作用和炎症反应节点。交互网络与并行表现注释的基因调控LH和FB LH和FB(再次强调差异图3 d、e和补充图S2)。我们还探讨了代表炎症和ECM KEGG通路和colour-mapped pirfenidone治疗后表现的变化(B - t细胞受体信号和ECM-receptor交互;补充图S3)。
之间的差异和一般监管基因肺匀浆(LH)和肺成纤维细胞(神奇动物)源自特发性肺纤维化(IPF) pirfenidone患者(P)。a)散点图呈现对数的值2(褶皱变化表达式)的每个基因IPF (LH)样品(轴)与IPF (FB)样品(轴)。彩色圆点代表不同的基因被pirfenidone监管只在一个组。基因被认为是专门监管在facebook或LH当他们的观点在虚线圈外的散点图(1.41)半径和仍在±0.5的组(分别由水平和垂直的虚线表示)。b)蜘蛛(雷达)图显示核心基因本体论(去)节点被管制在IPF (LH)(红色)和/或在IPF(神奇动物)(绿色),和c)显示最高的7个单节点为每个组显著。d, e)表示的最低核心蛋白质相互作用网络分析由NetworkAnalyst显示在最丰富的节点,细胞外基质(ECM) (d,表达式显示为神奇动物)和免疫细胞反应(e,表达对LH)。f)维恩图代表普遍增加,表达下调基因之间LH和FB pirfenidone-naive患者相比pirfenidone-treated病人(IPF + P)。g)散点图呈现log2(褶皱变化表达式)的值为每个基因调控在pirfenidone治疗IPF (LH)样品(轴)与IPF (FB)样品(轴)。标记点代表收敛的基因。h)热图代表个体病人的变化通常调控基因。
此外,五个最表达下调基因LH指向dysbalanced免疫系统:defensinβ4 (DEFB4A6)趋化因子配体(CXCL6)、血清淀粉样蛋白A2 (SAA2)、血清淀粉样蛋白A1 (SAA1)和BPI折叠包含家庭成员1 (BPIFA1)(补充表S2)。在facebook, pirfenidone表达下调的基因参与转录:同源框C9 (HOXC8);细胞信号:硫酸酯酶2 (SULF2);和成骨分化:刺激软骨形成1 (SCRG1)(补充表S3)。
收敛调节基因在LH和孤立FB由于pirfenidone治疗
申请的截止利物浦> | 1 |,我们发现803个不同调节基因(393和410年)在LH (补充表S2)和557年(282年和275年下降)在FB pirfenidone治疗后相比,相应的控件(补充表S3)。有11个注释基因与监管的方向相同(4和7)在两个比较组(图3 fg)。这些基因的个体病人的变化所示图3 h。这些11通常的功能责任人予以规范给出了带注释的基因补充表S4。
细胞migration-inducing HA-binding pirfenidone蛋白质作为目标
细胞migration-inducing hyaluronan-binding蛋白质(CEMIP)强烈表达下调pirfenidone治疗我们的方法(图3 g、h)和曾牵涉到一些流程相关肺纤维化,即ECM生产、炎症和细胞增殖(补充表S4)[16]。因此,我们更详细地探讨CEMIP的作用。减少CEMIP mRNA表达在IPF + P (LH)和IPF + P(神奇动物)观察到的微阵列实验证实使用验证队列(图4一c)。此外,IPF + P (LH)和IPF + P(神奇动物)表现出降低CEMIP蛋白表达与LH和FB pirfenidone-naive IPF患者(图4 bd)。重要的是,CEMIP mRNA和蛋白水平升高在IPF (LH)和IPF(神奇动物)相比,捐赠样本(图4一- d)。通过免疫组织化学方法证实这些结果显示,增加染色强度的肺部CEMIP pirfenidone-naive IPF患者相比捐赠者和pirfenidone-treated患者(图4 ef)。CEMIP肺泡II型细胞和免疫反应性主要是观察到(myo)成纤维细胞(被prosurfactant蛋白C的表达和α-smooth肌肉肌动蛋白(α-SMA),分别)在捐赠者和IPF肺。CEMIP阳性染色也观察到内皮细胞(如确定表达式的血管性血友病因子)在供体肺(图4 f)。这些发现表明facebook不是独家生产商CEMIP人类肺部。
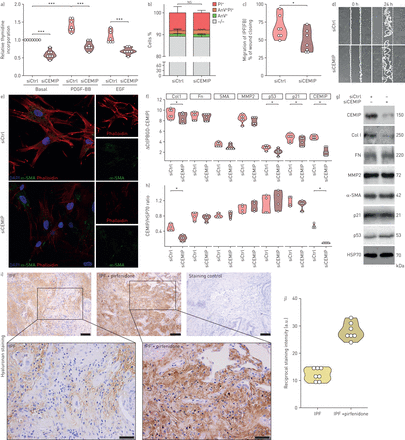
在肺纤维化在pirfenidone CEMIP监管(P)治疗。一)CEMIP mRNA表达肺匀浆(LH)一个独立的验证组(n = 20捐赠;n = 18对特发性肺纤维化(IPF);IPF + P n = 7)。b) CEMIP蛋白质含量的LH捐助者和pirfenidone-naive pirfenidone-treated IPF患者(n = 8捐赠;IPF n = 9;IPF + P n = 7)。c) CEMIP mRNA表达肺成纤维细胞(神奇动物)与供体肺隔离和pirfenidone-naive pirfenidone-treated IPF患者一个独立的验证组(n = 11捐赠;IPF n = 5;IPF + P n = 7)。 d) CEMIP protein levels in FB isolated from lungs of donors and pirfenidone-naïve and pirfenidone-treated IPF patients (n=8 for donor; n=8 for IPF; n=7 for IPF+P). mRNA levels were assessed by quantitative PCR, proteins levels by Western blotting.PBGD被用作参考基因定量PCR和HSP70免疫印迹的加载控制。生物复制。为统计分析、单因子变异数分析与图基使用了多个对比测试。* * * p < 0.05, p < 0.01。* * * p < 0.001。e)概述图像CEMIP免疫反应性肺的捐助者和pirfenidone-naive pirfenidone-treated IPF患者。同形像控制抗体被用来确认染色的特异性;酒吧= 200µm规模。CEMIP f)高放大图像,prosurfactant蛋白C (proSP-C)α-smooth肌肉肌动蛋白(α-SMA)、CD45和血管性血友病因子(vWF)疣状串行的部分肺从捐赠者和pirfenidone-naive pirfenidone-treated IPF患者;酒吧= 50µm规模。
分析循环CEMIP显示严重超标IPF样品相比年龄,sex-matched健康对照组(图5一个和表2)。因为pirfenidone减少CEMIP表达式在数组分析中,我们分析了循环CEMIP IPF患者pirfenidone之前和期间的治疗水平。这些患者的平均治疗期为7.1±2.5个月(图5 b)。的六个病人,pirfenidone治疗与CEMIP水平显著降低(图5 c)。
CEMIP健康对照组的血浆水平和pirfenidone-naive pirfenidone-treated特发性肺纤维化(IPF)的病人。)CEMIP等离子体水平的健康对照组和pirfenidone-naive pirfenidone-treated IPF患者。克鲁斯卡尔-沃利斯检验邓恩的多重比较测试;* p < 0.05。b)示意图IPF患者的随访pirfenidone之前和期间的待遇。c) CEMIP等离子体水平基线和pirfenidone 7.1±2.5个月后治疗。Wilcoxon配对测试。
CEMIP参与入侵IPF FB的属性
我们最近证明pirfenidone抑制了刺猬(Hh)信号通路通过瞄准GLI蛋白(14]。启动子的分析CEMIP基因显示GLI共识序列的存在GAACACCCA−820个基点的位置(补充图4)。符合这个观察、凹陷、受体激动剂合成Hh通路,诱导CEMIP捐赠人FB的蛋白表达。这种效应被pirfenidone GLI1/2抑制剂JQ1和有效。重要的是,没有观察到当pirfenidone JQ1添加剂的抑制作用是同时使用(补充图4 b),这表明pirfenidone本身块SAG-triggered CEMIP表达式通过干扰GLI转录因子。
接下来,我们调查的功能相关性CEMIP在IPF(神奇动物)通过损耗实验。击倒CEMIP减少扩散基底条件下以及与血小板源生长刺激后factor-BB或表皮生长因子(图6),但是并不影响细胞凋亡(图6 b)。此外,沉默CEMIP抑制迁移和增加伤口的时候关闭(图6 cd)。此外,击倒受损应力纤维的形成图6 e)和减少胶原蛋白的表达我但不影响纤连蛋白的表达,矩阵metalloprotease-2或α-SMA (图6 f- h)。p21 mRNA的表达衰老标记和p53表达下调后CEMIP损耗;然而,蛋白质含量没有明显变化(图6 f- h)。鉴于CEMIP有牵连的分解代谢哈,我们检查了pirfenidone治疗是否会影响HA在IPF患者的肺部的沉积。中所描绘的一样图6我j,更加突出积累观察HA在pirfenidone-treated pirfenidone-naive IPF患者。此外,我们的微阵列分析表明pirfenidone不同监管HA-mediated运动性受体(HMMR)和HA和蛋白聚糖连接蛋白4 (HAPLN4) IPF (LH)和IPF(神奇动物)。此外,pirfenidone显著影响的表达HA合酶1 (HAS1)和HA-binding蛋白2 (HABP2)特别是在IPF (LH),尽管有改变的表达inter-α-trypsin抑制剂重链3 (ITIH3) HA-binding蛋白质必不可少的ECM稳定,CD44分子只在IPF(神奇动物)(补充表S5和S6)。
击倒的CEMIP特发性肺纤维化(IPF)肺成纤维细胞(神奇动物)。一)扩散IPF (FB)处理CEMIP核(siCEMIP)或新控制核(siCtrl)基础条件和刺激血小板源生长因子(PDGF-BB)或表皮生长因子(EGF)。b)细胞凋亡的IPF(神奇动物)衡量AnnexinV-FITC (AnV)和propidium碘(π)染色。至少5000个细胞测量。c, d)量化(c)和代表图片(d)的IPF(神奇动物)迁移siCEMIP或siCtrl治疗24小时后。e)α-smooth肌肉肌动蛋白(α-SMA)(绿色)和phalloidin(红色)荧光染色的IPF siCEMIP或siCtrl治疗后(神奇动物)。在a e结合数据与n = 4生物复制的两个独立的实验。f) mRNA和g)蛋白水平的标记细胞外基质(ECM)生产/营业额(胶原蛋白我(Col1),纤连蛋白(FN)、矩阵metalloprotease-2 (MMP2)), FB分化(α-SMA)和FB衰老(p53、p21)。mRNA水平评估定量聚合酶链反应(n = 6)和蛋白质水平的免疫印迹(n = 4)。PBGD被用作参考基因定量PCR和HSP70免疫印迹的加载控制。h)的g。量化统计分析Mann-Whitney测试使用。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。i, j) Affinity-histochemical染色(i)和量化(j)透明质酸在IPF pirfenidone-naive和pirfenidone-treated病人的肺。上面板比例尺= 100µm插图/低面板栏= 50µm规模。部分与透明质酸酶预处理是用作染色控制。
转录组分析人类的肺成纤维细胞(神奇动物)处理pirfenidone (P)在体外。实验设计的原理概述。FB用于第一个转录组分析(原位)使用后立即隔离(通道)。在在体外设置,使用FB之间通过三至五(第二转录组分析)。b)热图表示基因表达之间的显著变化原位(特发性肺纤维化(IPF) + P(神奇动物)在体外(IPF (FB + P)对FB。c)维恩图显示的数量普遍起来,表达下调基因之间IPF + P (FB)和IPF (FB + P)。d)散点图呈现log2(褶皱变化表达式)的值为每个基因在IPF + P(神奇动物)样品(轴)与的在体外对待FB (IPF (FB + P))(轴)。标记点代表基因与绝对log2褶皱变化> 1的实验方法(原位和在体外)。e)热图代表个体病人的变化通常调控基因。
pirfenidone的影响在体外
在最后一组实验中,我们扩展我们的转录组分析在IPF(神奇动物)特异表达的基因,在文化的几个段落,然后pirfenidone处理在体外。这是1)背后的基本原理有一个互补的在体外实验设置pirfenidone行动和2)挑出的特定的信号机制pirfenidone在FB的影响全球应对pirfenidone当神奇动物在自然微环境。为此,我们之间进行了比较研究1)FB隔绝pirfenidone-treated (IPF + P (FB))与pirfenidone-naive (IPF(神奇动物))患者和2)肺FB隔绝IPF患者,培养和暴露于pirfenidone在体外(IPF (FB + P) (图7)。应用利物浦> | 1 |,我们发现总共有743个基因的监管在体外pirfenidone-treated FB (补充表S7)。层次聚类的前100名显示完全分离的调节基因转录从facebook档案,同时治疗在活的有机体内以及在体外(图7 b)。值得注意的是,我们发现基因表达FB之间的差异很大在活的有机体内和在体外设置,突显出的影响在体外培养在facebook上。然而,比较pirfenidone-regulated基因IPF (FB + P)和IPF + P(神奇动物)显示23相同的基因表达模式(17和6;图7 c,d和补充表S8)。中表达下调基因内皮素1 (EDN1)和5 -羟色胺受体2 b (HTR2B),这都是G protein-coupled受体信号转导途径的一部分。调节基因注释下面的生物过程:将增长factor-β(TGF-β)受体信号通路、转录的RNA聚合酶II启动子和细胞脂质代谢过程。的热图图7 e代表一般的个体病人的变化调节基因在两个设置。
讨论
pirfenidone治疗的临床成功IPF归因于其多向性的方式行动。众多在体外和在活的有机体内研究已经证明,pirfenidone展品anti-fibrotic、抗炎和抗氧化作用[15];然而,目前尚不清楚哪一个在人类出现在治疗剂量取得了良好的效果。
在目前的研究中,我们进行了基因表达分析分析识别pirfenidone行动的模式。分析了在多个层面上使用LH FB来自分离的样本和新鲜IPF患者或没有pirfenidone处理。这原位方法是通过我们进一步证实在体外研究中,成纤维细胞与IPF患者暴露于pirfenidone在细胞培养。Pirfenidone治疗与重大变化在LH的炎症过程,和联系人,在FB最显著的摄动通路相关代谢重编程,生长和细胞分裂。基因调控的主要属于ECM标本。
ECM分子之间的相互作用和炎症细胞/介质确保一个适当的反应肺的侮辱,和他们的失调会导致一个异常反应和损坏,最后,纤维化。这些ECM-producing FB之间的相互关系,不同的亚种肺纤维化的炎症细胞被大量研究支持。例如,发现了HA的降解产物刺激b细胞产生各种pro-fibrogenic细胞因子,包括FB如TGF-β1强有力的催化剂,白介素6 (IL)和IL - 417]。有趣的是,B -异常和t细胞聚集IPF所示肺和各种免疫球蛋白自身抗体在IPF等离子体(已报告2,18- - - - - -20.]。
ECM之间的密切相互作用和免疫反应是由我们的数据,证明中显著表达下调的基因通过pirfenidone LH是那些参与天然免疫与适应性免疫调节,包括CXCL617(和肿瘤坏死因子受体超家族成员TNFRSF17)。引人注目的是,TNFRSF17控制b细胞的发展已经证明,从而自身免疫反应(21]。在肺FB, pirfenidone疗法主要是抑制SULF2的表达,一种酶参与翻译修饰ECM组件(22]。增加ECM硫酸乙酰肝素蛋白聚糖的硫酸盐化作用已经被描述在IPF患者的肺,建议改变纤维的结构和生长因子结合能力矩阵(23]。
肺FB和LH源自pirfenidone-treated患者,其中最调节基因是小鬼2 (GREM2),而最明显的表达下调的基因CEMIP。小鬼在纤维发生的作用仍存在争议,研究证明其赞成和anti-fibrotic活动(24,25]。Anti-fibrotic小精灵与它相关联的属性能力移植纤维母细胞生长因子10 (FGF10),从而促进受伤的肺泡上皮的修复(26,27]。的贡献CEMIP IPF的发病机理尚未承认到目前为止;因此,我们的研究是第一个显示其强大的pro-fibrotic行动。
CEMIP参与分解代谢的细胞外环境影响HA (28],它不仅改变了力量,润滑和水化ECM但也调节附着力,各种细胞的迁移、增殖和分化(29日]。我们发现明显增加CEMIP mRNA和蛋白表达在LH和FB的IPF患者相比捐助者。最重要的是,CEMIP表达被抑制pirfenidone治疗主要和验证我们IPF患者群。此外,pirfenidone治疗导致大幅减少CEMIP IPF患者的血浆水平高CEMIP等离子体水平基线。这些发现强烈建议进一步调查和建议CEMIP可以作为预测生物标志物识别IPF深刻改变ECM架构和炎症患者最有可能对这种治疗反应积极。
虽然在活的有机体内研究需要划定的贡献CEMIP肺纤维化的发展,我们的研究结果表明,CEMIP损耗抑制IPF肺FB的扩散以响应不同pro-fibrotic刺激,影响这些细胞的迁移,降低胶原蛋白我生产。此外,CEMIP表达下降可能稳定公顷纤维,建议从我们的染色过程。哈哈可以不同促进或抑制纤维化根据其碳水化合物链的长度。bleomycin-treated小鼠的肺,低分子量哈施加有效的促炎效应加剧炎症反应,因此导致肺纤维化的进展(30.,31日]。相比之下,高分子量哈,主要是由HAS1和HAS2,再生组织修复的关键。在皮肤上,一个IL-10-triggered HAS1和HAS2表达和降低透明质酸酶(HYAL) 1, HYAL2和CEMIP表达减少疤痕形成不同的伤口模型(32]。在肺,损耗HAS2肺泡II型细胞(ATIIC)会损害ATIIC的更新能力和加剧肺纤维化在博来霉素滴剂(33]。因此,我们的数据支持一个重要的角色一个适当的组织再生和建议HA-rich伤口ECM CEMIP作为一个潜在的治疗目标疾病的炎症和特异表达HA相交(23,29日,34]。
基因的直接比较形象的变化IPF肺FB在体外治疗与肺pirfenidone FB隔绝pirfenidone-treated IPF患者显示只有23个基因匹配的表达变化。在这其中,只有两个蛋白编码基因,EDN1和5-HTR2B表达下调。EDN1 5-HTR2B参与IPF的发病机制;EDN1通过诱导成纤维细胞增殖和分化转移35)和5-HTR2B通过TGF-β1-triggered胶原蛋白生产的规定(36]。尽管EDN1的贡献和5-HTR2B肺纤维化的发展已经在实验性肺纤维化模型,研究这些分子的作用在人类IPF的发病机理尚不清楚。
即使可以获得有价值的见解在体外实验pirfenidone的直接影响,我们的结果表明,这些实验不提供完整的生物复杂性的照片在IPF pirfenidone行动,应该以谨慎的态度对待。在体外结果可以受到文化环境的影响,细胞通过单个细胞类型和直接接触药物化合物在non-physiological水平。我们之前的研究结果表明,pirfenidone抑制pro-fibrotic活动培养肺FB只有当它用于浓度强烈超过水平观察IPF等离子体(14]。我们不能排除这样一种可能性,即pirfenidone浓度高在体外可能会导致额外的脱靶效应,解释了小重叠IPF + P(神奇动物)和IPF (FB + P)组。因此,在体外研究可以用来生成一个假设,然后进行测试使用原位和在活的有机体内方法。
本研究的主要限制是,我们的肺样本并不代表一个随机样本的前瞻性随机对照研究pirfenidone与安慰剂。事实上,我们使用从外植终末期肺组织样本的IPF患者或没有pirfenidone处理。因此,它是可能的,这个病人选择可能有偏见的结果。尽管所有患者终末期肺部疾病,我们发现高度显著差异与pirfenidone治疗有关。此外,较低的患者数量用于分析可能会限制结果的可靠性;然而,两个独立的方法增加了结果的鲁棒性。结合生物材料的分析从pirfenidone-treated pirfenidone-naive IPF患者和肺孤立的FB pirfenidone处理在体外,我们能够确定一个一致的模式pirfenidone-induced基因表达谱的变化。
虽然我们远离完全理解pirfenidone IPF发病机理和效果,我们的研究结果指出,先天和适应性免疫反应的重要作用以及ECM组织进步的、不可逆的肺组织疤痕。我们的方法提供了一个依据新的combination-based治疗策略改善pirfenidone在IPF的有效性。
补充材料
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:a . Olschewski报告在辉瑞赠款和酬金,外提交的工作。
利益冲突:w·西格报告个人费用从辉瑞、诺华、联合疗法,Actelion股价,Vectura, Savara, Medspray以及拜耳股份公司,在提交工作。
利益冲突:h . Olschewski报告赠款Intermune /罗氏,和赠款和个人费用从勃林格,外提交的工作。所有其他作者没有披露。
支持声明:本研究经费是来自德国研究基金会(m . Wygrecka WY119/1-3), Else Kroner-Fresenius-Foundation (m . Wygrecka),卓越集群“心肺系统”(m . Wygrecka),德国肺癌研究中心(m . Wygrecka),吉森和马尔堡大学医学中心(m . Wygrecka),奥地利科学基金(P27848-B28 Kwapiszewska),奥地利国家银行的银禧基金会(16187 g . Kwapiszewska)和奥地利研究促进会(858308 g . Kwapiszewska和h . Thekkekara Puthenparampil)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年3月21日。
- 接受2018年8月3日。
- 版权©2018人队
本文是开放和分布式根据Creat188滚球软件ive Commons归因执照4.0。