抽象
慢性阻塞性肺疾病(COPD)的临床病程已被提出,但从未被实证证实。我们的目的是开发和验证一个综合的恶性循环模型。
我们采用两种方法。1) Identification and validation of all published vicious circle models by a systematic literature search and fitting structural equation models to longitudinal data from the Spanish PAC-COPD (Phenotype and Course of COPD) cohort (n=210, mean age 68 years, mean forced expiratory volume in 1 s (FEV1),检验模型中变量(“路径”)和模型拟合之间的假设关系。2)利用来自瑞士和荷兰ICE COLD ERIC(慢性阻塞性肺病国际合作研究:恶化风险指数群组)的纵向数据开发新模型并进行外部验证(n=226,平均年龄66岁,平均FEV)157%预计值)。
我们确定了9个恶性循环模型,其中结构方程模型证实了大多数假设的路径,但显示出不恰当的拟合。在新模型中,气流限制、恶性通货膨胀、呼吸困难、体育活动、运动能力和COPD加重仍与其他变量相关,模型适合。对冰冷的ERIC进行拟合,复制所有路径,模型拟合合适。
先前发表的恶性循环模型并不能完全解释恶性循环的概念。我们开发并从外部验证了一个新的综合模型,该模型对锻炼能力和COPD加重有更大的相关性。
抽象
一个外部验证的模型强调锻炼能力和COPD恶性循环的驱动因素http://ow.ly/NXvu30kW7CP
介绍
慢性阻塞性肺病(COPD)的特征是慢性气流受限和持续性呼吸道症状限制病人的活动[1,2]。体力活动的减少[3.]导致病人身体出现不适及进一步损害呼吸系统的病征[4]。这一过程被称为COPD呼吸困难-不活动的“疾病螺旋”或“恶性循环”理论[5],在了解患者的顾虑和生成研究假设[有帮助的,到目前为止的构建3.,6]。然而,文献中包含了恶性循环的几个版本,可能是因为它们是基于专家意见、临床观察和仅在横断面研究中报道的关联。5,7- - - - - -9]。此外,慢性阻塞性肺病的恶性循环理论从来没有前瞻性验证。
我们认为,不能运动的呼吸困难的恶性循环可以被理解为一个“概念模型”,即。涉及特定健康问题的变量之间的一组直接和间接关系,通常用图表表示[10]。为了建立这样的模型,它建立它们的变量和起到呼吸困难,活动恶性循环的一部分变量之间的关系(“路径”)是很重要的。因此,我们的目的是建立在COPD通过呼吸困难,活动恶性循环的经验验证模式:1)识别和使用真实病人的纵向测量所有已发布的恶性循环模型的验证和2号楼)和全面的新的外部验证恶性循环模型,使用来自两个欧洲COPD队列研究反复测量。
方法
系统文献综述
我们进行了一项系统的文献综述,根据综述与传播中心的指导方针,确定所有以前发表的COPD患者呼吸困难-缺乏活动的恶性循环的概念模型[11,科克伦协作组织[12],并为系统评价报告[中PRISMA声明13]。预先指定了与在协议记录所有的方法(参见补充材料)。简单地说,我们检索PubMed / MEDLINE和从最早到最近的2017年5月的记录SCOPUS数据库(见全搜索策略补充材料)。如果他们在图表中讨论或解释了运动障碍的恶性循环,文章就会被包括进来。没有日期或语言限制。两位共同作者(M.A. Ramon和E. Gimeno-Santos)独立审阅了数据库检索到的每条引文的标题和摘要,第三位作者(J. Garcia-Aymerich)在出现分歧时决定将其包括在内。在每一项研究中,我们以有向无环图的形式重建了其恶性循环图,描述了所涉及变量之间假设的纵向关系(直接和间接)。考虑到大多数恶性循环模型中涉及的变量之间的关系具有周期性,我们认为大多数变量都是时变的,包括几个时间点(例如呼吸困难,t1→身体活动在t2→呼吸困难在t3.)。我们联系了每一篇原始论文的一位代表(第一作者或通讯作者),所有人(除了一位没有回复邮件请求的人)都同意我们对他们的图表进行改编。
欧洲慢性阻塞性肺病队列研究的研究设计和参与者
我们获得了两个慢性阻塞性肺病多中心队列研究的患者个人数据,这些研究测量了可能涉及呼吸困难-不活动恶性循环的纵向变量。1) PAC-COPD (COPD的表型和病程)项目,该项目在西班牙8家医院招募慢性阻塞性肺病首次加重期患者(n=342),每12-18个月评估其临床稳定期特征,最多3次[14]。2) The ICE COLD ERIC (International Collaborative Effort on Chronic Obstructive Lung Disease: Exacerbation Risk Index Cohorts) study that recruited patients in primary care centres from the Netherlands and Switzerland (n=409) and evaluated them every 6 months up to 5 years [15];在本研究中,我们纳入了每2年至3次的数据,与PAC-COPD队列的有效时间跨度相对应。来自PAC-COPD和ICE - COLD ERIC组的210名和226名患者在三个连续的研究时间点均有呼吸困难和体育活动数据,因此纳入本分析(补充表S1和S2)。所有纳入的患者均有肺活量测定的COPD(支气管扩张剂后用力呼气量1s (FEV)1)/用力肺活量比<期间临床稳定的条件下0.70)。这两个队列研究是由相关伦理委员会批准,并从每个参与者获得书面知情同意书。
测量
在系统文献综述中确定的至少一个恶性循环模型中涉及的所有变量均可在PAC-COPD队列中重复测量,其中大多数在冰冷的ERIC队列中重复测量。这些包括以下内容。1)改良医学研究委员会(mMRC)对两组患者进行呼吸困难评分(0-4分),对日常活动中的呼吸困难进行评分[16]。2)体力活动按每周能量消耗估算(千卡·周)−1)使用耶鲁大学身体活动调查(YPAS) [17,18],以及运动总得分(0-23),这些分数来自于纵向老龄化研究阿姆斯特丹运动问卷(LAPAQ) [19在冰冷的埃里克队列中。YPAS和LAPAQ问卷分别询问与呼吸困难或其他呼吸系统症状无关的活动的频率、强度和持续时间,在前一个月和前两周。YPAS问卷允许计算每周体力活动的能量消耗,而LAPAQ问卷则根据代谢当量任务为每个活动分配权重,给出0到23之间的评分。3) PAC-COPD研究中,6分钟步行距离、增量试验中最大通气量和用摆线血压计进行的心肺增量运动试验中的乳酸,以及ICE COLD ERIC研究中1分钟站立-坐试验的重复次数[20.]。4)两项研究的握力。5)FEV1在两项研究中,支气管扩张术前和支气管扩张术后,以及肺功能测定的吸入量(IC);肺总容量(TLC),肺一氧化碳和动脉血氧张力的扩散能力。以IC和IC/TLC作为肺静止性恶性膨胀所致吸气受限的指标[21]。6) Charlson合并症指数,仅适用于PAC-COPD。7)从PAC-COPD研究的政府数据库收集的COPD加重情况,并通过ICE COLD ERIC研究中对患者访谈和患者记录复查的中央裁决。8)健康相关生活质量:采用St George’s呼吸问卷总分(0-100)进行PAC-COPD研究,采用ICE COLD ERIC研究采用慢性呼吸问卷总分。9)两组患者的医院焦虑和抑郁量表得分。
统计分析
样本量允许统计能力>99%确定我们的模型比以前发表的模型更适合于统计意义上的显著性补充材料)[24]。
我们通过拟合使用从纵向的数据的结构方程模型(SEM),在各定向非循环图(对应于每个所识别的恶性循环模型)中所描绘的变量和路径评估从系统综述(第一目标)中获得恶性循环模型的有效性的PAC-COPD队列和测试1)变量之间和2)全假设的模型如何装配在数据的假设的关系(“路径”)。简言之,SEM是统计建模技术,测试数据的构建体(包括变量和路径)来估计包含变量[之间的直接和间接关系25]。首先,由扫描电子显微镜估计的路径系数告知了模型中每个假设的路径。路径系数的标准化范围为- 1至+1,以方便涉及不同变量的路径之间的比较,并可解释为相关系数[25]。Nonstandardised系数也被用来更好地了解模型变量之间的关联的强度,并能够将它们与先前的研究相比较。在假设的方向统计学显著路径系数(例如呼吸困难与后来的身体活动负相关)支持模型的有效性。其次,模型拟合参数表明,特定模型中包含的变量和路径在多大程度上代表了潜在的概念(呼吸困难-不活动的恶性循环)[26]。
以下三种SEM适合标准被认为是[27- - - - - -31: 1)卡方/自由度(d.f.) <2.0且p值不显著(≥0.05),说明数据中存在未解释的不显著的方差[27,30.,31], 2)均方根逼近误差(RMSEA) <0.07, 90% CI在0.05 - 0.10之间,说明模型与种群协方差矩阵吻合较好[28,30.,313)比较拟合指数(CFI)≥0.95,表明模型中包含的变量之间具有较好的相关性[29,31]。一个模型必须满足我们所有的三个标准。如果不是,我们认为它没有很好地解释恶性循环理论(例如因为模型遗漏了一些与恶性循环相关的变量或路径)。
我们决定先天的提出一个新的恶性循环模型,如果在系统的文献综述中没有一个模型被证明是有效的。由于这种情况(见结果部分),我们构建了一个新的恶性循环模型(第二个目标),通过对PAC-COPD纵向数据进行新的SEM拟合,将之前确定的至少一个恶性循环所涉及的所有变量和路径作为候选变量。此外,我们允许SEM添加任何在统计上有意义的路径(在以前的模型中没有),并改进模型的适合度,只有当它在生物学上是可信的(例如气流受限和呼吸困难)之间的直接路径。在一次消除路径或一个变量的迭代过程中,我们从与无统计学显著路径系数(P≥0.05)和2)在该模型不相关的任何其他变量的变量(路径系数与SEM 1)的路径删除P≥0.05),其去除没有恶化的模型拟合。最终SEM保持变量显示与剩余的变量和/或改善显著模型拟合中的至少一个具有统计学显著关联。作为最后一步,我们安装有PAC-COPD队列到冰冷的ERIC纵向数据所获得的最终SEM模型。该模型被认为是恶性循环的有效表示,如果它符合我们上面(的路径确认和适当的模型拟合)详细的标准。
所有分析均使用Stata version 12.1 (StataCorp, College Station, TX, USA)进行。
结果
恶性循环模型的识别在系统的文献综述中
我们确定了9篇文章,报告了“运动障碍-不活动”恶性循环的概念模型,作为一个图表(补充图S1)[5,7,8,32- - - - - -37]。不同模型的变量和路径存在差异(表格1和图1)。所有模型均包括呼吸困难,8个模型包括运动能力,7个模型包括身体活动,6个模型包括肌肉力量。大多数模型(9个模型中有6个)将呼吸困难作为恶性循环的起始变量,而在其余3个模型中,气流限制被认为是初始因素。
有向无环图和验证#慢性阻塞性肺疾病(COPD)的呼吸困难-无活跃性恶性循环的确定图表:a) C提出的模型oop(5),b) Polkey和Moxhan(8],c c)oop(32),d) Reardon等。(7D, e)ecramer(33),f) Donaldson等。(34],克)M阿尔泰(35),G h)arcia -一个ymerich和P俄(36],以及i)Corhay等。(37]。mMRC:修改后的医学研究委员会;6MWD:6分钟步行距离;VEMAX:增量式摆线仪测试时的最大通气量;集成电路:吸气量;TLC:总肺活量;FEV1:用力呼气1 s;HADS-A/D:医院焦虑和抑郁量表焦虑/抑郁;SGRQ: St George’s Respiratory Questionnaire(得分越高说明局限性越大);PaO2:动脉氧张力;d.f。:degrees of freedom; RMSEA: root mean square error of approximation; CFI: comparative fit index;ns:不显着。#:使用标准化系数,两个变量之间的关联的大小取从- 1到+1的值,其中负值表示负关系。
对于每一个已识别的图,我们都构建了一个有向无环图(图1)。
系统文献综述中确定的恶性循环模型的验证
我们对PAC-COPD纵向数据的9个图表分别进行了扫描电镜分析。患者多为男性(93%),均有平均FEV154%预测mMRC呼吸困难评分中值为2 (表2)[38]。在随访期间,呼吸困难、体力活动和其他临床和功能变量恶化(补充表S3)。
慢性阻塞性肺疾病患者的PAC-COPD(慢性阻塞性肺疾病的表型和病程)和ICE - COLD ERIC(慢性阻塞性肺疾病的国际合作努力:恶化风险指数组)的特征在招募时进行分组
(9个模型中的)大多数路径被复制,其路径系数在假设的方向上具有统计学意义(图1)。然而,恶性循环模型均未表现出p值(均<0.05)、RMSEA值(0.176-0.352)和CFI值(0.347-0.629)的适当拟合(表3)。
建立一个全面的新的恶性循环模式
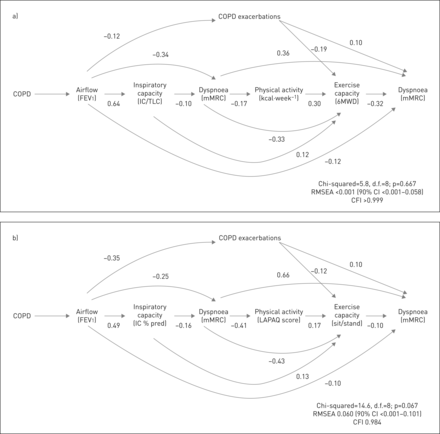
补充图S2显示在系统回顾中确定的至少一个恶性循环模型中涉及的所有变量和路径。经过多次使用PAC-COPD数据的迭代,我们得到了最终的模型(图2一个),1)气流限制和肺恶性通货膨胀都直接与呼吸困难有关,2)呼吸困难有关未来的运动能力直接或由身体活动的减少,3)体育活动和运动能力都与未来呼吸困难的水平,4)慢性阻塞性肺病急性加重,与气流限制之前,有关未来的运动能力和呼吸困难,其他结果(5)如。将上述变量和路径纳入模型后,生活质量、焦虑、抑郁、共病、低氧血症、肌无力等因素均未导致恶性循环,且模型各参数拟合良好(卡方=5.8,d.f.)。=8, p=0.667, RMSEA <0.001 (90% CI <0.001 - 0.058), CFI >0.999)。补充图S3a给出了利用非标准化系数的SEM模型。
一)推导和b)验证:在慢性阻塞性肺疾病(COPD)的呼吸困难,活动恶性循环的新模式。关系和标准化路径系数#慢性阻塞性肺病患者呼吸困难-不活动恶性循环的变量之间。FEV1:用力呼气1 s;集成电路:吸气量;TLC:总肺活量;mMRC:修改后的医学研究委员会;步行距离:6分钟;LAPAQ:纵向老化研究阿姆斯特丹身体活动问卷;d.f。:degrees of freedom; RMSEA: root mean square error of approximation; CFI: comparative fit index.#:使用标准化系数,两个变量之间的关联的大小取从- 1到+1的值,其中负值表示负关系。
验证新的恶性循环模型
为了验证这种新的模式,我们将其运用到冰冷的ERIC纵向数据。这些患者(60%为男性,平均FEV157%的预测值和mMRC dyspnoea评分中值(1)总体上比PAC-COPD轻(表2),但他们的临床及功能特征亦在跟进期间恶化(补充表S4)。图2 bshows results of the fitted SEM, which confirmed all paths with statistically significant path coefficients in the hypothesised direction and showed a good fit to the data according to all parameters (Chi-squared=14.6, d.f.=8, p=0.067, RMSEA 0.060 (90% CI <0.001–0.101) and CFI 0.984).补充图S3b给出了利用非标准化系数的SEM模型。最后,图3示出描绘新的恶性循环的概念模型。
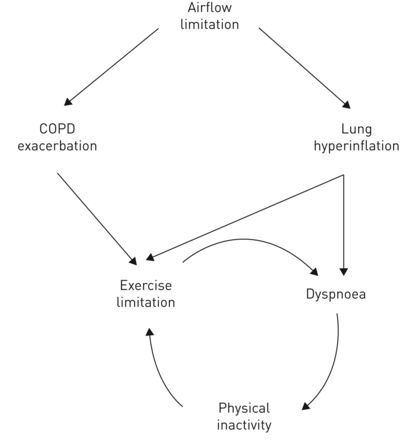
慢性阻塞性肺疾病(COPD)患者呼吸困难-不活动恶性循环新模型的图示。
讨论
据我们所知,这是第一个为慢性阻塞性肺病的呼吸困难-缺乏运动的恶性循环理论开发并从外部验证了一个模型的研究。我们发现,1)以前发表的概念模型包含关于恶性循环的有效信息(因为大多数路径可以使用纵向数据复制),但不太可能适当地解释恶性循环的概念(根据模型与患者数据的低契合度),2)建立了一个新的综合模型,该模型对锻炼能力和COPD加重有更相关的作用,并使用两个前瞻性队列进行了验证,其中包括来自不同地理区域和临床环境的疾病严重程度不同的COPD患者。
解释研究结果
我们发现,现有的恶性循环模型包括变量和相关的恶性循环变量之间的关系(“路径”)。这些变量和路径描述从呼气气流限制的事件序列,增加静息肺容积和动态过度充气,以浅和快速的呼吸模式与恶化呼吸困难,减少身体活动和运动能力,这进一步增强呼吸困难恶化,从而类似于对COPD的病理生理学当前所知[39,40]。
然而,我们观察到现有的恶性循环模型对真实患者纵向数据的拟合较差。我们的研究结果表明,以前的模型并不能完全代表潜在的理论(即。因为额外的变量和路径应该被考虑在内。用PAC-COPD数据建立的模型对ICE - COLD ERIC数据进行拟合时,获得良好的拟合指标支持了这一假设。我们的研究结果还表明,将当前的恶性循环模型应用于其他慢性呼吸系统疾病需要真实的患者数据,而不是简单地从COPD推断。
我们提出的新的恶性循环模型与以往的模型相比主要有两个不同之处。首先,我们发现慢性阻塞性肺病加重,慢性阻塞性肺病自然史中的关键事件,只在以前的一个模型中考虑过[33,与恶性循环是相关的,即使在初级保健COPD人群中,如ICE COLD ERIC,也很少发作。此外,我们的模型支持恶化的双向作用(两者都影响恶性循环的未来变量,如前所述[33],也受之前变量的影响),这与当前的观点一致,即COPD评估、管理和预后中恶化起着重要作用[1]。其次,我们的研究结果表明,运动能力在恶性循环中扮演的中心角色比以前认为的要大[5,32- - - - - -35,考虑到其他变量(肺恶性膨胀、体力活动、恶化)对呼吸困难的大部分影响是通过对运动能力的影响来调节的。再次,这一发现与COPD的现有知识相一致[41,42],由于运动能力的下降被发现是由于肺的恶性膨胀而加速的[41慢性阻塞性肺病加重[42],以及提高运动能力(例如通过运动训练计划[43)减少呼吸困难。
一些解释可能有助于解释为什么以前的恶性循环模型中包含的一些变量与COPD预后相关,例如骨骼肌无力,焦虑或抑郁和并存病,在我们最终的模型中都没有出现[32,34,35,37]。1)患有这些疾病发病率较高丢失跟进,这可能会阻碍我们在可能导致恶性循环的重要变量观察变化。2)有可能的是,一旦指定了其他变量和路径,这些变量没有提供的附加信息到的恶性循环。3)在PAC-COPD和冰冷ERIC队列这些概念的现有措施可能没有足够精确。例如,我们使用手柄力,而不是股四头肌力量可能阻止我们找到骨骼肌力量,并在模型的其他变量之间的强商会。4)变量COPD当然很重要,如吸烟史或身体质量指数,不包括在以前的恶性循环模式。其列入可能之后它们如何影响和/或在当前恶性循环变量影响适当的系统评价予以考虑。总之,未来在这个领域的研究将需要反复在潜在相关的恶性循环现象,所有变量的时间,有效的测量。
优势和局限性
我们的研究的一个优点是,我们遵循严格的系统回顾方法,以确定所有以前发表的模型的呼吸困难-不活动的恶性循环。此外,我们使用SEMs来验证每一个已确定的模型,这提供了一个广泛的深入了解参与恶性循环的变量之间的复杂关系。最后,我们使用了来自不同临床环境(初级保健和专科医院呼吸科)的两个不同的队列,包括疾病严重程度不同的患者,这增加了我们模型的外部有效性。
其中潜在的局限性,首先,上述一些缺乏相关变量,例如股四头肌的力量,可能导致相关的变量或路径不包括在我们的最终模型。第二,本文是基于对两个与其他主要研究问题招募的队列的二次分析。因此,分析中包含的一些变量可能不是最适合研究恶性循环概念的。例如,使用mMRC量表(而不是其他测量方法)来评估呼吸困难可能会使其与身体活动的关系的论点有点循环。第三,两组随访失败的患者在基线时的临床和功能状态均较差,这可能降低了某些参数的可变性,从而限制了识别相关性的能力。然而,在临床实践中出现恶性循环的典型表现的患者,实际上是那些COPD存活下来而没有严重并发症的患者,即。那些谁随访的调查研究。因此,我们的研究结果不能扩展到COPD患者非常有限的生存或严重的合并症。四,使用问卷测量两个同伙,这可能是受到精度差以可变的关键恶性循环的各个级别的体力活动。(值得注意的是,从加速计体力活动是在第二次后续的PAC-COPD的研究,但不包括在此分析,以保持所需要的时间顺序使用。)第五,两个同伙的样本量相对较小,没有允许在恶性循环测试的药物和非药物治疗的潜在作用。六,提供了三种不同的时间点,虽然数据(t1,t2和t3.),许多变量只在t1和t3.,这可能会阻碍对某些参数随时间变化的差异的识别。此外,相对较短的随访期(<5年)可能限制了我们识别与恶性循环相关的新变量或适当估计相关变量对恶性循环的贡献的能力。然而,在PAC-COPD和ICE - COLD ERIC患者中,我们观察到随着时间的推移,体力活动、肺功能、运动能力和肌肉力量的统计显著恶化。最后,在COPD进展参数存在较大异质性的情况下,我们的新恶性循环模型的外部有效性可能不成立。
结论
先前发表的恶性循环模型并不能完全解释恶性循环的概念。我们开发并从外部验证了一个新的综合模型,该模型对锻炼能力和COPD加重有更大的相关性。这种新的模式可能是帮助临床医生和研究人员更好地了解所涉及的呼吸困难,活动恶性循环COPD特性之间的关系,从而有利于设计和有针对性的治疗干预的测试。
补充材料
致谢
我们要感谢原文章的作者为阅读并接受我们的建议,以验证他们提出了呼吸困难,活动的恶性循环模式:克里斯托弗·库珀(医学,加州大学洛杉矶分校的大卫格芬医学院,CA,USA)让 - 路易·Corhay(大学医学中心,萨尔特 - 蒂尔曼,比利时列日),马克·Decramer(呼吸康复和呼吸师,大学医院鲁汶,比利时鲁汶),弗朗索瓦Maltais(心肺研究所,拉瓦尔,魁北克大学,QC,加拿大),迈克尔Polkey(呼吸内科,皇家布朗普顿医院,伦敦,英国)和理查德·ZuWallack(圣弗朗西斯医院医疗中心,哈特福德,CT,USA)的部门。
脚注
这篇文章有补充资料www.qdcxjkg.com
利益冲突:A. Agusti报告在提交的作品之外从阿斯利康(AstraZeneca)、葛兰素史克(GSK)和梅纳里尼(Menarini)获得资助和个人费用,从MSD获得资助,从诺华(Novartis)、梯瓦(Teva)和基耶西(Chiesi)获得个人费用。
利益冲突:在研究进行期间接收来自勃林格殷格翰,珍珠治疗和Teva及诺华和武田,讲课费的顾问委员会由ALMIRALL和Menarini,个人费补助金服务R.罗德里格斯罗伊辛报告,所有与COPD。
利益冲突:J.加西亚-艾默里奇向她的机构报告阿斯利康的咨询和演讲费用,并从Esteve和Chiesi收取演讲费,在提交的作品之外。
支持声明:本PAC-COPD研究是由丰多日InvestigaciónSANITARIA(FIS PI020541),卫生部,西班牙的资助;科特迪瓦通讯社德AvaluacióTECNOLOGIA我RecercaMèdiques(AATRM 035/20/02),加泰罗尼亚政府;肺病和胸外科(SEPAR137分之2002)的西班牙社会;肺病的加泰罗尼亚基金会(FUCAP 2003贝科玛丽亚RAVA);红色RESPIRA(RTIC C03 / 11);红色RCESP(RTIC C03 / 09),丰德InvestigaciónSANITARIA(PI052486);丰多德InvestigaciónSANITARIA(PI052302);Fundació拉Marató德TV3(041110);DURSI(2005SGR00392);和不受限制的诺华Farmacéutica,西班牙和阿斯利康Farmacéutica,西班牙教育补助金。 CIBERESP and CIBERES are funded by the Instituto de Salud Carlos III, Ministry of Health, Spain. ISGlobal is a member of the CERCA Programme, Generalitat de Catalunya. The ICE COLD ERIC COHORT study was funded by the Swiss National Science Foundation (grant 3233B0/115216/1), Dutch Asthma Foundation (grant 3.4.07.045) and Zurich Lung League (unrestricted grant). There was no involvement of these funding sources in study design; in the collection, analysis or interpretation of data; in the writing of the report; or in the decision to submit the article for publication. The researchers are independent from the funders. Funding information for this article has been deposited with the交叉引用出资者注册。
- 收到了2018年1月13日。
- 接受2018年7月6日。
- 版权©2018人队