抽象的
支气管热塑术是哮喘的治疗方法。目前尚不清楚其组织病理学影响是否通过暴露于影响细胞存活所必需的温度的气道壁的比例充分解释。
气道平滑肌和支气管上皮细胞暴露于培养基(37-70°C) 10 s模拟热成形术。在网上我们开发了一种气道热分配后热塑性术的数学模型。在活的有机体内我们测定了14例严重哮喘患者热成形术前后的气道平滑肌质量和上皮完整性。
体外在加热至≥65℃的培养基中,气道平滑肌肉和上皮细胞数显着下降。在网上模拟结果显示,在较大的气道中,热量分布不均,在内径为~ 4 mm的气道中,小于10%的气道壁被加热到>60°C。在活的有机体内热成形术后6周,哮喘控制有改善(测量值)通过哮喘控制问卷-6;平均差异0.7,95%CI 0.1-1.3;P = 0.03),气道平滑肌肉质量降低(绝对中值减少5%,间条形(IQR)0-10; p = 0.03)和上皮完整性增加(14%,IQR 6-29; P = 0.007)。后两种结果都不是与改善的哮喘控制有关。
集成体外和在网上模型表明,热成形术后气道平滑肌的减少不能完全用急性加热来解释,这种减少也不能使哮喘控制得到更大的改善。
抽象的
哮喘的支气管热塑术治疗具有意外的可能的行动机制http://ow.ly/zcue30jsasa.
介绍
支气管热塑术(BT)是一种非药理学治疗,用于通过用低功率电流从内腔内选择性加热导电气道(直径为3-10mm)来治疗严重哮喘治疗[1,2].在BT程序期间,热能输送到气道墙壁通过带支气管插入的导管,具有四个电极的远端篮,可扩展以与气道壁接触,旨在达到65℃的目标温度10秒。
BT的主要靶点是气道平滑肌(ASM),它是气道重塑的关键因素,特别是在严重哮喘中[2- - - - - -7].此前的动物研究表明,BT后气道超反应性降低,ASM组织学外观改变[8].随后的临床试验显示,接受BT治疗的患者的生活质量得到改善,严重病情加重的频率降低相对假手术,但由于治疗结果发现肺功能没有显着差异[9- - - - - -12].在非对照观察性研究中,BT与支气管活检确定的ASM肿块相对丢失有关[13- - - - - -16],通常在完成BT程序后1-3个月获得。虽然射频能量的热消融通常用于外科实践[17,18],有一个理论的缺乏[19] 和体外[20.这些研究评估了超热温度对ASM细胞存活和功能的直接影响,或BT对ASM质量和上皮完整性的早期影响。
我们假设,在BT期间,气道暴露于温度所必需的影响ASM和上皮细胞存活的比例,由体外实验,足以解释BT的影响。为了检验我们的假设体外,在网上和体内在ASM和上皮细胞上定义BT的急性撞击的方法。
方法
详细的方法包含在补充材料.
体外加热人原发药,上皮细胞和支气管上皮细胞
如前所述培养初级ASM和上皮细胞[21].该研究得到了莱斯特郡研究伦理委员会的批准(REC 08/H0406/189)。获得所有受试者的知情同意。人支气管上皮细胞(hBECs)取自英国Middlesex公司的LGC Standards。
细胞在6孔或24孔板中生长,然后按上述方法在加热的培养基中暴露10秒补充方法.测量了10-s期间的热损失,结果表明,在加入加热到65°C的介质后,6孔板和24孔板上的细胞暴露在平均温度为58-59°C的环境中(补充表S4)。
根据制造商的说明,使用PrestoBlue®(Thermo Fisher Scientific, Warrington, UK)评估加热后2周内残留的粘附活细胞数量,并在指定时间通过细胞计数进行确认。使用Alexa Fluor®488 Annexin V/Dead cell apoptosis Kit (Thermo Fisher Scientific)(如前所述)测定24 h后发生凋亡或坏死的粘附细胞群的剩余百分比[22].流式细胞仪在530 nm (Annexin V)和>575 nm(碘化丙啶)处采集荧光发射,分别使用WEASEL™软件(Frank Battye流式细胞术咨询公司,墨尔本,澳大利亚)提取凋亡和坏死细胞的百分比。
在网上生物健康数学建模
因为目前还无法测量BT期间气道壁内的传热体内,开发了一种二维数学模型,其由于BT电极产生的电流(具有集成温度控制反馈而导致的焦耳加热(具有类似于的[19])在气道墙壁和周围的实质组织中的生物发热。如图所示,将肺的材料特性应用于模型补充表S1.使用COMSOLMultibysics®5.2(斯德哥尔摩,瑞典)的有限元模型框架来实现耦合模型。热图集成在气道壁上,以表征加热模式异质性。
进行局部敏感性分析以识别关键的几何,生理和设备参数,并测试模型预测的稳健性。数学模型制定和进一步的技术细节可以在其中找到补充材料.用该方法对数学模型进行了验证体外多孔板中加热介质冷却的数据(见体外方法上面的方法,它表现出良好的一致性(补充图S3)。
预测气道壁温度分布,与ASM和支气管上皮细胞的热剂量依赖性响应组合体外,用于估计Bt在支气管壁上的整体急性撞击(所示的建模框架补充图S1)。
在活的有机体内应对英国电信
在BT之前和之后,从14个受试者获得支气管活组织检查。所有受试者都有严重的哮喘,如美国胸部社会/欧洲呼吸社会指导方针所定义,并作为其临床护理的一部分接受了BT。188bet官网地址
按照三个分阶段治疗课程的制造商的指南进行了BT,按以下顺序:右下叶,左下叶,左右上瓣。由于气道崩溃的风险和“右中叶综合征”的风险,右中叶未被治疗23].活检取自第一次BT治疗时未治疗的右上叶和第二次BT治疗时右侧下叶节段和亚节段气道。
将活组织检查嵌入石蜡中,并用Haematoxylin和eosin或抗-α-平滑肌肌动蛋白(α-SMA,克隆1A4; Dako,Stockport,UK)染色4μm部分。通过盲目的单一观察者(RJR)评估活组织检查,以确定1)ASM含量作为总活检区域的百分比;2)通过测量并表达完整,损坏和剥离的上皮的长度,上皮完整性,作为网状基底膜长度的百分比;3)肌纤维细胞的数量(椎间壳中的分离α-SMA阳性染色细胞,其既不都是ASM束的一部分,也不是血管平滑肌细胞,每毫米相邻的血管平滑肌细胞)2Lamina Propria。
统计分析
统计分析更详细地讨论补充方法.简而言之,在GraphPadPrism®7.0和R项目3.2.4中分析数据,使用参数和非参数测试。使用Bootstrap百分位方法(R引导包)估计细胞计数中位数的置信区间。p值<0.05被认为是统计学上的显着性。
结果
体外ASM和HBEC细胞的细胞凋亡和坏死
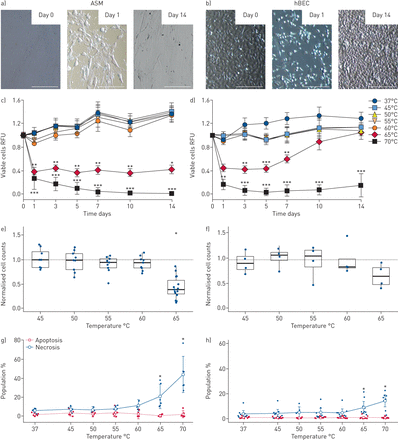
代谢测定证明,加热至65℃或70℃的培养基,但不是45-60℃,导致依赖于24小时后依赖于粘附的ASM和HBEC细胞的显着降低。37°C(图1a,b)。在加入到65℃或70℃的培养基中加入65℃或70℃的培养基和HBEC细胞的70℃的介质相比,这种降低的这种降低持续在2周后,与37℃相比,在65℃或70℃下持续2周。回收的可行HBEC细胞的数量,使得在加热至65℃的介质后10天的数量没有显着降低相对37°C(图1一个-D)。结果提出图1A-D在不同时间使用细胞计数(图1 e,f),支持代谢测定结果。ASM和HBEC细胞计数在24-48小时(未示出的数据)加热至65℃(未示出)后,ASM和HBEC细胞计数显着降低。持续为1周(图1 eASM的2周(未示出的数据未显示),在1周后恢复HBEC细胞数(图1 f)。除了减少ASM和HBEC细胞数的后加入到65°C或70°C的介质后相对37°C,细胞百分比的百分比显着增加,但不能细胞凋亡(图1 g, h)在剩余贴壁细胞群中。加入加热至65°C、24 h的培养基后,活ASM细胞数相对减少的中位数为60% (95% bootstrap CI 40-80%)。
的反应体外加热气道平滑肌(ASM)和人支气管上皮(hBEC)细胞。a, b)加入加热到65°C的培养基后,具有代表性的细胞形态;与hBEC (b)细胞相比,ASM (a)细胞在2周内恢复不完全。比例尺,0.1毫米。c, d) ASM (c)和hBEC (d)细胞在加入加热到规定温度(平均值±)的培养基后的纵向活力se)。E,F)在添加ASM(E)和HBEC(F)细胞的加热培养基后,相对于37°C匹配对照的总细胞计数。G,H)凋亡和坏死作用的比例(G)和通过流式细胞术中加入培养基加热到规定温度(平均值,95%CI)之后的流式细胞术例测定的HBEC(H)细胞。* P <0.05,** P <0.01,*** P <0.001相对37°C控制。
在网上加热异质性概要文件
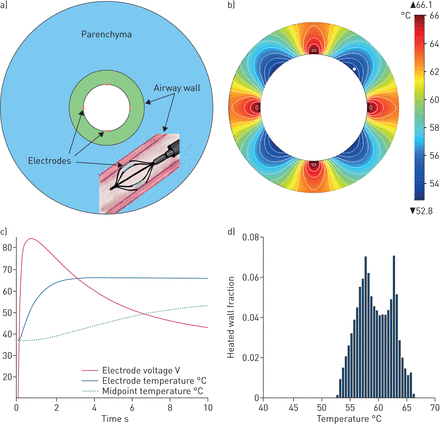
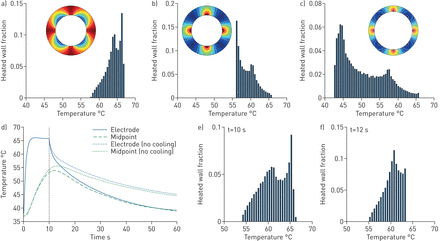
我们实现BT协议的基于计算有限元的模型在气道壁上显示了高度的温度变化。示出了具有参考模型几何(分别为2.2和3.3mm的内壁半径)的示例图2.为了评估数学模型中的每个参数对热分布的影响,我们进行了局部敏感性分析(补充材料)。这证明了模型预测对组织材料特性和加热控制参数相对不敏感(补充表S3),但强烈依赖于气道口径和壁厚(补充表S3和图S2)。该较大气道中的温度变化的扩增如图所示图3.,仅展示将壁的一小部分加热至65°C(图3.和表格1)。
支气管热塑术(BT)加热图案的表征。a)参考模型几何形状(内壁半径为2.2 mm,外半径为3.3 mm)。b)在单个BT激活(10秒)的末端的热图。c)两个电极之间的施加电压(红色),电极温度(固体蓝色)和温度的时间动力学(虚线;用B)标记为白点)。d)对应于B的加热壁面积分量的分布。
尽管能量转移在BT导管可访问的最小气道中更有效(图3一),在腔腔冷却减少的呼吸气道的情况下,可以进行次优化加热(图3 b),在较大的气道中,加热不均一性加剧(图3 c)。我们的模型表明,用BT处理的典型气道(内半径~4mm)的5%暴露于温度> 65℃,<10%至温度> 60°C(表格1)。BT后热平衡不会提高上温度范围内加热的程度,在能量递送结束后1-2秒内没有墙体的墙体的一部分> 65°C(图3 d, e),即使没有体积冷却由于组织灌注和肺泡水分蒸发。因此,除最小的经BT处理的气道外,只有一小部分气道可能暴露在>60°C的温度下。由于气道与支气管镜的可及性,这些气道活检近于用BT治疗的最小气道。
在活的有机体内BT对ASM肿块和上皮完整性的影响
14个受试者的基线和后续临床特征显示在表2..九次受试者接受常规全身皮质类固醇的处理(哮喘(吉纳)步骤5的全局倡议,其余受试者接受吉纳步骤4治疗。在最后一次BT干预后六周内没有肺功能变化,而哮喘控制问卷-6(ACQ6)的分数和哮喘的生命质量问卷(AQLQ)在0.5的临床上的重要差异中显着提高了显着提高(ACQ6平均差异-0.7,95%CI -1.3至-0.1,p = 0.03; AQLQ平均差0.8,95%CI 0.1至1.5,P = 0.03)(表2.)。
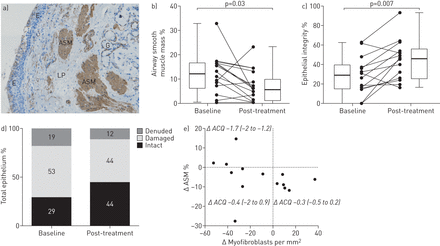
基线和随访活检之间的中位时间为28天(范围14-56天)。有代表性的支气管活检示图4一.从12%(IQR级(IQR)6-17)中的12%(IQR)6%(IQR 1-10)后的中位数(IQR级别)(IQR 1-10)(中位差5%,IQR 0-10,Wilcoxon P =0.03;图4 b)。ASM质量的中位相对降低为58%(IQR 6-90)。
支气管活检的气道平滑肌(ASM)含量和上皮完整性的组织学分析(基线和约1支气管热成形术(BT)后一个月)。a)例支气管内活检染色α.-平滑肌肌动蛋白(E:上皮;LP:固有层;G:腺)。b) bt前后ASM质量% (p<0.05)。c) bt前后的上皮完整性(p<0.01)。在b和c中,水平线代表中值,方框代表四分位数范围(IQR),须代表最小值和最大值。d)基线和bt后上皮结构的详细分解(平均值)。由于舍入关系,基线的总百分比不等于100%。e) ASM质量变化相对每毫米肌纤维细胞的数量2Lamina Propria之后的BT(Spearman的等级相关性r= -0.55,p = 0.046),随着哮喘控制问卷-6(ACQ6)的变化(ACQ6)评分(平均(IQR))报告每个响应子组(象限)。
29%(IQR 15-40)前的上皮完整性的中位上皮完整性也有显着改善(IQR 15-40)PRE-BT至46%(IQR 25-56)后BT(中值改善14%,IQR 6-29,P = 0.007;图4 c上皮完整性相对增加的中位数为56% (IQR 19-120)。
亚上皮肌纤维素细胞的数量减少了数值但不显着的减少(BT中位数25个细胞·mm−2,IQR 7-47相对后BT中位数13个细胞·mm−2差6-21;p = 0.17)。在BT (Spearman)后,ASM质量的变化与固有层的肌成纤维细胞计数呈显著负相关r= -0.55,p = 0.046;图4 e)。上皮完整性的变化与MyOfbroblast计数和ASM质量的变化无关(数据未显示)。
AQLQ得分的改善与层Pravria中的BT上皮完整性,ASM质量或肌纤维细胞数也不相关,也不与BT后的变化(数据未显示)。只有三个受试者有所改善≥1.0,因此没有进行响应者分析。在BT前上皮完整性,Lamina Propria中的ASM质量和肌纤维细胞数与ACQ6得分的变化无关(数据未显示)。ACQ6得分的变化与ASM群众的变化反向(Spearmanr=−0.67,p=0.018),但上皮完整性(r= -0.03,p = 0.09)或Lamina Propria中的my纤维细胞数(r= 0.41, p = 0.18)。5名受试者ACQ6评分改善≥1.0。与ACQ6未显示这种改善的受试者相比,这5名受试者在bt后ASM质量有小幅度增加(中位数为2%,IQR−2至8)相对中位数-10%,IQR -8至-12;p = 0.003)。与Lamina Propria中的更高BT肌纤维细胞数相反(59个细胞·mm−2,IQR 36-84相对7个细胞·mm−2差3-43;p=0.03), bt后减少更大(37个细胞·mm−2, IQR 30-51相对-8细胞·mm−2,IQR 3到-27;p = 0.048)。随着液相血管血管血管肌瘤的增加和肌纤维细胞数量增加的人对ACQ6得分的最大程度最大,而且与患有ASM质量的减少或降低的那些,并且肌纤维细胞数增加(图4 e)。
讨论
我们开发了一个综合的体外和在网上框架模拟BT对ASM和上皮细胞的急性效应。在这个框架中,在网上数学模型起到了桥梁的作用体外和体内热效应,即其他方式无法访问。这体外模型识别HBEC和ASM细胞对加热的响应的尖锐阈值。体外在加热到≥65℃的介质后,HBEC和ASM细胞数显着下降。重要的是,考虑到10秒的热量损失体外实验,将这些细胞暴露于58-59℃的平均温度。数学模型预测了对气道口径非常敏感的局部和高度异质的加热模式,其中支气管壁的相对较小的一部分加热至最小的气道,除了最小的气道(另见[25])。集成的体外和在网上对模型预测进行了测试体内支气管活组织检查预先和bt后。活组织检查样品显示上皮完整性的增加和BT后ASM质量的降低。
尽管比基于我们的数学模型预测的要大,但观察到的bt后ASM质量相对中位数减少58%,与之前的临床研究一致[13- - - - - -16].为了通过单独解释这种急性热损伤的这种水平降低,在支气管镜检查的气道中的大多数气道壁都需要加热至≥60°C。因此,如果体外和在网上预测是正确的,这种差异一定是由于BT引发的另一种生物机制,如主动热旁观者效应[26].
我们的体内BT后,活组织检查显示出显着改善的上皮完整性,这可能反映出响应热损伤的上皮修复。的确,我们体外数据显示急性期上皮修复响应热的证据。其他研究未发现在BT治疗完成3个月后获得的活组织检查上皮表型的变化,但报告了对胶原沉积和支气管神经的其他影响[16].尽管在这项小型研究中,ASM肿块的减少与上皮完整性的增加无关,但在BT后,上皮修复是否可能影响包括ASM肿块在内的气道壁结构的其他变化,值得进一步研究。
在哮喘患者中,肌纤维细胞数量在哮喘患者中增加,他们对损伤部位,分化和促进伤口修复[27- - - - - -29].我们考虑BT是否可能影响固有层中肌成纤维细胞的数量,以及这些细胞的流行是否可能与上皮和ASM中观察到的变化有关。我们确定了数值但无意义的总数减少myofibroblasts BT在固有层反应。然而,有显著负相关关系的变化ASM质量和myofibroblast BT后数量。这可能代表myofibroblasts和ASM包之间的动态关系,肌成纤维细胞在肌束之间的迁移。尽管我们的研究对象数量较少,但我们能够探索BT对ASM质量、固有层上皮完整性和肌成纤维细胞数量的影响与最后一次BT干预6周后评估的哮喘相关症状之间的关系。令人惊讶的是,我们发现哮喘控制的改善与bt后ASM质量的变化呈负相关,而且在ASM质量增加和肌成纤维细胞数量减少的患者中,哮喘控制的改善最大。观察到的上皮修复与改善哮喘控制无关,但上皮修复是否有助于减少BT后更大规模研究中观察到的加重率,还需要进一步研究。
我们的研究有很多潜在的限制。这体外研究无法完全重新承载ASM细胞和支气管上皮细胞的行为体内因为在分离中直接添加加热的介质。他们也没有考虑到哮喘相对非哮喘细胞表型,细胞 - 细胞相互作用或粘膜组织的存在。此外,在模型系统中的10-S曝光中存在少量的热量损失。但是,我们体外不同的方法和两个中心之间的数据非常一致。
数学模型涉及许多简化假设。我们以横截面为横截面和忽略的三维效果建模。与气道壁厚(~1mm)相比,该近似通过电极的相对长(~5mm)长度是合理的。计算模型还使用了气道壁和实质组织的平均均匀电热材料特性,并且不考虑治疗的个体内和之间可能的解剖学生理变异。还有可能是固有的操作员可变性,患者肺部运动和复杂的自动控制器保护,并入到BT协议中,该方案不包括在模型中。然而,我们已经测试了鲁棒性在网上建立模型并量化与模型预测相关的不确定性通过1)适当的网格收敛试验,2)在组织材料性质(结果未示出)和3)中施加随机空间扰动的综合参数灵敏度分析。实际上,敏感性分析表明,模型预测仍然不受组织材料特性的适度变异性的影响,而气道壁和腔形态格术对模型的影响最大。尽管如此,开发的数学建模框架旨在提供定性而不是定量洞察BT的影响。因此,尽管存在局限性体外和在网上在建模过程中,我们相信这些数据并不支持ASM大量急性损失的概念,这是对支气管镜下采样的气道中BT的加热效应的直接反应。
英国电信也有缺点体内临床试验。一,是体内基线时右上叶和BT后右下叶的支气管活检,基线时ASM肿块低于我们之前报道的[24].其中一些变化可能是由于肺叶之间基线重塑的变异性,以及与其他队列研究对象选择的变异性造成的。我们还观察到,在ASM对BT的反应中,患者之间存在高度的可变性。然而,尽管存在这些因素,但观察到的ASM减重的总体幅度与之前的报告中给出的相似,这给了观察到的变化是真实的可能性提供了信心。最后,我们的英国电信体内学习太小,无法确定观察到的气道重塑的变化是否涉及未来的临床风险,如恶化。确定这需要大的前瞻性研究或报告的BT活检研究的荟萃分析。
总之,我们的体内数据支持支气管活组织检查中的ASM质量降低,但我们的结合体外和在网上建模表明,ASM质量降低的程度不能完全通过ASM后热损伤的直接急性效应来解释。虽然我们不能排除有助于重塑的Peri-proplation indnisolone的可能性,但在所有程序之前施用泼尼松龙,并且重要的是,其对上皮的影响是不一致的,并且先前没有对ASM群众的影响[30.].因此,我们的数据挑战了BT潜在机制的当前概念,表明除了直接热损伤之外的替代机制可能有助于该过程。上皮完整性也显示出对BT的反应增加,并且薄层丙虫中的BT肌纤维细胞数与ASM质量相反。响应于热损伤和/或ASM和肌纤维细胞之间的动态相互作用的上皮修复是否对BT相关的降低的ASM质量仍有待确认的影响。是否可以优化BT协议以靶向特定的气道或气道重塑元件,也许与患者特异性建模组合以促进精确药物,需要进行研究。
补充材料
致谢
作者要感谢奥利弗·詹森、伊恩·琼斯和蒂莫西·韦特对手稿的建议和评论;鼓励所有AirPROM联盟成员在研究的各个阶段进行讨论;以及达文德·考尔和迈克尔·比德尔的协助体外实验。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
作者捐款:I.L.Chernyavsky和B.S.布鲁克参加了数学模型设计;I.L.Chernyavsky进行了数值模拟;I.L.Chernyavsky,r.m.桑德斯,G.E.莫里斯,F.R.A.J.玫瑰,S. Siddiqui,B.S. Brook and C.E. Brightling conceived the experimental model; R.M. Saunders and G.E. Morris conducted体外实验;I.L. Chernyavsky、R.J. Russell和R.M. Saunders进行了统计数据分析;R. Berair, A. Singapuri, A. h . Mansur, P. h . Howarth, P. Dennison, R. Chaudhuri, S. Bicknell, S. Siddiqui和C.E. Brightling协调了临床试验和程序;R. j . Russell, R. Berair和L. Chachi分析了患者活检数据;I.L. Chernyavsky、R.J. Russell、R.M. Saunders、S. Siddiqui、B.S. Brook和C.E. Brightling解释了研究结果并准备了手稿。所有作者阅读并批准了最终的手稿。
年代upport statement: The work was part supported by AirPROM 7th EU Framework grant 270194 (all authors), Medical Research Council (MRC) grant MR/N011538/1 (I.L. Chernyavsky), MRC grant MR/M004643/1 (B.S. Brook), Wellcome Trust Senior Fellowship WT082265 (C.E. Brightling) and by National Institute for Health (NIHR) Leicester Biomedical Research Centre. The views expressed are those of the authors and not necessarily those of the NHS, the NIHR or the Department of Health. Funding information for this article has been deposited with theCrossRef Resder注册表.
利益冲突:r.m.桑德斯在研究期间报道了来自第7欧盟框架,惠康信托和国家健康研究所的授权。
利益冲突:A.H. Mansur已获得阿斯利康制药的教育资助,用于服务支持,并获得诺华、葛兰素史克、阿斯利康、纳普制药、勃林格殷格翰等公司的演讲、顾顾团贡献和会议出席费用。
利益冲突:P.H.在研究期间,罗湖报告欧盟(AirProm协作授权)的赠款。
兴趣冲突:R. Chaudhuri提出的报告是Glaxosmithkline,Astrazeneca,Teva制药行业和诺华州的咨询委员会成员,以及从诺华学院接受教育补助金;收到由Glaxosmithkline,Astrazeneca,Chiesi组织的会议发言,以及参加由Novartis,Teva制药行业,Astrazeneca和Boehringer Igelheim赞助的国际会议。
利益冲突:S. Siddiqui报告Astazeneca和Boehringer Ingelheim的顾问委员会参与的个人费用,从Novartis的咨询/咨询,来自Novartis的演讲者费用,咨询咨询/咨询,来自Napp Pharmaceuticals的哮喘和发言者费用的成像研究从欧洲呼吸协会,在188bet官网地址提交的工作之外。
Conflict of interest: C.E. Brightling has received, paid to his institution, grants and consultancy fees from GlaxoSmithKline, Novartis, Chiesi, MedImmune/AstraZeneca, Boehringer Ingelheim, MSD Pharmaceuticals, PrEP Biopharm, Vectura, Teva Pharmaceutical Industries, Sanofi, Regeneron and Roche/Genentech.
利益冲突:I.L.Chernyavsky在研究期间,从欧洲委员会(FP7 Airprom)和医学研究委员会(新调查员研究资助)的批准者,Chernyavsky报告研究团契支持。
- 已收到2017年8月17日。
- 接受2018年3月29日。
- 版权所有©ers 2018
这篇ERJ开放文章是在知识共享署名许可证4.0的条188滚球软件款下开放存取和发布的。