摘要
肺结核(TB)的诊断可能会延迟,直到培养结果可用。
我们确定了逐步诊断算法的准确性,GeneXpert从痰和/或支气管肺泡灌洗(BAL)快速诊断肺结核结核分枝杆菌-在德国临床转诊中心对疑似肺结核患者进行特异性BAL ELISPOT检测。
166例假定诊断为肺结核的患者中,81例确诊为肺结核结核分枝杆菌痰液和/或BAL培养。在81例病例中,66例(81.5%)患者最初有结核分枝杆菌GeneXpert从痰液中检测;此外,81例患者中有6例(7.4%)经GeneXpert诊断为BAL液(共72例(88.9%))。在其余9例痰液和BAL GeneXpert结果阴性的患者中,BAL ELISPOT正确识别了8例培养确认的结核病患者(到培养阳性的中位时间为26天)。在>4000个早期分泌抗原靶点-6或培养滤液蛋白-10特异性干扰素-γ产生淋巴细胞的截止点为1 000 000个淋巴细胞时,BAL ELISPOT对活动性结核病的特异性为97%。
在结核病发病率低的国家,使用GeneXpert和BAL ELISPOT的逐步策略,几乎所有活动性肺结核患者都可以在临床表现的头几天内被识别出来。
摘要
当两种诊断方法结合使用时,几乎所有活动性肺结核患者都可以被迅速识别出来http://ow.ly/vinu30j5Yk7
简介
根据世界卫生组织的数据,2016年全球新发结核病病例为1040万例[1].结核病的早期诊断对避免结核病的传播至关重要结核分枝杆菌.结核分枝杆菌培养仍然是结核病诊断的金标准,但平均需要2-5周才能获得培养结果[2,3.].通过痰涂片显微镜检测抗酸杆菌(AFB)是一种广泛使用的廉价筛查试验,用于推定诊断为肺结核的患者。然而,在所有通报病例中,痰涂片阳性的比例<50% [4].此外,显微镜不能区分结核分枝杆菌来自其他分枝杆菌种类。核酸扩增技术如GeneXpert (Xpert MTB/RIF;造父变星,Sunnyvale, CA, USA)具有短时间<2小时的结果,对检测具有高度敏感性和特异性结核分枝杆菌AFB涂片阳性样本的DNA。然而,对于涂片阴性病例,GeneXpert诊断肺结核的敏感性下降至<70% [5].因此,在GeneXpert最初调查时,仍有15%的成年肺结核患者未被发现。
在与抗原提呈细胞接触后,结核分枝杆菌-特异性t细胞在局部淋巴结中扩增,并迁移到感染部位,在那里它们分化为效应t细胞[6- - - - - -8].在失去特殊的表型t细胞表面标记物后,这些细胞群可能无法重新进入血液,并在疾病部位变得丰富。9,10].相比之下,检测结核分枝杆菌-特异性效应t细胞在外周血中的检测结核分枝杆菌-特异性效应t细胞通过干扰素(IFN) γ释放试验在感染部位具有很高的诊断活动性结核病的准确性,即使AFB和结核分枝杆菌在支气管肺泡灌洗液等本地样本中无法检测到DNA [11- - - - - -15]、胸腔积液[16,17],心包液[18]、脑脊液[19]或腹水[20.].ELISPOT检测结果可在24小时内获得。
为了确定诊断的准确性,GeneXpert逐级检测痰液或BAL结核分枝杆菌-特异性BAL ELISPOT用于活动性肺结核的快速诊断,我们前瞻性地招募了在德国临床结核病转诊中心推定诊断为肺结核的患者。
方法
研究参与者
我们对2011年11月至2016年6月期间在德国Borstel研究中心医疗诊所接受治疗的所有患者(年龄≥17岁)进行了前瞻性分析,这些患者表现出提示肺结核的症状和/或胸部x线照片。入院前2年内接受过结核病治疗的患者和肺外结核病患者被排除在研究之外。作为初步诊断,对多达三个痰样本进行痰涂片镜检和/或GeneXpert检查。涂片未检测到AFB和/或阴性结核分枝杆菌-痰液特异性核酸检测、支气管镜及BAL检查均按国家指南进行[21].混合的BAL被分为两等份:一等份用于ELISPOT,另一等份被送往Borstel的国家分枝杆菌参考中心进行BAL镜检、GeneXpert和培养。研究流程图见图1.

研究流程图。结核病:肺结核;BAL:支气管肺泡灌洗;百慕大:结核分枝杆菌.
该研究得到了Lübeck大学伦理委员会的批准(14-031A)。报告遵循标准准则[22].
GeneXpert
根据国家分枝杆菌参考中心的制造商指南,对痰液和BAL进行GeneXpert检查[23].
结核分枝杆菌特殊技能ELISPOT
结核分枝杆菌如前所述,对外周血单个核细胞(pbmc)和BAL细胞(BALCs)进行特异性ELISPOT [12].的结果结核分枝杆菌如果在早期分泌抗原靶(ESAT)-6孔或培养滤液蛋白(CFP)-10孔中观察到5个以上的斑点形成细胞(SFCs),减去阴性对照孔中的SFCs数量,并且ESAT-6或CFP-10孔中的SFCs总数至少是阴性对照孔中的SFCs数量的两倍,则认为特异性ELISPOT阳性。如果不符合阳性结果的定义,并且阳性对照(抗cd3,克隆X35, 10 ng·mL)中的SFCs数量为阴性,则认为结果为阴性−1;Beckman Coulter, Krefeld, Germany)在减去阴性对照组井中的SFCs数量后,如果阳性对照组的SFCs数量至少为阴性对照组井的两倍,则为>20个SFCs。不确定结果被定义为不符合阳性或阴性检测结果的标准。由于BAL中细胞数量有限,一些ELISPOT测试在每孔中使用少于250000个细胞进行;这些结果以每孔250000个细胞归一化。
流式细胞术测定淋巴细胞群
为了调整血液和灌洗液中淋巴细胞的不同百分比,在FACSCalibur流式细胞仪上获得了50万个pmcs或BALCs (BD生物科学,海德堡,德国)。通过pbmc或BALCs群体中淋巴细胞的百分比来推断每孔每25万个细胞中的SFCs到血液或BAL标本中的100万个淋巴细胞[12].招聘结核分枝杆菌通过将BALCs中每100万个淋巴细胞中SFCs的数量除以外周血中每100万个淋巴细胞中SFCs的数量来计算肺特异性淋巴细胞。如前所述,如果分母上没有sfc,则赋值为0.1 [12,24].
统计分析
使用Stata版本14 (StataCorp, College Station, TX, USA)和CATmaker版本1.1(循证医学中心,牛津,英国)进行统计分析。Mann-Whitney u检验用于比较连续变量组。使用受试者工作特征(ROC)曲线分析选择截止点。显著性水平设为α=0.05。
结果
2011年11月1日至2016年6月30日期间,有412名推定或确诊为结核病的患者被Borstel研究中心医疗诊所收治。其中196名患者已被确诊为肺结核。另有50名患者被诊断为肺外结核。这些患者被排除在外。其余166名患者因疑似肺结核入院,其中66名患者通过痰液GeneXpert阳性结果进行了初步诊断的微生物学确认。其余100名患者的结核诊断不能通过痰涂片镜检和痰GeneXpert确诊,但肺结核仍然是鉴别诊断的一部分,他们接受了支气管镜和BAL检查。
这100例患者的中位年龄(四分位数范围(IQR))为52.0(35.5-63.0)岁,61例(61%)为男性。
一名培养确诊的结核病患者和一名非结核病患者的艾滋病毒检测呈阳性。
每100名患者中有15人经培养确诊为结核病。6例培养确诊的结核病患者(40%)通过BAL GeneXpert阳性结果快速诊断为结核病(其中2例在BAL镜检上也可检测到AFB;4例BAL中未检测到AFB)。因此,100名痰液和BAL显微镜和GeneXpert检测结果阴性的患者中有9人(9%)经培养确诊为结核,培养阳性的中位(IQR)时间为26天(16.5-34.5)。患者特征见表1.
在接受支气管镜检查的100例患者中,4例被诊断为非结核分枝杆菌(NTM)肺部感染。2例患者BAL中有AFB证据,GeneXpert未检测到结核分枝杆菌;从这些患者的培养中鉴定出的分枝杆菌种类为鸟型分支杆菌而且分枝杆菌simiae.2例BAL镜检阴性和GeneXpert BAL培养阳性分枝杆菌xenop我而且分枝杆菌kansasii.其余81例患者的样本未显示分枝杆菌生长。接受支气管镜检查但最终诊断为没有肺结核的患者的患者特征和最终诊断的细节显示在补充表S1.
PBMC和BALC elisa试剂盒
在100名推定诊断为肺结核的患者中,有一人在pmcs中有不确定的检测结果。1 / 100(1%)的PBMC ELISPOT阳性对照失败。100例中有5例(5%)BALC elisa pot不确定:2例阴性对照失败,3例阳性对照失败。根据制造商对阳性检测结果的定义,在有效检测结果的患者中,PBMC和BALC ELISPOT阳性的患者分别为62 / 99(62.6%)和40 / 95(42.1%)。62例PBMC ELISPOT阳性患者中34例(54.8%)和40例BALC ELISPOT阳性患者中25例(62.5%)可以排除活动性结核病。15例培养确诊肺结核患者中,PBMC ELISPOT阳性14例(93.3%),阴性1例(6.7%)。BALC ELISPOT阳性15例(100%)。
对于培养证实的肺结核患者,PBMC ELISPOT的敏感性为93% (95% CI 81-100%),特异性为50% (95% CI 38-62%),而当使用制造商对PBMC阳性和阴性检测结果的定义时,BALC ELISPOT的敏感性为100%,特异性为77% (95% CI 67-87%)。
表2显示了9例AFB阴性和BAL中GeneXpert阴性的培养确诊肺结核患者的所有个体检测结果。给出培养确诊肺结核患者和非肺结核患者PBMC和BALC ELISPOT阳性或阴性配对结果的数量补充图S1.
感染部位抗原特异性SFCs的浓度
在培养证实的肺结核患者中,ESAT-6的中位SFC计数为25(6.3-210)/ 25万pbmc, CFP-10的中位SFC计数为53.8(22.5-177)/ 25万pbmc。ESAT-6的BALC ELISPOT中位数(IQR)升高到295(52.5-489)个SFCs / 250000 BALCs, CFP-10升高到160(61-453)个SFCs / 250000 BALCs。相比之下,ESAT-6无结核患者的中位数(IQR)为3.8(0.1-17.5)/ 25万pbmc, CFP-10为4.3(0.1-16.9)/ 25万pbmc,而在BAL中,ESAT-6和CFP-10的中位数都很低,每25万BALCs为0 sfc。图2而且补充图S1显示培养证实的结核病患者中25万个pbmc和BALCs中sfc的数量,但显微镜下无法检测到AFB,与排除结核病的患者相比,GeneXpert结果为阴性。
早期分泌抗原靶点(ESAT)-6-和培养滤液蛋白(CFP)-10特异性外周血单个核细胞(pmcs)和支气管肺泡灌洗细胞(BALCs)的斑点形成细胞(SFCs)的数量,在排除结核病的个体(非结核病)和培养确认的肺结核患者中,显微镜下无法检测到抗酸杆菌和GeneXpert阴性结果(n=9)。建议的临界值为每250000个细胞>50个SFCs。
感染部位抗原特异性淋巴细胞浓度
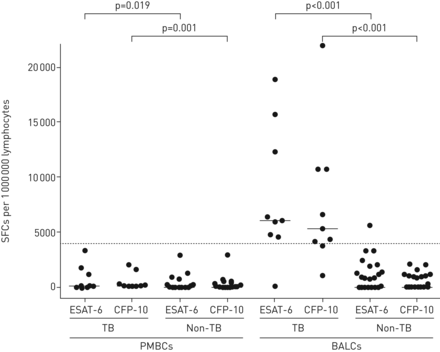
为了考虑个体间淋巴细胞百分比的差异,对100万个淋巴细胞的pbmc和BAL中的SFC结果进行归一化。在培养证实的肺结核患者中,外周血中抗原特异性淋巴细胞的中位数(IQR) ESAT-6为121 (43.9-1228.8)SFCs, CFP-10为270 (109.8-1363.8)SFCs,而在BAL中,ESAT-6的中位数(IQR)为6370 (4595.2-14 541.7)SFCs, CFP-10为6598.5 (3857.7-13 503.7)SFCs。相比之下,诊断为非结核的患者ESAT-6-的中位数(IQR)为25.5 (0.8-99.9)SFCs, cfp -10特异性淋巴细胞的中位数(IQR)为27 (0.7-93.8)SFCs,而BAL患者ESAT-6-的中位数(IQR)为0 (0 - 0)SFCs, cfp -10特异性淋巴细胞的中位数(IQR)为0 (0 - 0)SFCs / 1000000淋巴细胞。图3而且补充图S2显示培养证实的结核病患者的pbmc和BALCs中每100万个淋巴细胞中SFCs的数量,但AFB显微镜检查/ GeneXpert结果阴性与非结核病患者相比。
早期分泌抗原靶点(ESAT)-6-和培养滤液蛋白(CFP)-10特异性外周血单个核细胞(pmcs)和支气管肺泡灌洗细胞(BALCs)每100万个淋巴细胞中的斑点形成细胞(SFCs)的数量在排除结核病的个体(非结核病)和培养确认的肺结核患者中,显微镜下无法检测到抗酸杆菌和GeneXpert阴性结果(n=9)。建议的截断值为每100万个淋巴细胞>4000个SFCs。
活动性结核病与非结核病的区分
为了提高非结核患者与培养确诊但镜检未检测到AFB且BAL的GeneXpert结果为阴性的结核病患者之间的区别,研究了不同的截断值。从250000个BALCs中截断ESAT-6或cfp -10特异性细胞的>50个SFCs可提供100%的敏感性和91%的特异性(95% CI 84-98%)。考虑到淋巴细胞的比例,每100万个BAL淋巴细胞中对ESAT-6或CFP-10切断>4000个抗原特异性淋巴细胞的敏感性为89% (95% CI 68-100%),特异性为97% (95% CI 93-100%)。为考虑BAL和外周血中淋巴细胞的百分比不同,定义招募因子为BALCs中sfc / PBMCs中sfc乘以淋巴细胞因子(PBMCs中淋巴细胞百分比/ BALCs中淋巴细胞百分比)。ESAT-6或CFP-10招募因子≥6的敏感性为67% (95% CI 36-97%),特异性为83% (95% CI 74-92%)。
区分非结核患者与培养确诊但镜检未检测到AFB且GeneXpert阴性的结核患者亚组的ROC曲线下面积(AUC), ESAT-6和CFP-10特异性BALCs分别为0.968和0.985,而pmcs的AUC为ESAT-6为0.760,CFP-10为0.841。当仅评估来自BALCs的100万个淋巴细胞时,ESAT-6的AUC为0.973,CFP-10的AUC为0.978。
表3显示了使用这些不同的截断点ELISPOT在balc上的性能。补充图S3显示各auc的曲线图。
综上所述,在166例假定诊断为肺结核的患者中,该诊断由结核分枝杆菌81例(48.8%)。81人中有66人(81.5%)最初的痰检结果为阳性,另外81人中有6人(7.4%)由BAL GeneXpert诊断(共72人(88.9%))。在显微镜和GeneXpert检查痰液和BAL阴性结果的81例患者中,有8例(88.8%)的BAL ELISPOT能正确识别培养证实的结核病患者,特异性为97%。
GeneXpert (2 h)和BAL ELISPOT对BAL GeneXpert检测结果阴性的患者进行逐步分析,快速诊断肺结核的综合敏感性和特异性分别为98.8%和97.6% (表4).
讨论
我们评估了逐步方法的准确性,包括初始分子测试,即。GeneXpert,后面跟着a结核分枝杆菌特异性BAL elisa试剂盒用于肺结核诊断。依次应用BAL GeneXpert和BAL ELISPOT对痰涂片阴性和GeneXpert阴性肺结核的诊断准确率为97%。诊断结果在送到医院的头几天内就出来了。
GeneXpert极大地改善了结核病的诊断。如果对两种不同的痰样本进行GeneXpert检测,90%的成年肺结核患者在就诊的头几天内就能被GeneXpert正确识别[25].然而,GeneXpert对痰涂片阴性和肺外结核的敏感性较低[25,26].如果GeneXpert检测结果为阴性,患者可能会在几周内未被诊断,直到检查结果结核分枝杆菌培养成为可能。
结核分枝杆菌在BAL细胞上进行的特异性ELISPOT能够缩小这一诊断差距。在过去的十年里,一些研究表明结核分枝杆菌-特异性ELISPOT对来自疾病部位的标本进行检测,如。结核性肺泡囊,结核性胸膜炎或结核性心包炎的胸膜或心包积液,结核性腹膜炎的腹水,结核性脑膜炎的脑脊液[27- - - - - -30.],可提高结核病少菌病的检出率,但GeneXpert和ELISPOT逐步法的附加价值目前尚未被研究。
在活动性结核病中,结核分枝杆菌-特异性淋巴细胞从血液中被招募到受疾病影响的器官[31,32].活动性疾病的可能性随着浓度的增加而增加结核分枝杆菌与外周血相比,感染部位的特异性细胞[24].H土et al。[33]提示BAL中SFCs /血液中SFCs的比例,并以>1为临界值。然而,需要考虑到淋巴细胞在外周血中占主导地位,而BAL中的比例则低得多[34].通过计算血液和BALCs之间ESAT-6和CFP - 10特异性t细胞的淋巴细胞依赖招募因子,或将每250000个细胞的sfc归一化至1000000个淋巴细胞,应分别承认pbmc和BALCs中淋巴细胞百分比的这些差异[11,24].
本研究以BAL中每100万个淋巴细胞截断>4000个淋巴细胞为最佳结果。当应用这一临界值时,可以以89%的敏感性和97%的特异性识别出少杆菌性肺结核患者。这一临界值提供了98%的极好的阴性预测值和28.9的高阳性似然比。
与大多数来自结核病发病率低的国家的研究一样,我们的研究受到培养证实的活动性结核病患者的样本量的限制,而痰液和BAL的GeneXpert结果为阴性。进行BAL ELISPOT和流式细胞术也明显更加劳动密集型,需要比自动化更多的技术人员时间结核分枝杆菌-GeneXpert核酸特异性扩增。然而,在结核病发病率低、经济资源充足的国家,当痰涂片镜检和痰GeneXpert分析结果为阴性时,大多数被怀疑患有肺结核的患者将接受支气管镜检查,并排除其他疾病,如结节病、隐源性组织肺炎、肺癌等。此外,研究结果不能推广到结核病高负担国家,这些国家反复暴露于结核病结核分枝杆菌可能改变BAL ELISPOT反应[14]和ELISPOT的性能将受到实验室能力有限的挑战。
由于GeneXpert在呼吸标本上对肺结核的高度敏感性,其性能结核分枝杆菌-特异性BAL ELISPOT可局限于痰液和BAL的GeneXpert结果为阴性且仍需考虑活动性肺结核鉴别诊断的患者。
总之,在结核病发病率低的县,通过使用GeneXpert和BAL ELISPOT的逐步检测策略,几乎所有活动性肺结核患者都可以在临床表现的最初几天内被识别出来。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充表S1erj - 02189 - 2017 - _table_s1
补充图S1。抗酸杆菌镜检不出、GeneXpert阴性的培养确诊肺结核(TB)患者(上)与酶联免疫斑点法(ELISpot)排除结核(非结核)后其他诊断患者(下)早期分泌抗原靶点(ESAT)-6-和培养滤液蛋白(CFP)-10特异性外周血单个核细胞(PBMC)和支气管肺泡灌洗单个核细胞(BALC)斑点形成细胞(SFC)的比较。erj - 02189 - 2017 - _fig_s1
补充图S2。培养确诊肺结核(TB)和显微镜下检测不到抗酸杆菌、GeneXpert MT/B/RIF阴性(上)和酶联排除肺结核(非结核)后其他诊断患者(下)外周血(blood - ly)或支气管肺泡灌洗液(ball - ly)中早期分泌抗原靶(ESAT)-6-和培养滤液蛋白(CFP)-10特异性淋巴细胞(SFC)的斑点形成细胞(SFC)我mmunospot (ELISpot).erj - 02189 - 2017 - _fig_s2
补充图S3。培养滤液蛋白(CFP)-10特异性支气管肺泡灌洗细胞(BALC)的ROC曲线下区分非结核患者与培养确诊肺结核患者的面积。募集因子(Rec)为BALC中的斑点形成细胞(SFC) /外周血单个核细胞(PBMC)中的斑点形成细胞(SFC)乘以PBMC中的淋巴细胞百分比/ BALC中的淋巴细胞百分比。比值(ratio)计算为BALC中的SFC除以PBMC中的SFC。结果每250000个BALC(250个细胞)或1000000个bal -淋巴细胞(1000个Ly)表达。erj - 02189 - 2017 - _fig_s3
确认
作者感谢国家分枝杆菌参考中心(Borstel,德国)的工作人员,特别是Birgit Voss和Kerstin Klein对分枝杆菌培养结果的行政支持,以及Cordula Ehlers和Dagmar Schaub(临床感染性疾病,Borstel,德国)对数据库的支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:J. Heyckendorf在提交的工作之外,在Chiesi、Gilead、Janssen、Lucane和Hain的赞助研讨会上接受了独立于赞助商的讲座的个人费用。C. Lange在提交的工作之外,在基耶西、吉利德、艾伯维、MSD、Becton Dickinson、杨森、Lucane、诺华和赛默飞世尔的赞助研讨会上接受了赞助商独立讲座的个人费用。B. Kalsdorf在提交的工作之外,在牛津免疫中心和Lucane赞助的研讨会上接受了独立于赞助商的讲座的个人费用。
支持声明:C. Lange和J. Heyckendorf得到了德国感染研究中心(DZIF)的支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2017年10月24日。
- 接受2018年3月14日。
- 版权所有©ERS 2018