摘要
欧洲慢阻肺患者管理试验(COMET)调查了一种基于家庭的慢阻肺疾病管理干预对严重慢阻肺患者的有效性和安全性。
该研究是一项国际开放设计的COPD患者临床试验(1秒用力呼气量<预测值的50%),以1:1的比例随机分为疾病管理干预组或研究中心的常规管理实践组。疾病管理干预措施包括自我管理方案、家庭远程监测、护理协调和医疗管理。主要终点是意向治疗(ITT)人群的非计划全因住院天数。次要终点包括急性护理住院天数、BODE(身体质量指数、气流阻塞、呼吸困难和运动)指数和病情加重。安全终点包括不良事件和死亡。
在符合ITT分析条件的157例(疾病管理)和162例(常规管理)患者中,每年全因住院天数(平均±sd)分别为17.4±35.4和22.6±41.8(平均差值为- 5.3,95% CI为- 13.7 ~ - 3.1;p = 0.16)。疾病管理组每年按方案急性护理住院天数更少(p=0.047), BODE指数更低(p=0.01),死亡率更低(1.9%)与14.2%;P <0.001),加重频率无差异。不同国家的患者情况和住院做法有很大差异。
COMET疾病管理干预并未显著减少非计划全因住院天数,但减少了严重COPD患者的急性护理住院天数和死亡率。
摘要
在以家庭为基础的多成分疾病管理方案中降低全因死亡率vs重度COPD的常规护理http://ow.ly/sykh30gS5XO
简介
慢性阻塞性肺病(COPD)是一种可治疗的疾病,严重影响日常生活,影响超过10%的40岁以上成年人[1].重度至重度COPD患者健康状况较差[2]、更高的住院恶化风险、更高的急性护理负担[1,3.],死亡率高于轻至中度疾病患者[4- - - - - -7].TIOSPIR (Tiotropium Safety and Performance in Respimat)试验也显示了这一点,其中GOLD(全球阻塞性肺疾病倡议)C或D患者的呼吸相关死亡和住院病情加重的风险比GOLD A患者更大[8].更好地控制病情加重频率和严重程度可减缓疾病进展并减少住院治疗[9,10],特别是对于在日常生活中难以控制病情的严重慢性阻塞性肺病患者。
COPD患者及其家属有义务承担日常护理的责任,必须承担大部分的护理负担。重要的是,患者必须学会如何应对疾病,认识到何时需要专业护理,采取健康的生活方式,避免病情恶化和住院的可改变风险因素。为了填补这一护理空白,在临床试验中研究了许多自我管理方案[11- - - - - -17].尽管这些研究的方案和结果差异很大,从而使最有效策略的确定复杂化,但重要的方案考虑因素包括COPD严重程度、患者共病以及对患者个人目标的灵活性[18].有效的自我管理方案侧重于病人教育、行为改变、通过卫生专业人员的指导激励病人,以及在需要时迅速获得医疗保健[11,19,20.].
COPD患者管理欧洲试验(COMET)是一项国际随机对照临床试验,用于调查专门适用于严重COPD患者的多组分家庭COPD疾病管理干预措施的有效性、安全性和成本效益与通常的病人管理[21].COMET方案的设计是很好地整合和连贯,并仔细调整患者的需要和疾病严重程度。这是通过综合护理方法实现的,包括:标准化的自我管理方案和训练有素的病例管理员的指导;通过电子保健平台进行密切的家庭监测和护理协调,以便早期发现病情恶化;以及反馈和质量控制,以优化干预措施的交付[22].据假设,以家庭为基础的疾病管理干预措施将帮助患者采取必要的应对行为,从而避免一些住院治疗,并减少其他人的住院时间。
方法
病人
年龄≥35岁的COPD患者符合入选条件,前提是:支气管扩张剂后1秒的强迫呼气量(FEV)1)/用力肺活量(FVC)比值≤70%;一个FEV1<预测值的50%;吸烟史≥10包年;而且前一年至少有一次严重恶化。患者可以接受所有相关的COPD治疗,包括长期氧疗(LTOT)和家庭机械通气(HMV)。在招募研究者看来,患者不符合以下条件:预计生存时间不超过6个月;不能阅读或说该国语言或患有认知/精神疾病;连续治疗>,每天10毫克强的松或同等药物,持续6周以上;或者住在养老院。
研究设计
COMET是一项随机、开放设计、平行组试验,在法国(12个中心)、德国(8个)、意大利(6个)和西班牙(7个)的33个中心进行,并在一篇包括研究方案的方法论文中进行了描述(补充材料) [21].简而言之,严重COPD患者被以1:1的方式随机分组,仅通过常规护理和随访(UM组)进行管理,或在常规护理和随访之外接受基于家庭的多成分COPD疾病管理干预(DM组)。在3- 5周的适应期内评估每位入选患者的呼吸和整体健康状况,然后在随后的12个月期间进行随访。在随访期间,要求患者每3个月进行一次医院访视,并在访视期间由医院工作人员通过电话联系,以使用标准化脚本收集医疗保健使用信息。本研究的伦理操守已于先前描述[21].所有患者均提供书面知情同意书。在研究期间,对方案进行了修订,以加速招募并允许研究完成(补充材料).
根据研究前由部分最小化计算机算法在研究发起人的监督下生成的预先指定的随机列表,将患者按1:1的方式分配到各个组。每个中心的研究人员通过一个基于电话的交互式语音应答系统,按顺序给患者分配一个随机数字。随机分组按吸烟状况(现在或以前)、是否需要呼吸辅助(不需要,或在LTOT和/或HMV)和中心进行分层。出于实际原因,这项研究是开放的;患者和研究人员都对COPD管理策略不知情。
多组分家庭疾病管理干预和常规护理
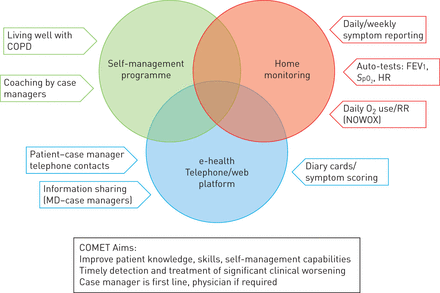
COMET以家庭为基础的疾病管理干预措施包括自我管理方案、家庭监测和电子健康电话/网络平台(图1) [21].
COMET的多组分家庭疾病管理干预。在COMET的疾病管理部门[21],患者接受了基于“COPD患者健康生活”自我管理计划(www.livingwellwithcopd.com) [13]来自comet培训的病例管理人员,他们是熟悉以家庭为基础的干预和慢性患者护理的卫生保健专业人员。该计划的主要方面包括:1)病例管理人员对患者进行教育和激励,目标是获得可持续的自我管理技能和行为改变;2)预防病情恶化的行动计划,包括在症状恶化时采取的决策和行动。患者在症状恶化时主动通报健康状况更新,或至少每周通报一次。信息被自动转发到电子健康网络平台,该平台登记了健康、恶化或警报状态。对于症状恶化或报警状态,病例管理员联系患者确认症状状态。已确认的报警状态提交调查人员进行当日医疗评估和随访。患者还自我监测1 s的用力呼气量(FEV)1)、用脉搏血氧计测量动脉氧饱和度(年代阿宝2)和心率(HR)。对于长期氧疗的患者,使用NOWOX在线监测仪记录每日耗氧量和呼吸频率(RR)。COPD:慢性阻塞性肺病。
自我管理方案是基于加拿大蒙特利尔的麦吉尔大学卫生中心蒙特利尔胸科研究所制定的“COPD患者良好生活”方案(www.livingwellwithcopd.com) [13].对原方案进行了调整,以考虑到COPD的严重程度和氧气使用量增加,并考虑到每个国家的具体语言、文化和医疗做法。家庭监测包括患者通过电话问卷传递健康状况信息,每周至少一次,每天患者开始出现症状恶化。电子健康电话/网络平台使病例管理人员能够及时随访患者,以便早期发现潜在的恶化和症状恶化。信息已传递给医院的医生通过在必要时协调医疗保健和早期治疗的网络平台。医生在用药方面做出所有决定,以减少不适当用药的风险。
UM(对照组)组接受了每个研究中心使用的常规或常规COPD护理和患者随访实践。个别地盘的一般管理措施(如.在患者纳入期开始和结束时收集中心特定的COPD教育手册或项目信息(如有)。
所有LTOT患者均使用NOWOX医疗设备(法国巴黎液化空气公司)进行监测,记录每日耗氧时间和呼吸频率。
结果
主要结局是每个随机患者的非计划全因住院天数,正常化为1年的随访。住院天数包括如果住院后没有回家,则随后在护理机构住院。由于住院决定可能受制于当地惯例、社会考虑因素、床位可用性等,所有住院都由一个独立的三人终点验证委员会(EVC)进行审查,以评估每次住院的原因和适当性,确定住院是否符合方案定义,并确定在疗效评估中考虑的程度(完全、部分、完全)。
支持性住院结局为COPD加重在急性护理病房的非计划全因住院天数(不包括在护理机构的天数);EVC证实了这一点。
次要结局包括:COPD加重次数(轻度:症状恶化;中度:需要抗生素或皮质类固醇治疗;严重:导致住院和/或死亡);6分钟步行距离(6MWD);BODE(身体质量指数、气流阻塞、呼吸困难及运动)指数及其独立组成部分[23];焦虑和抑郁,按医院焦虑和抑郁量表(HADS)评估[24];和健康状况,由圣乔治呼吸问卷(SGRQ-C)的copd特定版本评估[25].
安全性结果包括不良事件、严重不良事件和死亡。
医学-经济结果包括总成本、成本效益和成本效用;他们的评价将分别发表。
统计分析
在意向治疗(ITT)人群(所有进入随访期的患者)中进行主要结局的初步分析。对每位患者符合既定标准的住院天数每年进行归一化,并使用非参数Wilcoxon秩和检验对两组进行比较。
在支持性分析中,以描述性和探索性的方式对每个国家的整个方案(PP)人群以及ITT和PP人群重复了主要结局的主要分析。对ITT和PP人群进行了主要结局的参数方差分析(ANOVA),以了解研究组和国家效应,以及组和国家之间的相互作用。用Wilcoxon秩和检验比较两组经EVC证实的非计划全因住院的平均年累计时间。所有其他次要疗效和安全性结果都是探索性的、完全描述性的,仅在ITT人群中进行分析。
计算样本量的主要目的是比较两组之间的非计划全因住院天数。根据之前的研究,DM组和UM组之间每年平均住院天数的差异为10天,共同标准偏差为25天[16].双侧I型误差设为α=0.05,幂为0.90,最小样本量估计为每组143例可评估患者。预计年辍学率为25%,至少前3个月的随访目标是每组153名患者。
结果
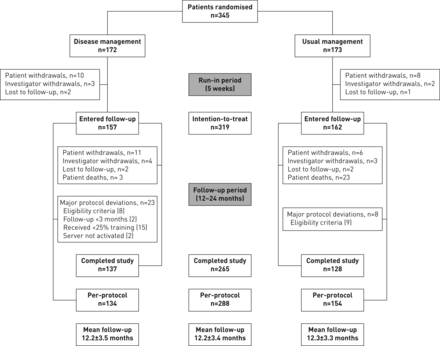
该研究于2010年9月至2015年3月期间进行。共有345名患者被随机分为DM组(n=172)或UM组(n=173) (图2).在法国招募患者(125例;36.2%),西班牙(94;27.2%),德国(82人;23.8%)和意大利(44;12.7%)。糖尿病组包括36.0%来自法国,26.2%来自西班牙,24.4%来自德国,13.4%来自意大利。UM组有36.4%的患者来自法国,28.3%来自西班牙,23.1%来自德国,12.1%来自意大利。在DM组和UM组中,分别有15例(9%)和11例(6%)患者没有完成最初的5周磨合期,ITT组中有157例(91%)和162例(94%)患者,其中137例(80%)和128例(74%)患者完成了至少12个月的随访。从PP人群中排除患者(DM组,n=134; UM group, n=154) for major protocol deviations, most of which involved unmet eligibility criteria or involved patients who had received less than 25% of the planned coaching sessions.
病人的流动和性情。参与研究的患者以1:1的方式随机分组,接受COMET多组分家庭疾病管理(DM)干预或在中心实施的常规管理(UM)。在进入随访期之前,随机分组的患者在5周的磨合期接受了DM或UM的培训和教育,随访期最初设定为2年,但通过方案修订减少到1年。在磨合期退出的患者可以由新患者替代。进入随访期的患者包括意向治疗(ITT)人群;随访期间无重大方案偏差的患者为每方案人群。在ITT人群中,DM组平均随访12.2个月,UM组平均随访12.3个月。协议偏差的总数显示在括号中。
患者人口统计和疾病特征
住院模式和主要结局
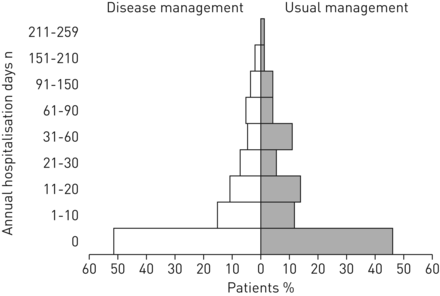
根据非计划全因住院天数,每组患者的分布相似(图3).半数患者在随访期间没有住院。对于住院的患者,最大的患者群体有1 - 10至11 - 20天的非计划住院天数。各组超长住院(> ~ 60天)患者数量相似。年非计划住院天数(平均±sd)各国家差异很大,西班牙最低,为9.7±22.7分,德国最高,为28.7±40.9分(补充表E1).
年化非计划全因住院天数的分布情况。意向治疗人群中每组患者根据他们每年报告的非计划全因住院天数进行分类。每组中约有50%的患者在研究期间没有计划外住院天数。两组中有相似数量的患者住院时间很长,家庭疾病管理组有3名患者,常规管理组有2名患者,住院时间在151-210天之间,无疾病管理组患者和2名常规管理组患者,住院时间在211-259天之间。
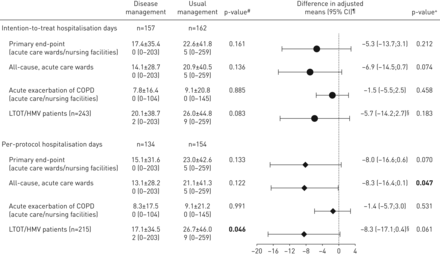
年非计划全因住院天数(平均±sdDM组为17.4±35.4,UM组(ITT人群)为22.6±41.8,中位数(四分位数范围)分别为0(0 ~ 203)天和5(0 ~ 259)天(图4).在主要非参数分析(p=0.161)中,组间差异不显著(- 5.3天,95% CI - 13.7至3.1;p = 0.212)。
按子类别和人群比较各组的年度计划外住院天数。在急性护理病房或护理设施中花费的非计划全因住院天数的年平均值和中位数显示了每个组的意向治疗和每个方案。还显示了仅在急性护理病房度过的非计划全因住院天数的年平均值和中位数;由于慢性阻塞性肺病(COPD)急性加重;以及接受家庭氧疗和/或家庭机械通气(LTOT/HMV)的患者。加粗的p值表示差异有统计学意义。数据以均数±表示sd,中位数(四分位范围),调整后的均值差异以95%置信区间表示。#:非参数Wilcoxon秩和检验;¶:除LTOT/HMV外,对平均值进行国家差异调整,并以年平均非计划住院天数作为响应变量进行方差分析比较;+:方差分析;§: LTOT/HMV患者的均值根据呼吸辅助需求进行调整,并以年平均计划外住院天数作为响应变量进行方差分析比较。
支持性住院治疗结果
evc确认的住院天数(平均±sd), DM组为15.5±32.9,UM组为20.8±38.8 (p=0.15, ITT),对于PP人群的主要终点(图4).PP人群在急症护理病房度过的非计划全因天数显著不同,国家调整平均值差异为−8.3天(95% CI为−16.4至−0.1;p = 0.047)。在两个研究组中,COPD加重的住院天数占非计划住院天数的50%以下,国家调整均值差异为- 1.5天(95% CI - 5.5至2.5;ITT公司,p = 0.46)。LTOT/HMV患者各研究组的全因住院天数均高于总体研究人群,但仅在PP人群的非参数比较中发现组间差异有统计学意义。在多因素回归分析中,只有每天LTOT≥15小时的需求是计划外住院的显著危险因素,风险比为2.55 (95% CI 1.17-5.57;p = 0.02)。
两组的非计划住院总人数相似(DM组,n=157;UM组,n=160),以及evc确定的这些入院的主要原因(补充表E2).慢性阻塞性肺病加重(69.1%)、肺炎(9.5%)和急性心力衰竭(4.4%)是住院最常见的主要原因。
二次结果
随访12个月后,两组患者病情加重的人数、频率和首次病情加重的时间相似(表2).糖尿病组中42.4%的患者BODE指数改善与UM组为30.6%。DM组基线调整后的平均BODE评分显著降低,差异为- 0.5 (95% CI为- 0.9至- 0.1;p = 0.01)。6MWD、SGRQ-C或HADS的其他次要结果组间无显著差异。在研究期间,糖尿病组更多的患者停止吸烟(p=0.02),平均每日LTOT的使用情况相似。
安全的结果
每组患者中经历至少一次不良事件的患者比例相似(~ 90%),其中大多数为COPD加重(表3).每组中约60%的患者经历了至少一次严重不良事件,最常见的是COPD加重、肺炎和急性心脏或呼吸衰竭。
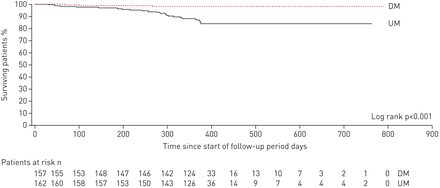
研究期间共有27例患者死亡,其中1例在随机分组前死亡。DM组的死亡率(3例,1.9%)明显低于UM组(23例,14.2%;p < 0.001;表3而且图5).DM组的3例死亡是由于呼吸衰竭、心肺呼吸骤停和外伤性气胸。UM组超过一半的死亡(13)归因于COPD加重;没有其他原因导致超过两人死亡。死亡患者(确定)的显著基线特征事后)为低FEV1(预测的35%),GOLD D类(84.6%),LTOT(84.6%),健康状况不佳(SGRQ-C平均得分63.7)和多种伴随疾病(平均4.3)(补充表E4).这些患者在研究期间也累积了大量的非计划住院天数(中位数为68.0天)。在一个事后多因素回归分析,基线BODE指数(p=0.03)和研究期间住院总天数(p<0.001)是死亡的显著独立预测因素。
患者死亡率的Kaplan-Meier分析。在研究的每一天,意向治疗人群的总体累积生存率都显示出来。每50天,每组中有风险的患者数量都会显示出来。在研究过程中,72名患者已经入组,通过修改方案,随访时间从2年缩短至1年。因此,部分患者随访时间超过1年。在研究期间,疾病管理(DM)组共有3例(1.9%)患者死亡,常规管理(UM)组共有23例(14.2%)患者死亡(p<0.001),主要原因是呼吸衰竭(16例死亡)。均值±sd该研究的死亡时间为236±111天。
COMET疾病管理干预和技能获取
总体而言,DM组100%的患者在磨合期间完成了所有四次初始的个人家庭指导课程,66.7%的患者实现了至少80%的计划电话和小组指导课程,89.7%的患者实现了至少80%的每周电话健康状况传输依从性。掌握28项管理技能(如.在第一次评估(75%的>患者完全掌握了8项技能)和最后一次评估(80%的>患者完全掌握了24项技能)之间,吸入技术、咳嗽技术、嘴唇收缩呼吸和身体定位、感觉更糟时应采取的行动)有所改善。
中心慢性阻塞性肺病管理常规实践
独立于COMET疾病管理干预措施而在两组中常规实施的COPD教育方案方面,中心的做法因国家和中心而有很大差异(补充表E3).总体而言,22.6%的中心为患者提供了教育小册子,18.8%的中心提供了COPD教育课程,40.6%的中心提供了锻炼计划。
讨论
虽然DM组患者的全因住院天数比UM组患者少23%,但一项横跨四个欧洲国家的新型多组分家庭COPD疾病管理干预措施在预定义的主要结局上没有实现统计学上的显著差异。PP人群的急性护理住院天数、12个月时BODE指数评分以及总死亡率,DM组均显著低于UM组。然而,由于这些是支持性或次要结果,旨在支持主要结果的解释,并且死亡率是一种安全结果,因此应谨慎考虑这些结果。
迄今为止,COPD自我管理干预在临床试验中的结果并不一致[26],这造成了关于自我管理干预措施的模糊,并阻碍了其在临床实践中的实施。最近,一组专家就慢性阻塞性肺病自我管理的概念定义达成了共识:“慢性阻塞性肺病自我管理干预措施是结构化的,但是个性化的,通常是多成分的,其目标是激励、参与和支持患者积极适应他们的健康行为,并培养技能以更好地管理他们的疾病”[19].回顾过去,COMET仍然应用了许多这些概念,并包括了质量控制来优化自我管理组件的交付。三分之二至90%的DM组患者接受了至少80%的计划指导次数,或80%的患者遵守了每周电话传递健康状况,大多数患者获得了疾病管理技能。对COPD患者的培训和教育是必要的,但还不够,必须成功地改变行为,以实现切实的利益[22,26].
虽然在许多支持性住院治疗结果中似乎存在研究组效应,但许多因素可能导致缺乏统计学意义。大约一半的患者没有住院,不到一半的住院天数是由于COPD加重,考虑到COPD严重程度高以及LTOT和/或HMV患者比例高,这两者都是意料之外的。DM组因COPD加重而住院的人数略高,这可以解释为DM组严重加重的平均次数略高,但不显著。统计效力基于两组之间10天的非计划住院天数的差异,标准差为25天;但实际差异仅为5.2天,标准差为>35天。这可能是因为四个国家的住院率和住院天数差异很大,这是由于各国在患者基线特征、住院做法、入院标准、资源和床位可用性以及医疗保健报销方案方面存在差异。例如,各国在医院床位供应方面存在很大差异,西班牙最低(297张/10万居民),德国最高(823张/10万居民)[27].这也与每年住院天数大致相关(补充表E1).也有可能我们高估了该患者群体的住院风险,如果我们纳入了由于合并症或COPD严重程度较高而住院风险较高的患者,则组间可能存在统计学上的显著差异。然而,由于这种不可预见的低住院率,COMET在统计上不足以检测非计划住院天数的显著差异,需要更大的样本量来弥补各国之间的这种差异。在设计COPD干预措施的未来研究时,应仔细考虑这些因素。
DM组的12个月死亡率(1.9%)显著低于UM组(14.2%),后者与12个月死亡率(12.5%)一致或低于UM组[28], 16.8% [29], 21% [30.]和>23% [31]以前曾报道过因慢性阻塞性肺病急性加重住院治疗的慢性阻塞性肺病患者。DM组的死亡率低于预期,UM组的死亡率没有过高,这表明疾病管理干预降低了死亡率。这可能是因为UM对照组的大多数死亡(56%)是由于COPD加重。疾病管理干预有可能通过成功优化病情恶化的自我管理,从而导致早期和及时的治疗,从而降低死亡率,这本可以防止包括死亡在内的其他并发症。干预措施的家庭监测方面可能也有助于干预措施的成功,因为它提供了一种向病例管理人员迅速传达症状和疾病严重程度变量的手段,这可能缩短了从病情恶化开始到采取适当治疗的时间。
在COMET中,死亡率作为一项安全性结果被仔细监测,因为疾病管理干预是在严重COPD患者中实施的,其中许多患者有多种合并症,死亡风险高。事实上,F一个et al。[15]由于自我管理组的死亡率过高而停止。COMET疾病管理干预措施与F一个et al。[15].COMET的重点是:密切的医患沟通;通过电子卫生系统定期传播症状,及时识别病情恶化;对病例管理人员进行全面培训和监测,在研究期间对他们进行跟踪以提高质量;还有负责所有用药决定的医生[21].相比之下,由于这项研究是在医疗资源有限的美国退伍军人管理局医院进行的,F一个et al。[15大多数护理决定都是由他们自己决定的。尽管医生告诉患者,如果他们需要开始治疗病情恶化,可以打电话来,但只有4.5%的人打电话来。此外,加重评估由专业人员完成,他们可能没有管理这类患者的经验。
COMET中所有的研究死亡病例都经过了发起人和EVC的仔细审查。虽然研究组之间的死亡率存在如此大的明显差异,本可以中断研究,但COMET的死亡率最终下降幅度如此之大是预料不到的,特别是因为常规管理部门的死亡率并不高。此外,许多死亡的患者是在第一年随访接近结束时死亡的,当时大多数患者几乎完成了研究。死亡的患者往往具有较高的BODE指数,并在研究期间记录了较高的住院天数,这两者都被认为是COPD患者死亡率的预测因素[32- - - - - -34].
本研究的优势包括使用和调整以前被证明是临床有益的自我管理方案,而不是一个新的方案。因此,COMET疾病管理方案可为今后的自我管理干预措施或设计评估此类干预措施的研究提供基础。特别关注医疗保健专业人员(病例管理人员)对患者的指导,旨在通过4天的培训优化自我管理,其中包括特别关注激励沟通,持续获得规划资源(规划目标、干预措施、建议问题、预期结果),以及通过每月与各国协调研究中心的肺病学家电话联系获得反馈。疾病管理干预措施的新方面包括一个电子健康平台,用于报告经常更新的健康状况,必要时进行快速干预,以及氧疗监测。另一个优势是COMET的国际化设计,这是第一项专门针对严重COPD疾病管理干预的研究,由中央培训和支持的病例管理人员提供,涉及四个不同医疗实践和医疗保健系统的国家。最后,虽然试验是开放式设计的,但EVC对住院治疗进行了严格和盲目的审查,并在必要时进行额外的询问,以确保结果的可靠性。
这项研究有一些局限性。将在急症护理病房的住院天数以及随后在护理机构的住院天数纳入主要结果可能不是最优的。在护理机构的停留时间有时会超出明确的住院医疗需求,这可能会影响结果。然而,EVC审查了所有超过30天的停留,如果有必要,这些停留将从EVC分析中删除。此外,两组患者住院时间较长(图3).单独的急性护理住院可能被认为更合适,不那么主观,比资源可用性或当地报销惯例更好地反映患者的即时需求。事实上,在COMET中,急性护理住院似乎是住院需求的一个更敏感的指标,但由于该研究不是专门设计来衡量这一结果作为主要终点,因此这些结果的价值有限。尽管病例管理人员在研究开始前接受了正式培训,并在整个研究过程中作为质量保证的一部分得到了支持,但没有可量化的措施来确认干预交付的质量。然而,研究中使用的质量保证被认为是现实和实际的疾病管理方案。尽管使用了三个分层因素来促进均衡研究组的分配,但并不能避免各国在基线特征和住院天数方面的差异。这些因素,加上常规护理的地点和国家特定差异,可能降低了在许多研究结果中发现显著差异的可能性。虽然由于两种疾病管理方案之间存在很大差异,研究的开放式设计是必要的,但可能会导致一些偏见,因为医生可能倾向于让疾病管理部门的患者比普通管理部门的患者更早出院。
总之,尽管DM组的非计划年度住院天数往往低于UM组,但仅在接受至少25%计划指导课程的患者的急性护理住院天数减少具有统计学意义。疾病管理干预的一个明显好处是死亡率显著降低,其中通常管理对照组的大多数死亡是由急性加重引起的。疾病管理方案可能促进更早地对病情加重进行适当治疗,从而可以防止一些致命并发症。然而,这一结果应被视为信息性结果,因为死亡率是一种安全结果,而不是主要结果。即将进行的医学经济分析也可能揭示疾病管理干预措施的成本效益和成本效用效益。这项国际研究支持了对严重COPD患者(许多患者正在进行LTOT)进行多成分家庭疾病管理干预的可行性,并证明大多数患者坚持干预。但是,可以更仔细地评估患者的需求和规划开始时的自我管理技能,并随着时间的推移进行跟踪,以便后续规划的调整。一些有严重合并症的非常严重的患者应明确识别,因为他们可能无法完全实施该方案,从而受益于该方案。最后,在研究多成分疾病管理干预措施时,需要仔细考虑医疗保健系统和医疗保健协调的特点。
补充材料
披露的信息
补充材料
J-M。Arnalerj - 01612 - 2017 - _arnal
答:Bergeron-Lafaurieerj - 01612 - 2017。拉法莉- _bergeron有幸参加
C.G. Cornelissenerj - 01612 - 2017 - _cornelissen
r·凯斯勒erj - 01612 - 2017 - _kessler
g . Niliuserj - 01612 - 2017 - _nilius
j•Randeratherj - 01612 - 2017 - _randerath
J.B. Texereauerj - 01612 - 2017 - _texereau
确认
Kurt Liittschwager (4Clinics, France)提供了本手稿准备过程中的医学写作帮助。该援助由液化空气医疗集团提供支持。作者还感谢法国、德国、意大利和西班牙的家庭保健提供商VitalAire的保健专业人员和人员,他们参与了方案的制定和实施,并慷慨地分享了他们的经验和反馈。
贡献者:J. Bourbeau(麦吉尔大学健康中心研究所,Montréal,加拿大),B. Celli(圣伊丽莎白医疗中心,波士顿,美国),J. Rocca(医院诊所,巴塞罗那,西班牙),J. Wedzicha(皇家自由医院,伦敦,英国)和B. Housset(跨社区医院中心Créteil, Créteil,法国)担任初始研究设计专家委员会成员。C. Bucknall(格拉斯哥皇家医院,米尔加维,英国),P.R. Burgel(科金医院,巴黎,法国)和C. Vogelmeier(马尔堡大学医院,马尔堡,德国)担任终点验证委员会成员。以下个人在各自的调查地点为研究做出了贡献。法国:M. Canuet、T. Degot、S. Hirschi Santelmo和A. Schuller,斯特拉斯堡市民医院,斯特拉斯堡;马赛北部医院的D.A. Charpin, N. Lesavre和A. Palot;C. Chenivesse, J. Gonzalez和T. Similowski, Pitié-Salpétrière巴黎医院集团;D. Demory和A. Garnero,圣穆斯医院,土伦;F. Goupil, O. Molinier和A. Paris,勒芒医院中心,勒芒;J.L. Jagot、M. Lafay和S. Salmeron,巴黎圣约瑟夫医院集团;D. Laugros, Beauregard医院,蒂昂维尔; L. Lerousseau, Antibes-Juan-les-pins Hospital Center, Antibes; G. Lorillon and F. Schlemmer, Saint-Louis Hospital, Paris; I. Olaru, N. Paillot, F. Renolleau and E. Voicu, Metz-Thionville Regional Hospital Center, Metz; J.L. Pepin and R. Tamisier, Grenoble University Hospital Center, Grenoble. Germany: F. Bornitz and F. Herth, Heidelberg Thorax Clinic Gmbh, Heidelberg; M. Dreher, S. Krüger, S. Kweider and T. Müller, University Hospital Aachen; S. Fleimisch, P. Haidl and D.C. Heyse, Kloster Grafschaft Specialized Hospital, Schmallenberg; K.J. Franke, HELIOS Klinik Hagen-Ambrock, University of Witten/Herdecke, Hagen; C. Kropf, University Clinic Ulm, Ulm; D.U. Lange and M. Westhoff, Hemer Pulmonary Clinic, Hemer; C. Priegnitz, Bethanien C.V. Hospital, Solingen; S. Verlaan, St Mary Hospital Kassel GmbH, Kassel. Italy: S. Amaducci, S. Colato, A. Pietra and M. Villani, San Carlo Borromeo Hospital, Milan; S. BErtacco, F. Trevisan and L. Bonadiman, Bussolengo General Hospital, Bussolengo; S. Guarnaccia and P. Scavalli, Andosilla di Civita Castellana Hospital, Civita Castellana; G.P. Mattioli, A. Re and A. Tubaldi, Macerata General Hospital, Macerata; E. Micallef and J. Rolo, Niguarda Hospital Group, Milan; C. Motta and C. Rampoldi, Desio & Vimercate Hospital Group, Seregno. Spain: C. Aguar Benito, B. Brotons and F. Sanchez-Toril, Arnau de Vilanova Hospital, Valencia; F. Caballero, P. De Lucas and L. Morán, Gregorio Marañón Hospital, Madrid; R. Gallego Dominguez and J.A. Riesco, San Pedro de Alcantara Hospital, Caceres; A. Garcia Garcia and M. Iscar Urrutia, Asturias University Hospital, Oviedo; R.M. Gómez Punter and E. Vázquez Espinosa, La Princesa Hospital, Madrid; M.L. Martinez and T. Pena Miguel, Burgos University Hospital, Burgos; S. Mayoralas and J.L. García González, Ramón y Cajal University Hospital, Madrid.
脚注
这篇文章有补充资料可从www.qdcxjkg.com
这项研究注册在ClinicalTrials.gov与标识符NCT01241526.
支持声明:本研究由液化空气医疗集团资助。本文的资助信息已存入交叉参考基金注册.
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2017年8月7日。
- 接受2017年10月13日。
- 版权所有©ERS 2018