文摘
背景慢性阻塞性肺疾病(COPD)患者表现出更低的峰值耗氧量(V′O2峰),改变肌肉代谢及运动耐量受损而同年龄组。这些特征是否反映muscle-level去适应作用(影响通气约束)和/或功能障碍在线粒体ATP生产能力是讨论。通过研究有氧运动训练(让)匹配的相对强度和随后的撤军时间锻炼我们旨在阐明全身肌肉线粒体健康年轻的响应能力(衔接),健康的老年慢性阻塞性肺病(HO)和志愿者全身锻炼。
方法HY (n = 10), HO (n = 10)和慢性阻塞性肺病(n = 20)志愿者学习之前和之后让(65%的8周V′O2峰),经过4周的锻炼撤军。V′O2峰、肌肉最大线粒体ATP产量(MAPR),线粒体,线粒体DNA (mtDNA)拷贝数和大量的59跨度为目标确定燃料代谢mrna。
结果肌肉MAPR(正常的线粒体内容)没有不同基质组合在HO在基线HY和慢性阻塞性肺病,但mtDNA拷贝数相对于nuclear-encoded看家基因(意味着±sd)是更大的在HY(804±67)比在HO (631±69;p = 0.041)。让增加V′O2峰在何鸿燊(17%;p = 0.002)和衔接(21%;p < 0.001),但不是慢性阻塞性肺病(p = 0.603)。肌肉MAPR的棕榈酸酯增加培训HO (57%;p = 0.041)和衔接(56%;p = 0.003),减少锻炼撤军HO (−45%;p = 0.036)和衔接(−30%;p = 0.016),但没有改变在慢性阻塞性肺病(p = 0.594)。mtDNA拷贝数增加而让衔接(66%;p = 0.001),但不是HO (p = 0.081)和慢性阻塞性肺病(p = 0.132)。 The observed changes in muscle mRNA abundance were similar in all groups after AET and exercise withdrawal.
结论内在的线粒体功能未受老化或慢性阻塞性肺病在未经训练的状态。全身和肌肉线粒体反应让健壮的衔接,在何鸿燊明显,但缺乏慢性阻塞性肺病。所有组显示健壮的肌肉mRNA的反应。可能需要更高的相对运动强度在全身训练全身最大化和肌肉线粒体适应在慢性阻塞性肺病。
文摘
肌肉线粒体功能没有受损的年龄或慢性阻塞性肺病。全身和线粒体运动训练适应年轻健壮,明显在老年慢性阻塞性肺病和缺乏。慢性阻塞性肺病适应可能需要高强度运动训练项目。https://bit.ly/3oe0k0S
介绍
与年龄的健康志愿者相比,慢性阻塞性肺病(COPD)患者表现出更低的全身最大耗氧量(1- - - - - -3)和骨骼肌代谢异常特征。改变肌肉纤维成分(4,5),低纤维横截面积(6和降低毛细现象7在慢性阻塞性肺病)明显。在线粒体水平,降低ATP生产能力(反映在低最大线粒体酶的活动1]),改变线粒体效率(8(mtDNA)],降低线粒体DNA拷贝数和更流行的mtDNA删除9描述了在慢性阻塞性肺病。总的来说,这些差异影响肌肉的代谢反应急性运动,如。大non-mitochondrial ATP生产和腺嘌呤核苷酸损失(10),强调周边肌肉疲劳发展和降低运动能力在慢性阻塞性肺病。
是讨论到什么程度不同的肌肉能量代谢在慢性阻塞性肺病反映muscle-level去适应作用(与线粒体数量减少和/或数字)和/或针对疾病的慢性阻塞性肺病mitochondropathy(特点是内在的能力受损的线粒体呼吸或ATP生产单位)(8,9,11- - - - - -15]。同样,实足老化有关肌肉线粒体蛋白质含量较低(16和降低线粒体内在的能力17,18慢性阻塞性肺病),线粒体功能障碍的病因学可能是年龄和/或疾病相关。
有氧运动训练(让)强劲增加肌肉线粒体内容和功能的几个标记在年轻19)及以上(16志愿者,但是否类似线粒体反应让发生在COPD患者是不确定的,尤其是因为通气限制在慢性阻塞性肺病可以防止骨骼肌充分挑战,从而减少训练适应(20.,21]。
重要的是,据我们所知,有限的数据是可用的描绘让影响线粒体丰富和高度敏感的标记,直接线粒体ATP生产能力的措施与全身心肺适应健康,年轻的和年长的志愿者和并发COPD患者训练。同样,这些反应在回归后习惯性的身体活动培训没有描述。这些数据将提供关于线粒体随年龄下降的病因学和慢性阻塞性肺病,和运动干预的机制在应对时代和COPD-related肌肉衰退和运动不耐受。这样的见解也会有利于欣赏的效用线粒体作为治疗目标。
我们因此旨在确定匹配的相对强度的影响让在一个8周有氧训练以65%的峰值耗氧量(V′O2峰),4周后锻炼撤军在健康年轻的和年长的志愿者和慢性阻塞性肺病患者。结果措施包括全身心肺反应,肌肉线粒体的标志内容,最大肌肉线粒体ATP生产速度(MAPRs)和mrna的表达密切相关,肌肉燃料利用率。我们提出MAPR的反应V′O2峰运动干预和撤军会年轻和老年健康组之间差异,老年健康和COPD组之间由于先进的年龄和疾病病理学的影响肌肉功能和通气的潜在影响限制在慢性阻塞性肺病运动强度。
方法
额外提供了所有方法的详细信息补充材料。
主题
三组的久坐不动的志愿者招募:COPD患者(和显著的运动限制由于呼吸困难;医学研究理事会等级≥3)60 - 80岁(慢性阻塞性肺病),和年龄年轻健康的老(HO)和健康(衔接)18到35岁的受试者(入选标准提供补充表S1)。
研究设计
一个准,non-randomised介入队列研究。人体测量学,肺功能和股四头肌的力量在基线评估和两个symptom-limited增量(第一是熟悉)轻快和一个高频的自行车心肺运动试验(CPET)执行。七天的身体活动水平进行评估(个加速器)前禁食状态得到休息四头肌活检(22]。参与者开始8周完全监督骑车让(每周30分钟的三个交易日)工作负载对应于65%V′O2峰。这个强度是选择引起通量增加肌肉脂类和碳水化合物(23,24]。训练强度重置在星期4如果工作负载V′O2峰增加了。经过8周的训练中,参与者被指示恢复训练的“习惯性的身体活动水平后,随访4周(一周12)。CPETs重复在周4、8和12。进一步休息肌肉活检进行8周后(前训练后24 h)和4周运动后撤军(12周)。研究设计中列出补充图S1。
伦理批准被授予由NHS国家科研伦理和审判是注册服务ISRCTN注册表与标识符ISRCTN10906292。所有参与者提供书面知情同意。
肌肉线粒体制备
肌肉样本立即被均化作用,离心分离和再悬浮协议,然后保存在冰立即MAPRs量化之前。
最大MAPR(内在线粒体功能)
MAPR评估利用bioluminometric方法所描述的W邦et al。(25]。短暂,稀释线粒体悬架,ADP和ATP监测试剂(萤火虫荧光素酶)结合以下基质组合:谷氨酸和琥珀酸;谷氨酸和苹果酸;丙酮酸和苹果酸;棕榈酰-l肉碱和酸盐(棕榈酸酯);琥珀酸;和重蒸馏的水。所有值都是正常肌肉柠檬酸合成酶活性。
相对mtDNA拷贝数
丰富的mitochondrial-encoded (mtDNA) NADH:泛醌氧化还原酶的核心单元1建立了使用实时PCR和表示相对于基因编码(核DNA) hydroxymethylbilane合酶(如前所述)(28]。
目标肌肉mRNA表达
信使rna提取从snap-frozen肌肉如前所述29日)和定量实时聚合酶链反应进行。丰富的59记录参与肌肉燃料代谢评估(补充材料和补充表S2)和创新路径分析(IPA)(试剂盒、希尔登,德国)是用来询问这些差别监管。
统计分析
数据提出了均值与标准差(基线)或平均数标准误差(随时间变化)。假设正常的使用正态概率图和Shapiro-Wilk测试评估。群体间的均值差异在基线评估使用单向方差分析和类内跨时间的变化进行了测试使用单向重复测量方差分析事后费舍尔最显著差异测试使用IBM SPSS统计为Windows版本21(美国、IBM、纽约Armonk)。计算统计中可以找到补充材料。为了清楚起见,慢性阻塞性肺病与HY比较是没有报告由于缺乏相关性研究的目标。
结果
基线
基线报告主题特征表1。身体质量指数和无脂质量指数并没有统计上的不同组间基线。虽然所有非活动组,在慢性阻塞性肺病低于平均步数HO (p = 0.046)和久坐不动的生活方式指数以下的成年人每天5000步(31日]。
肌肉柠檬酸合成酶最大活动(线粒体内容),MAPR(内在线粒体功能)和mtDNA拷贝数在基线所示表2。无统计差异在柠檬酸合成酶活性组(p = 0.070)。何鸿燊的肌肉mtDNA拷贝数较少比(p = 0.041)(为什么表2)。MAPR不是何鸿燊与统计不同的衔接或慢性阻塞性肺病基线的基质组合使用(p > 0.05) (表2)。
在增量运动测试基线,HY达到一个更高的工作负载(p = 0.001)和V′O2峰(p < 0.001)与何鸿燊相比,而V′O2峰(p = 0.026)和峰值工作效率(p = 0.003)是相对于HO在慢性阻塞性肺病(补充表S3)。措施与V′O2峰显示,相比之下,HO COPD患者达到了下呼吸道交换率(r) (p < 0.001),每分通气量(V′E)(p = 0.020)和心率(p = 0.071),但利用显著更大比例的预测最大呼吸量(p < 0.001) (补充表S3)。轻快反应高频的稳态运动所示补充表S4。
有氧训练的影响和随后的锻炼撤军
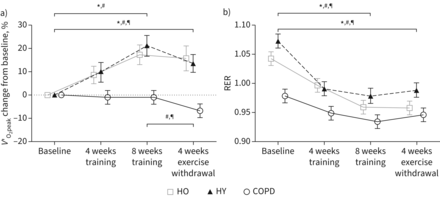
习惯性的身体活动水平在第一周(9)和第四(12周)周的锻炼撤军没有不同于基线组(p = 0.961, p = 0.765和慢性阻塞性肺病为什么p = 0.686) (补充表S5)。何鸿燊和重增加V′O2峰18% (p = 0.002)和21% (p < 0.001),分别在8周的训练(图1一个),但是没有变化V′O2峰在慢性阻塞性肺病(p = 0.603)。经过4周的锻炼,V′O2峰仍明显大于基线HO和衔接(分别为p = 0.017, p = 0.004),V′O2峰低于基线(p = 0.026)和第八周的运动训练在慢性阻塞性肺病(p = 0.033)。
在峰值摄氧量()类内变化V′O2峰)正常化瘦体重百分数表示从基线后4和4周后8周的训练和锻炼撤军(受试者回到习惯性的身体活动水平)健康老年人(HO),健康的年轻(重)和慢性阻塞性肺疾病(COPD)组。b)呼吸道交换比(r)在轻快稳态高频运动在同一跨度为(a)。数据均值±扫描电镜。何*:会改变p < 0.05;#衔接:会改变p < 0.05;¶:慢性阻塞性肺病会改变p < 0.05。
在轻快稳态高频运动(65%的rV′O2峰在基线)减少在所有组8周的训练(类内变化(p < 0.001, p < 0.001为什么和慢性阻塞性肺病(p = 0.003)图1 b4周后),仍低于基线的运动撤军(HO p < 0.001, p < 0.001为什么和慢性阻塞性肺病p = 0.013)。在轻快稳态高频运动时心率降低所有组的训练状态(p = 0.002, p < 0.001为什么和慢性阻塞性肺病p = 0.003)V′E减少在HO和重(p < 0.05)所示补充图S2。
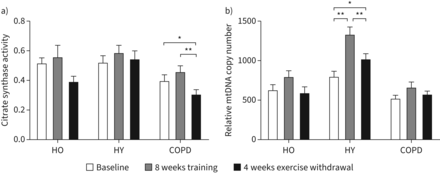
没有统计增加肌肉柠檬酸合成酶在任何团体活动培训(p = 0.120, p = 0.682和慢性阻塞性肺病为什么p = 0.133),但在4周的运动提取柠檬酸合成酶活性在慢性阻塞性肺病低于基线(p = 0.015)和8周的训练(p < 0.001) (图2一个)。在统计层面mtDNA拷贝数与基线让和恢复习惯性的身体活动HO (p = 0.120)和慢性阻塞性肺病(p = 0.132) (图2 b)。相比之下,有一个健壮的与让mtDNA拷贝数增加(p < 0.001),为什么拒绝在回到习惯性的身体活动(p < 0.001),尽管剩余大于基线(p = 0.024) (图2 b)。
肌肉柠檬酸合成酶活性(更易与乙酰辅酶a·最小值−1·L线粒体悬−1)和b)线粒体DNA (mtDNA)拷贝数(相对于核DNA拷贝数)基线,后4周后8周的训练和锻炼撤军(受试者回到习惯性的身体活动水平)对健康老年人(HO),健康的年轻(重)和慢性阻塞性肺疾病(COPD)组。数据意味着±扫描电镜。*:p < 0.05;* *:p < 0.01。
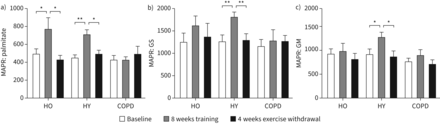
从基线运动训练干预增加MAPR HY三基质组合(棕榈酸酯p = 0.003;谷氨酸和琥珀酸p = 0.008;苹果酸和谷氨酸,p = 0.011) (图3)和棕榈酸酯(p = 0.041) (图3一),但是没有健壮的影响与底物结合在慢性阻塞性肺病(p > 0.05)。撤军让导致MAPR的回归基准利率在沪元(棕榈酸酯p = 0.016;谷氨酸和琥珀酸p < 0.001;苹果酸和谷氨酸,p = 0.003)和棕榈酸(p = 0.036),但是MAPR没有改变基线的慢性阻塞性肺病(所有基质p > 0.05) (图3)。没有变化的MAPR的基线线粒体基质丙酮酸琥珀酸和苹果酸或在任何组志愿者(所有p > 0.05;数据未显示)。
肌肉内在线粒体功能评估确定最大线粒体ATP产量(MAPR)(μmol ATP·更易−1乙酰辅酶a·敏−1)基线,后4周后8周的训练和锻炼撤军(受试者回到习惯性的身体活动水平)健康老年人(HO),健康的年轻(重)和慢性阻塞性肺疾病(COPD)组。棕榈酸),b)谷氨酸和琥珀酸(GS)、谷氨酸和c)和苹果酸(通用)。数据意味着±扫描电镜。*:p < 0.05;* *:p < 0.01。
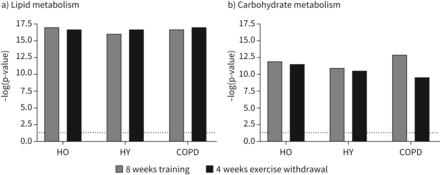
根据基线,肌肉mRNA表达的变化图4说明IPA确定肌肉脂类和碳水化合物代谢被改变后8周的训练和4周锻炼撤军HO HY和慢性阻塞性肺病。的y设在中图4显示−日志的假定值对于每个细胞功能,这是一个测量的可能性之间的联系的一组集中记录和一个给定的函数是由于随机机会类内变化的阈值的意义相当于p < 0.05。图4说明基于集体mRNA丰度的变化,反应的一致性这两个细胞功能的运动训练和4周锻炼撤军非常相似的HO HY和慢性阻塞性肺病。
肌肉细胞功能被聪明才智通路分析从基线被修改后4周后8周的训练和锻炼撤军(受试者回到习惯性的身体活动水平)基于mRNA表达数据生成使用定量实时PCR。a)脂质代谢和b)碳水化合物代谢有显著影响训练和锻炼后撤退。的y设在显示器−日志(假定值)计算确切概率法right-tailed。统计意义的虚线表示阈值会变化相对于基线(−日志(假定值)= 1.3相当于p = 0.05)。
图5强调个体基因的mRNA丰度的变化从基线被IPA妥协所示的脂质代谢功能图4后8周的训练。mrna的数量和每一个相似的大小和方向的变化相比,HY和慢性阻塞性肺病。个别mRNA表达的也是如此变化从基线后4周的运动对脂质代谢功能(撤军补充图S3)。信使rna变化丰富后8周的训练(图6)和4周锻炼撤军(补充图S4),单个基因被认为代表了碳水化合物代谢广泛遵循相同的大小和方向变化比较HO HY和慢性阻塞性肺病。
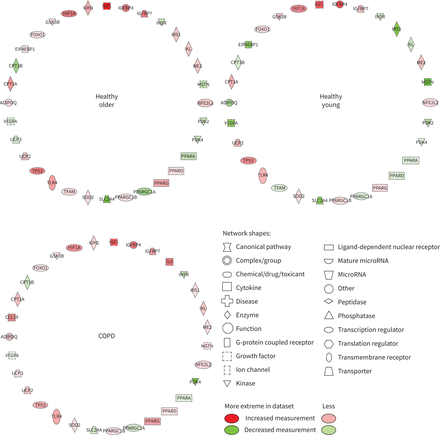
不同调节肌肉mrna与脂质代谢相关的后8周的训练与基线相比健康长大,健康的年轻和慢性阻塞性肺疾病(COPD)组。缩写基因中定义的名称补充表S2。
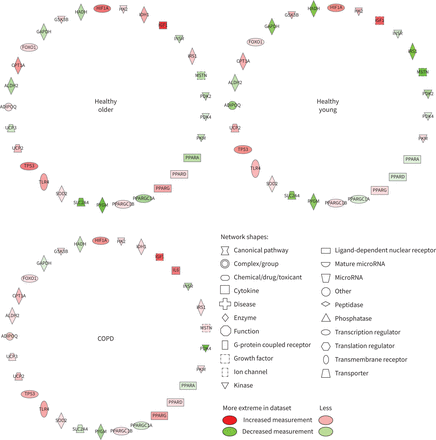
不同调节肌肉mrna与碳水化合物代谢后8周的训练与基线相比健康长大,健康的年轻和慢性阻塞性肺疾病(COPD)组。缩写基因中定义的名称补充表S2。
讨论
主要小说研究的发现,首先,内在的线粒体功能没有明显不同,衔接和COPD组在基线,表明线粒体功能没有受损的基底在COPD患者或健康老龄化。第二,全身和肌肉线粒体功能的变化,以应对8周的耐力运动训练在同一相对强度是健壮的志愿者,为什么那么健壮的HO COPD患者的志愿者和很大程度上缺席。这些减少反应可能较低的结果绝对肌肉装载有经验的培训期间,尤其是在慢性阻塞性肺病的潜在影响通气限制运动训练负荷存在,但健壮的肌肉转录响应运动干预在所有团体说反对,指出转录后调节肌肉在运动训练适应不同。最后,符合观测在HY志愿者19),4周的锻炼撤军返回内在线粒体功能的衔接和HO志愿者的基线状态。
这是讨论在多大程度上肌肉能量代谢的变化在慢性阻塞性肺病反映muscle-level退化疾病和/或研究慢性阻塞性肺病mitochondropathy [8,9,11- - - - - -15]。一些数据表明,肌肉线粒体呼吸(总线粒体含量校正)在COPD患者与老年健康志愿者(受损11,13),据报道在其他慢性疾病,如。2型糖尿病(32]。相反,然而,有证据表明,低肌肉线粒体氧化能力在慢性阻塞性肺病无法解释muscle-level独自去适应作用,可能是由于疾病病理生理学,包括转变从复杂I-driven呼吸对新陈代谢低效复杂II-driven呼吸(8),大mtDNA删除,增加标记异常fibre-specific呼吸和抑制线粒体增生(如。mtDNA拷贝数)9,12]。由于线粒体氧利用率可以从ATP生产病理生理状态(非耦合33),一个明确的结论是否COPD-related mitochondropathy真正存在可能会受到测量线粒体呼吸ATP生成的代理(11,13),一个问题解决的研究,利用直接测量的最大MAPRs敏感。这些数据,结合量化线粒体密度(柠檬酸合成酶)和扩散(mtDNA拷贝数),符合内在线粒体功能的证据在患者不受损老化16)或慢性阻塞性肺病的存在(11,13]。
慢性让增加肌肉线粒体内容和功能的几个标记在年轻19)及以上(16志愿者,但有限的信息是否可用类似的线粒体反应让发生在COPD患者,尤其是因为通气限制在慢性阻塞性肺病可以防止骨骼肌充分挑战在全身运动,从而减少训练适应(20.]。高强度限制肌肉组织培训已被证明在COPD患者恢复线粒体功能观察年龄组(尽管n = 5),尽管它是未知是否功能能力也提高13]。Picardet al。(11)还指出,肌肉退化,而不是线粒体功能障碍,降低最大利率的司机在COPD患者线粒体呼吸。在目前的研究中,运动训练的肌肉进行在一个足够高的强度增加线粒体脂质和碳水化合物的氧化,然而在所有组的公差范围。这种运动方式产生强大的全身和肌肉线粒体功能的变化和扩散在HY志愿者,在何减少COPD患者的志愿者和缺席。我们承认muscle-level加载可能被截断在COPD组由于通气限制限制全身锻炼耐力。然而,重要的是,运动干预后肌肉基因转录反应直接与肌肉脂质和碳水化合物在COPD患者使用相似与何鸿燊和HY志愿者。此外,减少稳态轻快r在高频运动在8周的训练在所有组明显,证明在慢性阻塞性肺病慢性运动适应不是燃料动员和有限的可用性在运动。看来,使用的训练并不足以引起适应转录后调控线粒体生物起源或线粒体功能,尤其是在慢性阻塞性肺病患者。这可能源于通气限制限制muscle-level挑战的大小;然而,它也被提出,骨骼肌适应性反应的塑性收缩活动是减少与年龄和年龄相关的疾病,这延伸到线粒体细胞增殖和功能,表明更大的收缩刺激需要达到一个类似的表型适应(34]。转录后等新兴网站的限制包括肌肉转化效率(核糖体活动)和转化能力(核糖体数量)35]。
值得注意的是,V′O2峰和肌肉COPD患者中柠檬酸合成酶活性下降低于值记录在基线和运动训练干预后,并没有观察到在衔接和HO志愿者。没有明显的解释观察给定习惯性的身体活动水平在第一和第四一周锻炼撤军没有显著的不同,测量基准。然而,应该承认,三轴accelerometery,用来量化步骤计算在当前的研究中,无法量化日常生活活动的强度,因此也许解释明显退化观察COPD组4周锻炼后撤退。
久坐不动的这项研究中,通过深思熟虑的选择健康志愿者,更好的匹配习惯性的身体活动状态的主题与以前的出版物相比比较慢性阻塞性肺病和健康,而且采用严格监督行使协议。承认,样本量(虽然大,用人要求干预研究和详细的代谢和生理指标)限制的generalisability发现更广泛的人群。COPD患者的无脂质量在这个研究是正常的,进一步限制这些发现的generalisability低脂体重患者的差异对有氧训练(特别是在mRNA水平)曾被观察到(36]。最后,优惠的I型氧化纤维曾被观察到在慢性阻塞性肺病,留下一个较大比例的II型纤维与健康对照组相比(4,5]。不同的肌肉fibre-type反应运动训练会增加额外的洞察力;然而,由于组织的可用性有限,不可能描述个体肌肉fibre-type反应在这项研究。进一步的当前研究的局限性在于,它不报告肌肉反应在蛋白质水平的下游肌肉mRNA丰度的变化。
我们的数据与视图对齐,在慢性阻塞性肺病患者最大肺通气量是受限的,分区训练策略等间隔或限制肌肉组织培训旨在最大化muscle-level强度可能会刺激更大的muscle-level适应(21,37),因此可能病人受益。此外,研究结果提供机械支持目前临床康复指南推荐的高相对全身的处方锻炼对慢性阻塞性肺病患者低强度相对强度可能不足以引发健壮的全身和muscle-level适应(38]。同样重要的是要承认的更广泛影响肺康复信心,如改善公差的呼吸困难和情绪可能影响其他临床结果的措施反映了病人受益(如。实地测试的运动性能)无论相对运动强度。尽管如此,增强适应肌肉水平有可能造福患者,我们建议新药物疗法针对线粒体转录响应函数应该考虑保护的COPD组的运动训练。损伤的识别转录后的轨迹是一个关键的研究问题需要解决在开发这样的疗法。
总之,内在线粒体功能没有受损老化或慢性阻塞性肺病。然而,全身反应运动变化的大小,线粒体ATP生产和线粒体增生以应对慢性让不定地削弱了随着年龄的增长,进一步削弱了在慢性阻塞性肺病,可能由于通气的限制。肌肉mRNA的相似反应直接联系到脂肪和碳水化合物氧化在HY, HO和慢性阻塞性肺病患者团体指出,骨骼肌运动压力的可塑性降低COPD在转录后水平。有关我们的发现在肺康复运动处方,表明相对较高工作强度可能需要在全身有氧训练来刺激适应肌肉水平在慢性阻塞性肺病,从而最大限度地提高病人受益。
补充材料
可共享的PDF
确认
作者欣然承认人类的贡献这个工作研究技术人员大卫·格林菲尔德的人类生理单位,诺丁汉大学(英国诺丁汉),格伦Hearson(国立卫生研究所诺丁汉生物医学研究中心——呼吸,诺丁汉,英国)和所有参与者自愿参加本研究。
脚注
这项研究是在注册ISRCTN注册表与标识符ISRCTN10906292。
利益冲突:L.E.拉蒂默没有披露。
利益冲突:d Constantin-Teodosiu没有披露。
利益冲突:b Popat没有披露。
利益冲突:d江诗丹顿没有披露。
利益冲突:l . Houchen-Wolloff没有披露。
利益冲突:石球博尔顿报告,在研究过程中,资金从MRC / ABPI慢性阻塞性肺病联盟和国家卫生研究所;从英国肺脏基金会赠款或合同,H2020,葛兰素史克公司和辉瑞公司;外旅游基耶西的支持,提交工作。
利益冲突:哈默斯坦纳没有披露。
利益冲突:P.L. Greenhaff没有披露。
支持声明:本研究由COPDMAP财团MRC-Versus关节炎肌肉骨骼老化研究中心(医学研究理事会资助数字先生/ K00414X / 1 - 19891),美国国家卫生研究所(NIHR)莱斯特生物医学研究中心和NIHR诺丁汉生物医学研究中心。作者的观点是,不一定NHS, NIHR或健康和社会保健部门。支持L.E.拉蒂默NIHR莱斯特生物医学研究中心——呼吸。刚建成时支持博尔顿NIHR诺丁汉生物医学研究中心——呼吸。d .江诗丹顿得到了MRC-Versus关节炎肌肉骨骼老化研究中心和NIHR诺丁汉生物医学研究中心。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年5月27日。
- 接受2021年9月19日。
- 版权©2022年作者。
这个版本分布在Creative Commons归因执照的条款4.0。