摘要
背景Navafenterol (AZD8871)属于一类新的支气管扩张剂,单分子毒蕈碱拮抗剂和β-激动剂,开发用于治疗COPD。本研究旨在评价navafenterol的疗效、药代动力学和安全性与安慰剂和积极比较治疗中重度COPD。
方法这项2a期随机、多中心(德国和英国)、双盲、双假、三方完全交叉研究(ClinicalTrials.gov标识:NCT03645434)与每日一次600µg navafenterol治疗2周相比通过吸入安慰剂和固定剂量联合支气管扩张剂(umeclidinium/vilanterol (UMEC/VI);62.5 μ g/25 μ g)在中度至重度COPD参与者中。主要结局是1 s内用力呼气量(FEV)从基线变化1)第15天。次要终点包括FEV峰值较基线的变化1;呼吸困难、咳嗽和痰液量表(BCSS)较基线的变化;COPD评估工具(CAT)较基线的变化;不良事件;和药物动力学。
结果73名参与者被随机分配。14天后,FEV低谷1与安慰剂相比,navafenterol显著改善(最小二乘(LS)平均差0.202 L;p < 0.0001)。两组FEV差异无统计学意义1navafenterol和UMEC/VI之间(LS平均差- 0.046 L;p = 0.075)。COPD症状(CAT和BCSS)在两种积极治疗中均有显著改善与安慰剂(均p<0.005)。新的客观监测(VitaloJAK)显示,与安慰剂相比,两种积极治疗都减少了咳嗽。整个治疗组的安全性相似,在navafenterol治疗期间没有严重不良事件的报告。
结论每日一次的纳芬特醇耐受性良好,改善了肺功能,减少了copd相关症状,与已建立的每日一次固定剂量联合支气管扩张剂类似。
摘要
Navafenterol是一种用于COPD的新型双药理学支气管扩张剂,可改善肺功能,减轻COPD症状并减少客观咳嗽次数,其程度与umeclidinium/vilanterol相似https://bit.ly/3lV886y
简介
慢性阻塞性肺病是一种常见疾病,是全球发病率和死亡率的重要原因[1,2].慢性阻塞性肺病的主要临床症状是慢性进行性呼吸困难、咳嗽和咳痰[1,3.].咳嗽和咳痰常被报告为令人不安的症状,早晨发生率增加,对健康相关的生活质量产生负面影响[4,5].
定期使用吸入性长效支气管扩张剂进行药物治疗可缓解和减轻COPD症状[1].长效毒蕈碱拮抗剂(LAMAs)和长效β2-激动剂(LABAs)是治疗COPD的主要药物,比短效治疗更受欢迎[1].LAMA/LABA联合治疗,如umeclidinium/vilanterol (UMEC/VI),在改善COPD患者的肺功能、症状和健康相关生活质量方面比单一治疗更有效[6,7].LAMAs和LABAs诱导平滑肌舒张和支气管扩张通过不同的作用机制,导致临床实践中的加性效应[8].
双药理学支气管扩张剂,一类结合毒蕈碱拮抗剂和β的新型化合物2-肾上腺素能受体激动剂在单一分子中发挥作用,称为毒蕈碱拮抗剂和β-激动剂(MABAs),可能比使用两种独立药物实体的联合治疗更具优势[9].由于MABAs是单分子,两种药物都以固定比例输送,具有单一的药代动力学特征,相对于LAMA/LABA联合疗法具有简化的临床开发计划[9,10].
在体外研究表明,纳芬enterol (AZD8871),一种吸入性长效MABA,具有强大的M3.抗马碱和β2-肾上腺素受体激动剂活性[11].在一项针对COPD患者的1期随机双盲交叉研究中,将单剂量navafenterol 400µg或1800µg与安慰剂、indacaterol和噻托溴铵进行比较,navafenterol提供持续支气管扩张超过36小时;navafenterol的两种剂量均优于安慰剂,高剂量优于indacaterol和tiotropium,没有出现安全问题[12].一项2a期随机双盲交叉研究表明,与安慰剂相比,COPD患者在第15天24小时内支气管扩张的剂量依赖临床有意义的改善[navafenterol 100 μg, navafenterol 600 μg和安慰剂每日1次,持续14天]13].预计navafenterol作为单分子MABA,可以为COPD患者的治疗提供一种新的方法,其疗效优于长效支气管扩张剂单药治疗;至少与LAMA/LABA双联疗法疗效相当,且安全性相似;并可能为未来与吸入性抗炎药的联合提供一个平台。
关于COPD治疗对减轻咳嗽的影响的数据有限,对影响COPD患者咳嗽频率的因素知之甚少。希望客观的咳嗽监测将为COPD咳嗽治疗的影响提供重要信息[14].
目前的研究(ClinicalTrials.gov标识符:NCT03645434)首次将navafenterol与临床实践中使用的LAMA/LABA联合治疗(UMEC/VI)进行了比较。这项研究的主要目的是比较navafenterol的效果与UMEC/VI对肺功能的影响。次要终点包括COPD症状和安全性评估,而咳嗽次数的客观减少是一个探索性终点。
方法
研究设计
这项2a期随机、双盲、双假、三路完全交叉研究比较了navafenterol 600µg与安慰剂和活性比较器LAMA/LABA支气管扩张剂(UMEC/VI) 62.5µg/25µg,每日一次,由干粉吸入器设备(Genuair/Pressair设备(SD3FL)用于navafenterol, Ellipta设备用于UMEC/VI)用于中度至重度COPD患者。该研究于2018年10月10日至2019年8月7日在德国的三个地点和英国的两个地点进行。
在三个为期14天的治疗期间,参与者以不同的顺序接受了所有三种治疗,其中42 - 49天的洗脱期(图1一个).患者在洗脱期维持每日异丙托品(20 μ g×2泡次,每天4次)。参与者使用交互式网络和交互式语音响应系统进行随机分配。本研究的完整方法细节载于补充的方法.
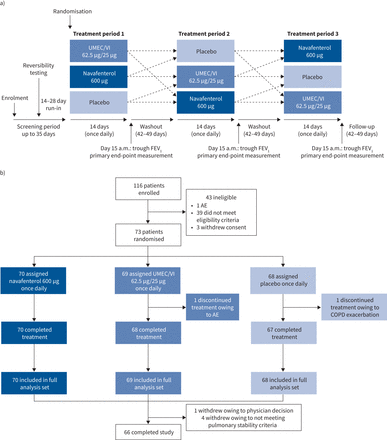
a)研究设计;B)耐心的性格。UMEC / VI: umeclidinium / vilanterol;FEV1:用力呼气量1 s;AE:不良事件。
本研究遵循起源于《赫尔辛基宣言》的伦理原则,并符合国际协调理事会/良好临床实践适用的监管要求,以及阿斯利康的生物伦理政策。研究方案由独立的伦理委员会根据当地要求批准。所有患者均提供书面知情同意书。本手稿已按照试验报告综合标准指南撰写[15].
病人
研究对象包括年龄在40-85岁之间的中重度COPD患者。患者目前或曾经吸烟,支气管扩张剂后用力呼气量为1秒(FEV)1)吸入沙丁胺醇400µg和支气管扩张剂后FEV后/强迫肺活量比<70%1第二次就诊时预测正常值≥40%,≤80%。
如果患者有明显的合并症,则排除在外(如。筛查来访前6个月内有明显心血管疾病,如心肌梗死,严重肝功能损害);α1抗胰蛋白酶缺乏症;其他活动性肺部疾病(主要哮喘、活动性肺结核、肺癌、支气管扩张、结节病、特发性间质性肺纤维化、原发性肺动脉高压或无法控制的睡眠呼吸暂停);筛查前一年发生两次或两次以上中度至重度COPD加重;筛查前3个月COPD急性恶化需要抗生素或皮质类固醇治疗;或在筛查前3个月因COPD控制不佳而住院。
符合条件的患者在入组时从常规的COPD维持药物切换到异丙托溴铵(20 μ g×2次,每天4次)。LABA、LAMA、LABA/LAMA和吸入皮质类固醇/LABA治疗在研究开始时被停用。接受吸入性皮质类固醇成分的患者被允许继续以稳定剂量作为单一疗法。
在先前COPD药物被冲洗后进行可逆性测试,其中可逆性状态定义为支气管扩张剂后FEV增加1≥12%(百分比可逆性)和≥200 mL(绝对可逆性)。可逆性地位不是资格标准的一部分。
结果
主要目的是评估navafenterol 600µg对中重度COPD患者的疗效。主要终点是最低FEV的基线变化1第15天。
次要终点包括FEV1曲线下面积;最低FEV与基线相比的变化1第2天和第8天测量;FEV峰值与基线的变化1;呼吸困难、咳嗽及痰液量表(BCSS)问卷总分较基线的变化[16,17];COPD评估工具(CAT)评分较基线的变化[18];使用抢救药物(沙丁胺醇100 μg);治疗产生的不良事件;耐受性;以及纳芬特醇及其主要代谢物的药代动力学,LAS191861 (补充图S1).
在第1天和第14天使用VitaloJAK咳嗽监测仪采集客观咳嗽计数作为探索性结果(Vitalograph, Buckingham, UK) [19].咳嗽监测器记录病人24小时内的咳嗽频率通过可穿戴式麦克风。制作并分析一份浓缩记录,以评估每小时咳嗽的次数[20.,21].使用视觉模拟量表评估感知的咳嗽严重程度[20.].
统计分析
所有参与者纳入完整的分析集,用于分析疗效变量。完整分析集定义为所有随机分组并接受研究治疗的参与者,无论他们是否遵守方案并继续参与研究。从基线到最低FEV的变化1以及FEV峰值与基线的变化1采用固定效应的混合模型对治疗、顺序和周期进行分析。参与者被设定为随机效应和剂量前FEV1作为协变量被包括在内。数据分析采用SAS 9.4版本(SAS Institute, Cary, NC, USA)。该研究旨在证明navafenterol与UMEC/VI相比在主要疗效终点(补充的方法).所有接受至少一剂研究治疗的随机患者都被纳入安全人群。明确同意的患者被纳入药代动力学分析子集。药代动力学分析的细节包括在补充的方法.
结果
病人
共有116名患者被纳入研究,其中73人被随机分配到研究中。所有随机分组的患者接受了至少一剂量的研究治疗,71例患者完成了至少一个研究期,66例患者完成了所有三个治疗期(图1 b).两名患者在研究期间停止治疗:一名患者在接受UMEC/VI治疗时发生严重急性冠脉综合征不良事件,另一名患者在接受安慰剂治疗时出现中度COPD加重。平均参与时间为186天。药代动力学分析组包括41名参与者。
患者人口统计数据和基线数据总结于表1.参与者的平均年龄为66.0岁,大部分为男性(68.5%)。预测FEV的平均支气管扩张剂后值1筛查时为58.7%;46例(63.0%)患者在筛查时处于可逆状态。大多数患者(76.7%)在过去一年中没有COPD加重,28例患者(38.4%)继续使用吸入皮质类固醇。均值±sd基线时CAT评分为15.4±6.1。
肺功能
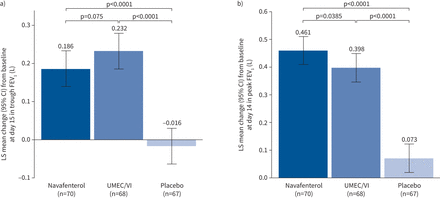
第15天,FEV低谷1与安慰剂相比,navafenterol或UMEC/VI治疗均显著改善(navafenterol最小二乘(LS)平均差0.202 L, 95% CI 0.151-0.253 L;p < 0.0001;UMEC/VI LS均值差0.248 L, 95% CI 0.197 ~ 0.300 L;p < 0.0001) (图2一个).与navafenterol相比,UMEC/VI的效果在数值上更大,但差异无统计学意义(LS平均差- 0.046 L, 95% CI - 0.097-0.005 L;p = 0.075)。
a) 1 s内用力呼气量(FEV)较基线变化的最小二乘(LS)均值1)第15天。b) LS从峰值FEV基线变化的平均值1第14天。UMEC / VI: umeclidinium / vilanterol。
第14天,FEV峰值较基线有显著差异1与安慰剂比较(navafenterol LS平均差0.388 L, 95% CI 0.329-0.447 L;p < 0.0001;UMEC/VI LS均值差0.326 L, 95% CI 0.226 ~ 0.385 L;p < 0.0001;图2 b).Navafenterol表现出快速起作用,Navafenterol对FEV峰值基线变化的影响1显著高于UMEC/VI (LS平均差0.062 L, 95% CI 0.003-0.121 L;p = 0.0385)。此外,navafenterol对FEV峰值有更大的影响1高于第1天的UMEC/VI (p<0.05)。第2天,FEV槽1UMEC/VI高于navafenterol (p<0.05);然而,在治疗期间,这种差异减少了(图3).
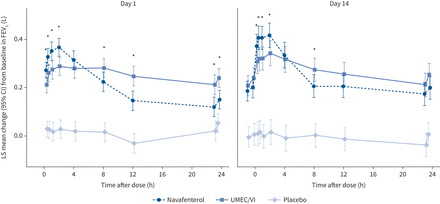
1秒内用力呼气量(FEV)1)在第1天和第14天超过24小时。LS:最小二乘;UMEC / VI: umeclidinium / vilanterol。*: p<0.05, navafenterol与UMEC/VI差异有统计学意义。
Navafenterol对FEV有显著改善1第14天各时间点(给药后0-4、0-8、0-12和0-24 h)的AUC均高于安慰剂。Navafenterol对FEV有显著改善1第14天给药后0 ~ 4 h AUC高于UMEC/VI (LS平均差0.062 L, 95% CI 0.006-0.117 L;p = 0.031;表2而且补充表S1).
事后根据可逆性状态定义的亚组分析表明,对于navafenterol和UMEC/VI, FEV峰值的增加1从基线开始,筛查时处于不可逆状态的患者与处于可逆状态的患者相比,其数值更小(补充图S2a).对navafenterol有更大峰值反应的模式与两亚组均观察到UMEC/VI,但无统计学意义(两亚组p=0.12),而UMEC/VI显示槽期FEV显著增加1与仅可逆性亚组第15天的navafenterol相比(p=0.008);不可逆亚组无治疗差异(p=0.65) (补充图S2b).
嗜酸性粒细胞计数≥150×10定义的亚群6或< 150×106细胞·L−1基线时,基线和当前吸烟者吸入皮质类固醇的使用情况与对前吸烟者进行分析事后.所有分析均显示navafenterol和UMEC/VI可显著改善FEV的低谷和峰值1与不依赖嗜酸性粒细胞计数、吸入皮质类固醇使用或当前吸烟状况的安慰剂组相比(补充图S3-S5).
症状减轻
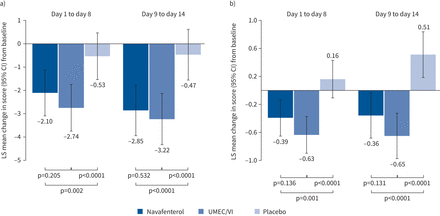
CAT和BCSS问卷显示,与基线评估相比,在治疗的第1-8天和第2周(9-14天),navafenterol和UMEC/VI均显著改善COPD症状(所有比较)与安慰剂,p < 0.005;图4).在治疗的第1周和第2周之间,CAT评分的LS平均值与基线变化相似(第1-8天:navafenterol - 2.10, UMEC/VI - 2.74,安慰剂- 0.53;第9-14天:navafenterol−2.85,UMEC/VI−3.22,安慰剂−0.47)。对于BCSS,第1周和第2周之间LS平均值与基线评分的变化也相似(第1-8天:navafenterol - 0.39, UMEC/VI - 0.63,安慰剂0.16;第9-14天:navafenterol - 0.36, UMEC/VI - 0.65,安慰剂0.51)。navafenterol和UMEC/VI在CAT或总BCSS(所有navafenterol与UMEC/VI比较p>0.05;图4).navafenterol和UMEC/VI的CAT应答者比例(定义为2.0点改善)都更高与但UMEC/VI和navafenterol之间没有差异(补充表S2).两种积极治疗的救援药物的使用明显低于安慰剂(所有比较与安慰剂p<0.0001),在navafenterol和UMEC/VI治疗组(所有navafenterol与UMEC/VI比较p>0.05;补充图S6).
治疗对COPD症状的影响,通过a) COPD评估工具(CAT)和b)呼吸困难、咳嗽和痰量表(BCSS)来衡量。LS:最小二乘;UMEC / VI: umeclidinium / vilanterol。
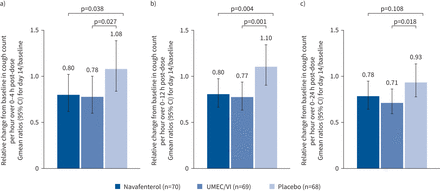
在一项探索性分析中,VitaloJAK客观咳嗽监测在基线和第14天测量了24小时内的咳嗽频率。目前吸烟者在基线时报告的咳嗽频率高于戒烟者(补充表S3).在第14天,与安慰剂(navafenterol与安慰剂p = 0.108;UMEC /六世与安慰剂p = 0.018;图5).此外,在肺功能测定的最大峰值效应对应的时间段内(0-4 h),与安慰剂相比,navafenterol和UMEC/VI在咳嗽频率方面表现出更大的改善(p=0.038和p=0.027)。这种效果持续了整个白天(0-12小时;P =0.004和P =0.001)。在第14天,与安慰剂相比,使用navafenterol和UMEC/VI的咳嗽改善使用视觉模拟量表(补充表S4).
在a)给药后0-4小时,b)给药后0-12小时和c)给药后0-24小时内,第14天客观咳嗽计数相对基线的相对变化(几何平均值(Gmean ratio)。UMEC / VI: umeclidinium / vilanterol。
安全
61名(83.6%)受试者在研究期间发生不良事件。治疗组中报告治疗引发不良事件的患者比例相似:navafenterol治疗期间39名(55.7%)参与者,UMEC/VI治疗期间38名(55.1%)参与者,安慰剂治疗期间35名(51.5%)参与者(表3并在文中详细描述补充结果).
在navafenterol治疗期间没有严重不良事件的报告。4名参与者报告了严重的不良事件:在安慰剂治疗期间报告了前庭神经炎(n= 1.5%)和肱骨骨折(n= 1.5%),在UMEC/VI治疗期间报告了牙脓肿(n= 1.4%)和急性冠状动脉综合征(n= 1.4%)。研究人员没有考虑到任何严重不良事件与研究治疗有关。报告急性冠状动脉综合征的参与者停止了UMEC/VI并退出了研究。治疗组间生命体征、实验室检查结果或超声心动图结果无临床相关差异。研究期间没有死亡报告。
药物动力学
单剂量(第1天)和多次剂量(第14天)后,Navafenterol被迅速吸收(补充表S5,补充图S7).中位时间至最高血浆浓度的范围(t马克斯)为0.45 ~ 2.05 h。在重复给药后出现了积累的证据,最大血药浓度的积累比为1.72,AUC的积累比为2.41。代谢产物LAS191861迅速形成(中位t马克斯给药后~ 2小时),AUC比navafenterol低约2倍。额外的药代动力学参数示于补充表S5.在25个样本中,有15个样本的navafenterol浓度为3.63-15.85 pg·mL−1在纳芬特醇治疗期后立即在治疗期的剂量前样品中检测到。25份样品中有20份检测到LAS191861,浓度为2.02 ~ 17.71 pg·mL−1.这可能是由于navafenterol和LAS191861的终末半衰期都很长。槽型FEV变化的敏感性分析1从基线到第15天表明,结转对navafenterol或活性比较剂观察到的估计治疗效果的影响可能很小(数据未显示)。
讨论
这项随机对照试验显示,navafenterol在改善中重度COPD患者的肺功能预后方面优于安慰剂。第15天的主要终点分析显示,navafenterol和UMEC/VI在槽期FEV上无统计学差异1.通过CAT、BCSS和客观咳嗽监测,这两种治疗对COPD症状的改善相似。
在第1天和第15天的24小时内,navafenterol和UMEC/VI的肺功能特征显示出不同的模式。第1天,navafenterol表现出比UMEC/VI更大的峰值效应。然而,navafenterol表现出数值较低的FEV低谷1高于UMEC/VI。治疗14天后,navafenterol保留了更大的FEV峰值1相比UMEC/VI, FEV下降更为缓慢1在峰值后,因此两种治疗在给药后12至24小时具有相似的值。navafenterol更大的峰值效应可能会降低早晨的症状负担,尽管本文没有对此进行研究,需要进一步评估。navafenterol对槽型FEV的影响1从第1天增加到第15天;这种影响在UMEC/VI治疗的患者中不太明显。药代动力学分析表明,纳芬特醇的吸收和其代谢产物LAS191861的出现是迅速的。重要的是,在反复给药后,有大量的积累。第1天至第14天navafenterol的积累与FEV的变化模式一致1在同一时期。
CAT的最小临床重要差异(MCID)估计为1-3分,BCSS为> - 0.3分[17,22].对于BCSS, 1分的变化代表显著的症状改善,0.6分的变化被认为是中度的,0.3分的变化被认为是小的[22].在这项研究中,navafenterol的改善比MCIDs更大与在14天治疗期结束时,CAT和BCSS均为安慰剂。目的评价咳嗽监测和视觉模拟量表作为探索性终点。咳嗽视觉模拟量表是一种用于评估咳嗽严重程度的实用工具,但它是一种主观评估,反映了患者对自身症状的感知[20.,23].VitaloJAK是一种测量咳嗽频率随时间变化的客观方法,可能比主观视觉模拟量表更敏感[24].一些COPD和哮喘患者的临床研究使用VitaloJAK来评估咳嗽及其与其他疾病参数的关系[21,25- - - - - -27].虽然COPD咳嗽次数减少的MCID尚未确定,但来自难治性慢性咳嗽的数据表明,减少20%将被认为具有临床意义[28].本研究首次证明长效支气管扩张剂可降低COPD患者的咳嗽频率,与安慰剂相比,白天的咳嗽频率显著且持续降低。由于咳嗽会降低患者的生活质量,敏感客观的咳嗽监测技术在COPD临床试验中可能具有相当大的价值[4].
在这项研究中,我们发现患者符合支气管扩张剂可逆性标准的比例高于长效支气管扩张剂3期试验中观察到的比例以及之前对COPD患者的真实研究[29- - - - - -32].在已发表的研究中,11-34%的患者被归类为可逆状态,而在本研究中,63%的患者被归类为短效支气管扩张剂可逆状态。
其他一些用于治疗COPD的maba正在开发中,包括batefenterol、AZD8999、AZD2115、CHF6366和THRX200495 [33].其中大多数已不再处于积极的临床开发阶段。Batefenterol完成了2b期临床试验,但尚未进展到3期。用β表示2-肾上腺素受体激动剂/毒蕈碱拮抗剂活性比,batefenterol具有更强的β2-肾上腺素受体激动剂的功能,而navafenterol有更强的M3.毒蕈碱拮抗剂活性[33].在2期试验中,300 μg巴特芬特醇联合100 μg糠酸氟替卡松可改善FEV较基线的变化1在42天的治疗中与安慰剂相比[34].试验设计的差异使得在不同研究之间进行比较具有挑战性。尽管LABA和LAMA疗法之间的协同作用已被证实在体外这在临床实践中尚未得到证实。maba的一个潜在好处是未来可能与抗炎化合物共配方,这可能为新型三(或四)药理学固定剂量组合产品提供了机会,从技术上讲,开发这种产品的要求比含有LAMA和LABA作为单独的分子实体的产品更低。
本研究采用双假人双盲交叉设计。交叉设计最大限度地减少了参与者间的差异性并优化了样本量。为了减少由于navafenterol和LAS191861的终末半衰期较长而导致的结转效应的可能性,实施了较长的洗脱期。虽然冲洗后有可测量的navafenterol浓度,但进行了包括携带变量在内的敏感性分析,并没有表明FEV中存在显著的携带1疗效结果。该研究的一个局限性是navafenterol的治疗剂量尚不清楚,因为尚未探索全剂量反应。虽然这可能会限制与已知的支气管扩张剂治疗剂量的比较,但与安慰剂的疗效比较不受影响。鉴于到目前为止navafenterol的耐受性良好,可能会探索更高剂量的navafenterol,以检查对疗效的潜在积极影响。该研究的另一个局限性是,对于任何次要终点,都没有对I型错误进行强有力的控制,尽管这是2期研究的标准。这项研究可能不能完全代表更广泛的COPD患者群体,因为短效支气管扩张剂可逆状态的患者比例很高。
结论
navafenterol 600µg,每日1次,耐受性良好,整体肺功能改善,COPD症状减轻,与UMEC/VI(一种已建立的LAMA/LABA联合支气管扩张剂)的程度相似。这项研究的结果支持在COPD患者中进行更大规模和更长期的临床试验。
补充材料
可共享的PDF
确认
我们感谢患者和他们的护理人员,以及参与这项研究的现场工作人员和调查人员。我们感谢Laura Drought (PharmaGenesis London, London, UK),她提供了由阿斯利康(AstraZeneca)资助的医学写作支持。我们感谢Evelina Björnsson、Henrik Forsman和Victor Balaguer(阿斯利康,哥德堡,瑞典)对研究执行和开展的支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
本研究已在clinicaltrials.gov上注册NCT03645434.本文所述研究结果的数据可根据阿斯利康的数据共享政策获得https://astrazenecagrouptrials.pharmacm.com/ST/Submission/Disclosure
作者贡献:D. Singh, J. Beier, C. Astbury, M.G. Belvisi, C.A. Da Silva, A. Jauhiainen, E. Jimenez, A. Lei, S. Necander, J.A. Smith, U. Wählby Hamrén和I. Psallidas对研究设计和概念做出了重大贡献。D. Singh和J. Beier参与了数据采集。A. Jauhiainen, E. Jimenez, A. Lei, S. Necander, U. Wählby Hamrén, W. Xin和I. Psallidas进行了数据分析。D. Singh, J. Beier, C. Astbury, M.G. Belvisi, C.A. Da Silva, A. Jauhiainen, E. Jimenez, A. Lei, S. Necander, J.A. Smith, U. Wählby Hamrén, W. Xin和I. Psallidas协助解读数据,参与起草手稿,对重要的知识内容进行关键修订,批准提交出版的最终版本,并同意对所有方面的工作负责。
利益冲突:D. Singh接受了Aerogen、阿斯利康、勃林格殷格翰、Chiesi、CSL Behring、Epiendo、葛兰素史克、格伦马克、Gossamerbio、Kinaset、Menarini、蒙迪制药、诺华、辉瑞、Pulmatrix、赛诺菲、梯瓦、Theravance和Verona的资助和个人费用,以及Cipla、Genentech和Peptinnovate的个人费用。J. Beier曾获得阿斯利康、柏林化学/梅纳里尼、基耶西和波尔-博斯坎普的咨询费,并参与了由阿斯利康和基耶西资助的科学顾问委员会。C. Astbury, M.G. Belvisi, C.A. Da Silva, A. Jauhiainen, E. Jimenez, A. Lei, S. Necander, U. Wählby Hamrén, W. Xin和I. Psallidas是阿斯利康的员工,可能持有股票或股票期权。VitaloJAK算法已由曼彻斯特大学基金会信托(MFT)和曼彻斯特大学授权给Vitalograph Ltd和Vitalograph Ireland (Ltd);MFT获得的特许权使用费可能与J.A. Smith工作的临床部门共享,J.A. Smith从阿斯利康获得个人费用。
支持声明:阿斯利康资助了这项研究,并参与了研究设计、数据收集、数据分析、数据解释和研究报告的撰写。阿斯利康在不影响作者意见的情况下审查了该出版物,以确保医学和科学的准确性,并保护知识产权。通讯作者有权访问本研究中的所有数据,并对是否发表稿件负最终责任。M.G. Belvisi和J.A. Smith接受来自威康基金会(207504/B/17/Z)的资助。J.A.史密斯还得到了国家卫生研究所曼彻斯特生物医学研究中心的资助,是NIHR的高级研究员。D. Singh得到了国家卫生研究院曼彻斯特生物医学研究中心的支持。
- 收到了2021年4月1日。
- 接受2021年8月8日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org