抽象
妊娠期哮喘与胎儿发育迟缓有性别特异性。乳酸菌影响婴儿的生长。这项研究旨在确定患有哮喘的母亲所生婴儿的肠道内乳酸菌和其他微生物是否减少,以及是否因婴儿性别不同而有所不同。
从加拿大健康婴儿纵向发展足月队列对母婴(N = 1021)进行了研究。联丰infant faecal microbiota at 3–4 months, profiled by gene sequencing, was compared between both women with and without asthma treatment during pregnancy. Infant sex, maternal ethnicity, pre-pregnancy overweight and atopy status, birth mode, breastfeeding status and intrapartum antibiotic treatment were tested as covariates.
与出生方式和其他协变量无关,患有产前哮喘的女性所生的白人男性婴儿在3-4个月大时肠道内的乳酸菌较少。如果患有哮喘的母亲在怀孕前体重超标,则肥胖的几率更大乳酸杆菌雄鼠的肠道菌群进一步减少,而雌鼠的肠道菌群则增加拟杆菌。根据产妇的产前哮喘状态,在婴儿肠道微生物组成类似的差异也妇女与食物或环境过敏更加明显。
肠道乳酸杆菌在雄性以内的婴幼儿丰富,但拟杆菌were more abundant in female infants at 3–4 months of age, following maternal asthma during pregnancy.
抽象
Gut lactobacilli are less abundant at 3–4 months in male but not female infants following maternal prenatal asthmahttp://ow.ly/jXnl30fU9xH
介绍
哮喘是怀孕期间常见的慢性疾病,影响8%至13%的孕妇[1]。它往往是与食品和环境过敏[共病条件2]。怀孕期间哮喘急性发作率较高[3],和更严重的哮喘或症状控制差已经与低出生体重相关联4-7]。以下不受控制的儿童哮喘的风险更大与怀孕期间母体控制哮喘有报道[8]。这些对后代的风险的变化表明了一种可能性在子宫内母体哮喘的影响。妊娠期哮喘常常导致孕妇使用抗生素治疗和剖腹产[7,9],干预可以打断母亲的乳酸杆菌的转移,这在胎盘,肠道和阴道在怀孕的最后三个月变得更加突出[10-13]。乳杆菌的丰度降低已在母亲的新生儿胎粪被观察到与特应性疾病[14]。
女婴儿出生通常比男性婴儿小;然而,响应于母体哮喘,高加索男性胎儿更可能当在术语比女性胎儿递送到具有较低的出生体重,并显示生长迟缓[五]。中号阿廷等。[15]最近报道大便少定植乳酸杆菌足月男婴与女婴出生时和出生后第一个月的物种比较。出生后,取决于乳酸杆菌种类,由于重量推广是物种特异性的,在婴儿肠道的乳杆菌的主导地位,将决定的体重增加和随后的特应性疾病[程度16-18]。总之,越来越多的证据进行产前哮喘的一个计划中的作用,可能会影响婴儿肠道微生物。这些意见使我们研究怀孕对加拿大健康婴儿纵向发展(儿童)总人口出生队列婴儿肠道菌群中的孕产妇哮喘状态的影响。具体而言,我们确定是否属乳酸杆菌在出生哮喘的母亲的婴儿的肠道减少,尤其是在男性婴儿的肠道。其次,我们寻求证据产妇哮喘的胎儿程序化作用,这是独立的出生方式和相关事件,并经产妇合并症,如超重和过敏性疾病增加。
材料与方法
研究设计和样本收集
全国人口为基础的出生队列( - 这项研究是在1021名母亲及其婴儿谁参加了加拿大健康婴儿纵向发展(儿童)进行研究www.canadianchildstudy.ca)[19-21]。孕妇在马尼托巴,埃德蒙顿(阿尔伯塔)和温哥华(安大略省)的儿童群体的网站他们孕中期或孕晚期被招募。从所有的母亲获得书面知情同意书。这孩子队列的微生物研究经阿尔伯塔大学(#Pro00010073)的人类研究伦理委员会。医院出生记录分娩过程中提供的交付,性别和婴儿曝光模式数据。从标准化的问卷调查和医院的记录获得了母亲的人体测量孕前和婴儿的饮食。哮喘during pregnancy was defined as present, if mothers had responded ‘yes’ to the question ‘Have you had any treatment for asthma or wheezing in the last 12 months?’ in prenatal questionnaires. Any treatment for asthma, as indicated by hospitalisation, a physician's visit or medication use, has been validated as a measure for asthma morbidity during pregnancy [22]。哮喘治疗的12个月的考核期包含在时间刚好在受孕前。由于哮喘的女性23-30%在怀孕期间停止治疗,由于减轻症状,[22,23儿童研究问卷将会正确地分类在怀孕前报告治疗的妇女,而不是在怀孕期间。
对产妇在怀孕期间特应性状态数据也从产前调查问卷,作为症状响应一种或多种食物或环境过敏原,如花粉热,过敏性皮炎,以及花粉,草,树木,杂草,食品,昆虫或宠物过敏获得。Faecal samples were obtained from infants at 3–4 months of age for microbial profiling. Parents were instructed to refrigerate soiled diapers prior to retrieval by a CHILD research assistant during a home visit. Faecal samples were then transported to the laboratory in a cooler, where they were divided into aliquots and stored at −80°C prior to DNA extraction and sequencing.
测序和数据处理
多伦多大学基因组进化与功能分析中心使用MiSeq Illumina测序方法对汇集的16S rRNA片段进行测序。使用QIIME管道(版本1.8.0)将序列解复用并根据它们的条形码绑定到单个样本中。然后,通过去除Phred质量评分低于20的10个以上位点的reads,对序列进行质量过滤。在QIIME中使用封闭式挑选算法,通过质量控制的序列以97%的相似性分界点聚成操作分类单元(OTUs)。最后,OTUs与Greengenes细菌学参考数据库(v. 13.5)进行比对,以识别门、科和属层次的微生物。总体相对丰度低于0.0001的otu被排除在后续分析之外[24]。清洁和处理之后,独特的OTU的总数为1325和总数为读取2.7亿(中值2.3×10五每个样品,范围6.7×103-8.3×106)。data were rarefied to 13 000 sequences per sample. The metrics of OTU (microbial) relative abundance and diversity (Shannon and Simpson diversity indices, Chao1 species richness index) were generated in QIIME to profile infant gut microbiota in individual faecal samples.
统计分析
与统计分析系统(SAS)软件(版本9.4; SAS公司,卡里,NC,USA)进行数据的统计分析。微生物类群(在门,科或属级)和生物多样性的措施(超1,香农和辛普森指数)的相对丰度表示为中位数和四分位范围,因为这些措施不是正态分布。中值是使用非参数Wilcoxon秩和检验或Kruskal-Wallis检验> 2组的比较,有统计学意义在p <0.05相比。虽然有关的假设是乳酸杆菌先验中,的Benjamini-Hochberg的方法对错误发现率进行调整的p值(FDR,其中p
为了测试先验对婴儿性别研究问题并调整为假定的混杂因素,分析由婴儿性别,出生模式,哺乳状态和产抗生素曝光(也可用于婴儿使用抗生素强大的标志分层;28])。使用调整等级转换(ART)相互作用非参数检验[29],用于在婴儿性别和产妇产前哮喘之间的相互作用的p值乳酸杆菌丰度为0.001。要确定的母体合并症的影响,统计检验也被母体产前遗传性过敏症的状态和孕前体重(;超重≥25.0体重指数正常体重≤24.9)执行以下分层。产妇在怀孕期间哮喘之间的关联的独立性,以及最高或最低组乳酸杆菌使用目的的逐步逻辑回归模型,调整混杂因素进一步确定水平。为了鉴定判别分类生物标记物,线性判别分析效果大小(LEfSe)用线性判别分析(LDA)的日志积分截止的2,接着Kruskal-Wallis检验与Dunn的多重比较检验进行的,不使用产前产妇哮喘为参照组。
结果
在研究婴儿的9%是天生的妇女在怀孕期间哮喘,多数经阴道分娩;这些婴儿的8%被紧急剖腹产和选择性剖宫产7%诞生。小号imilar to the whole cohort, 79% of infants born to asthmatic mothers were fed breast milk at 3–4 months. Prenatal maternal asthma was not differentially distributed by infant sex or ethnicity, birth mode, early term birth, birthweight, breastfeeding status, maternal pre-pregnancy weight and maternal intrapartum antibiotic treatment (表格1);它往往是在两个最低和最高的婴儿体重增加三分位数越高。食品和怀孕期间的环境过敏是妇女产前哮喘比那些没有哮喘更常见。相较于完整儿童出生队列[20.],我们的1021对母婴儿童研究人口是在男性方面是相似的(53%与52%),白种人(78%与73%)和母的特应性状况(61%与58%)。
Gut microbiota of all infants at 3–4 months of age were dominated by members of the phyla Bacteroidetes, Firmicutes and Proteobacteria (supplementary figure S1). Microbiota in female infants tended to be enhanced with Bacteroidetes (median relative abundance, 20.8%与9.3%)。随着厚壁菌门的例外是在出生的女性患有哮喘(P = 0.03)女婴不丰富,没有其他的区别在门丰富,微生物丰富的多样性或妇女所生的婴儿与之间是明显与那些没有产前哮喘(补充图S1,补充表S1)。在中位数和高丰度原油差异用属的成员发现肠道定植乳酸杆菌据婴儿喂养和母亲的哮喘状态(表格1)。
联丰乳酸杆菌非白种人妇女和怀孕期间患有哮喘的妇女(表格1)。基于本领域的测试,用于产前哮喘和白种人之间的相互作用术语p值为0.002。在高加索人婴儿,产前产妇哮喘显著与属的下部的相对丰度相关联乳酸杆菌(中位数0.001%与0.002%,P = 0.01;表2)。该属是不是由非高加索婴儿产妇哮喘状态差异丰富(未示出数据)。通过分层婴儿性别产生统计学显着性在肠道减少乳酸杆菌白种男婴(中位数0.002%)与0.0005%, p=0.02),但不包括女性哮喘患者所生的女婴。内脏没有区别乳酸杆菌丰度被发现之间非高加索男性母亲所生与(中位数0.0005%,N = 5)和不具有(中位数0.0007%,N = 112)产前哮喘。
中号edian relative abundance of dominant bacterial taxa at the phylum, family and genus levels in infant gut microbiota at 3–4 months, according to maternal prenatal asthma in all Caucasian infants
为了减少围产期暴露的偏见,比较是只在阴道分娩,母乳喂养的婴儿,出生谁在不暴露于母亲的抗生素进行。受限制的分析显示类似的趋势属乳酸杆菌在男性的肠道菌群,高加索人婴儿(p值= 0.06)所生哮喘母亲(表3,补充表S2)。其他性别特异性差异发现。继产前哮喘,女性,白人婴儿的肠道,阴道分娩和母乳喂养,不暴露于母亲分娩抗生素,拟杆菌门的成员更丰富(P = 0.02,表3)和较少的肠杆菌科(p = 0.03)。差异也很明显拟杆菌家庭水平(p=0.02,补充表S2)在所有未使用产时抗生素的女性母乳喂养婴儿中,以及厚壁菌门的丰度降低(p<0.05)。
中号edian relative abundance of dominant bacterial taxa at the phylum, family and genus levels in infant gut microbiota at 3–4 months, by maternal prenatal asthma and infant sex in Caucasian, vaginally delivered, breastfed infants, not exposed to maternal antibiotics during birth
中号edian relative abundance of selected infant gut microbiota at 3–4 months, by maternal prenatal asthma, stratified by infant sex and maternal comorbid conditions during pregnancy
最高组的可能性乳酸杆菌abundance in the infant gut at 3–4 months of age according to maternal prenatal asthma, all children and sex-specific#
乳杆菌在妇女所生患有哮喘和伴随食物或环境过敏或哮喘和孕前超重的男性婴儿低丰度;统计显着性未在不存在任一合并症的观察(表4)。基于现有技术的测试,对产前哮喘和婴儿性别之间的交互作用项的p值乳酸杆菌丰度为0.003产妇特应性合并症和0.06超重合并症。继在怀孕期间同产妇哮喘合并症,丰拟杆菌基本上和在女性婴儿显著更高。该性别相互作用项的p值是0.001产妇特应性合并症和0.002超重(ART检验)。厚壁菌门均出生哮喘超重母亲的女性更丰富。中厚壁菌门门,属巨型球菌在患有超重或特异反应性哮喘的母亲并发哮喘后,婴儿的肠道内的含量较少,而这一差异在患有特异反应性哮喘母亲的女性中具有统计学意义(表4)。p值为性别交互项,表示差异Megasphera与母亲变应性哮喘丰度为0.14(ART测试)。怀孕期间继变应性哮喘,肠杆菌科在后代的肠道微生物不太常见,更多的是在男性比女性;只要拟杆菌富集存活校正多个测试。有一个例外(当粗p值0.06与以下限制减小的样品大小,如在呈现表3),减少乳酸杆菌丰也的FDR校正后的统计显著。
在调整了多变量回归协表明产前产妇哮喘和后代肠道乳酸杆菌之间的关系是相当强劲(表5)。独立的产妇过敏体质状况和怀孕前的体重,出生模式,产抗生素预防,母乳喂养状况和性别,怀孕期间暴露产妇婴幼儿哮喘是三分之一一样可能有乳酸杆菌abundance in the highest tertile at 3–4 months of age. Statistical significance was confirmed in male (aOR, 0.26, 95% CI 0.07–0.89), but not female infants (aOR, 0.48, 95% CI 0.17–1.32). Regression models to predict the lowest tertile乳酸杆菌结果显示,丰富的婴儿,没有显示出与产前哮喘状态的统计相关性(数据未显示)。只有2%的白人婴儿接受益生菌产品;他们被排除在分析之外并没有改变任何发现。
最后,使用LEfSe方法在种的水平测试差异(图1),未分类的乳酸杆菌种被发现是在出生与变应性哮喘母亲男性白种人的婴儿低丰度(LDA得分2.93,P <0.05)。未分类Megasphera物种(LDA得分3.34,P = 0.003)是相对较不丰富的和脆弱拟杆菌(LDA 3.29, p=0.02)在特应性哮喘母亲所生的白人女性婴儿中更为丰富。
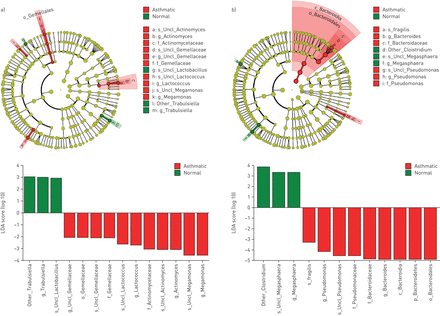
分支图和线性判别分析(LDA)曲线进行产前产妇变应性哮喘通过)的雄性和b)从LDA效果大小(LEfSe)方法女性白人的婴儿。
讨论
一世n a birth cohort study of 1021 full-term Canadian infants, we detected alterations to gut microbial composition at 3–4 months following pregnancy complicated with asthma与妊娠无哮喘。患有哮喘的母亲所生的婴儿窝藏较少乳酸菌在他们的肠道菌群,特别是如果他们是男性和白种人(p值= 0.02)的。此外,在还原乳酸杆菌物种丰富度是最明显的,如果白人母亲患有哮喘有怀孕前超重或食物或环境过敏史。虽然没有现有的证据将母体产前哮喘,这些发现与在与湿疹母亲新生儿胎粪中观察到的减少的乳杆菌丰度相容,并且降低与粪便定植乳酸杆菌种过敏的父母的婴儿[14,28]。在我们的研究中,出生于产前哮喘的母亲男婴是三分之一(AOR 0.26,95%CI:0.07-0.89)的可能与高水平的自主产妇超重或过敏体质状况,出身模式或乳酸杆菌,定植婴幼儿的饮食。这些协会是不存在的雌性后代。
男婴儿婴儿时期比女婴在发展中喘息的风险较高,特别是如果他们是白种人[27],虽然在肠道菌群组成的性别差异没有得到关注的焦点直到最近[15]。文学报告与男性抗生素使用超重的风险较高,但并非女婴表明男性肠道菌群环境扰动[的敏感性差17]。在他们的澳大利亚白人群体,C利夫顿等。[6)发现,男性胎盘母体哮喘发作的反应是最小的女性胎盘相比,很少有炎性基因表达变化和11在胎盘β-hydroxysteroid脱氢酶活动。胎盘反应的减少增加了男婴宫内生长受限的风险。值得注意的是,在我们的研究中,没有发现哮喘母亲所生的男婴的肠道微生物组成有其他显著变化乳酸杆菌差异幸存多个修正。与用于婴儿生长产前哮喘编程影响的证据,和婴儿的生长和肠道微生物组合物和特应性皮炎[之间的链路对准16,30.],我们的研究结果暗示了产前哮喘对婴儿肠道菌群可能的性别二态性的影响。
在婴儿期即在人类胃肠道内长期居住[31],在5岁患上特应性疾病的婴儿的肠道内,产生乳酸的乳酸菌较少[32,33]。乳酸杆菌当产前给予母亲物种都记录在母乳和脐带血,抗炎细胞因子水平ELEVATE生长和免疫因子[34]。和出生后,乳酸杆菌益生菌促进增重的婴儿[35]。最近的一项研究用FARR等。[36] observed birthweights of less than 2500 g to be more common following a mid-pregnancy vaginal microbiota dominated by non-lactobacilli与乳酸杆菌微生物。此外,在羊水乳杆菌找到的能够在胎儿肠调节的toll样受体的基因表达[的37]。在我们的研究中,在减少乳酸杆菌丰度为婴儿的母亲有哮喘和超重或过敏史中最为明显。事实上,在5岁时风险特应性敏感据报道升高,低乳酸杆菌colonisation by the age of 2 months in infants born to atopic parents [33]。其他高危队列研究也发现了不一致的特应性疾病的粪便微生物生物标记,如拟杆菌门菌或Ruminococcaceae或较高丰度的的梭状芽胞杆菌产业集群,但这些意见是很明显无论是在一个更年轻或年长的婴儿年龄;此外,在这些研究[未报告性别特异性结果38]。
孕妇孕期超重与后代患哮喘和其他特应性疾病的风险较高有关[39,40]。在我们的研究中,婴儿的母亲哮喘共病与这一增加的后代风险也产生了丰富的粪便减少巨型球菌在女婴和丰富的海拔拟杆菌。经罗斯福调整后,后者在统计上仍然显著;用LEfSe方法鉴定这两个物种在统计上更丰富。这两个巨型球菌和拟杆菌微生物在相反的条件下产生丙酸盐。的巨型球菌种利用乳酸作为底物生产丙酸盐[41],而拟杆菌物种产生丙当乳酸水平低[42]。丙酸盐被宿主吸收进行糖异生,具有抗炎和饱腹的特性[43,44],和防止过敏性哮喘的小鼠模型的发展[45]。
乳酸杆菌细菌可用于阴道分娩和哺乳期间的新生儿,且对抗生素治疗敏感[10,46,47]。剖宫产分娩和配方喂养必须减少乳酸杆菌和其它微生物的产妇转移到婴儿的潜在[13,48]。然而,在减少乳酸杆菌丰度也是在谁是母乳喂养以下无母抗生素阴道分娩男婴明显,尽管统计学意义的样本量减少后丢失。相同的情况下,的富集拟杆菌和枯竭Enterobactericeae在下面的产妇产前哮喘女微生物进行检测。有趣的是,在婴幼儿的同一队列中,我们发现,大量粪便的比率低Enterobactericeae来拟杆菌保护,以防止食物过敏[49]。因此,我们的研究结果表明,在塑造早期肠道定植编程作用,为孕产妇哮喘,不能归因于剖腹产手术,抗生素使用或配方奶喂养,并通过不同性别和可能赋予对女婴过敏[更少直接风险45]。
我们的研究有几个优点。我们的研究结果是基于一大群足月婴儿,其中包括早期足月婴儿,他们更有可能由患哮喘的妇女分娩并发展为哮喘[7,50]。大样本量也通过协变量进行分层,以确定微生物群与母体哮喘之间的关系,这与出生相关事件无关[28]。我们调整了多重检验的p值,并用非参数检验验证了性别和种族的相互作用。高通量基因测序能够在婴儿粪便样本中对整个微生物群落进行分析,而迄今为止的大多数研究都以单个物种为目标。另一方面,虽然妊娠调查表所列的标准已被证实为产前哮喘发病率的衡量标准,但孕妇在妊娠期间的哮喘状况并没有得到医生的证实;我们也没有测试哮喘的严重程度,这可能解释了母亲哮喘对出生体重的适度影响[51]。
产前和产后暴露是在婴幼儿健康编程电位刺激,通过肠道菌群的修改[52,53]。新生儿肠道定植初期起着免疫系统发展的核心作用[54]。我们的研究结果提供的产前产妇哮喘对肠道微生物组成的节目效果,是独立的出生和出生后的活动的第一个证据。除了更小尺寸的肺在出生[20.]或其他导致喘息的风险因素[27,肠道乳酸菌的减少为高加索男性婴儿的持续性哮喘指明了另一条途径。较少的肠道乳酸菌对男婴也有额外的影响,如降低对病原体的抵抗力[55]。而肠道微生物的变化,如丰度的增加的拟杆菌,可能有女婴有保护作用。
补充材料
致谢
我们感谢所有参与本次研究的家庭和整个儿童团队,其中包括采访者、计算机和实验室技术人员、文书工作人员、研究科学家、志愿者、经理、接待员和护士。我们感谢Sarah Bridgman帮助完成了最终版本的手稿,感谢Konstantin Shestopaloff完成了艺术测试。Anita Kozyrskyj将作为本文内容的担保人。
儿童研究调查:SS阿南德,麦克马斯特大学;MB阿扎德,曼尼托巴大学;AB贝克尔,曼尼托巴大学;AD Befus,加拿大阿尔伯塔大学;中号布劳,英属哥伦比亚大学;JR布鲁克,多伦多大学;Ë陈,西北大学,芝加哥;MM CYR,麦克马斯特大学;d戴利,英属哥伦比亚大学;SD戴尔,在病童医院和多伦多大学; JA Denburg, McMaster University; QL Duan, Queen’s University; T Eiwegger, The Hospital for Sick Children and University of Toronto; H Grasemann, The Hospital for Sick Children and University of Toronto; K HayGlass, University of Manitoba; RG Hegele, The Hospital for Sick Children and University of Toronto; DL Holness, University of Toronto; P Hystad, Oregon State University; M Kobor, University of British Columbia; TR Kollmann, University of British Columbia; AL Kozyrskyj, University of Alberta; C Laprise, Université du Québec à Chicoutimi; WYW Lou, University of Toronto; J Macri, McMaster University; PJ Mandhane, University of Alberta; G Miller, Northwestern University, Chicago; TJ Moraes, The Hospital for Sick Children and University of Toronto; P Paré, University of British Columbia; C Ramsey, University of Manitoba; F Ratjen, The Hospital for Sick Children and University of Toronto; A Sandford, University of British Columbia; J Scott, University of Toronto; JA Scott, University of Toronto; MR Sears (Founding Director), McMaster University; F Silverman, University of Toronto; E Simons, University of Manitoba; P Subbarao (Director), The Hospital for Sick Children and University of Toronto; T Takaro, Simon Fraser University; SJ Tebbutt, University of British Columbia; T To, The Hospital for Sick Children and University of Toronto; SE Turvey (Co-director), University of British Columbia.
作者投稿:公厕Koleva进行统计分析,编写数字和表格,并写手稿的第一稿。A.L. Kozyrskyj设想的研究并获得资金,设计,分析和撰写文章的最终版本。H.M.墩进行的LEfSE分析。在J.A.的监督斯科特,T.科尼亚在D.古特曼的实验室中进行DNA提取和样品制备用于测序。生物信息学菌群被J.A.进行斯科特D.格特曼,A.B贝克尔,P.J. Mandhane,P.的Subbarao,S.E. Turvey; and M.R. Sears helped obtain funding, advised on the study design, and coordinated data collection. All authors provided critical comments on the manuscript content and approved the final version of the manuscript.
脚注
这篇文章有提供补充材料www.qdcxjkg.com
支持声明:卫生研究院(CIHR)和过敏,基因和卓越中心的环境(过敏原)网络的加拿大学院提供给儿童学习的核心支持。这项研究是专门由CIHR微生物组计划团队资助,#227312资助。本文资金的信息已交存交叉引用出资者注册
利益冲突:无申报。
- 收到2017年2月8日。
- 公认2017年8月16日。
- 版权所有©ERS 2017年
这篇ERJ开放文章是在知识共享署名非商业许可4.0188滚球软件条款下开放获取和发布的。















