抽象的
需要靶向慢性阻塞性肺疾病(COPD)中长期活化激酶途径的新型抗炎方法。我们评估了rV568,P38丝裂原激活的蛋白激酶-α和-γ和SRC系列激酶抑制剂,细胞和在活的有机体内与COPD相关的模型,并检查了COPD患者的安全性和疗效。
RV568的抗炎活性在初级培养的单核细胞,巨噬细胞和支气管上皮细胞中进行测试在活的有机体内脂多糖和香烟烟雾暴露小鼠模型。在一项为期14天的COPD患者试验中评估了RV568。
RV568对单核细胞和巨噬细胞显示出有效的抗炎作用,其通常大于皮质类固醇或P38抑制剂BIRB796。RV568结合皮质类固醇具有抗炎作用,暗示Poly I:C刺激的BEA-2B细胞和卷烟模型中的协同相互作用。在COPD患者中,吸入的RV568(50μg和100μg)改善了1 s(分别为69ml和48毫升)的前支气管扩张剂强制呼气量,与安慰剂相比,显着降低了痰丙醛(P <0.05),尽管没有变化在痰细胞计数中。RV568和安慰剂治疗期间的不良事件相似。
RV568显示了与COPD相关的细胞和动物模型的有效的抗炎作用。RV568耐受良好,并在14天的COPD临床试验中表现出适度的临床益处。
抽象的
激酶抑制剂RV568是COPD模型的抗炎,并在小试验中显示出临床疗效的迹象http://our.ly/aasj30fjoql.
介绍
慢性阻塞性肺疾病(COPD)的特征是由于接触有毒颗粒(通常是吸烟引起的)而导致肺部过度发炎[1].吸入的皮质类固醇(IC)是COPD中最常用的抗炎药,但这些药物有限的临床益处,可引起副作用[2].需要新的抗炎方法来治疗COPD。
COPD中的气道炎症涉及不同的炎症细胞类型,包括中性粒细胞,巨噬细胞,淋巴细胞和上皮细胞[3.].一系列细胞内激酶调节这些细胞的炎症反应。P38丝裂原激活的蛋白激酶(P38 MAPK)涉及炎症细胞因子转录,mRNA稳定化和蛋白翻译[4.那5.].COPD患者肺中p38 MAPK激活增加,p38 MAPK抑制剂抑制COPD肺泡巨噬细胞、淋巴细胞和支气管上皮细胞中细胞因子的分泌[6.-9.].然而,p38 MAPK抑制剂在COPD临床试验中显示了不同的效果,一些长期研究显示没有临床益处[10.-12.].p38 MAPK有4种亚型:α、β、γ和δ。具有α亚型选择性的p38 MAPK抑制剂已用于临床试验,因为这种亚型在免疫细胞上表达。γ亚型在COPD肺组织中表达,并在皮质类固醇抵抗性炎症中发挥作用[13.].单独的P38 MAPK-α同种型的靶向不会抑制其他P38 MAPK同种型的促炎信号传导,或由参与COPD病理生理学的其他激酶途径[14.].
最近开发了一系列抑制参与COPD炎症的选定激酶的小分子试剂,包括RV568 [15.].这些所谓的“窄光谱激酶抑制剂(NSKIS)”设计用于P38 MAPK的α和γ同种型的高效力。此外,化学修饰确保了对SRC激酶家族的活性,特异性血糖激酶(HCK)。Hck参与普丙比丙酮糖(LPS)刺激的巨噬细胞炎症反应,并在来自COPD患者的外周血单核细胞(PBMC)中过表达[16.那17.].这些NSKI设计用于吸入肺部保留,以便促进一次每日给药,并最大限度地减少系统副作用的潜力。此外,P38 MAPK抑制可能通过增强的糖皮质激素受体易位的机制增加皮质类固醇的抗炎作用[18.].NSKI的潜在属性,例如RV568可以是具有皮质类固醇的协同药理活性。
我们表征了使用RV568的抗炎活动体外和在活的有机体内与COPD炎症相关的模型。将RV568与皮质类固醇的影响进行比较,并且当与皮质类固醇组合使用时,我们研究了药理学效应。我们还在COPD患者中报告了吸入的RV568的随机,安慰剂对照临床试验,主要是这种新药的安全性,还提供了研究抗炎作用的机会。
材料和方法
细胞测定
用细菌蛋白LPS刺激单核细胞和巨噬细胞样细胞;使用THP1细胞,PBMC,分化的THP1,Phorbol 12-Myristate 13-醋酸酯分化的U937(D-U937)细胞和痰巨噬细胞。使用Toll样受体3(TLR3)激动剂多I:C和细胞因子肿瘤坏死因子-α(TNF-α)刺激以下上皮细胞:来自健康受试者和BEA-2B细胞的原发性支气管上皮细胞。测定RV568,BiRB796(PAN-P38抑制剂)和皮质类固醇丙酮丙酸酯(FP)对细胞因子释放和细胞间粘附分子(ICAM)-1蛋白表达的影响。这些方法的完整细节可以在线补充材料中找到。
鼠标模型
使用吸入的LPS诱导的肺炎症的小鼠模型和肺炎症的鼠烟烟雾模型如前所述[15.].进行支气管肺泡灌洗(BAL)以测量细胞计数和炎症蛋白。进一步的详细信息位于在线数据补充中。
临床试验
随机,双盲,并联群体研究(临床试验.GOVnct01475292.)在药物评估处(英国曼彻斯特)进行。30例COPD患者被招募。研究对象为吸烟者或戒烟者,年龄40-75岁,沙丁胺醇后1秒强迫呼气量(FEV)1预测和一个FEV,≥40%和≤80%1/强制生命能力比率≤0.70。患有重要其他医疗条件的患者被排除在外。参与者被允许在整个研究中留下目前的吸入治疗。在整个研究中禁止使用全身皮质类固醇(口服,肠胃外或仓库),口服β-2激动剂,茶碱,磷酸二酯酶抑制剂,口服白三烯抑制剂或抗生素治疗。受试者被随机(1:1:1的比例),每天一次接收RV56850μg,RV568100μg或安慰剂14天。
所有给药剂量均使用飞利浦呼吸器I-neb自适应气溶胶输送(AAD)系统(飞利浦呼吸器公司,阿姆斯特丹,荷兰)。以下预先定义的标准用于在治疗期间撤出受试者,以确保安全性:1)加重需要口服皮质类固醇和/或抗生素治疗,2)支气管扩张剂后FEV下降1> 20%和3)FEV1<35%预测。主要终点是安全性,如评价:不良事件,心电图参数,临床实验室评估(血液学,临床化学和尿液分析)和FEV1。其他端点包括药代动力学(PK)参数和痰生物标志物分析治疗效果(在线补充材料中描述了免疫测定)。
统计分析
临床研究的样本量基于安全考虑因素,将有限数量的COPD患者暴露给新型药物。安全分析包括所有接受≥1剂量的受试者。PK分析包括≥1个PK样品的所有受试者。FEV.1使用协方差分析进行痰生物标志物分析。分析体外和在活的有机体内通过ANOVA或T检验进行实验。IC.50.(中值抑制浓度)使用GraphPad Prism(GraphPad Software Inc.,La Jolla,CA,USA)或XLFIT软件包(IDB,Guildford,UK)计算。两种药物之间相互作用的组合指数如前所述进行[19.].
结果
RV568在单核细胞和巨噬细胞中的影响
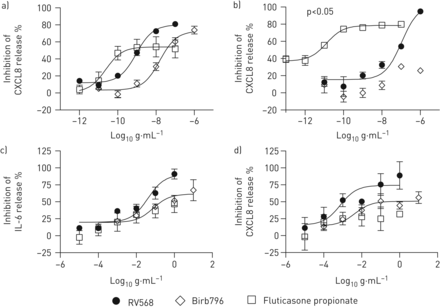
在健康志愿者的pbmc中测量脂多糖诱导的CXCL8释放。RV568或Birb796具有浓度依赖性的CXCL8抑制作用(无花果。1A).E.最大限度(81%)的(最大响应)大于BIRB796(60%)和FP(50%)的大于那。使用THP1细胞和COPD PBMC的类似实验的结果描述于在线补充(在线补充表S1)。
RV568减少单核细胞,巨噬细胞和上皮细胞中的炎症。a)抑制脂多糖(LPS) - 在健康外周血单核细胞(PBMC)中抑制CXCL8释放。从健康志愿者(n = 3)的全血中分离出PBMC,并用0.1μg·ml处理-1LPS 4小时。b)在D-U937细胞中抑制LPS诱导的CXCL8释放。将U937细胞与Phorbol 12- myristerate 13-乙酸盐(n = 3)分化成巨噬细胞样电池中,并用0.1μg·mL处理-1LPS 4小时。c)抑制肿瘤坏死因子(TNF)-α-诱导的白细胞介素(IL)-6在正常人支气管上皮细胞(NHBE)中的释放。用50 ng·mL刺激NHBEs (n=3)-1TNF-α 4 h。d)抑制tnf α诱导的CXCL8在NHBEs中的释放。用50 ng·mL刺激NHBEs (n=3)-1TNF-α 4 h。通过ELISA在无细胞上清液中测量细胞因子释放;通过与载体对照进行比较计算百分之规的抑制。数据显示为平均值±SEM.;ANOVA与DUNN的测试,P <0.05至RV568。
检查LPS刺激的D-U937细胞中的CXCL8释放(无花果。1B.).Birb796对CXCL8影响不大,而RV568和FP均显示出浓度依赖性CXCL8抑制,RV568达到比FP(80%)达到更高的Emax值(95%),而FP效力较高> 100倍下层IC50.值(92海里相对0.006 nm)。在线补充(在线补充表S1)中描述了使用D-U937和分化的THP1细胞的其他实验的结果。只有RV568显着抑制COPD痰巨噬细胞的CXCL8释放(55%抑制;在线补充图S1B,在线补充表S3)。
RV568抑制上皮细胞系统中细胞因子的释放
使用初级正常支气管上皮细胞,我们检查了TNFα诱导的白细胞介素(IL)-6和CXCL8释放;RV568以浓度依赖的方式抑制细胞因子释放,BIRB796和FP展示较低效果(无花果。1C和d)。用Poly I:C刺激BEA-2B细胞:C增加了ICAM-1蛋白表达。再次,这是由RV568抑制的(例如最大限度97%),而Birb796和FP没有影响(在线补充图S2)。
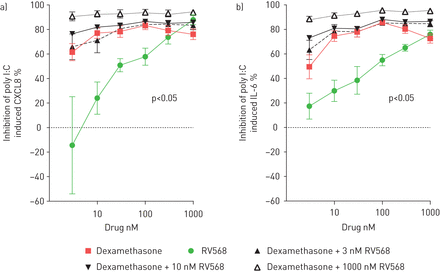
在Poly I:C刺激的BEA-2B细胞中检查了地塞米松(DEX)和RV568对IL-6和CXCL8释放的影响(无花果。2和在线补充图S3)。只有两种药物都显示出浓度依赖性细胞因子抑制。用10nm rv568的地塞米松引起了对单独的地塞米松的细胞因子释放的更大抑制。进一步增加了RV568的浓度与皮质类固醇组合产生逐渐更大的细胞因子产生抑制。许多这些组合条件使用组合指数分析时展示了协同作用(在线补充表S4)。
抑制poly i:C诱导的BEA-2B细胞细胞因子释放。将细胞单独使用与地塞米松预孵育,单独的RV568和两种药物在用Poly I:C刺激之前在所有指示的浓度下组合1小时。a)抑制poly i:c诱导的cxcl8。b)抑制聚I:C诱导的白细胞介素(IL)-6。通过ELISA在无细胞上清液中测量细胞因子释放;通过与载体对照进行比较计算百分之规的抑制。数据显示为平均值±SEM.;n = 8;ANOVA与DUNN的测试,P <0.05至RV568。
体内RV568的分析
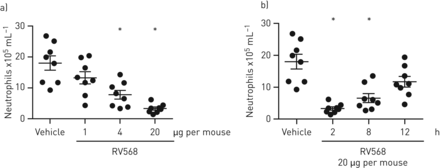
鼠LPS模型用于评估RV568的效力和行动持续时间。在LPS吸入之前,RV568在溶液制剂中肿瘤内递送2小时。RV568阻止在BAL流体中积聚中性粒细胞(在线补充图S4)。使用悬浮制剂重复该实验,RV568显示出类似的效果(无花果。3A).此外,在吸入LPS前8小时,RV568可显著抑制中性粒细胞积累(无花果。3B.).
RV568抑制脂多糖(LPS)诱导的中性粒细胞,在小鼠中具有很长的作用。a)在LPS暴露之前,脑内(n = 8)在脑内(n = 8)在载体或RV568 2 H溶液中施用通过吸入。b)在LPS暴露之前,在指定的时间点,在脑内(n = 8)在载体或RV568的溶液中进行肿瘤内施用。在LPS挑战和中性粒细胞流入测量后,收集支气管肺泡灌洗8小时。数据显示为平均值±SEM.;ANOVA与Dunnett的测试,*:P <0.05到车辆控制。
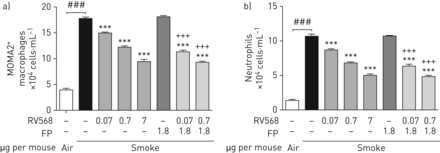
研究人员对暴露于香烟烟雾11天后的小鼠进行了RV568的治疗效果研究。图4.表明,氟丙酮在第15天减少了Bal巨噬细胞和中性粒细胞数。RV568以剂量依赖的方式减少这些细胞系数。当RV568与无效的FP剂量相结合时,与单独的RV568的效果相比,效果显着增强。在BAL上清液中测量炎症介体水平。RV568显着降低了趋化介质介质,TH1和TH17细胞因子,重塑标记以及氧化应激标记物丙二醛(MDA)(在线补充表S5)。在所有情况下,RV568和FP的组合导致单独的RV568或FP有显着差异。
RV568的治疗给药衰减在小鼠中吸烟诱导的炎症。每日暴露于30分钟的香烟烟雾11天,然后持续3天的载体,氟基丙酸酯(FP),RV568或指出的药物组合(μg/μg鼠)。在最后一次药物管理后24小时收集支气管肺泡灌洗(BAL),通过荧光激活细胞分选(FACS)分析测定肺泡巨噬细胞和中性粒细胞的数量。a)moma2+-Macrophage积累BAL。b)BAL中的中性粒细胞累积数据显示为平均值±SEM.;ANOVA与Dunnett的测试:***:与P <0.001的卷烟烟斗控制有显着差异。###: 显着差异相对空气控制p<0.001和+++: 显着差异相对通过与韦尔奇的矫正进行T检验,在P <0.001处进行FP处理。
RV568在COPD患者中的临床试验
有71个屏幕故障,主要是由于存在其他重要的医疗条件(在线补充表S2)。30名参与者的人口统计显示在表1。平均fev.1和吸烟状态(当前或以前)和吸入的药物在群体之间是相似的,尽管使用安慰剂组使用三重治疗的更多患者(两个长效的支气管扩张剂加入吸入皮质类固醇)。
由于FEV的跌倒,从研究中撤出了两名患者1>从基线值20%;在单个RV568100μg剂量后被撤回,没有随附的症状发生变化,另外6天后用RV56850μg治疗流感样症状。不良事件配置文件在治疗组之间类似(在线补充表S6)。任何科目都没有重大的心电图变化。
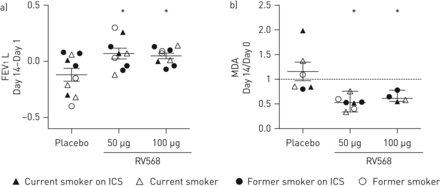
支气管扩张剂前FEV有显著改善114天后用RV568100μg和50μg处理与安慰剂相比(平均处理差异为48mL(p = 0.014)和69ml(p = 0.0067)(无花果。5A)),患者使用类似的效果而不是使用IC。与安慰剂(与基线相比,14天的中位变化分别为-0.06L和0.125L,分别有改善RV568100μg(24天的中值变化)。在线补充图S5)。其他肺部量测量或特定的气道电导没有显着变化。
临床和痰生物标志物在慢性阻塞性肺病患者中14天施用14天施用后改善。a)预先支气管扩张剂强制呼气量1 s(fev1)用RV568治疗后第14天发生变化。数据显示为平均值±SEM.;与Bonferonni的Anova与安慰剂的多重比较,*:P <0.05。安慰剂n = 10;50μgn = 9;100μgn = 9。b)用RV568处理后第14天痰上清液丙二醛(MDA)变化。数据显示为平均值±SEM.;与Bonferonni的Anova与安慰剂的多重比较,*:P <0.05。安慰剂n = 6;50μgn = 7;100μgn = 4。ICS:吸入皮质类固醇。
痰细胞计数没有变化(n = 17名在基线和第14天生产痰样品的患者)。RV568显着降低MDA水平(两种剂量的P <0.05);用RV568治疗的每个受试者在第14天减少了MDA水平(无花果。5B.).CXCL8和基质金属蛋白酶-1水平有数值减少(在线补充表S7),但没有RV568对痰生物标志物的其他显着影响。
药代动力学总结在在线补充表S8和S9中,并进一步在于在线补充材料中描述。
讨论
我们已经表现出RV568对与COPD相关的细胞和动物模型的抗炎作用。我们还表明,RV568在14天的临床试验中耐受良好,具有改善肺功能和对痰生物标志物的抗炎作用的初步证据。临床前数据显示RV568比P38抑制剂BIRB796具有更大的抗炎作用,这可能是由于RV568靶标的激酶的不同型材。此外,RV568表现出比巨噬细胞和上皮细胞模型的皮质类固醇更大的抗炎活性,以及香烟烟鼠模型。RV568与皮质类固醇的组合带来了抗炎作用,表明协同相互作用。这些结果促进了对RV568的更长临床研究的情况。我们现在从临床前和临床调查中讨论了调查结果。
蜂窝模型
我们设计了使用LPS模仿细菌感染对单核细胞和巨噬细胞对单核细胞和巨噬细胞的影响,以及使用与TLR3激动剂多I:C刺激的上皮细胞的病毒感染的影响。RV568在两种细胞模型中表现出抗炎作用。上皮模型特别是皮质类固醇抗性,而BIRB796也没有效果。这表明RV568至少部分地通过SRC激酶抑制来施加抗炎作用。在支气管上皮细胞的人鼻病毒感染后SRC激活,TLR3和ICAM-1都是人鼻病毒感染的受体[20.那21.].
用地塞米松的组合研究对多种I:C刺激上皮细胞的细胞因子产生表现出协同抗炎作用。Birb796具有抗炎症协同作用,其在LPS刺激的COPD巨噬细胞中的地塞米松[7.]和P38 MAPK抑制可以从哮喘患者中逆转细胞模型和细胞中的皮质类固醇细胞内不敏感性[22.-24.].P38 MAPK磷酸化糖皮质激素受体(GR)[25.].mercado.和同事[13.那18.[证明P38Mapk-α/β和/或MAPK-γ参与缺陷GR核转移,RV568可以通过调节P38磷酸化来增强GR核转移。我们的体外数据表明RV568的潜力抑制COPD患者病毒感染过度炎症反应。
在单核细胞和巨噬细胞模型中,RV568始终表现出比Birb796更强的药理作用。先前的报道显示,化学上不同的p38抑制剂对原发性肺巨噬细胞有有效的抑制作用(E最大限度大约70%的TNF-α释放,但对其他炎症介质的效果较低,包括CXCL8 [26.那27.].我们的实验类似于CXCL8,因为BiRB796对来自分化成巨噬细胞(D-THP-1细胞或D-U937细胞)或COPD痰巨噬细胞的CXCL8分泌物的影响最小。相比之下,RV568引起了显着的CXCL8抑制作用最大限度分化巨噬细胞的值> 70%,并在痰巨噬细胞中抑制> 50%。RV568针对P38 Mapk-α和-γ,并与Birb796的效力不同于这些同种型。此外,针对SRC激酶的RV568的活性也可能有助于观察到的差异;SRC系列激酶参与LPS和氧化应激的巨噬细胞活化[28.].
皮质类固醇和RV568在单核细胞模型和D-U937细胞中具有类似的效果,这些药物之间没有一致的差异。然而,在分化的THP-1细胞和COPD巨噬细胞中,皮质类固醇对CXCL8分泌具有最小的影响。多种研究表明,来自COPD和对照肺巨噬细胞的CXCL8分泌是皮质类固醇不敏感的,在高皮质类固醇浓度下具有<60%的抑制[29.那30.].此外,巨噬细胞衍生的细胞因子在对皮质类固醇的敏感性之间存在相当大的变化,尽管对细胞因子之间的这些差异负责的机制尚不清楚。RV568的效果比巨噬细胞衍生的CXCL8生产上的皮质类固醇更大。CXCL8是中性粒细胞趋化因子,在COPD肺中发现水平增加[31.那32.];CXCL8过生产的抑制可能具有治疗性益处。
鼠标模型中的影响
RV568显示了对小鼠中LPS诱导的嗜中性气道炎症的剂量反应影响。在LPS挑战之前8小时给药导致约60%的抑制,在单剂量后表明延长的气道活动。
香烟烟鼠模型通常用于模拟COPD的病理生理学特征。在与以前的出版物的一致意见中,我们发现皮质类固醇治疗对炎症反应没有影响[33.那34.].相反,RV568对中性粒细胞和巨噬细胞数和一系列细胞因子引起了显着抑制。这些结果表明了RV568能够解决烟雾诱导的皮质类固醇抗性炎症的能力。烟雾激活SRC,其抑制可防止烟雾诱导的P38在上皮细胞中激活[35.].
有趣的是,RV568与皮质类固醇的给药导致炎症的抑制作用于单独的RV568,暗示协同效应并与我们的细胞结果一致。这在活的有机体内观察表明这些药物在临床实践中同时施用的可能性可能会提高整体疗效。
COPD患者的临床试验
临床试验主要进行调查安全性,因为RV568尚未向以前给COPD患者施用。因此,我们使用了小的样本量,限制临床发展早期患者的患者暴露。这两周的研究中没有任何安全问题。
本研究提供了探讨临床疗效的机会,尽管使用小样本。FEV有一个改善1与安慰剂分别为100μg和50μg相比,48毫升和69毫升。较低剂量似乎引起更大的效果。然而,对于残余体积,仅在更高剂量的剂量下观察到RV568的效果。MDA是一种氧化应激生物标志物,其在COPD患者中升高[36.那37.].在用RV568处理的每只患者中观察到显着一致的MDA还原,强烈表明对氧化应激水平的影响。小患者数意味着从这些肺功算或生物标志物测量中不太可能获得准确的剂量 - 响应信息。此外,不可能确定患者的哪个亚组可能导出更多的好处,如。那些采取IC或现任或出吸烟者。然而,这些结果表明,应在临床试验中进一步研究的临床益处,较大的患者数量。鉴于少数科目和短暂的试验持续时间,我们决定不使用患者报告的结果工具测量症状分数,因为这需要更大的样本尺寸来鲁棒地检测治疗效果。
RV568对痰液细胞计数无影响,但对痰液MDA水平有影响。关于治疗效果的痰数据的不一致性可能是由于样本量,因为COPD患者的痰中性粒细胞测量容易出现日间变异性[38.].除了MDA水平外,我们还没有证明药物的抗炎作用,但肺功能数据表明了一些药理作用。总体而言,我们认为这些结果是COPD患者在需要验证的COPD患者中的抗炎作用的初步发现。
结论
与COPD中炎症相关的细胞和动物模型的结果表明,RV568具有抗炎活性,其通常超过皮质类固醇的影响。此外,有证据表明RV568与皮质类固醇之间的协同相互作用。小型临床试验为COPD患者提供了抗炎和肺功能效益的初步证据,需要进一步调查较大,长期试验。
补充材料
披露的信息
致谢
作者贡献:CEC,PR,KI,YK,SL和DS构思和设计了这项研究;CEC和SL执行了实验;CEC,KI,CB和SL分析了数据;CEC,PR,KI,YK,CB,SL和DS解释了结果;CEC,PR和SL准备了这些数字;CEC,PR和DS起草并修订了稿件;所有作者批准了最终版本。
脚注
本文提供了补充材料www.qdcxjkg.com
支持声明:本报告包括国家卫生研究所(NIHR)南部曼彻斯特呼吸道和过敏临床研究设施的独立临床研究,并在南部曼彻斯特NHS基金会基金会信托大学医院。本出版物中表达的观点是提交人,而不一定是NHS,国家卫生研究所或健康部的国家。本文的资金信息已存入Crossref资助者注册表。
利益冲突:可以在本文中找到披露www.qdcxjkg.com
- 已收到2017年1月26日。
- 公认2017年7月27日。
- 版权所有©2017