摘要
背景2019年传染性冠状病毒病(COVID-19)大流行是一项持续的全球卫生保健挑战。多达三分之一的住院病人会出现严重的肺部并发症和急性呼吸窘迫综合征。COVID-19后的肺部预后尚不清楚。
方法瑞士COVID-19肺部研究是一项多中心前瞻性队列研究,研究COVID-19肺部后遗症。根据世界卫生组织的严重程度分类,我们报告了COVID-19轻度/中度或重度/危重症4个月后的初步随访情况。
结果113例COVID-19幸存者(轻度/中度47例,重度/危重66例)。我们确认了几种合并症是严重/危重疾病的危险因素。严重/危重疾病与肺功能受损相关,即。肺对一氧化碳的扩散能力(DLCO) %,减少6分钟步行距离(6MWD)和运动引起的氧饱和度降低。在对年龄、性别和身体质量指数(BMI)等潜在混杂因素进行调整后,重症/危重型COVID-19患者的预后呈下降趋势DLCO20.9% pred下降(95% CI 12.4-29.4% pred, p=0.01)。DLCO当年龄、性别、BMI、6MWD和运动时最小外周氧饱和度纳入多变量模型时,% pred是与既往严重/危重疾病相关的最强独立因素(调整后每10%的优势比预测为0.59,95% CI 0.;37 - 0.87;p = 0.01)。随访时胸部ct马赛克低衰减与既往严重/危重COVID-19显著相关,包括年龄和性别调整(校正OR 11.7, 95% CI 1.7-239;p = 0.03)。
结论在严重急性呼吸综合征冠状病毒2型感染后4个月,严重/危重型COVID-19与显著的功能和放射学异常相关,可能是由于小气道和肺实质疾病。需要评估幸存者的系统随访,以优化COVID-19康复患者的护理。
摘要
COVID-19肺部后遗症未知。瑞士COVID-19肺部研究报告了初步随访结果。4个月后,严重或危重型COVID-19与显著的功能损害和放射学异常相关。https://bit.ly/34sNVvi
简介
严重急性呼吸综合征2型冠状病毒(SARS-CoV-2)是导致2019年冠状病毒病(COVID-19)的冠状病毒,目前的大流行是全球卫生保健领域最严重的持续问题。迄今为止,已有140万人死于COVID-19 [1].截至2020年11月25日,瑞士共有309 469名患者被诊断为COVID-19, 4030名患者死亡[2].
COVID-19是一种异质性疾病,大多数患者病情轻微并可自行康复,但有相关亚群患者因肺炎和其他并发症需要住院治疗。在来自中国武汉的初步报告中,多达三分之一的患者出现严重肺炎伴急性呼吸窘迫综合征(ARDS) [3.].虽然我们已经发现了很多关于急性SARS-CoV-2疾病的发病机制和治疗方法,但中期和长期结果仍然未知,特别是在严重病程的幸存者中。
此前的冠状病毒感染包括严重急性呼吸综合征(SARS)和中东呼吸综合征(MERS)。与COVID-19类似,SARS和中东呼吸综合征通常始于急性疾病,大多数患者在2周后康复。然而,高达三分之一的沙士病人出现严重的肺部并发症及急性呼吸窘迫综合征[4].一组SARS幸存者出现持续性肺实质异常,包括肺纤维化[5,6].肺纤维化的出现与急性疾病的严重程度和持续时间有关[7,8],在3个月和6个月后,约30%的患者的放射学特征仍然存在纤维化[9,10].年龄较大和男性被认为是预后不良和肺纤维化发展的危险因素[9,11].
考虑到COVID-19后可能出现的长期后遗症,来自美国、英国、中国和印度的几个小组提出了后续战略[12- - - - - -15].
瑞士是最早受到COVID-19影响的欧洲国家之一,自2020年2月25日起,确诊病例数量不断增加[2].2020年3月16日,中国开始在全国范围内实施封锁,以防止疫情进一步蔓延。6个月后,我们不仅在COVID-19急性患者护理方面面临挑战,而且在COVID-19幸存者出现疾病后遗症的随访和管理方面面临挑战。
我们发起了多中心瑞士国家COVID-19肺部研究小组,以评估COVID-19的肺部后遗症。在我们的前瞻性队列的第一次分析中,我们报告了经历过轻度至中度(轻度/中度)和严重至危重(严重/危重)COVID-19的患者的慢性肺后遗症,目的是提高目前对COVID-19异质性轨迹的理解。
方法
研究环境、患者和临床测量
这项全国性、多中心、前瞻性观察队列研究包括急性COVID-19存活下来的成年人,并在轻度/中度或重度/危重型COVID-19后进行临床随访。
瑞士COVID-19肺部研究的贡献中心有伯尔尼大学医院(Inselspital和tiefenaunital)、洛桑大学医院、日内瓦大学医院、苏黎世大学医院、圣加伦康顿医院、弗莱堡康顿医院、锡安医院、巴塞尔医院(Claraspital)和泰辛医院(卢甘那蒙库科诊所)。所有患者入组前均提供书面知情同意书。研究于2020年5月1日开始前获得了伦理批准(KEK 2020 - 00799)。基线信息,如。最初出现的症状是从医疗记录中提取的肺功能测试,测量肺对一氧化碳的扩散能力(DLCO)和6分钟步行试验(6MWT)均采用既定方案[16- - - - - -19].通过测量口腔最大静态吸气压力和最大静态呼气压力来估计呼吸肌力量[20.].对有临床症状的患者进行胸部计算机断层扫描。
根据世界卫生组织描述的四种严重程度,患者被分为以下两组:1)轻度疾病,或中度疾病,临床症状为肺炎和外周氧饱和度(年代阿宝2)≥90%(轻度/中度);2)重症肺炎等年代阿宝2<90%,呼吸频率>30次·min−1或者严重疾病,即。急性呼吸窘迫综合征、败血症、感染性休克及多器官衰竭(严重/危重)[21].
胸部CT采集
根据参与中心的当地协议进行标准胸部CT扫描。113例纳入患者随访52例胸部CT扫描。所有胸部CT扫描均以约1mm的切片厚度重建。只有在怀疑肺栓塞和/或临床情况恶化时才使用碘造影剂。根据需要在轴向面、冠状面和矢状面进行多平面重建。所有图像用肺和软组织核重建,存储在本地图像存档和通信系统(PACS)中。
图像分析
所有可用的CT扫描均收集自伯尔尼和洛桑,并在当地图像档案系统中去识别(洛桑的PACS Carestream Health, Rochester, NY, USA;Sectra PACS, IDS7, Linköping,瑞典伯尔尼)。来自两家三级保健中心的两名亚专科胸科放射科医生对患者的临床状况不知情,进行了共识读出。在阅读过程中,放射科医生在线回顾了病例通过屏幕共享(Cisco Webex, Milpitas, CA, USA),因为当前的大流行法规限制了实体会议。读者评估了以下胸部CT表现:实变、磨玻璃样影(局灶性、多灶性、弥漫性)、马赛克状衰减模式(低衰减区、高衰减区)、小叶周围实变(有组织的肺炎样)、网状、结构扭曲、蜂蜂窝、牵引性支气管扩张、气囊肿、曲线线、结节、胸膜增厚或胸腔积液、粘液堵塞、血管异常及其他征象分别标注。此外,还记录了模式分布(上叶、中叶/舌叶、下叶)。基于F .提出的系统,对疾病程度进行半定量估计rancone等.[22].CT评分来源于大叶受累程度,采用五分制(0:0%,1:<5%,2:5 - 25%,3:26-50%,4:51-75%,5:>75%;范围0 - 5;全球得分0-25)。
统计分析
描述性统计报告为均数±sd或中位数(四分位差(IQR))。对类别变量采用卡方检验或Fisher精确检验,对连续变量采用双样本t检验或Wilcoxon秩和检验,分析轻/中、重/危重组间差异是否具有统计学意义。在适用的情况下,使用线性或逻辑回归模型估计人口统计学因素、肺和身体功能测试以及放射学体征与COVID-19严重程度组的相关性。对模型进行了调整,以排除概念重要性(年龄、性别)或与COVID-19严重程度存在统计学显著关系(p<0.1)的潜在混杂因素。使用受试者工作特征曲线(AUC)下的面积来检验模型拟合。AUC的95%置信区间由2000次重复的自举重采样计算。根据整体AUC选择最终模型。所有比较均考虑双侧p<0.05。数据分析采用R(3.6.0版本;R统计计算基金会,维也纳,奥地利)。
结果
基线特征和症状
从2020年5月1日至2020年9月15日(图1).从最初症状到随访的中位时间(IQR)为128(108-144)天。
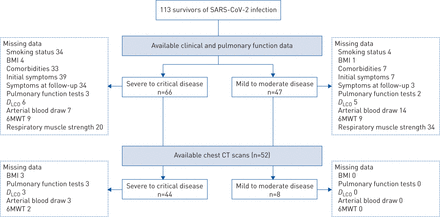
系统评价和元分析的首选报告项目研究流程图。SARS-CoV-2:严重急性呼吸综合征冠状病毒2;BMI:身体质量指数;DLCO:肺对一氧化碳的扩散能力;6MWT: 6分钟行走试验;CT:计算机断层扫描。
COVID-19重症/危重期存活患者的年龄比轻/中度随访患者的年龄大(平均±sd60.3±12岁与52.9±11岁,性别分布相等)(表1).轻/中、重/危重患者吸烟史差异无统计学意义。然而,意味着±sd重/危重型患者的体质指数(BMI)明显高于轻/中度患者(29.8±5.7)与25.5±4.7公斤·m−2, p = 0.02)。两组的初始合并症列于表1.随访时,两组患者均未出现相关咳嗽症状(中位数(IQR)咳嗽视觉模拟评分为0(0 - 2))。然而,随访时两组患者均报告有持续的运动性呼吸困难(经医学研究委员会IQR修正的中位数评分为1(0-1))。
对排除既往诊断为慢性肺部疾病的患者进行敏感性分析,以估计观察到的随访肺功能差异是否主要由既往肺部疾病所致。补充表S1展示了在这个亚组中基本不变的发现。
肺功能,物理性能和氧合
总体而言,轻度/中度COVID-19患者的平均肺功能正常。重症/危重型COVID-19患者的肺容量一般较低,仍在正常范围内,而平均扩散能力(DLCO),身体机能和氧合下降。具体为总肺活量(TLC)、用力肺活量(FVC)、1 s用力呼气量(FEV)1),DLCO重症/危重型患者的发病率明显低于轻/中度患者。轻、中度病程患者FEV比例较低1/FVC高于重症/危重症患者(表1).重症/危重症患者功能受损,明显降低DLCO轻、中度疾病患者(均数±sd73.2±18.4% pred与95.3±20.3% pred, p=0.003)。重症/危重症组6分钟步行距离(6MWD)平均低120米年代阿宝2重症/危重组降低5.6±3.8%,轻/中度组降低2.6±3.1% (p=0.02)。同样,在COVID-19后4个月,原重症/危重症患者动脉氧张力降低(PaO2)与先前轻度/中度患者(PaO279±12.2与87.5±9 mmHg, p=0.0002) (表1).两组的呼吸肌力量没有差异。
在需要机械通气的患者亚组(39例重症/危重症患者)中,随访时肺功能的多项指标与急性COVID-19机械通气时间呈负相关(补充表S2).具体地说,DLCOTLC与通气时间呈中强负相关(r=−0.43,p=0.008, r=−0.42,p=0.01)。
与严重/危重症病程的临床联系
未经调整的分析显示,重症/危重型COVID-19患者年龄为7.4岁(95% CI 3-11.7) (p=0.002),体重为4.4 kg·m (95% CI 2.3-6.4)−2BMI (p<0.001)高于轻/中度疾病患者。与轻度/中度COVID-19相比,重型/危重型COVID-19后预测的FVC %降低9% (95% CI 1.5-16.4%), TLC %预测的降低16% (95% CI 8.3-23.6%)。经年龄、性别和BMI调整后,重症/危重症组TLC仍显著降低(14.6%,95% CI 6.3-22.8%;p<0.001),而植被覆盖度无统计学意义(5.6% pred, 95% CI−2.6 ~ 13.8% pred;p = 0.18)。DLCO在未经调整的分析中,轻度/中度COVID-19后显著升高(22.1%,95% CI 14.4-29.8%;p=0.001),对上述混杂因素进行校正后(20.9%,95% CI 12.4-29.4%;p = 0.01)。
同样,重症/危重型COVID-19幸存者在未调整的情况下的6MWD明显较低(120米,95% CI 80-160米;p=0.001)和调整分析(86 m, 95% CI 45-127 m;p = 0.001)。经过年龄、性别和BMI调整后,最小值年代阿宝26MWD为2.2% (95% CI 0.4 ~ 4.0%, p=0.01)PaO2严重/危重症后降低5 mmHg (95% CI 0.3-10.2 mmHg) (p=0.06)。
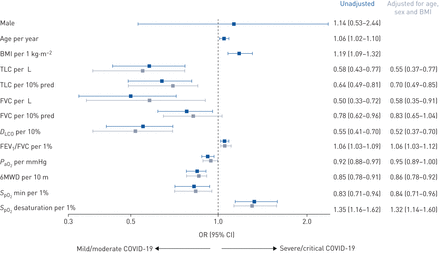
图2显示了随访临床变量与初始重症/危重症和轻中度COVID-19的相关性。表2说明了最终的多变量模型,包括在统计上和概念上与我们队列中COVID-19严重/危重病程相关的临床和功能变量。高DLCO随访时预测的%是与既往病程更有利的独立相关性最强的因素(p=0.01)。模型拟合良好,总体AUC为0.95 (95% CI 0.88-1.00)。
与2019年冠状病毒疾病(COVID-19)严重程度相关的变量。人口统计学和功能参数与轻/中、重/危重COVID-19的相关性来自未调整分析和个体多变量模型的优势比和相应的95%置信区间,对每个参数进行年龄和性别混淆调整。BMI:身体质量指数;TLC:总肺活量;FVC:强迫肺活量;DLCO:肺对一氧化碳的扩散能力;FEV1:用力呼气量1 s;PaO2:动脉血氧张力;6MWD: 6分钟步行距离;年代阿宝2:周围氧饱和度。
辐射特性
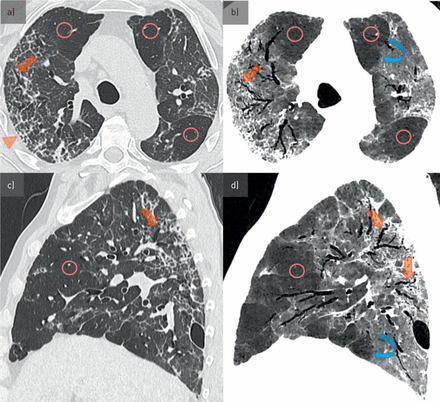
在我们的队列中,典型的COVID-19放射随访后遗症包括单叶或多叶低衰减区,无或伴小叶边缘隆起,马赛克衰减模式的磨玻璃样混浊,线性/曲线密度,网状,蜂窝状,牵引性支气管扩张,不同位置的结构扭曲,以及气膨出(图3).广泛的肺纤维化很少观察到(补充图S1).
一例2019冠状病毒病(COVID-19)肺炎后3个月严重后遗症患者的特征性影像学改变。1例重症COVID-19肺炎患者3个月后出现双肺广泛受累。a)轴向1毫米厚计算机断层扫描(CT)和b) 10毫米厚最小强度投影(mIP)切片,c) 1毫米厚CT和d)肺窗口中10毫米厚mIP矢状面重格式化所见的所有肺叶弥漫性镶嵌衰减模式。这结合了肺纤维化的典型特征,包括结构扭曲、网状、蜂窝状(a中箭头)和牵引性支气管扩张(a - d中直箭头),以及双肺中界限分明的低衰减区域(a - d中圆圈)。相邻的低衰减小叶和牵引性支气管扩张在狭窄窗口设置的mIP图像上更清晰可见(b和d)。注意小叶间隔膨大(b和d,曲线箭头)以及胸膜下气膨出(c和d)。
与轻度/中度COVID-19相比,严重/危重型COVID-19放射学特征明显更普遍,包括镶嵌衰减模式和低衰减区域(66%)与13%, p=0.007)和网状(59%)与13%, p=0.02)和建筑失真(52%与13%, p=0.055)在重症/危重症(补充表S2).
在我们的研究中,在胸部CT扫描上出现镶嵌衰减模式和低衰减区域的患者遭受严重/危重疾病病程的可能性超过13倍(表3).考虑到年龄和性别的潜在混淆,这种相关性仍然具有统计学意义(OR 13, 95% CI 1.7-239 p=0.03)。同样,网状结构使过去患严重/危重型COVID-19的几率增加了10倍(95% CI 1.6-198, p=0.04) (表3).
讨论
据我们所知,这是欧洲第一项报告SARS-CoV-2感染后呼吸道随访结果的研究。在平均4个月的观察时间后,我们的队列发现,与轻度/中度疾病患者相比,先前患有严重/危重性COVID-19病程的患者肺功能和身体表现受损更为明显。具体地说,DLCO%的预测在4个月是最重要的独立相关更严重的初始疾病。此外,在可用胸部CT扫描的患者亚队列中,我们发现了马赛克衰减模式,受地理边缘限制的各种大小的低衰减区域,伴继发性肺小叶膨大,以及严重/危重型COVID-19后明显的影像学特征为网状。
关于COVID-19肺炎发展和严重病程的危险因素的信息正在增加,我们的研究支持了以前报告中的许多发现[23- - - - - -25].在我们的队列中,我们证实,年龄和年龄相关的共病显著影响了急性COVID-19严重程度的个体间异质性[24].例如,随着肥胖成为严重COVID-19和死亡的风险因素[26- - - - - -28],来自瑞士COVID-19肺部队列的研究结果证实了这一可改变的危险因素的重要性。
COVID-19主要影响肺部和气道,并可能导致呼吸衰竭[25].ARDS的5年幸存者被发现功能受损,6MWD中位数为预测的76% [29].类似地,一项关于SARS和MERS后长期结果的荟萃分析发现,6MWD和DLCO与健康人相比[30.].一项为期3个月的武汉队列随访研究(主要是轻度肺炎)显示55例患者中有14例肺功能下降,其中55例患者中有9例肺功能下降DLCO[31].在我们的研究中,减少DLCO, 6MWD下降和6MWT期间饱和度降低与COVID-19表型严重受损有关,重要的是,这种关系不受年龄、性别或BMI的影响。
COVID-19不同临床病程后肺功能和身体损伤的发生率和程度仍不确定。在我们的队列中,我们发现肺容积(TLC, FVC和FEV)较低1)在重症/危重型COVID-19患者中;较高FEV1重度/危重亚组的FVC比值提示限制性生理倾向,呼吸肌力量缺乏差异提示肺实质问题而不是呼吸肌问题。此外,我们发现急性期机械通气时间与随访4个月时肺功能呈负相关。这可能是由于在非常严重的COVID-19后出现了长时间的损伤,或与易感患者更严重的病程有关。另外,呼吸机诱导的肺损伤是ards后的一个很好的挑战,它可以影响急性疾病恢复后的肺功能[29].
在胸部CT扫描上,急性COVID-19典型表现为进行性磨玻璃样影、肺泡实变(胸膜下和基底位置相同)、圆形病灶、疯狂铺展型、线性密度、实质带和结构扭曲(可能代表组织性肺炎和/或纤维化改变)[32].这是一个整体的放射学图像,不同于其他病毒感染,如流感[33,34].与临床演变相似,放射学模式的轨迹据报道是不均匀的。在平均10天的观察时间后,大多数病例的肺实质异常似乎有所改善,而部分患者持续表现出轻度肺纤维化征象[35].在短期随访中,最常见的影像学异常包括毛玻璃样影、实变和实质带[36].关于放射性异常中期或长期发展的报道目前非常有限。
在初步诊断4个月后,我们的重症/危重亚队列的主要发现是马赛克衰减模式,其特征是对应于一个或几个相邻继发肺小叶的异常低密度区域与正常或异常高密度区域交替出现(即。磨玻璃衰减),以及更频繁的网格。在大多数病例中,受累的继发性肺小叶边缘有明显的分界线和轮廓,有时有高密度的条带勾勒出异常小叶。镶嵌衰减模式与受损组合DLCO可归因于远端气道异常,如缩窄性细支气管炎伴空气滞留和继发性反射性血管收缩,或原发性肺血管疾病可诱发继发性气道疾病。这两种机制都可能导致通气/灌注不匹配,从而导致我们在重症/危重亚队列中观察到的体能下降和低氧血症。内皮损伤和肺泡毛细血管微血栓形成被认为是肺血管疾病的潜在机制[37].此外,在流感、中东呼吸综合征和严重急性呼吸系统综合症(SARS)背景下的成人急性呼吸窘迫综合征(ARDS)后,已发现呼吸道疾病和空气滞留[6,38,39].总体而言,以往研究的观察结果,加上我们的重症/危重型COVID-19亚队列中镶嵌衰减模式的高流行率,表明这种模式是重症COVID-19的一个重要晚期特征。我们在队列中观察到的纤维化征象(网状、支气管扩张和蜂窝状)在ARDS幸存者中经常遇到。虽然初步观察报告了covid -19相关ARDS后的纤维化[38],镶嵌衰减和空气捕获在COVID-19之后从未被描述过。我们最近报道了放射镶嵌衰减和空气滞留可能提示小气道疾病[40].这一发现此前在冠状病毒感染和病毒相关ARDS后也有报道[6,38,39].在我们的研究中观察到的放射学和功能异常可能代表了一般的ARDS、呼吸机诱导的肺损伤或SARS-CoV-2感染后的残余损伤。COVID-19后进行性间质性肺疾病的潜在发展可能归因于SARS-CoV-2引发的自身免疫途径的刺激,或从已有的间质性肺异常发展为临床显著的间质性肺疾病。
急性呼吸窘迫综合征(ARDS)后数年内出现长期功能损害且恢复缓慢的情况并不少见[29];然而,特别是COVID-19后的潜在长期后果仍需要在未来的观察性研究中进行调查。
我们的研究设计不允许对严重/受损和轻度/中度COVID-19的患病率进行任何推断,因为不包括死亡患者,我们也没有纳入无症状患者进行随访。无法进行初始肺功能检查和影像学检查;因此,经历严重/危重疾病的患者在随访时可能有易感的未诊断肺部疾病和较差的肺功能。彻底询问患者的症状和病史,可能表明以前有肺部疾病。然而,不能完全排除无症状的潜在慢性肺部疾病。此外,在大多数病例中,由于缺乏既往胸部CT扫描,无法评估COVID-19感染的初始肺间质异常或气道累及。然而,我们的研究结果与以前的研究相结合,支持了严重COVID-19导致中期死亡率下降的假设DLCO例如,在气体交换方面的限制,以及此前未报道的一系列放射学特征,都指向了相当大的小气道成分。
总之,通过分析COVID-19后4个月的肺功能、身体表现、氧合和放射学结果,我们的研究增加了关于COVID-19后轨迹的越来越多的证据。我们确定了DLCO%的预测是与严重/危重呼吸道COVID-19相关的唯一最重要因素,这意味着步行距离缩短和运动时氧饱和度降低。特殊的放射学表现应进一步调查,以结合其他功能参数对疾病进行全面评估。这些结果强调了在严重和危重型COVID-19后进行系统随访并适当管理肺部后遗症的重要性。
补充材料
可共享的PDF
确认
我们要感谢本次研究的所有参与者,我们的研究协调员Kurt De Jaegere,所有研究护士和所有其他帮助进行本次研究的工作人员:Anja Renner(伯尔尼),Jasmin Lippuner(伯尔尼),Ilena Müller(伯尔尼),Wiasemsky Mary-Line(洛桑),Estelle Clément(洛桑),Noriane Sievi (Zürich), Verica Filipin(圣加仑),Sandra Widmer(圣加仑),Kei Kozu(圣加仑),Florent Baty(圣加仑),Pier Andrea Maida(卢加诺),Maira Biggiogero(卢加诺),Marlène Salamin (Sion), Martine Rime(弗里堡),Sandrine Foucras(弗里堡)。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
应要求并经瑞士COVID-19肺部研究小组指导委员会批准后可提供数据。
利益冲突:古勒检察官没什么可透露的。
利益冲突:L. Ebner没有什么可透露的。
利益冲突:C. Beigelman报告阿斯利康和勃林格的个人讲座费用,在提交的工作之外。
利益冲突:P-O。布里德沃没有什么可透露的。
利益冲突:M. Brutsche没有什么可透露的。
利益冲突:C. Clarenbach报告的个人费用来自罗氏,诺华,勃林格,葛兰素史克,阿斯利康,赛诺菲,Vifor和蒙迪制药,在提交的工作之外。
利益冲突:C. Garzoni没有什么可透露的。
利益冲突:T.K.盖瑟没有什么可透露的。
利益冲突:A.勒努瓦没有什么可透露的。
利益冲突:曼西内蒂先生没什么可透露的。
利益冲突:B.纳奇尼没有什么可透露的。
利益冲突:S.R.奥特没有什么可透露的。
利益冲突:L. Piquilloud没有什么可透露的。
利益冲突:普雷拉先生没有什么可透露的。
利益冲突:Y-A。Que没有什么可透露的。
利益冲突:下午Soccal没有什么可透露的。
利益冲突:c·冯·卡尼尔没有什么可透露的。
利益冲突:M. Funke-Chambour没有什么可透露的。
支持声明:伯尔尼Lungenliga, Johanna Dürmüller基金会,伯尔尼精确医学中心(BCPM)和伯尔尼Inselspital的für Lehre und Forschung (DLF)部门资助了本研究的部分研究,但在调查的进行中没有任何作用。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年9月30日。
- 接受2020年12月13日。
- 版权所有©ERS 2021
本版本根据知识共享署名非商业许可4.0的条款发布。