摘要
2019冠状病毒病(COVID-19)的长期肺部预后尚不清楚。我们旨在描述因COVID-19入院3个月后自我报告的呼吸困难、生活质量、肺功能和胸部计算机断层扫描(CT)结果。我们假设重症监护室(ICUs)患者与非icu患者相比,预后较差。
从挪威六家医院出院的COVID-19患者连续入选一项前瞻性队列研究。目前的报告描述了前103名参与者,包括15名ICU患者。改良的医学研究委员会(mMRC)呼吸困难量表、EuroQol小组的问卷、肺活量测定法、肺对一氧化碳的扩散能力(DLCO),出院后3个月行6分钟步行试验、脉搏血氧测定及低剂量CT扫描。
54%的参与者mMRC评分为>0,19%的参与者为>1。1秒内用力肺活量和用力呼气量的中位数(25 - 75百分位)分别为预测值的94%(76-121%)和92%(84-106%)。DLCO在24%的参与者中低于正常下限。25%的参与者在四个肺区中至少有一个出现>10%的毛玻璃样影(GGO), 19%的参与者在胸部CT上出现实质样带。ICU幸存者与非ICU患者呼吸困难评分和肺功能相似,但GGO患病率更高(校正OR 4.2, 95% CI 1.1-15.6),日常活动表现较低。
入院3个月后,四分之一的参与者出现胸部CT混浊和弥散能力降低。ICU入院与病理CT结果相关。这没有反映在呼吸困难增加或肺功能受损。
摘要
出院3个月后,四分之一的COVID-19幸存者出现气体扩散能力下降和持续的实质混浊。ICU治疗与持续性实质混浊有关,但与呼吸困难或弥散能力降低无关。https://bit.ly/2J3xH4x
简介
下呼吸道和肺部是严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)的主要目标。大多数因2019冠状病毒病(COVID-19)入院的患者除出现不同程度低氧血症的肺功能受损迹象外,还伴有咳嗽和呼吸困难等呼吸道症状[1].这些症状与胸部计算机断层扫描(CT)和胸部x光片上广泛的毛玻璃影(GGO)有关[2,3.].住院的COVID-19患者中有15% - 30%会出现严重呼吸衰竭和急性呼吸窘迫综合征(ARDS),需要入住重症监护室(icu),可能需要进行机械通气[1,4,5].根据世界卫生组织(世卫组织)的数据,COVID-19的病死率为1-10%,取决于年龄和潜在的合并症[6].
由于COVID-19大流行是一种新疾病,COVID-19幸存者的长期肺部预后尚不清楚。来自其他冠状病毒肺炎的证据,如SARS和中东呼吸综合征(MERS),表明肺功能受损和实质不透明仅在少数不需要机械通气的患者中持续存在[7].然而,在ARDS患者中,多达11-45%的患者在10-12个月后出现肺功能受损和影像学上持续浸润[8].为了识别和管理COVID-19的潜在长期后遗症,有必要对疾病的自然病程进行更多研究[9].COVID-19住院后幸存者的早期报告显示,近50%的患者在1个月后弥散能力、总肺活量、运动能力或胸部CT扫描异常[10].
在目前的研究中,我们评估了因COVID-19入院3个月后患者报告的呼吸困难、肺功能、生活质量(QoL)和胸部CT扫描的实质不透明,这些患者均接受了或未接受ICU治疗。
材料与方法
设计与参与者
患者报告的COVID-19住院后预后和肺功能(PROLUN)是一项在挪威六家主要医院进行的多中心前瞻性队列研究。该研究得到了挪威东南部地区伦理委员会的批准(no。125384),由每个参与中心的数据保护官员提供,并在ClinicalTrials.gov (NCT04535154).
年龄>,18岁,>8小时入院,出院诊断(疾病及相关健康问题国际统计分类10)为U07.1 (COVID-19,病毒已识别),U07.2 (COVID-19,病毒未识别)或J12。x(病毒性肺炎,结合鼻咽拭子SARS-CoV-2阳性鉴定)被考虑为合格。排除标准包括居住在医院集水区以外、无法提供知情同意或参与世卫组织团结试验。
符合条件的患者在出院后6周通过邮件邀请。通过返回书面签署的同意书或安全数字同意书(敏感数据服务(TSD),奥斯陆大学,挪威奥斯陆)获得知情同意。对未应答者进行一次电话提醒。
根据研究方案,计划对前100名参与者进行中期报告。这一数字是在2020年6月24日实现的。因此,目前的研究包括了截至2020年6月24日参加了为期3个月随访的所有参与者(n=103)。
数据收集
参与者返回各自医院的门诊进行为期3个月的随访。入院和3个月随访之间的中位数(25 - 75百分位)时间为83(73-90)天;非ICU组82(73 ~ 90)天,ICU组85(81 ~ 90)天(p=0.090)。各中心ICU的入院标准相似:无法维持满意的脉搏血氧饱和度(年代阿宝2)通过鼻插管或无呼吸面罩补充氧气。此外,在转移到ICU之前,参与者由麻醉师进行了评估。
自我报告的呼吸困难
使用改良的医学研究委员会(mMRC)呼吸困难量表,范围0-4,[11,12].前18名参与者或St Olavs医院(挪威特隆赫姆)没有实施这一措施。然而,对于这些参与者,我们在访问前4-6周对自我报告的mMRC进行了额外的分析。
生命质量
EuroQol Group的EQ-5D-5L问卷[13]用于测量与健康相关的生活质量。它包含五个项目,从1(没有问题)到5(无法/极端问题)按顺序打分。调查问卷在访问前4-6周通过邮件或网络进行。88名(89%)参与者的分数可用。EQ-5D指标值采用英国权重的人行横道法[14].
肺功能检查
测定肺活量(FVC)和1 s内用力呼气量(FEV)1)(积家MS-PFT分析仪,Höechberg,德国;CareFusion型MasterScreen PFT,约巴林达,CA,美国;软件SentrySuite V03.0.5;Vyaire Medical, Höechberg)。FEV的比值1/FVC计算。肺部对一氧化碳的扩散能力(DLCO)及肺泡通气(V一个)进行测量,并且DLCO/V一个(肺对一氧化碳的转移系数)进行计算。所有手术均按照美国胸科学会(ATS)和欧洲呼吸学会(ERS)指南执行[188bet官网地址15,16].使用全球肺功能倡议(GLI)网络参考值计算预测值的百分比、正常下限(LLN)和z-评分[17,18].根据ATS/ERS指南进行6分钟步行试验(6MWT),基线年代阿宝2用食指脉搏血氧仪测量[19].
胸部CT
在仰卧位和俯卧位,屏气和深吸气时,获得低剂量的薄层CT图像。所有检查均采用相同的CT方案,并根据所使用的不同CT扫描仪进行了调整。根据每个患者的体重调整管电流设置,低剂量参考120kvp,高音调和尽可能短的旋转时间。对于肺实质的评估,我们使用了薄重建切片厚度(0.9-1.25 mm),具有高空间频率的内核,以及较厚(2-3 mm)切片的软内核用于纵隔评估。两名经验丰富的胸科放射科医生独立审查了所有图像,不考虑参与者的临床病史。意见一致程度很高。间质发现的存在、范围和分布均使用Fleischner学会推荐的命名法进行登记[20.].为了当前分析的目的,评估了GGO和实质带。利用纵隔解剖标志,在肺的四个独立尖基区记录了发现[21].
其他临床变量
基线人口统计学特征(性别、年龄、身高、体重、吸烟史)、体重指数(BMI)、共病(糖尿病或高血压)和COVID-19入院数据来自电子患者记录。反映COVID-19严重程度的临床变量为吸氧、入住ICU、机械通气、c反应蛋白(CRP)和d -二聚体最高水平。
所有收集的数据都存储在TSD中,该系统是根据挪威《个人数据法》和《卫生研究法》设计的,用于存储和后处理敏感数据。
统计分析
对于连续数据,描述性统计中报告了中位数和25 - 75百分位数。组间比较酌情采用Mann-Whitney u检验或卡方检验。对于肺功能变量,计算预测值,报告LLN和z-score。
对队列的描述性分析被认为是本临时报告的重要内容。我们还验证了以下假设:入住ICU的参与者比未入住ICU的参与者有更多的呼吸困难、肺功能下降、生活质量下降和更多的病理CT表现。
主要观察指标为:1)mMRC≥1;2)DLCO低于LLN;3)至少一个肺区>10% GGO;4)实质带的存在。次要结果为6MWT距离,年代阿宝2、EQ-5D- 5l评分和EQ-5D指数。采用单因素logistic回归分析评估COVID-19严重程度指标与主要预后的相关性。ICU入院(预先定义为COVID-19严重程度的主要指标)与主要结局之间的相关性通过多变量分析进行调整。由于参与者数量有限,只允许使用几个自变量:年龄和性别,除了DLCO在LLN下面,其中当前/以前吸烟与不吸烟也算在内。所有统计分析均使用Stata(版本16.1;StataCorp, College Station, TX, USA)。p水平<0.05为有统计学意义。
结果
入院的人口学和临床特征显示在表1.ICU患者COVID-19严重程度的几个指标高于非ICU患者:住院时间、氧治疗、CRP和d -二聚体的最高水平以及双侧肺密度的患病率。然而,两组之间的人口统计学变量(性别、年龄、BMI和吸烟状况)具有可比性。ICU患者的高血压发生率低于非ICU患者。ICU和非ICU患者从症状出现到入院的中位时间(25 - 75百分位)分别为7(5-9)天和9(6-11)天(p=0.125)。
表2介绍全组及住院期间按ICU入院亚组自述的呼吸困难、肺功能检查及胸部CT检查结果。37例(54%)受访者报告呼吸困难(mMRC评分>0),13例(19%)受访者报告mMRC评分>1 (n=69)。ICU和非ICU患者出院后3个月呼吸困难的发生率相似(表2).在敏感性分析中,包括另外23名几周前报告的mMRC评分的参与者,mMRC评分>0和mMRC评分>1的患病率分别为52(56%)和22 (24%)(n=93)。对于所有的肺功能测试,大多数参与者的值都在正常范围内。~ 10%有FVC或FEV1低于LLN, 24%显著降低DLCO.此外,入院期间入住ICU的患者与未入住ICU的患者相比,肺功能、6分钟步行距离或氧饱和度没有降低(表2).
GGO常见;24%的参与者有一个或多个肺区,GGO≥10%。在单变量logistic回归分析中,GGO的存在与年龄和CRP相关(p=0.009和p=0.001) (补充表S1).GGO的粗患病率在ICU和非ICU患者之间无显著差异;然而,在对年龄和性别进行调整后,与未入住ICU的患者相比,入住ICU的患者出现这些病理CT表现的几率显著更高(表3).在五分之一的参与者中发现了表明纤维化早期进展的实质带。关于实质带,观察到CRP和呼吸机治疗的相关性(p=0.018和p=0.038) (补充表S1).入住ICU的参与者与未入住ICU的参与者之间没有差异(表3).
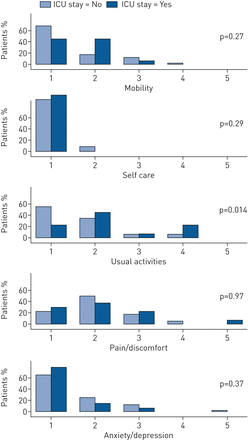
EQ-5D-5L的五个项目的分数显示在图1.入住ICU的患者在日常活动方面的中位数得分高于仅入住普通病房的患者:4(25 - 75百分位2-4)与2(1-2),分别为(p=0.014)。中位数±sdICU患者EQ-5D评分为0.61±0.23,非ICU患者EQ-5D评分为0.72±0.19 (p=0.087)。
重症监护室(ICU)患者(n=13)和非ICU患者(n=75) EQ-5D-5L维度评分的分布。1:没有问题,2:轻微问题,3:中度问题,4:严重问题,5:不能/极端问题。
讨论
在对因COVID-19住院而幸存的患者进行的为期3个月的前瞻性队列研究随访中,大约一半的参与者在运动时持续呼吸困难,四分之一的患者呼吸困难减轻DLCO.四分之一的参与者在CT扫描上出现持续的GGO,五分之一的参与者有实质带。入院期间入住ICU的患者持续CT异常的患病率更高,日常活动中报告的问题更多,但肺功能和自我报告的呼吸困难与未入住ICU的患者相似。
在该队列中观察到的良好的肺活量测定结果伴随着低流行率的外周氧水平降低和运动能力降低,如6MWT所示。总的来说,我们的研究结果表明,在COVID-19住院幸存者(包括ICU住院幸存者)中,3个月后发生慢性呼吸衰竭的情况并不常见。入院后3个月自我报告的呼吸困难程度与之前的ICU住院时间无关,我们将其作为COVID-19严重程度的标志。呼吸困难是主观的,可能受到许多其他变量的影响。在我们的研究中,3个月后扩散能力下降的参与者比例与SARS和中东呼吸综合征的研究以及COVID-19幸存者的其他早期报告相当[7,10,22,23].
CT评估,约四分之一的参与者在3个月后出现一个或多个肺实质区域≥10%的持续性不透明。与另一组随访4周后的报告相比[10],这一发现表明,与COVID-19相关的GGO可能在不发展为持续性纤维化的情况下得到解决。然而,其中一些CT表现可能持续存在,并逐渐发展为纤维化改变,在我们的研究人群中有五分之一的人发现了实质带[24].在一项对出院后8周的COVID-19患者的回顾性研究中,约25%的患者出现早期纤维化迹象[22].这与我们的队列研究结果一致。在我们的材料中,我们发现年龄与持续GGO有关,这与关于社区获得性肺炎的研究结果一致[25].此外,探索性分析发现炎症标志物CRP与持续性GGO和实质带相关。有趣的是,实质带也与呼吸机治疗有关。然而,目前尚不清楚持续的病理CT表现是否会随着时间的推移发展为症状性肺纤维化,以及COVID-19的各种治疗是否会影响实质浑浊的长期结果。
我们发现ICU入院患者3个月后CT异常更为常见。然而,肺功能或弥散能力没有差异,年代阿宝2这些参与者与未入住ICU的参与者之间的距离为或6MWT,尽管ICU患者在入院期间胸片上有更多的双侧肺混浊和更高水平的全身炎症标志物。此外,除了更多入住ICU的患者报告日常活动能力受损外,各组间所有患者报告的结果相似。如果在其他研究中重复,ICU入院、持续病理性CT模糊和日常活动能力下降之间的联系可能表明,ICU患者比其他因COVID-19住院的患者需要更密切的临床随访。
该研究的一个优势是多中心前瞻性设计,其中涵盖180万居民的医院的所有幸存者都接受了资格评估。在我们的样本和挪威COVID-19统计数据元数据之间,ICU入院的年龄和患病率相似(https://www.fhi.no/sv/smittsomme-sykdommer/corona).然而,我们不能排除参与偏见。参与世卫组织团结试验是一项排除标准,但本研究中的医院仅在本研究纳入期即将结束时才开始纳入团结试验。总的来说,我们认为该研究队列具有挪威COVID-19住院幸存者的代表性。最后,由于样本量有限,目前的研究未能探讨可能的病理生理机制与持续性呼吸困难、弥散能力降低或实质混浊之间的关系。
结论
在我们的挪威队列中,大约一半的参与者在因COVID-19入院3个月后报告了用力呼吸困难。大多数参与者的肺容量在参考范围内,而四分之一的扩散能力下降。CT扫描显示,四分之一的人患有持续性GGO,五分之一的人有实质带。ICU入院患者在出院3个月后出现持续CT异常和正常活动能力下降,但无呼吸困难、肺功能受损或功能能力下降。
补充材料
可共享的PDF
脚注
这篇文章有补充资料可从www.qdcxjkg.com
完整的协议已发布在www.clinicaltrials.gov (NCT04535154).发表后,匿名数据文件将通过期刊网站共享。
作者贡献:G. Einvik构思了这项研究。该方案由T.M. Aaløkken、E. Brønstad、E. Ikdahl、M.T. Durheim、K. Stavem、O.H. Skjønsberg、H. Ashraf和G. Einvik合作设计。患者纳入和数据收集由T.V. Lerum、E. Brønstad、B. Aarli、K.M.A. Lund、K. Tonby、K. Stavem、O.H. Skjønsberg和G. Einvik完成。T.M. Aaløkken, J.R. Rodriguez, C. Meltzer和H. Ashraf解释和分析了CT结果。由T.V. Lerum, K. Stavem和G. Einvik进行统计分析。手稿的初稿由T.V. Lerum、O.H. Skjønsberg、K. Stavem和G. Einvik撰写。所有作者都对手稿进行了相当多的批判性审查,并批准了最终版本。
利益冲突:t·v·勒伦没什么可透露的。
利益冲突:T.M. Aaløkken没有什么可透露的。
利益冲突:E. Brønstad没有什么可披露的。
利益冲突:B. Aarli报告阿斯利康的讲座和顾问委员会工作的个人费用,葛兰素史克、诺华、勃林格殷格翰和基耶斯制药的讲座的个人费用,在提交的工作之外。
利益冲突:伊克达尔没有什么可透露的。
利益冲突:K.M.A.伦德没有什么可透露的。
利益冲突:M.T. Durheim报告了勃林格殷格翰的资助和个人费用,罗氏和阿斯利康的个人费用,在提交的工作之外。
利益冲突:j·r·罗德里格斯没什么可透露的。
利益冲突:C. Meltzer没有什么可透露的。
利益冲突:K. Tonby没有什么可透露的。
利益冲突:K. Stavem没有什么可透露的。
利益冲突:O.H. Skjønsberg没有什么可披露的。
利益冲突:H. Ashraf报告勃林格殷格翰在研究期间的资助。
利益冲突:在研究进行期间,G. Einvik报告了勃林格殷格翰的资助;阿斯利康公司的个人咨询费,在提交的工作之外。
支持声明:阿克舒斯大学医院的肺部和放射科已获得勃林格殷格翰公司的无限制资助,用于资助当前研究中的CT扫描和研究协调。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年9月9日。
- 接受2020年11月18日。
- 版权所有©ERS 2021
本版本根据知识共享署名非商业许可4.0的条款发布。