摘要
严重哮喘是一项未得到满足的主要临床需求。尽管大剂量吸入皮质类固醇治疗,许多哮喘患者的气道仍存在嗜酸性炎症。细胞因子信号抑制因子(suppressor of cytokine signaling, SOCS)是一类参与细胞因子信号调控的分子通过Janus激酶信号转导和转录途径激活子的抑制。我们检测了哮喘患者气道中SOCS的表达,并研究了这是否与持续性嗜酸性粒细胞增多有关。
研究对象为健康对照组、轻/中度哮喘患者和重度哮喘患者。采用全基因组表达谱、定量PCR和免疫组化方法检测支气管活检中SOCS1、SOCS2和SOCS3的表达。利用支气管上皮细胞研究SOCS1在调节白细胞介素(IL)-13信号通路中的作用在体外.
SOCS1基因在重度哮喘患者气道中的表达明显低于轻/中度哮喘患者,且与气道嗜酸性粒细胞增多和其他T-helper型2 (Th2)炎症指标呈负相关。免疫组化显示SOCS1主要定位于支气管上皮。SOCS1过表达抑制il -13介导的趋化因子配体(CCL) 26 (eotaxin-3) mRNA的表达。
严重的哮喘患者持续气道嗜酸性嗜胞粒细胞和TH2炎症具有降低的气道上皮SOCS1表达。SOCS1抑制上皮细胞IL-13信号,支持其在严重哮喘中调节TH2驱动的嗜酸性粒细胞症方面的关键作用。
摘要
重度哮喘中持续性气道嗜酸性粒细胞增多/Th2炎症与上皮细胞SOCS1表达减少有关http://ow.ly/Mlgl3001UMU
介绍
哮喘是最常见的慢性疾病之一,影响着全球约3亿人[1].大多数哮喘患者通过支气管扩张剂和吸入皮质类固醇治疗获得充分的疾病控制[2].然而,尽管使用了大剂量吸入性皮质激素,在许多情况下,全身皮质激素,仍有大约10%的患者患有严重的无法控制的哮喘。这组哮喘患者的临床需求明显未得到满足[3.].
哮喘是一种异质性疾病,因此目前的研究正在努力识别和描述不同的表型,特别是在严重疾病中[4,5].临床表型和分子表型都被用于描述哮喘患者群体的炎症生物学[6- - - - - -8].
许多严重哮喘患者的一个关键特征是,尽管接受大剂量皮质类固醇治疗,但嗜酸性气道炎症仍持续存在[9,10].导致这种炎症的主要细胞因子是辅助性t - 2相关细胞因子,即白介素(IL)-4、IL-5和IL-13。IL-13是一种关键的细胞因子,有助于哮喘的病理生理特征,包括气道高反应性、黏液高分泌和气道重塑,IL-13过表达在严重哮喘亚组患者中持续存在,尽管接受了高剂量类固醇治疗[10,11].
Th2细胞因子介导它们的作用通过Janus激酶信号转导和转录激活子(JAK-STAT)途径和细胞因子信号通路受到包括细胞因子信号抑制子(SOCS)在内的多种分子的严格调控。SOCS是8个蛋白家族,包括SOCS1-7和细胞因子诱导含sh2蛋白(CIS),通过负反馈方式抑制JAK-STAT通路抑制细胞因子信号[12].SOCS1是第一个被发现的SOCS家族[13].在体外细胞培养和在活的有机体内动物模型已经证明,SOCS1是th2依赖通路的负调控因子,通过抑制信号传感器和转录激活因子(STAT)的磷酸化实现[14,15].SOCS2抑制生长激素和胰岛素样生长因子[16],并已被证明可以调节其他SOCS分子的表达[17].最近,我们发现由于SOCS3水平升高,SOCS2敲除小鼠与野生型小鼠相比,对th2介导的气道炎症的易感性增加[18].据报道SOCS3 mRNA在哮喘患者外周血T细胞中表达增加[19,20.]和小鼠T细胞中组成性SOCS3表达导致哮喘小鼠模型肺炎症加重[20.].
本研究的主要目的是检测SOCS1、SOCS2和SOCS3在健康对照组、轻/中度哮喘患者和重度哮喘患者气道中的表达,并探讨SOCS表达与气道内持续性嗜酸性炎症的关系。
方法
病人群
这一特征明确的研究对象队列的数据此前已发表[10,21,22].健康对照组(n=17)、轻度/中度哮喘患者(n=29)和重度哮喘患者(n=18)从英国贝尔法斯特的贝尔法斯特城市医院和英国莱斯特的格伦菲尔德医院这两个哮喘专科中心招募表1).临床评估方案确保患者患有严重的哮喘,如当前的欧洲呼吸学会/美国胸部社会指南所定义[188bet官网地址23].本研究中哮喘患者的进一步细节,包括哮喘治疗,可在在线补充文件中找到(表E1)。本研究经两家机构的研究伦理委员会批准,并获得所有受试者的书面知情同意(见在线补充文件)。
支气管镜检查
每位受试者均接受支气管镜检查,活检标本取自右肺中叶和下叶隆突。活组织切片立即放入RNA防腐剂(Ambion;ThermoFisher Scientific, Waltham, MA, USA)或如前所述,在嵌入甲基丙烯酸乙二醇前固定过夜[24].
基因表达分析
支气管活检均质,提取RNA,扩增用于双色全人类基因组4×44k基因表达微阵列分析(Agilent, Santa Clara, CA, USA),如前所述[25].Th2评分按先前所述计算,详情可参阅网上补充档案[8,10,25].TaqMan基因表达检测(应用生物系统,沃尔瑟姆,MA,美国)按照制造商的说明书使用。GAPDH作为家兔的保持基因。定量PCR值采用ΔΔCt法计算,相对基因表达量为-ΔΔCt [26].详情请参阅在线补充档案。
免疫组织化学
将支气管活组织检查部分切割为2μm,如前所述免疫染色[24然后用梅耶尔的苏木精进行反染色。采用同型和/或省略一抗体的阴性对照。使用计算机分析系统(LAS V3.7软件,Leica Microsystems, Wetzlar, Germany)在活检切片中测量固有层。为计数细胞炎症浸润,每mm计数单个阳性染色的有核细胞并表达2的组织。在线补充文件中的图E1显示了炎症细胞染色的范例显微照片。此外,还使用免疫组化(IHC)来确定患者活检中SOCS蛋白的定位。抗体的详细信息可在在线补充文件中找到。
支气管上皮细胞培养物
BEAS-2B细胞系(ATCC, Manassas, VA, USA)在添加5%胎牛血清和1%青霉素/链霉素的Dulbecco's Modified Eagle培养基中培养。原代支气管上皮细胞(PBECs)取自健康志愿者。本研究经研究伦理委员会批准,详见在线补充文件,并获得所有受试者的书面知情同意[22].PBECs在含有补充包(Promocell, Heidelberg, Germany)的气道上皮细胞基础培养基中培养。使用人重组IL-13 (R&D Systems, Minneapolis, MN, USA),浓度为50 ng·mL−1.在体外实验至少进行了三次。
转染
pcDNA3质粒中带有myc标记的全长SOCS1和空载体是a . Yoshimura(庆应义塾大学医学院,东京,日本)慷慨的礼物。BEAS-2B细胞被置于无抗生素培养基中,并用Lipofectamine 2000 (ThermoFisher)转染。使用NEON转染系统(ThermoFisher)电穿孔转染PBECs。转染6 h后更换培养基,转染24 h后进行细胞刺激。
西方墨点法
按照在线补充文件中描述的方法,裂解细胞并使用针对SOCS1、SOCS2、SOCS3、c-Myc和γ-微管蛋白的抗体对30 μg蛋白进行免疫印迹。
统计分析
采用Prism 5软件(GraphPad, San Diego, CA, USA)进行数据分析。在适当的情况下,数据以中位数(四分位数范围)表示。除另有说明外,统计检验采用Kruskal-Wallis检验、Mann-Whitney u检验、t检验和Spearman’s Rank相关性。PBEC数据在统计分析前进行转换(log10)。
结果
哮喘研究参与者的炎症措施增加
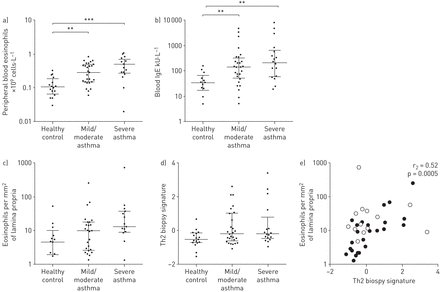
轻/中度和重度哮喘患者与健康对照组相比,外周血嗜酸性粒细胞数量和血液IgE水平显著升高(图1A和b分别)。免疫组化对嗜酸性粒细胞的定量显示,支气管活检固有层嗜酸性粒细胞的数量随着哮喘严重程度的增加而增加(健康对照组、轻/中度哮喘组和重度哮喘组的中位数分别为4.59、9.70和12.93;p = 0.07) (图1C.).研究组之间的中性粒细胞或肥大细胞数量没有显著差异(表E2在在线补充文件)。先前从哮喘患者中生成的基因表达微阵列Th2标记是il -13诱导的上皮基因的复合测量[8,10,25].随着哮喘严重程度的增加,Th2活检特征值也有增加的趋势(p=0.057)。Th2活检标记的强度与每毫米嗜酸性粒细胞的数量之间存在显著的正相关2哮喘患者固有层(图1E.).中性粒细胞和肥大细胞与Th2标记无相关性(在线补充文件图E2)。
哮喘研究参与者T-helper型2 (Th2)炎症测量值增加。a)外周血嗜酸性粒细胞和b)血液IgE水平随哮喘严重程度的增加而增加。c和d)固有层嗜酸性粒细胞数量和Th2特征值随哮喘严重程度的增加而增加。e)固有层嗜酸性粒细胞数量与Th2活检特征呈正相关(n=40)。黑色圆圈代表轻/中度哮喘患者,白色圆圈代表重度哮喘患者。统计分析采用Kruskal-Wallis秩和Spearman秩检验。数据以中位数(四分位数范围)表示。* *: p < 0.01;* * *: p < 0.001。
与轻/中度哮喘患者相比,重度哮喘患者的支气管活检中SOCS1 mRNA表达降低
采用定量PCR检测健康对照组、轻/中度哮喘患者和重度哮喘患者支气管活检中SOCS1、SOCS2、SOCS3 mRNA的表达情况。SOCS1在重度哮喘患者的支气管活检中表达明显低于轻/中度哮喘患者(图2A).而SOCS2和SOCS3基因表达水平在组间无差异(图2B.和c分别)。值得注意的是,在接受高剂量吸入皮质类固醇的哮喘患者的呼吸道中减少了SOCS1 mRNA,比较了接受低剂量吸入皮质类固醇的哮喘患者,但SOCS2或SOCS3表达没有差异(图E3)。
与轻/中度哮喘患者相比,重度哮喘患者支气管活检中细胞因子信号抑制因子(SOCS)1 mRNA表达减少。a) SOCS1, b) SOCS2和c) SOCS3 mRNA表达采用定量PCR分析健康对照组(n=17)、轻/中度哮喘患者(n=29)和重度哮喘患者(n=18)的活检匀浆。价值观代表——ΔΔCt。采用Kruskal-Wallis检验进行统计学分析。数据以中位数(四分位数范围)表示。*: p < 0.05。
SOCS1基因表达在气道持续性Th2炎症和嗜酸性粒细胞增多的患者中降低
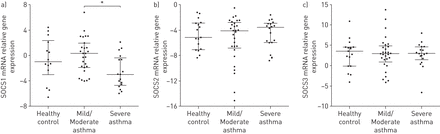
SoCS1基因表达与哮喘患者支气管组织的椎相色组织中的Th2活检签名和嗜酸性血粒细胞数观察到阴性相关性(图3一和b分别)。在SOCS2或SOCS3和Th2活检特征或支气管活检中嗜酸性粒细胞数量之间没有发现显著相关性(在线补充文件中的图E4)。为了进一步研究SOCS1表达与组织嗜酸性粒细胞之间的关系,研究对象被支气管活检固有层嗜酸性粒细胞的数量一分为二(嗜酸性粒细胞计数在每毫米嗜酸性粒细胞的中位数附近一分为二)2在Lamina Propria)。高嗜酸性粒细胞的参与者(≥9.2嗜酸性粒细胞·mm−2与那些呈现低嗜酸性粒细胞(<9.2嗜酸性粒细胞·mm)的患者相比,固有层内的SOCS1水平显著降低−2固有层内)(图3 c).被分为嗜酸性粒细胞高亚群和嗜酸性粒细胞低亚群的受试者在两组中SOCS2和SOCS3表达无差异(在线补充文件中的图E5)。由于趋化因子配体(CCL) 26在2型炎症反应中是高度诱导的,因此我们探讨了该趋化因子与SOCS1的关系。如预期的,SOCS1低表达的患者无法抑制Th2诱导的CCL26 (图3 d).
在气道持续性t辅助型2 (Th2)炎症和嗜酸性粒细胞增多的患者中,细胞因子信号抑制因子(SOCS)1基因表达降低。a) SOCS1和Th2活检特征(n=47)和b)固有层SOCS1和嗜酸性粒细胞数量(n=40)呈负相关。c) SOCS1在高气道嗜酸性粒细胞增多的受试者中表达降低(≥9.2个嗜酸性粒细胞/mm)2固有层,n=26)与低气道嗜酸性粒细胞增多(每毫米<9.22固有层;n = 26)。d) SOCS1与CCL26在气道中的表达呈显著负相关(n=44)。黑色圆圈代表轻/中度哮喘患者,白色圆圈代表重度哮喘患者。统计分析采用Mann-Whitney u检验和Spearman’s Rank检验。数据以中位数(四分位数范围)表示。* * *: p < 0.001。
支气管活组织检查中SoC蛋白的定位
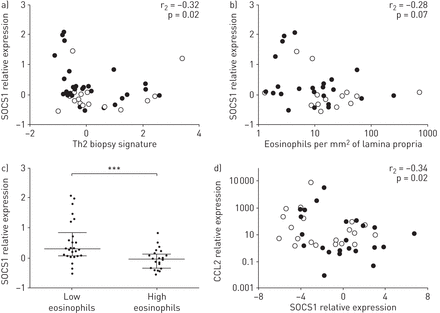
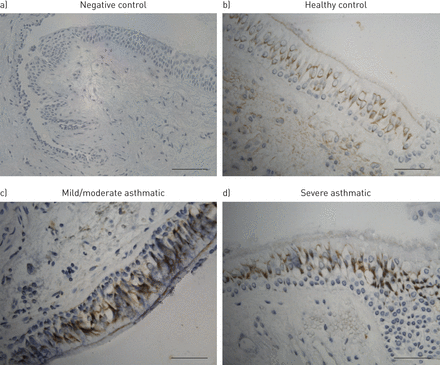
为了检测SOCS蛋白表达的细胞定位,我们在支气管活检中使用IHC对SOCS1、SOCS2和SOCS3进行染色。SOCS1主要定位于支气管上皮,并在分化的假柱状细胞中观察到,而不是基底细胞(图4a)阴性对照染色;以及b)健康对照组、c)轻度/中度哮喘患者和d)重度哮喘患者的SOCS1染色。在整个支气管活检中可见少量SOCS2染色明显,只有少量固有层中浸润的炎症细胞SOCS2染色阳性(在线补充文件中的图E6)。SOCS3同时存在于上皮细胞和固有层的单核/巨噬细胞样大细胞中(在线补充文件中的图E6)。
细胞因子信号抑制蛋白(SOCS)1主要定位于支气管上皮。a) SOCS1染色阴性对照。采用免疫组化方法对b)健康对照组、c)轻/中度哮喘患者和d)重度哮喘患者的甲基丙烯酸乙二醇包被支气管活检切片进行SOCS1染色。棕色染色显示SOCS1定位于支气管上皮。代表性图像为阴性对照染色和SOCS1上皮活检染色。比例尺= 100 μm。
在支气管上皮细胞SOCS1过度表达模型中抑制IL-13诱导的CCL26 mRNA
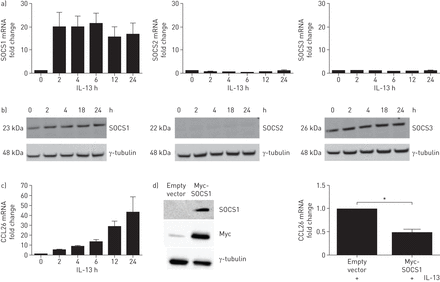
由于SOCS1定位于支气管上皮及其在严重哮喘气道中抑制Th2炎症的潜在作用,最初使用BEAS-2B细胞系来进一步研究SOCS1在支气管上皮中IL-13信号通路中的作用。我们检测了IL-13 (50 ng·mL)诱导BEAS-2B细胞中SOCS1 mRNA的表达−1),发现它在刺激2小时内迅速上调,并在24小时的时间过程中保持升高。SOCS2和SOCS3 mRNA未被IL-13诱导(图5A).然后,我们研究了IL-13刺激下SOCS1、SOCS2和SOCS3蛋白的表达,观察了SOCS1的诱导(SOCS1/γ-微管蛋白比率从0 h的1增加到24 h的1.3),但SOCS2或SOCS3 (图5B.).CCL26 (eotaxin-3) mRNA上调在体外通过IL-13刺激和气道Th2高水平炎症的哮喘患者的支气管活检[25].在IL-13刺激的BEAS2-B培养物中证实了CCL26 mRNA的上调(图5C.).为了研究SOCS1在il -13诱导的CCL26调控中的作用,我们使用myc标记的SOCS1质粒在BEAS-2B细胞中过表达SOCS1。与空载体对照相比,转染SOCS1质粒导致SOCS1在细胞中过表达(图5D).接下来,用空载体或myc标记的SOCS1质粒转染细胞24小时,然后用IL-13进一步刺激24小时。SOCS1过表达细胞中CCL26 mRNA显著下降(图5D).
在BEAS-2B培养中,过表达细胞因子信号抑制因子(SOCS)1可以抑制白介素(IL) 13诱导的CCL26 mRNA。a) IL-13刺激的细胞(50 ng·mL)−1), SOCS1 mRNA表达上调,SOCS2和SOCS3 mRNA表达不上调(n=3)。b) IL-13刺激的细胞(50 ng·ml)−1) 24 h后,SOCS1蛋白表达上调,而SOCS2和SOCS3蛋白表达不上调。c) IL-13刺激的细胞(50 ng·mL)−1) 24 h后显示CCL26 mRNA表达上调。d)用空载体或SOCS1过表达质粒转染细胞,然后检测SOCS1和质粒Myc-tag,确认SOCS1过表达。然后用空载体或SOCS1过表达质粒处理细胞24小时,再用IL-13刺激24小时,然后用定量PCR检测CCL26 mRNA。数据以中位数(四分位数范围)表示。采用Mann-Whitney u检验进行统计分析(n=4)。*: p < 0.05。
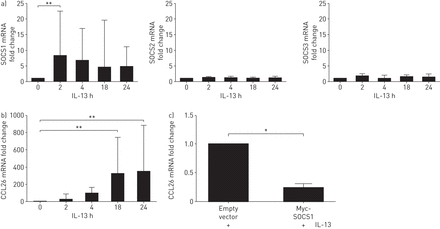
然后我们希望在原发性支气管上皮细胞(PBECs)中证实这些观察结果。IL-13 (50 ng·mL)刺激PBECs−1)超过24小时的课程。SOCS1 mRNA在刺激后再次迅速上调2小时,并在24-H次课程中保持升高,并且没有诱导SOCS2和SOCS3 mRNA(图6A).如预期的那样,在il -13刺激的细胞中也诱导了CCL26 mRNA (图6B.).电穿孔转染PBECs(如图E7所示,转染效率通常大于55%),同样,与空载体对照相比,SOCS1过表达降低了IL-13对CCL26 mRNA的诱导(图6C.).
原代支气管上皮细胞(PBEC)中过表达细胞因子信号抑制因子(SOCS)1抑制白介素(IL) 13诱导的CCL26 mRNA。a) IL-13刺激的细胞(50 ng·mL)−1), SOCS1 mRNA表达上调,SOCS2和SOCS3 mRNA表达不上调(n=5)。b) IL-13刺激的细胞(50 ng·mL)−1) 24 h后显示CCL26 mRNA表达上调。c)用空载体或SOCS1过表达质粒转染细胞24 h,再用IL-13刺激细胞24 h,然后用定量PCR检测CCL26 mRNA。数据以中位数(四分位数范围)表示。采用Kruskal-Wallis和t检验进行统计分析(n=3)。*: p < 0.05;* *: p < 0.01。
讨论
严重的哮喘影响所有哮喘患者的10%,但仍然引起持续嗜酸性炎症的潜在机制,尽管高剂量吸入皮质类固醇治疗,但尚未完全阐明[10,27].已经证明了SOC分子调节TH2细胞因子信号在体外而在在活的有机体内过敏气道炎症的小鼠模型;然而,如果存在类似的调节机制,则目前尚不清楚人类哮喘。
在本研究中,我们首次研究了SOCS1、SOCS2和SOCS3在健康对照组、轻/中度哮喘患者和重度哮喘患者气道中的表达。我们发现,重度哮喘和持续性嗜酸性气道炎症的患者与轻度更稳定的哮喘患者相比,上皮性SOCS1基因表达降低。SOCS1 mRNA的减少与IL-13依赖的Th2基因标记和组织嗜酸性粒细胞增多呈负相关,这似乎是矛盾的,因为人们可能会预期IL-13信号与SOCS1表达的增加有关,试图“关闭”IL-13驱动的反应。值得评论的是,健康受试者中SOCS1基因的基线表达水平较低(与严重哮喘患者没有区别),这可能反映了促炎细胞因子刺激的缺失,因此不需要负反馈调节器。关键的区别在于,在Th2信号和嗜酸性粒细胞增多的严重哮喘人群中,SOCS1 mRNA上调的失败是不合适的。
这种效应对于SOCS1似乎是特异性的,因为我们发现SOCS2或SOCS3基因表达在疾病严重程度、Th2特征或嗜酸性炎症浸润方面没有差异。SOCS2和SOCS3在哮喘动物模型中有牵连,SOCS分子之间可以相互作用。例如,SOCS2已经被证明可以调节SOCS1和SOCS3的表达通过直接相互作用[17]和SOCS2敲除小鼠的T细胞中SOCS1和SOCS3水平升高[18].然而,我们的数据检测了人类哮喘中SOCS分子的基因表达,表明在Th2持续炎症的严重哮喘中,尽管有高剂量吸入糖皮质激素,但SOCS1的特定调节异常。我们研究的一个限制因素是横断面设计;因此,我们不能对SOCS表达的动态变化进行评论。然而,SOCS1特异性下调的模式在伴有持续性嗜酸性粒细胞增多的严重哮喘患者中是一致的,因此这表明它不太可能是一个短暂的特征。
我们使用免疫组化方法检测SOCS蛋白的定位,更好地为后续研究提供信息在体外机械的分析。SOCS1主要定位于气道组织的支气管上皮。这与之前的数据一致,在气管内注射IL-13的小鼠显示出定位于气道上皮的SOCS1诱导[15].未来定量健康对照、轻/中度和重度哮喘患者支气管上皮细胞中SOCS1蛋白的工作将是有价值的。
在体外研究和在活的有机体内动物模型显示SOCS1可减轻Th2炎症。IL-13在局部气道诱导SOCS1在活的有机体内小鼠模型与eotaxin水平的抑制有关[15].在另一项研究中,使用了卵清蛋白诱导的气道炎症模型和SOCS1−−/干扰素-γ−−/与IFN-γ相比,小鼠肺部嗜酸性粒细胞浸润增加,Th2细胞因子升高−−/对照小鼠[14].这些动物研究支持了我们在人类哮喘中的数据,重度哮喘中SOCS1表达的减少也与气道嗜酸性粒细胞增多和IL-13依赖的Th2基因特征相关,表明上皮性SOCS1在调节气道和气道嗜酸性粒细胞增多中IL-13信号通路中具有核心作用。确实,有报道称,气道嗜酸性粒细胞中SOCS1高表达可抑制其对IL-5家族细胞因子的应答[28].因此,重度哮喘患者气道中嗜酸性粒细胞SOCS1的缺失可能导致IL-5细胞因子信号的敏感性增加,从而导致气道中嗜酸性粒细胞的生存和病理增强。
IL-13是一种Th2细胞因子,与人类哮喘有关,并在伴有持续性嗜酸性粒细胞增多的严重哮喘患者中升高[10,29].IL-13信号通过STAT6通路和SOCS1在减轻Th2炎症反应中的绝对需求通过在SOCS1缺陷的小鼠胚胎成纤维细胞中观察到STAT6磷酸化抑制[15,30.].由于SOCS1定位于支气管活检的支气管上皮,我们希望研究SOCS1在调节IL-13上皮信号通路中的作用在体外使用支气管上皮BEAS-2B细胞系和原发性支气管上皮细胞(PBECs)。CCL26 (eotaxin-3)的表达作为IL-13信号的下游readout被检测,因为之前的研究发现,它是Th2炎症哮喘患者气道中最上调的基因之一,它依赖于IL-13,是一种有效的嗜酸性粒细胞趋化剂[25,31,32].与轻度哮喘患者相比,严重哮喘患者的支气管上皮细胞对IL-13的反应最容易诱导CCL26,这与气道嗜酸性粒细胞增多相关[33].IL-13刺激的细胞显示SOCS1 mRNA被迅速诱导,但SOCS2和SOCS3并非如此。SOCS1的选择性诱导进一步支持了其在抑制IL-13驱动的Th2炎症中的作用,这与我们的患者数据相符,该数据显示SOCS2或SOCS3的表达与IL-13依赖的基因特征或气道嗜酸性粒细胞增多没有关系。正如预期的那样,与其他系统一致,在BEAS-2B细胞和PBECs中IL-13诱导了CCL26 mRNA的表达。与SOCS1调节IL-13信号通路的作用一致,SOCS1在BEAS-2B和PBEC培养物中过表达时,IL-13对CCL26的诱导受到抑制。我们之前报道过,在同一组严重哮喘患者中,IL-13依赖的th2基因标记升高的患者,IL-13的数量增加+渗透上皮的细胞[10].综上所述,这些严重哮喘患者,尽管接受了高剂量吸入皮质类固醇治疗,仍有持续性气道嗜酸性粒细胞增多,上皮内IL-13增加+IL-13在气道中持续信号传递(Th2基因特征),SOCS1表达减少。这表明,在这些患者中,SOCS1对IL-13的调控出现了故障,评估SOCS1的表达是否在IL-13抑制的基础上被修饰,将是我们感兴趣的,例如,在使用IL-13拮抗剂(如目前处于2/3期临床试验中的那些)治疗后[28,34,35].
一项在日本成人哮喘患者人群中评估SOCS1功能变异的研究发现,SOCS1启动子多态性−1478CA
总之,我们已经调查了SOCS1,SOCS2和SOCS3在健康对照,轻度/中度哮喘和严重哮喘的气道内表达。我们发现,与轻度/中度哮喘患者相比,SoCS1基因表达在严重哮喘患者的气道中显着降低。具有持久性嗜酸性粒细胞的受试者和气道内增加Th2炎症的上皮SOCS1 mRNA表达。在体外对BEAS-2B和原代支气管上皮细胞培养的研究表明,IL-13刺激诱导SOCS1,而SOCS1过表达导致IL-13刺激导致CCL26 mRNA诱导减少。进一步的工作将集中于为什么严重哮喘患者的上皮细胞中SOCS1上调不恰当,尽管气道中存在持续的Th2信号。
确认
我们要感谢贝尔法斯特皇后大学(贝尔法斯特,英国)的Lorcan McGarvey为我们提供了初级支气管上皮细胞。
脚注
编辑评论欧元和J2016;48: 608 - 610。
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:该研究得到了北爱尔兰就业与学习部的博士学位的支持;北爱尔兰胸部心脏和中风的支持;并授予Genentech Inc和国家卫生研究所Leicester呼吸生物医学研究单位的支持。表达的观点是作者的观点,不一定是NHS,NIHR或健康部的观点。本文的资助信息已被存入资助者打开注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2015年3月11日。
- 接受2016年4月24日。
- 版权所有©ers 2016